摘要
共聚焦激光显微内镜是一种新型的内窥镜技术,其可以允许活细胞成像肺组织中体内.我们评估了这种技术在筛查支气管镜检查肺癌期间的组织学的潜力。
32例疑似恶性肿瘤的患者接受盐酸吖啶黄支气管镜和显微内镜检查。标准化区域和局部病变的分析体内共焦成像期间,支气管镜和活检。共聚焦图像被分级,并与活检的常规组织学前瞻性相关。
盐酸吖啶黄产生高质量的共聚焦图像和强烈标记的气道上皮细胞。没有发现任何副作用。来自56个不同位置的75 522张共聚焦图像与活检标本的组织学数据进行了前瞻性比较。显微内窥镜可以对细胞和亚细胞结构进行详细的分析。预测肿瘤变化具有较高的准确性(敏感性96.0%,特异性87.1%,准确度91.0%)。
用吖啶黄素共聚焦激光显微内镜为活细胞的支气管镜检查过程中分析一个新的诊断工具,并允许在气道以高精度肿瘤改变虚拟组织学。患者疑似肺癌正在进行的内窥镜过程中,该技术可以使肿瘤的快速诊断。
共聚焦激光显微内窥镜(CLE)是一种在内窥镜中成像活细胞的新技术[1-8.].在系统施用染料荧光素,CLE可以进行体内在持续内窥镜检查期间,允许粘膜中的细胞和亚细胞结构的实时地下成像。最初,这种技术适用于胃肠道的各种炎性疾病,如炎症性肠病,巴雷特食管和乳糜泻。有人发现高品质体内可以进行成像,并且CLE用于快速诊断和靶向活组织检查。此外,CLE显示在胃中的肿瘤,食管和结肠高精度[1-8.].
与胃肠内镜检查相比,肺病中只有少数研究CLE。最近,T.希维尔等等。[9.在没有造影剂的情况下,CLE发布了肺泡的图像。他们描述了肺泡结构体内并确定Elastin作为主要内源荧光团。在吸烟者中,携带自发荧光颜料的肺泡巨噬细胞是唯一可以可视化的蜂窝结构。此外,Cle允许的中央气道成像,但是这种成像仅产生了关于弹性蛋白纤维的信息[10.].因此,没有造影剂的Cle不能用于评估气道上皮细胞和肺癌。为了规避中央气道中缺席的问题,fuchs.等等。[11.]用于CLE成像染料荧光素在肺类似于胃肠病学的领域中,其中,该染料产生结肠上皮细胞的优良染色。然而,荧光辅助CLE不允许在中心气道上皮细胞的染色,但只有在肺间质和肺泡腔的染色结果。因此,基于荧光素 - CLE不能分析上皮细胞的细胞结构的患者疑似肺癌体内.
在胃肠内镜内窥镜检查中,最近已用于补充静脉内或局部应用荧光素的Acriflavine,以便在CLE期间可视化蜂窝结构[9.].使用这种方法,CLE有助于识别细胞结构(例如细胞核)和细菌在胃和结肠粘膜。然而,目前还没有关于中央气道的吖啶黄辅助CLE的数据。本研究的目的是评估使用吖啶黄作为对比剂的中央气道病变的CLE成像。我们证明了吖啶黄辅助CLE可用于气道上皮细胞的分析体内高精度诊断肺癌。
方法
支气管镜检查
这项研究是经大学医院埃尔兰根(德国埃尔兰根)的伦理委员会。所有患者知情同意。
支气管镜检查和CLE在32名连续招募的患者中进行(九个女性,23名男性;平均值±SD.年龄64.5±11.3岁)中央气道的结节病变。患者的最终诊断是基于活组织检查的组织学(表1).支气管镜下进行I.v.有意识镇静(Midazolam 3-7毫克和Pethidine 50-100 mg),带视频芯片内窥镜(Olympus BF 1T180或BF Q180; Olympus,Tokyo,Japan)。患者被监测通过心电图、脉搏血氧测量和间歇性无创血压测量。氧气(≥2 L·分钟-1)给了通过鼻探头。

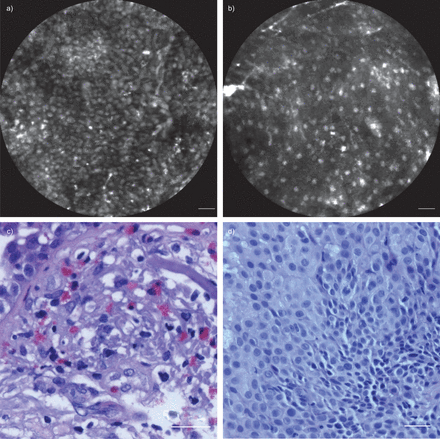
示例显示为a)普通粘膜,b)炎症再生和c)肿瘤病变。秤条=50μm。请参阅表2..
继续教育
用Cellvizio系统(Mauna Kea Technologies,巴黎,法国)进行CLE,在488nm的波长下工作。使用1.4毫米直径的共聚焦小纤维(Alveoflex; Mauna Kea Technologies)。共聚焦探针的技术细节如下。探针具有3.5μm的横向分辨率,视场为600×500μm,渗透深度为0-50μm。在宏观正常,标准化区域和突出的结节病变中染料施用后2分钟进行CLE。图像存储为数字文件。完成CLE分析后,采用活组织检查。使用标准血红素和曙红方法制备和染色部分。
图像分析
通过包括(CellVizio Viewer,1.4.1版本1.4.1; Mauna Kea Technologies)的软件分析了视频序列。使用了用于最佳分析的自动灰度特征。将Cle分析的结果与两种经历过的细胞病变学家(J.Schubert和M. Vieth)的组织病理学分析进行了比较。
染色剂
在本研究中,我们使用吖啶黄进行成像,因为没有染色的CLE和荧光素辅助的CLE不允许气道上皮细胞成像[11.].据我们所知,这是第一份关于局部使用吖啶酮治疗中央气道CLE的报告。虽然吖黄素由于其核染色特性被认为是一种潜在的致癌和致突变物质,但在流行病学研究中没有发现这方面的证据[12.].因此,ARIFLAVINE被描述为第3组(“不可分类为其致癌性对人类”)1987年和1991年的癌症报告研究机构的致癌物[13.那14.],并被归类为“可能对人类不致癌”[14.].此外,关于HIV疗法的长期使用的长期使用的数据的数据并未显示出在肿瘤疾病的高风险下这种群体肿瘤率的增加[15.-17.].这些研究中的后续时间≤38个月[16.].然而,这种观察期在以后的时间点不排除潜在的致癌作用。最后,Acriflavine显示出抗癌活动在体外在最近发表的研究中[18.那19.].因此,Acriflavine可能是人类各种诊断和治疗目的的有趣物质。始终如一地,胃肠疾病患者已用于CLIFlavine,而无需报告副作用[4.].此外,关于中央航空公司的Acriflavine使用的试验研究表明,Acriflavine给药是一种安全的程序。在这项研究中,10名患有2%Acriflavine溶液的局部施用的局部施用,在5个月观察期内未注意到副作用[20.].因此,我们认为再稀释40倍的0.05%吖啶黄溶液,由于剂量小且外用,不太可能产生相关副作用。然而,在符合伦理批准的情况下,在本研究中,吖黄素只用于疑似肿瘤的患者。
在目前的试验研究中,施加10毫升0.05%Acriflavine溶液(每位患者5mg Acriflavine)通过支气管镜进入远端气管和双主支气管的工作通道。施用随后是2分钟的等待时间,以允许分布和蜂窝摄取Acriflavine。2分钟后,注意到染色的均匀呼吸依赖性分布。随后用CellviziOs系统进行CLE,如上所述,并将内部瘤显微镜放置通过支气管镜的工作通道在中央气道的局部病变顶部。使用1.4毫米直径的共焦微型细胞,这种方法是可能的。除了局部病变之外,所有患者都会通过CLE检查在外观上宏观正常的中心气道的区域。
结果
在目前关于使用Acriflavine用于Cle的试点研究,施用了Acriflavine通过支气管镜进入远端气管和双主支气管的工作通道。随后,利用探针内镜分析宏观正常区域和外生的、局部的病变。32例患者均可在支气管镜检查时局部应用吖啶黄治疗CLE。在中央气道和气管远端进行吖啶黄染色,然后在这些区域进行CLE。CLE的耐受性良好,没有明显的副作用。在所有患者中,外生病变的上皮细胞都得到了很好的染色,并且使用吖啶黄辅助CLE可以看到中央气道的正常粘膜。
正常粘膜
在宏观正常支气管粘膜的所有区域中,鉴定了独特的均匀染色图案(图2一个).通过Acriflavine存在呼吸道上皮细胞核的强烈荧光染色,导致在内部质子检查期间检测小,浅灰色,密集填充且大多数重叠的斑点体内.与核的从相同的组织学区域样品中检测到这种染色模式很好的相关性(无花果。2b和c.)进一步表明,硬质药物检查能够分析气道上皮细胞。
体内支气管镜检查期间的吖啶黄素局部给药后正常的气道粘膜的共聚焦激光显微内镜(CLE)的成像。共焦探头与吖啶黄染色后定位在中央气道。共聚焦图像记录,并比传统的组织学。对应于小的,浅灰色的核的均匀分布,密集和大多重叠斑点注意到显微内镜期间:1)概述;b)和详细视图。c)中苏木精和从在该领域肺活检曙红染色的切片示出用于比较。应当指出的是,部分被切断在水平方向,以促进与CLE图像对比分析。秤条=50μm。
非肿瘤病变
在伴有局部炎症的外生性和浸润性病变中,可见大量突出的气道上皮细胞丧失细胞均匀性。细胞间距离扩大,气道上皮细胞细胞核明亮,胞浆暗(无花果。3A和C.).在患者的鳞状上皮细胞化生,共聚焦显微内镜检测众多的大细胞。而其细胞核相对较小,它们的细胞质被极度增大导致“煎鸡蛋”样细胞结构(无花果。3B和D.).
体内支气管镜检查期间的成像。ARIFlavine辅助共焦激光端子复合体的中央气道中炎症和B)炎症和B)血流变化。炎症和元塑病变导致核之间的距离增加,并且注意到核的很少或没有重叠。细胞具有扩大的细胞质,特别是在常规疾病中。支气管活检的组织学证实了C)炎症的存在和D)鳞状细胞元。秤条=50μm。
肿瘤病变
在非小细胞肺癌(NSCLC)和肺外癌转移外生性,暗肿瘤细胞进行鉴别。这些细胞显示出大的细胞核,在大小异质性。具体地,核表明较弱吖啶黄摄取和被安排比在正常黏膜密度较低(无花果。4.).此外,围绕异质核的宽和深细胞质所指出的,允许正常和暗,肿瘤性气道上皮细胞之间的区别。因此,吖啶黄辅助共焦成像可用于肿瘤细胞在气道上皮细胞扩展的精确映射。
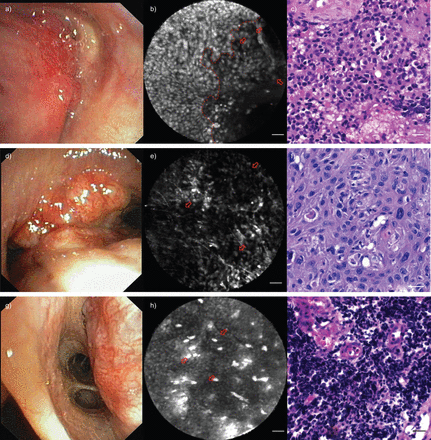
肺的腺瘤癌:a)支气管中间体的支气管镜视图,几乎被引发的病变堵塞;b)共用体内在与吖啶黄外用染色病变的成像显示很少或根本没有摄取吖啶黄暗区,指示瘤。一些肿瘤细胞被突出显示(箭头)。此外,发炎区域具有增加的距离之间细胞核注意到肿瘤周围的。发炎(左侧)和肿瘤组织(右侧)之间的边界线是清晰可见的(红色虚线)。C)从)通过共聚焦激光内镜(CLE识别的肿瘤组织学区域活检用苏木精和伊红(H&E),并确认该赘生瘤的存在(腺瘤性癌)染色。肺的鳞状细胞癌:d)主隆突支气管镜视图,示出大结节性病变。共焦探针放置在病灶的顶部体内成像。e)持续支气管镜检查期间的共聚焦成像在用Acriflavine染色后显示出大的暗区,具有非均相细胞群,表明存在瘤形成。几个肿瘤细胞被突出显示(箭头)。f)取活检,并用H&E染色切片。组织学分析证实存在肺癌(肺的鳞状细胞癌)。肺部小细胞癌:g)右下叶中的小细胞肺癌患者的支气管镜视图(SCLC)。h)用Acriflavine染色后CLE鉴定了许多小的圆形肿瘤细胞体内.这些细胞具有暗淡的外观,少于或不含加吸收(箭头)。i)该区域中活组织检查的组织学分析证实了SCLC的许多肿瘤细胞的存在。秤条=50μm。
在小细胞肺癌(SCLC)的患者中,观察到具有小黑暗圆形细胞较弱的Acriflavine吸收的均匀模式。与NSCLC患者的细胞相比细胞比较少得多(无花果。4G-I.).此外,与炎症病变相比,细胞胞浆非常小。因此,吖啶黄辅助CLE在SCLC中形成了一种特征性的染色模式,可用于体内诊断这种疾病。
CLE诊断率
使用新设计的共聚焦模式分类分析了气道的共聚焦图像以进行肿瘤的存在。因此,来自12名患者的初始数据与病理标准一起使用,用于设计共聚合模式分类(表2.).通过内窥镜医师和病理学家对图像的综合分析,发现细胞结构和一般组织结构是鉴别肺部肿瘤组织和非肿瘤组织的重要依据。因此,共焦模式分类根据气道上皮细胞的细胞质和细胞核的特征结构以及CLE分析中的组织结构,将肿瘤组织和非肿瘤组织分为正常组织、炎症/再生组织和瘤变组织三种不同类型。然而,在正常组织中可见明亮的、部分重叠的细胞核,其组织结构均匀;在组织结构不均匀的炎症/再生组织中可见细胞核没有重叠但胞浆扩大的细胞。此外,细胞核不均匀的深色细胞分布混乱,提示肿瘤发生。
共聚焦模式分类预期以预测组织病理学。因此,具有75个522个共焦图像的96个视频序列(九个框架·s-1平均每周2.5分钟)从56个不同的位置,包括来自宏观正常的粘膜和37个来自突出或渗透病变的37个活组织检查,以致盲的方式分析。在服用活组织检查之前,用CLE评估所有网站,并将组织学结果与CLE发现进行比较。
共聚焦成像和组织学的结果显示在表3.CLE对恶性病变的检测灵敏度为96.0%,特异性为87.1%。阳性预测值为85.7%,阴性预测值为96.4%。总体而言,91.0%的网站被正确分类。
讨论
CL是一种新颖的技术体内粘膜的成像。在目前的试点研究中,我们使用造影剂ARIFlavine用于疑似肺癌患者支气管粘膜的共焦成像。我们观察到该技术有助于检测气道病理学。通过直接将来自CLE的数据与活组织检查中的组织病理学发现进行比较,我们证明这种加芳林助缘CLE检测中心气道中局部病变的肿瘤变化,高精度。
支气管镜见证了近年来许多改进,包括视频和高分辨率内窥镜的发展。另外,自体荧光支气管镜(AFB)引入作为红旗技术来识别局部病灶,但不幸的是,得到的假阳性结果的高速率21.].此外,已经使用诸如窄带成像(NBI)的过滤技术,以便于检测气道中的局部病变[22.].但是,这些技术都不允许体内中央气道的细胞分辨率成像。
以前用于检测胃肠道中的粘膜变化[1-8.].此外,最近的研究使用这种方法对肺部成像[9.-11.].发现自发荧光和荧光素助剂CLE可用于肺泡和肺插形的成像。然而,与胃肠道相比,荧光素不能渗透到气道中的上皮细胞中。因此,使用荧光素的Cle不能用于分析肺癌。
在这里,我们使用吖啶黄素辅助CLE作为一种新的方法对气道上皮细胞的成像体内.在使用基于探针的CLE系统和局部染色的试验研究中,我们可以表明,在气道中的Acriflavine的局部应用是安全的,可以很容易地完成。除了在放置共聚焦探针时,在一些癌症患者中渗透血液的最小渗透,在支气管镜检查期间,我们看不到CL的任何不良事件。该技术的局限性与探针的系统无法以目标方式引入较小的气道的事实有关,从而限制CLE到中心气道的使用。此外,成本可能是支气管镜检查期间CLE实施的另一个限制。应该指出的是,功能共聚焦单位的成本目前〜120 000欧元。此外,至少在我们的临床环境中,单一程序的成本为耗材〜250欧元。执行每个支气管镜检查所需的时间是5-10分钟。
Acriflavine辅助CL的图像质量非常高。事实上,基于Acriflavine的成像允许细胞分析体内并可用于区分炎症和肿瘤区域正常气道上皮细胞和改变的上皮细胞。粘膜炎症的评估可以在宏观炎症区域进行,也可以在外生性肿瘤生长的边界区域进行。因此,这项技术可能是一个有价值的工具,为未来的研究瘤周炎症。由于CLE可以识别肿瘤病变边界区域的肿瘤细胞,而粘膜在宏观上是正常的,因此在肺癌治疗手术前评估肿瘤扩散可能是CLE的另一个潜在应用。此外,它可能有助于描述哮喘和慢性阻塞性肺病等慢性疾病的气道炎症,并可能影响治疗策略。最后,CLE可能为气道上皮细胞的分子成像打开大门体内,因为该技术已被最终超出血管内皮生长因子受体和结肠上皮细胞CD44V6染色的Acriflavine染色[23.-27.].
引入共聚焦显微内镜时需要考虑的另一点与图像分析有关。为了达到这个探索性初步研究的目的,我们必须分析大量的单一图像。这对于开发能够进行组织评价的图像分类是必要的。为了发展这种分类,必须仔细审查所有图像和视频序列。然而,在未来的研究中,我们认为回顾视频序列就足够了体内共焦分析。随着视频的平均长度为2.5分钟,我们觉得将来2.5分钟就足以进行最终分析。通过关于局部损伤的直接信息和必要的活检数量的潜在降低,这种额外时间可以是合理的。在这方面,应该指出的是,已显示共聚焦内镜检查显着减少了胃肠学领域所需活检的数量[27.].
Acriflavine辅助CL可以区分肿瘤和非肿瘤病变。特别地,与组织学结果的直接比较表明,该技术具有高灵敏度,特异性和准确性,用于检测在持续的支气管镜期间的肿瘤病变。基于我们目前的试点研究,Acriflavine-Aided CLE作为一个有希望的新方法出现体内肺癌的影像,并可能有助于澄清局部的视觉表现。然而,我们不能断定CLE优于AFB或NBI。因此,今后的研究应侧重于AFB、NBI和CLE在支气管镜检查中的联合应用。然而,无论如何,CLE可能会降低AFB或nbi引导活检假阳性结果的比率。
总之,在支气管镜检查中,吖啶黄辅助中央气道CLE是一种可行和安全的检测肿瘤改变的方法。尽管该方法目前存在一些局限性,但该技术允许对气道上皮细胞的细胞结构进行独特的观察,并允许进行地下成像。事实上,在肿瘤组织和非肿瘤组织的鉴别方面,在大多数病例中,吖啶黄辅助CLE的诊断产量与肺活检的组织学相当。因此,CLE可能有助于减少活组织检查的次数,并优化肺的靶向活检。此外,该技术允许详细评估细胞结构和肺癌,并预测肿瘤变化的存在,具有很高的准确性。而吖啶黄辅助CLE先前已被证实用于胃肠道疾病[4.那26.-28.],需要进一步研究阐明吖啶黄辅助CLE在炎症性和肿瘤性肺部疾病中的临床意义。然而,吖啶黄辅助CLE不太可能取代传统的肺癌活检,因为目前组织学分析是确定肿瘤亚型和预测分子标志物的关键(例如表皮生长因子受体突变状态)。然而,CLE引导的组织采样可以提高常规活组织检查的准确性,因此可以提供更高的肿瘤组织的产量,以便随后分析。此外,CLE可能导致快速优化体内疑似肺癌患者肿瘤变化的诊断。
致谢
作者谨此感谢S. Alikovic,J.Gebelein和T.Vilusic(Medicine 1,Erlangen-Nuremberg大学,Erlangen,Erlangen,Erlangen,德国)在支气管镜检查期间的援助。此外,作者还感谢A. Watson(East Anglia大学,英国诺里奇,英国)的批判阅读稿件。
脚注
利益声明
没有宣布。
- 已收到2012年4月15日。
- 公认2012年8月27日。
- ©2013年