摘要
在早产儿中,短暂的氧浓度升高与血液趋化因子浓度的长期升高和支气管肺发育不良(BPD)的发生有关。研究表明,给予早产儿咖啡因以预防或治疗呼吸暂停可降低BPD的发生率。
我们测试了以下假设:与单独暴露于高氧环境的幼鼠相比,暴露于咖啡因和高氧环境的幼鼠对肺损伤的敏感性更低,并且咖啡因降低了高氧环境下趋化因子的肺组织表达和白细胞内流。
使用6日龄大鼠幼鼠,我们证明了80%氧暴露24小时可引起中性粒细胞和巨噬细胞的肺募集。高水平的氧上调CXC趋化因子、细胞因子诱导的中性粒细胞趋化因子-1和巨噬细胞炎症蛋白-2的表达;cc趋化因子单核细胞趋化蛋白-1;通过实时荧光定量PCR检测,在给药咖啡因(10 mg·kg)后,促炎细胞因子肿瘤坏死因子-α和白细胞介素-6−1.体重);以及减弱的趋化因子和细胞因子的上调,以及CD11b的流入+, ED-1+和髓过氧物酶+白细胞。
这些实验表明,咖啡因对新生儿肺的保护作用是通过减少肺部炎症介导的,至少部分是这样。
支气管肺发育不良(BPD),也称为早产儿慢性肺病,影响∼50%胎龄<28周的极低出生体重儿[1.]是工业化国家婴儿期最常见的慢性肺病[2.]BPD与生命第一年内的一系列再住院、长期肺部问题和持续的神经发育延迟有关[2.]氧化应激在BPD的发生发展中起着重要作用[3.].出生后肺部通气已经表明肺组织局部氧张力突然增加四到五倍,早产儿对此准备不足。此外,其中一些婴儿暂时需要增加吸入氧的分数(高达100%)用于肺部疾病,如呼吸窘迫综合征、肺炎或原发性肺动脉高压。组织学上,BPD具有不同阶段炎症的特征,但试图通过全身或吸入性皮质类固醇治疗BPD的早期阶段只能获得暂时缓解,并伴有严重副作用,如脑瘫与胃肠道出血[4.].
目前,很少有预防性干预措施通过随机对照试验证明能显著降低BPD的发生率:外源性表面活性物质给药[5.],在产房用低浓度吸入氧气而不是高浓度吸入氧气开始复苏[6.];维生素A (7.];以及咖啡因[8.].咖啡因是一种用于治疗早产儿呼吸暂停的药物[9].为预防或治疗呼吸暂停而给予早产儿的咖啡因已被证明可降低BPD的发生率,但尚不清楚这种保护作用是由于机械通气时间缩短还是咖啡因的直接肺部效应。在一项涉及2006年早产儿的大型随机安慰剂对照多中心试验中研究发现,咖啡因的使用可以缩短正压通气的持续时间,并降低BPD的发生率,这是由妊娠36周时补充氧气的需求所定义的[8.].早期开始服用咖啡因时,保护作用最大,即。在生命的前3天[10].咖啡因的保护作用被认为是由于改善了呼吸肌肉的力量和降低了呼吸暂停的发生率[11,从而减少呼吸机诱导的肺损伤,降低机械通气的需求。然而,咖啡因对未成熟肺的直接药理作用尚未被探索。
在动物模型中,早期暴露于高氧浓度会导致进行性肺部疾病,这与早产儿的BPD非常相似[12,13]我们通过在肺发育的囊状期到肺泡期的过渡期向P6大鼠幼鼠给予高浓度吸入氧,研究了在实验性急性肺损伤模型中给予咖啡因的效果[14],并分析肺趋化剂、促炎细胞因子、白细胞外溢入肺组织及组织破坏的组织学征象。
材料和方法
动物
来自定时怀孕的雌性Wistar大鼠(Charité - Universitätsmedizin Berlin, Berlin, Germany)被分为4个生物学组:1)常氧(吸气氧分数(FIO2.)21%(室内空气)和0.9%氯化钠溶液i、 p。;2)常氧和咖啡因(Sigma, Steinheim,德国)10 mg·kg−1.体重i、 p。; 3) 高氧(F一、 O2.80%, OxyCycler;BioSpherix, Lacona, NY, USA)和0.9% NaCl溶液i、 p;4)高氧和咖啡因10mg·kg−1.体重i、 p.小狗治疗一次盐水或咖啡因normoxia初氧过多持续6日24或48 h。两种情况下,幼崽都与他们的大坝,48小时崽,护理大坝切换每24 h之间常氧和氧室每个垃圾提供平等的营养。所有程序都由国家当局批准(德国柏林LAGeSo),并遵循制度指导方针。
组织准备
在氧气暴露6、24和48小时后,用安眠药麻醉幼崽i、 p。氯胺酮注射液(50mg·kg−1.)和噻嗪(10 mg·kg)−1.).为了进行分子分析,犬只经心脏灌注生理盐水,取下肺,在液氮中快速冷冻,保存在-80°C。免疫组化分析,经心脏灌注pH 7.4的生理盐水,然后在pH 7.4下灌注4%多聚甲醛。取肺,4℃固定3天,石蜡包埋,组织染色。
RNA提取与实时PCR
通过酸性苯酚/氯仿萃取法(peqGOLD RNApure;PEQLAB Biotechnologie,Erlangen,Germany)分离总RNA,并反向转录2μg RNA。PCR产物为细胞因子诱导的中性粒细胞趋化因子(CINC)-1、巨噬细胞炎性蛋白(MIP)-2、单核细胞趋化蛋白(MCP)-1、肿瘤坏死因子(TNF)-使用染料标记的荧光报告寡核苷酸探针/序列实时定量α和白细胞介素(IL)-6(表1).PCR和检测进行了一式三份11 -μL反应混合物中含有5μL(2×KAPA探针快速qPCR Mastermix (PEQLAB Biotechnologie), 2.5μL 1.25μM寡核苷酸,0.5μL 0.5μM探针(BioTeZ,柏林,德国)和3日- 15日ng cDNA模板StepOnePlus™实时PCR系统(应用生物系统公司,生活技术,Carlsbad, CA, USA)与次黄嘌呤鸟嘌呤磷酸核糖转移酶(HPRT)作为内参。PCR产物水平归一化为HPRT水平。根据2-ΔCT方法[15].
免疫组织化学
组织固定
石蜡包埋的肺组织被切成10 μm切片,并安装在SuperFrost Plus涂层切片(Menzel, Braunschweig, Germany)上。每个切片在Roti-Histol (Carl Roth, Karlsruhe, Germany)中脱链两次,每次10分钟,然后在乙醇(100、90、80和70%)、蒸馏水和PBS中室温再水合3分钟。
形态学检查
水合切片用苏木精和伊红染色。使用配备了×200放大镜的徕卡DM2000显微镜(德国Wetzlar Leica Microsystems)通过光学显微镜观察肺组织学和形态计量学变化。然后使用徕卡应用套件(LAS)软件分析数字存储的图像。
免疫染色
为了增加细胞膜的通透性,从而去除细胞内的表位,切片在600 W的柠檬酸盐缓冲液(pH 6.0)中在微波炉中固定12分钟。切片在PBS中冷却和清洗三次。切片在含有2%山羊血清、1%牛血清白蛋白、0.1%Triton X-100、0.05%吐温20和0.1%牛明胶的PBS中培养60分钟,以阻断非特异性蛋白质。切片用PBS洗涤一次,随后在4°C下与单克隆小鼠抗鼠CD11b(OX42)孵育过夜,该单克隆小鼠抗鼠CD11b主要表达于单核细胞和粒细胞,1:200(英国剑桥大学Abcam)和单克隆小鼠抗鼠ED-1,粒细胞表达的糖蛋白,单核细胞和组织巨噬细胞,包括肺泡巨噬细胞,1:100(Abcam);或在室温下用多克隆兔抗髓过氧化物酶(MPO)表达30分钟,其由中性粒细胞、1:200(THEMOFISHER SCORE,施韦尔特,德国)稀释在抗体稀释剂中(ZYMED实验室,旧金山,CA,美国)。为了检测,在抗体稀释液(酵素实验室)中以1:200的稀释度应用二级荧光素结合的山羊抗鼠IgG(德国汉堡Dianova)或荧光素结合的山羊抗兔IgG(Dianova),并在室温下培养1小时。在用PBS洗涤三次后,对载玻片进行复染,并用含有荧光保护安装介质的4,6-二氨基-2-苯基吲哚(DAPI)水溶液(含DAPI的Vectashield硬装安装介质;Vector Laboratories,Burlingame,CA,USA)进行安装。
在荧光灯下,使用配备有×200放大镜的Leica DM2000显微镜观察切片,并使用LAS软件进行分析。在每只动物的10个单独区域中,对相关隔间内的CD11b-、ED-1-和MPO阳性细胞进行阳性染色计数。我们使用ImageJ分析了细胞数量(美国马里兰州贝塞斯达国立卫生研究院)通过设定颗粒大小阈值。
统计分析
所有数据均表示为平均值±扫描电镜使用单因素方差分析对各组进行比较,并使用Bonferroni的多重比较校正和独立样本t检验确定显著性。双侧p值<0.05被认为是显著的。
结果
高氧导致肺泡发育紊乱,咖啡因可减弱这种紊乱
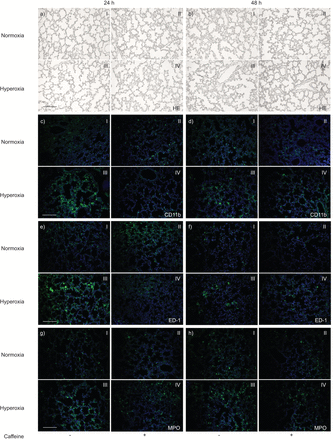
6日龄大鼠幼崽暴露于高氧环境中24小时(至出生后第7天(P),图1aIII)或48小时(至P8,图1 biii)导致不均匀分布的扩大的空气空间,间隔变薄和水肿形成,咖啡因减少了这种情况(图1一个和bIV)。
石蜡肺切片:出生后第7天(P)和第8天(b)用苏木精和伊红(HE)a染色;第7天(P)和第8天(d)用抗CD11b(绿色)和4,6-二氨基-2-苯基吲哚(DAPI)核染色(蓝色)进行双重免疫荧光染色;第7天和第8天(d)用抗ED-1(绿色)和DAPI核染色(蓝色)[续下页]e)在P7和f)P8;抗髓过氧化物酶(MPO)(绿色)和DAPI核染色(蓝色)g在P7和h)P8。这些图片代表了常氧(I,II)或高氧(III,IV)、无(I,III)或咖啡因给药(II,IV)的肺切片。常氧组的肺没有(aI和bI)和有(aII和bII)咖啡因给药显示P7和P8肺泡发育正常。高氧暴露破坏了P7(aIII)和P8(bIII)肺泡发育,咖啡因给药(aIV和bIV)减弱了肺泡发育。高氧引起肺白细胞浸润,咖啡因减少了肺白细胞浸润。注意:大量CD11b的存在+c)P7和d)P8处的细胞;ED-1+e) P7和f) P8;和MPO+高氧暴露动物的g)P7和h)P8细胞(III)。咖啡因给药完全消除(24小时:cIV、eIV和gIV)或显著减弱(48小时:dIV、fIV、hIV)这种增加。所有显微照片均以相同的放大倍数拍摄。标尺=200μm。
高氧会引起肺白细胞浸润,咖啡因会减少这种浸润
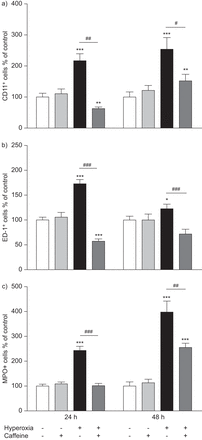
高氧导致涉及白细胞(CD11b)的明显炎症反应+)尤其是单核细胞和巨噬细胞(ED-1)+)和中性粒细胞(MPO+).在对照动物室内空气中,少量常驻CD11b+(图1cI和dI),ED-1+(图1eI和)及MPO+(图1gI在肺的间隔和肺泡中发现hI)细胞。在暴露于高氧的幼鼠中,CD11b的数量显著增加+(图1cIII和dIII),ED-1+(图1eIII及(ii)及MPO+(图1gIIICD11b在暴露于高氧的24小时(p<0.001)和48小时(p<0.001)时分别增加115±22.9%和152±38.6%,ED-1在暴露于高氧的24小时(p<0.001)和48小时(p<0.001)时分别增加72±9%和22±10.1%,MPO在暴露于高氧的24小时(p<0.001)和48小时(p<0.001)时分别增加142±17.2%和296±45.2%(图2,黑色条)与室内空气中的对照幼崽相比(图2,白色的酒吧)。咖啡因治疗显著减少了CD11b的流入+(图1cIV及分区),ED-1+(图1eIV和fIV)和MPO+(图1 IV与注射生理盐水的高氧动物相比,高氧后幼崽肺中的免疫细胞和hIV)免疫细胞。单剂量咖啡因(10 mg·kg)对幼崽的治疗−1.在高氧暴露之前,体重)显著降低:CD11b的数量+细胞,24小时为3.4倍(p<0.01),48小时为1.7倍(p<0.05)(图2一个,深灰色条);ED-1+细胞,24小时为3倍(p<0.001),48小时为1.7倍(p<0.001)(图2 b,深灰色条);及+细胞,24 h 2.4倍(p<0.001), 48 h 1.6倍(p<0.01) (图2 c在室内空气中饲养的幼鼠中,咖啡因处理对肺组织中的免疫细胞数量没有显著影响(图2,浅灰色条)。
a)CD11b的定量分析+, b) ED-1+,及c)MPO+石蜡切片上的细胞计数显示,在高氧条件下保存24和48小时的幼鼠肺组织样本中有明显的聚集,而咖啡因治疗减少了不同亚型白细胞的流入。在室内空气条件下咖啡因处理没有显示出明显的调节作用。数据以常氧暴露对照组的平均值表示+扫描电镜每个常氧组至少有四只幼鼠,每个实验组至少有六只幼鼠。100%的值为a)1.985和0.537 CD11b+细胞·毫米−2.,b)1.963和2.302 ED-1+细胞·毫米−2.和c)1.030和0.603 MPO+细胞·毫米−2.,分别用于24小时和48小时组。*:p<0.05、***:p<0.01和***:p<0.001对控制#:p<0.05,##:p<0.01和###:p<0.001对高氧(t检验)。
高氧增加,咖啡因降低肺部趋化因子和促炎细胞因子的mRNA表达
趋化因子是白细胞外渗进入炎症组织的先决条件。因此,我们使用实时PCR测定两种关键CXC趋化因子CINC-1和MIP-2以及CC趋化因子MCP-1和两种早期促炎细胞因子TNF-α和IL-6的差异表达。高氧导致mRNA表达的时间依赖性增加三种趋化因子均表达(图3)研究了两种促炎细胞因子(图4).
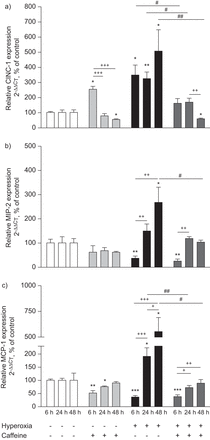
咖啡因可防止高氧诱导的CXC-(细胞因子诱导的中性粒细胞趋化因子(CINC)-1和巨噬细胞炎性蛋白(MIP)-2)和CC-(单核细胞趋化因子蛋白(MCP)-1)的肺mRNA表达增加趋化因子。与室内空气中的动物相比,实时PCR检测到的高氧6、24和48小时大鼠肺提取物中a)CINC-1、b)MIP-2和c)MCP-1的mRNA水平明显升高。通过全身咖啡因预处理,这些水平降低。室内空气中的咖啡因处理没有显示相关的调节作用。R实时PCR定量结果显示为平均值+扫描电镜.数据标准化为暴露于含生理盐水的常氧环境中的幼鼠水平(对照组100%)。CT:循环阈值。*:p<0.05、***:p<0.01和***:p<0.001对控制#: p < 0.05##:p<0.01对氧过多;+:p<0.05,++:p<0.01和+++:p<0.001对组内(t检验,n=6 /组)。
咖啡因可防止高氧诱导的肺早期细胞因子肿瘤坏死因子(TNF)-α和白细胞介素(IL)-6 mRNA表达增加。与室内空气中的动物相比,高氧6、24和48小时时,通过实时PCR检测到的大鼠肺总提取物中a)TNF-α和b)IL-6的mRNA水平明显升高。通过全身咖啡因预处理,TNF-α(a)在所有时间点以及IL-6(b)在24小时和48小时的水平都会降低。在室内空气条件下咖啡因处理对TNF-α无相关调节,在6和48小时时IL-6显著降低。实时PCR定量结果显示为平均值+扫描电镜.数据标准化为暴露于含生理盐水的常氧环境中的幼鼠水平(对照组100%)。CT:循环阈值。*:p<0.05、***:p<0.01和***:p<0.001对控制#:p<0.05,##:p<0.01和###:p<0.001对氧过多;+: p < 0.05+++:p<0.001对组内(t检验,n=6 /组)。
高氧导致CINC-1表达在6小时(247±66.5%;p<0.05)、24小时(222±44.1%;p<0.01)和48小时(405±141.7%;p<0.05)显著增加(图3a6小时时MIP-2表达显著降低(65±10.6%;p<0.01),48小时时显著增加(167±63.7%;p<0.05)(图3b6 h时显著降低(64±6.7%;P <0.001), 24 h显著升高(91±32.7%;P <0.05)、48 h(450±140.2%;p<0.05); MCP-1 (图3c黑条)。高氧条件下促炎细胞因子mRNA表达6 h TNF-α显著升高(199±88.6%;P <0.05)、24 h(117±37.0%;p < 0.05) (图4a6 h时显著降低(88±1.7%;p<0.001), IL-6在24 h显著升高(122±38.3%;P <0.01)、48 h(323±34.8%;p < 0.01) (图4b黑条)。
咖啡因治疗有效地消除了任何高氧介导的趋化因子和促炎细胞因子mRNA表达的增加。用单剂量咖啡因(10 mg·kg)治疗幼崽−1.与常氧对照组相比,ccin -1的mRNA表达显著降低,6 h时为2.2倍(p<0.05), 24 h时为2.0倍(p<0.05), 48 h时为8.9倍(p<0.01)。图3a,深灰色条);48 h MIP-2, 2.6倍(p<0.05) (图3b,深灰色条);MCP-1在24h时为2.7倍(p<0.01),在48h时为6.2倍(p<0.05)(图3c,深灰色条);TNF-α, 6 h时3.5倍(p<0.01), 24 h时2.2倍(p<0.05), 48 h时1.8倍(p<0.05) (图4a,深灰色条);IL-6在24小时时为2.0倍(p<0.05),48小时时为9.8倍(p<0.001)(图4b,深灰色条)。
在常氧动物中,咖啡因治疗导致CINC-1表达在6小时时短暂增加(253±18.8%;p<0.05),然后在48小时显著降低(53±5.3%;p<0.05)(图3a咖啡因在6小时(52±9.9%;p<0.01)和24小时(76±3.5%;p<0.05)也降低了MCP-1(图3c6小时(23±9.0%;p<0.01)和48小时(59±8.4%;p<0.05)时的IL-6(图4b,浅灰色条),与常氧对照组相比。
讨论
这些研究的结果表明,6-48小时的高氧足以引起幼鼠明显的肺部炎症。研究发现,短期高氧可在很大程度上防止趋化因子和促炎细胞因子的上调、中性粒细胞和巨噬细胞的流入以及组织破坏咖啡因的服用。
研究发现,将新生啮齿动物暴露于长时间的高氧环境(60-100%氧气,持续7-14天)会导致与早产儿相似的慢性肺病,因此已成为BPD的一种已建立的动物模型[12,13,16].与之前报道的大多数实验相比,我们的研究侧重于高氧的前48小时,并支持这样一种观点,即即使是短暂暴露于吸入氧气的增加部分也有利于婴儿的肺部。我们的动物数据与一项前瞻性随机试验的临床数据相关,该试验分配了m婴儿≤从胎龄28周到出生后5分钟内用90%或30%的氧气复苏。在该研究中,用30%氧气复苏的婴儿随后的BPD发生率显著降低。此外,CXC趋化因子IL-8(CINC-1的人类同源物)的血浆浓度在婴儿出生后的前3周内,被随机分配到90%氧气的婴儿的血压持续升高,而被随机分配到30%氧气的婴儿的血压持续升高[6.].
在本文报道的动物实验中,短期高氧可上调CXC趋化因子CINC-1和MIP-2以及CC趋化因子MCP-1。这些趋化因子先前已被证明是白细胞募集到肺组织中的关键[17,18].此外,高氧导致促炎核因子-κ b调节的细胞因子TNF-α和IL-6的连续诱导,这有助于增强入侵白细胞的活性[19]。BPD早产儿气道分泌物中也检测到趋化因子(IL-8、MIP-1和MCP-1)和细胞因子(TNF-α和IL-6)水平升高[20,21].
在高氧开始时用咖啡因治疗可阻断趋化因子和促炎细胞因子的上调以及高氧时出现的髓系白细胞的流入。咖啡因不仅降低了mRNA表达,减少了炎性细胞向肺组织的浸润,而且还改善了动物的组织学损伤我们认为,在这些动物实验中观察到的咖啡因的抗炎作用至少在一定程度上是服用咖啡因的早产儿BPD发病率降低的基础[8.].然而,尽管我们发现咖啡因可以有效地减弱氧诱导的趋化因子表达、白细胞内流和随后的组织损伤,但在室内空气中给动物服用咖啡因也会促进鼻中隔变薄。这种看似矛盾的观察结果被最近油酸诱导的急性肺损伤小鼠模型的数据所反映,高剂量咖啡因获得的中性粒细胞募集减弱,而低剂量咖啡因增强了肺组织损伤[22].
咖啡因的药理作用是众所周知的[23,24,但其对炎症等其他过程的影响尚不清楚[25–27]咖啡因是一种非特异性腺苷受体(AR)拮抗剂;阻断一种或多种AR亚型可产生相反的效果[27,28].答案:C哈维兹valdez等. [29研究表明,超出治疗范围的咖啡因血浆水平与促炎细胞因子谱有关,但其临床意义尚不明确。因此,我们细胞因子表达数据的可变性可以用咖啡因及其代谢物的非线性药代动力学来解释[30,31].
这项研究有几个局限性,指向未来的研究领域。首先,我们没有评估更短的氧气暴露时间是否足以引起持续的炎症,正如Vento等[6.]第二,咖啡因只给动物服用一次,而早产儿服用咖啡因达数周之久[10].第三,咖啡因被认为发挥了它的大部分作用通过竞争性非特异性拮抗ARs [32,33]研究这些受体的参与已经超出了我们实验的重点。
来自腺苷A2a受体敲除小鼠的数据表明,咖啡因可能的损伤作用是介导的通过腺苷A2a受体,而保护作用遵循不同的途径。腺苷A2b受体在调节各种动物模型的肺部炎症和慢性阻塞性肺疾病的发病机制中具有重要作用[34,35].
需要进一步研究以确定A2a和A2b受体和AR非依赖性机制的作用,例如然而,根据随机临床试验结果和我们的实验数据,咖啡因和可能的其他甲基黄嘌呤是预防早产儿氧诱导肺损伤的有希望的候选药物。
致谢
我们感谢M. Blanco(范德比尔特大学,纳什维尔,TN,美国)对手稿的校对。
脚注
感兴趣的语句
没有宣布。
- 收到2012年1月20日。
- 认可的2012年7月19日。
- ©2013人队