摘要
以粟粒性肺内癌(MIPC)为表现的非小细胞肺癌(NSCLC)是罕见的。我们观察了其临床特点及表皮生长因子受体(表皮生长因子受体) MIPC NSCLC患者初诊时的突变率。
从2004年6月到2008年12月,我们使用基于图像的标准对新诊断的NSCLC患者进行了MIPC筛查。记录临床资料并进行分析表皮生长因子受体突变状态。为了进行比较,我们收集了未进行MIPC检测的IV期NSCLC患者的标本表皮生长因子受体2001年4月至2008年11月的突变。
在3612例NSCLC患者中,初步诊断为MIPC的患者有85例;81例为腺癌。在85例患者中,有60例进行了标本测序检测表皮生长因子受体突变;42例(70%)阳性。与673例无MIPC的IV期患者相比,MIPC患者的发病率更高表皮生长因子受体突变率(p=0.036);即使是男性吸烟者也会感到兴奋表皮生长因子受体突变率(91%)。85例MIPC患者的总生存期预后因素的多因素分析显示,腺癌,无肺外转移和有表皮生长因子受体突变与较长的总生存期相关。
早期诊断为MIPC的NSCLC患者有较高的腺癌发生率和表皮生长因子受体突变。EGFR酪氨酸激酶抑制可能是亚洲人中初诊断为MIPC的NSCLC患者的治疗选择。
肺癌是癌症相关死亡的主要原因,占美国所有癌症死亡人数的28%,全球每年死亡人数达100万[1,2].尽管成像技术已经进步,但70%的非小细胞肺癌(NSCLC)患者直到疾病的晚期才被诊断出来。他们的预后也很差[2,3.].
肺通常是非小细胞肺癌的转移器官,肺转移在胸片上表现为多种不同的模式,包括多发肺结节、胸腔积液和淋巴结肿大[4- - - - - -7].然而,肺癌合并粟粒性肺内癌(MIPC)是一种罕见的现象。粟粒样的定义是胸片上有弥漫性、微小和离散的≤5mm的肺小结节[7],表示血源播散[5,8].高分辨率计算机断层扫描(CT)可以更好、更准确地检测广泛分布的小结节[5,7].
初诊时表现为MIPC的NSCLC患者可迅速死亡,尽管一些病例报告描述了患者对表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗有良好反应[9,10].EGFR控制细胞增殖、分化和侵袭[11].研究发现,女性、非吸烟者、腺癌患者和东亚人对EGFR-TKI治疗反应增强[12,13],与增加有关表皮生长因子受体突变率[14- - - - - -19].19外显子L858R突变和缺失(del-19)占的90%表皮生长因子受体突变(15,17,18,20.].
laacket al。[21]报告了5例不吸烟的粟粒型肺腺癌del-19表皮生长因子受体突变。他们对EGFR-TKIs有良好的反应。但是,未描述伴有MIPC的NSCLC患者的临床特征和治疗结果。
本研究调查了临床特征,表皮生长因子受体突变率和治疗反应,并探讨初诊时表现为MIPC的NSCLC患者的预后因素。
材料与方法
病人
所有2004年6月至2008年12月诊断的非小细胞肺癌患者均通过台北市国立台湾大学医院(NTUH)医疗信息管理处癌症登记处确认。初步诊断为MIPC的患者纳入研究。本研究由NTUH研究伦理委员会批准(批准号9561705036)。
为作比较,表皮生长因子受体鉴定无MIPC的IV期肺癌患者的突变状态。接受筛查的患者表皮生长因子受体突变为:1)2004年7月以后接受细针活检(CT/超声引导)或胸腔穿刺术治疗胸腔积液的患者表皮生长因子受体突变测试在医院开始[22];或2)纳入回顾性NSCLC研究的患者[19,23- - - - - -25].
临床数据
记录符合条件的患者的临床特征。体重减轻定义为6个月内体重减少10%。我们将一生中吸烟少于100支的患者定义为非吸烟者,诊断后一年内吸烟的患者定义为目前吸烟者,其余患者定义为前吸烟者。疾病分期由肿瘤淋巴结转移系统决定[28].
肺癌组织学依据世界卫生组织标准分类[29].经病理或细胞学诊断证实为肺癌。
接受一线全身治疗的NSCLC患者的疗效评价
不同治疗方案的时间和顺序由医生在考虑患者的临床情况并与患者充分讨论后自行决定。NSCLC患者的一线全身治疗包括化疗和EGFR-TKI治疗。EGFR-TKIs吉非替尼250 mg·天−1(艾瑞莎®;阿斯利康,威尔明顿,DE,美国)或厄洛替尼150毫克·天−1(特罗凯®;OSI Pharmaceuticals, Inc., Melville, NY, USA)。未接受全身治疗的患者接受最好的支持性护理。为了评估治疗效果,每2-4周进行一次胸片检查,每2-3个月进行一次胸部CT检查。
所有图像均由肺科医生(S-G。Wu)和一位放射科医生(Y-C。昌),他们对表皮生长因子受体研究对象的突变分析结果及治疗过程。使用实体瘤指南(1.1版)中的疗效评价标准评估治疗效果[30.].对于可测量的病变,反应分为完全缓解、部分缓解、疾病稳定或疾病进展。对于仅有无法测量但可评估的粟粒病变的患者,治疗反应被分为非进展性疾病(NPD)或进展性疾病。NPD定义为没有新的病变,现有病变没有明确的进展[30.].从完全缓解、部分缓解、病情稳定或NPD的患者中计算疾病控制率。
总生存期定义为从NSCLC诊断之日到死亡之日。无进展生存期(PFS)定义为从开始一线全身治疗到出现疾病进展或死亡的第一个客观或临床体征的时间。
组织采购表皮生长因子受体突变分析
从肺肿瘤、转移部位和恶性积液细胞块获得肿瘤标本进行突变分析。在标本采集时,从患者处获得使用组织进行分子分析的书面知情同意。用苏木精和伊红染色显微镜检查组织切片是否充足;肿瘤含量为>80%的组织样本被选择用于研究。
PCR扩增和直接测序
肿瘤DNA使用QiAmp DNA Mini试剂盒(Qiagen, Valencia, CA, USA)从石蜡块中获得表皮生长因子受体上文所述的突变分析[19,23,25].的酪氨酸激酶结构域表皮生长因子受体编码序列(外显子18-21)经独立轮PCR扩增。PCR扩增物使用BigDye Terminator测序试剂盒(Applied Biosystems, Foster City, CA, USA)进行纯化和测序。
统计分析
所有分析使用统计软件SPSS 15.0 (SPSS公司,芝加哥,伊利诺伊州,美国)或SAS 9.1.3 (SAS研究所公司,卡里,北卡罗来纳州,美国)进行。双侧p值<0.05为有统计学意义。除期望频率小于5的分类变量采用费雪精确检验外,所有分类变量均采用卡方检验进行分析。两组间连续变量的均值比较采用非配对t检验。生存曲线采用Kaplan-Meier法绘制,组间比较采用log-rank检验。
对病人没有交代表皮生长因子受体测序结果,对“缺失”的预测因素进行logistic回归分析。表皮生长因子受体测序结果与用“nonmissing”来估计“missing”的概率。进一步的回归分析表皮生长因子受体变异作为协变量,用拟合的逻辑回归模型中“缺失”的“非缺失”预测概率的倒数进行加权,得到有效结果。采用加权Cox比例风险模型来确定非失踪MIPC患者总生存期的预测因素[31,32].
结果
初诊MIPC患者的临床特点
在2004年6月至2008年12月期间,共有3,612名非小细胞肺癌患者在癌症登记处登记。其中85例(2%)患者初诊时表现为MIPC。85例患者中41例(48%)为男性。年龄28.3 ~ 87.7岁,平均59.8岁。63人(74%)不吸烟。81例(95%)患者为腺癌,1例为鳞状细胞癌。其余3例患者为非小细胞肺癌。最常见的远处转移部位为骨(64%)和脑(37%)。其他临床特征表现在表1.
最常见的呼吸道和非呼吸道症状分别是咳嗽(66%)和体重减轻(45%)。表S1列出了其他症状。
表皮生长因子受体初诊时MIPC患者的突变状态
表皮生长因子受体在知情同意和足够的组织样本的情况下,对60例(71%)患者进行了突变检测。样本来自肺部肿瘤(n=23)、胸腔积液(n=28)、颈部淋巴结(n=4)、脑转移病灶(n=3)、骨转移病灶(n=1)和腹水(n=1)。患者人口统计数据显示在表1.
42例(70%)患者表皮生长因子受体突变。突变率与性别(p=0.052)或吸烟状况(p=0.194)无显著差异(表2).男性和吸烟者的突变率分别为84%(25人中有21人)和85%(13人中有11人)。最常见的突变是del-19(n=21, 35%)和L858R (n=12, 20%)(表S2)。
的特点和表皮生长因子受体初诊无MIPC的IV期肺癌患者的突变状态
从2001年4月到2009年11月,673例没有MIPC的IV期肺癌患者被确诊表皮生长因子受体突变筛查。与MIPC患者相比表皮生长因子受体两组间基因突变状况、性别、年龄、吸烟史或肿瘤类型均无差异。MIPC患者骨转移率(p=0.022)、脑转移率(p=0.021)、肝转移率(p=0.010)较高(表3).
初诊时表现为MIPC的患者有更高的发病率表皮生长因子受体突变率高于无MIPC患者(70%)与56%, p=0.036) (表4).L858R突变的存在在两组之间没有显著差异(20%与22%, p = 0.433)。然而,MIPC患者的死亡率明显较高del-19变异(35%与25%, p=0.024) (表4).
一线全身治疗后的有效率和PFS
在85例初诊断为MIPC的患者中,80例接受了全身治疗。3例患者诊断时在东方肿瘤合作组表现状态量表上为4级,其临床病情迅速恶化。2例患者拒绝全身治疗。治疗方法的选择取决于医生的判断。处理序列及其分布表皮生长因子受体患者突变情况见表S3。
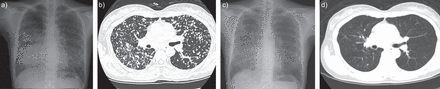
一线治疗为EGFR-TKI 43例,化疗37例。在EGFR-TKI组,33例接受吉非替尼治疗,10例接受厄洛替尼治疗。其中29例有部分反应(图1c和d), 1人患有NPD, 13人表现为病情进展;疾病控制率为70%。化疗组一线化疗方案为铂类双重化疗(n=29)、吉西他滨(n=4)、长春瑞滨(n=3)、紫杉醇(n=1)。无患者接受贝伐单抗联合化疗。本组11例患者部分缓解,4例患者NPD, 22例患者病情进展;疾病控制率为41%。两组之间的疾病控制率不同(p=0.009)。此外,EGFR-TKI组有较长的中位PFS (5.8与2.9个月,p=0.001) (图2).
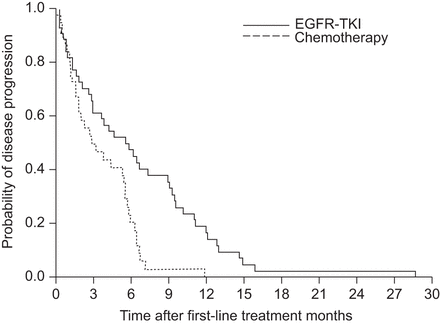
初诊时接受表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗的非小细胞肺癌患者(n=43)一线治疗和全身化疗(n=37)无进展生存(PFS) Kaplan-Meier曲线。PFS的差异有统计学意义(中位数为5.8与2.9个月,log-rank检验p=0.001)。
总体生存和预后因素
本文对85例MIPC患者的预后因素进行单因素分析表5.腺癌和非腺癌患者的总生存期差异有统计学意义(p=0.049)。无肺外转移的患者总生存期长于有肺外转移的患者(p=0.032) (图3).在患病期间接受EGFR-TKI治疗的患者总生存期明显长于未接受治疗的患者(p<0.001)。
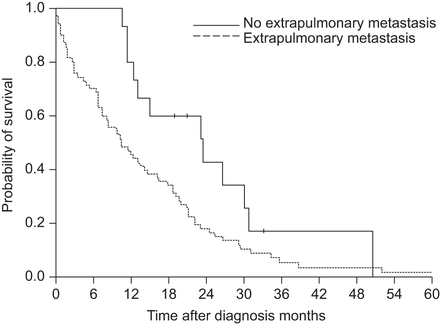
非小细胞肺癌合并粟粒性肺内癌患者初诊时总生存Kaplan-Meier曲线无肺外转移患者(n=15)和有肺外转移患者(n=70)的总生存期差异有统计学意义(中位数23.5)与10.4个月,log-rank检验p=0.032)。
在60个已知患有表皮生长因子受体序列中,55例接受EGFR-TKI治疗;其中有38人(69%)有表皮生长因子受体突变。在接受EGFR-TKIs治疗的患者中,35例作为一线治疗,21例作为二线或后续治疗。患者表皮生长因子受体突变的PFS比野生型的更长表皮生长因子受体(9.2与2.7个月,p<0.001)(图S1)。患者和非患者的总生存期的差异表皮生长因子受体突变有统计学意义(17.8与10.6月,p=0.008) (图4).
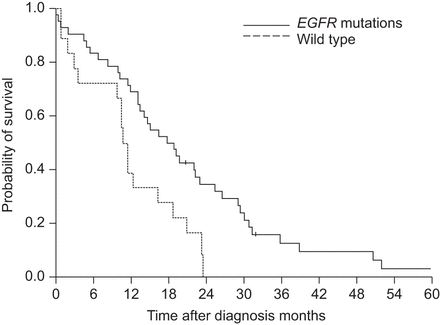
初诊断为粟粒性肺内癌的非小细胞肺癌患者一线治疗后总生存Kaplan-Meier曲线表皮生长因子受体(表皮生长因子受体)突变(n=42)和野生型表皮生长因子受体(n=18)差异有统计学意义(中位数为17.8与10.6个月,log-rank检验p=0.008)。
根据治疗顺序进行总生存期分析,一线EGFR-TKI治疗、二线化疗的患者总生存期最长(中位数20.9个月)。随后依次为一线和二线化疗、化疗合并EGFR-TKI、仅EGFR-TKI、仅化疗和仅支持治疗(p<0.001) (表5).
对25例未确诊的患者进行Logistic回归分析表皮生长因子受体测序结果显示,患者以男性为主(p=0.052),表现较差(p=0.035),一线治疗以化疗为主(p=0.006)。他们的表皮生长因子受体地位是根据这些因素来衡量的。然后使用Cox比例风险模型对总生存期进行多因素分析,以评估潜在的预后因素,包括性别、年龄、吸烟状况、肿瘤类型、肺外转移、表皮生长因子受体突变状态,EGFR-TKI的使用和治疗顺序。
较长的总生存期与腺癌相关(危险比(HR) 0.16, p=0.0448),无肺外转移(HR 0.45, p=0.0514)表皮生长因子受体突变(HR 0.19, p=0.0001)。对总生存期有显著负面影响的因素是最佳支持治疗(HR 106.19, p<0.0001)和使用一线EGFR-TKI治疗作为唯一治疗(HR 4.46, p=0.0003) (表5).实测拟合优度值和拟合优度检验结果表明,Cox比例风险模型对观测到的二进制数据拟合良好。
讨论
非小细胞肺癌患者表皮生长因子受体已知突变对EGFR-TKI治疗有更好的反应[14,16].本研究显示,初诊时表现为MIPC的NSCLC患者具有更高的预后表皮生长因子受体突变率高于无MIPC的。我们纳入了更多的患者,而不是Laacket al。[21];因此,我们能够呈现完整的临床特征,转移部位和表皮生长因子受体该亚组患者的突变类型。目前已知的临床特征与表皮生长因子受体包括女性、腺癌、从不吸烟和亚洲人[17,33].我们发现了快感表皮生长因子受体在初次诊断时表现出MIPC特殊图像模式的患者中的突变率为医生选择可能对EGFR-TKIs有更好反应的患者提供了额外的特征。
Iressa泛亚研究(IPASS)对东亚非吸烟者和轻度吸烟者肺腺癌患者进行了研究,结果显示,与卡铂-紫杉醇治疗相比,初始吉非替尼治疗具有更好的缓解率和更长的PFS [16].的表皮生长因子受体IPASS的突变率为60%,低于本研究的70%。此外,与一般有关高的概念相反表皮生长因子受体突变亚群[12,13],我们还发现伴有MIPC的NSCLC患者亚组(男性和吸烟者)的发病率较高表皮生长因子受体变异率。高表皮生长因子受体在EGFR-TKI作为一线治疗的患者中,突变率与更好的治疗反应和更长的PFS相一致。
初诊时的MIPC是一种侵袭性更强的疾病状态。大多数早期诊断为MIPC的NSCLC患者通常表现不佳,病程很快就会死亡[34],而通常不建议进行化疗[35].目前的研究显示高表皮生长因子受体该亚组NSCLC患者的突变率。此外,最佳支持治疗的总生存期非常短。EGFR-TKIs可能是伴有MIPC的NSCLC患者的治疗选择,特别是对于性能状态较差的患者。
的突变率del-19MIPC患者的发病率高于非MIPC患者(35%与25%)。高del-19突变率较高表皮生长因子受体在初诊时,MIPC患者的突变率高于非MIPC患者。需要进一步的研究来调查两者之间的关系del-19非小细胞肺癌的突变与粟粒性肺转移。
肿瘤细胞转移通过血源途径可导致弥漫性粟粒播散[36].Umekiet al。[34]表明肺癌的MIPC与骨转移有关,因为他的五位患者都有骨转移。他们认为骨转移来自肺部通过而MIPC源于继发性骨转移灶的多发性肿瘤栓子[34].Kolsuzet al。[37]描述了一例伴有MIPC和骨髓累及的肺腺癌患者,这被认为是由肿瘤细胞扩散引起的通过血源途径。本研究还显示,初诊时MIPC的NSCLC患者中有63.5%发生同步骨转移(表1).与初诊断时未出现MIPC的IV期NSCLC患者相比,MIPC患者的肝脏、骨骼和大脑转移率更高,所有部位都是血源性扩散。这一结果支持了血源性扩散在非小细胞肺癌的MIPC和骨转移中都起着重要作用。
本研究显示,初诊时MIPC的NSCLC患者大多为腺癌。既往报道的MIPC患者均为腺癌[21,34].可能的病理生理学是,粟粒的表现是血源性扩散的表现,这与癌症的血管生成有关[5].与肺鳞状细胞癌相比,肺腺癌具有更大的肿瘤血管生成潜力,这可能有助于高血源性扩散[38].此外,肺腺癌可发生早期转移通过血源性传播[5,8,39].因此,在初步诊断时,腺癌是MIPC的主要组织病理学类型。
尽管有多重肺转移,患者仍可能对EGFR-TKIs有反应。C挂et al。[10]报道了吉非替尼成功治疗2例多灶性细支气管肺泡细胞癌患者。Gotoet al。[40]表明,有6个以上转移性肺结节(特别是弥漫性粟粒转移)的NSCLC患者对吉非替尼的阳性反应显著相关。然而,表皮生长因子受体突变状态是决定EGFR-TKI治疗反应的最重要因素,当时尚不清楚。2006年,K大林et al。[9)联系表皮生长因子受体2例弥漫小结节性肺转移患者吉非替尼反应良好的突变。在我们的研究中,我们还表明,出现MIPC的患者对EGFR-TKIs反应良好,这可能与高剂量的EGFR-TKIs有关表皮生长因子受体我们病人的突变率。
本研究存在一定的局限性。首先,患者数量很少,因为MIPC是肺癌诊断时的罕见表现。其次,这是一项回顾性观察性研究,不能完全排除固有偏见。第三,在非小细胞肺癌的粟粒性肺结节中,区分肺内转移与独立多发原发肿瘤是很困难的。不同结节的综合组织学评估和分子分析是有力的工具[41],但由于病灶太小,很难从多个小结节中获得标本。最后,本研究中所有入组患者均为亚洲人,已知其发病率较高表皮生长因子受体变异率。结果可能并不适用于所有MIPC患者。
总之,初诊时表现为MIPC的NSCLC患者具有较高的腺癌和腺癌发生率表皮生长因子受体突变率甚至在男性和吸烟者之间。MIPC模式有助于识别患有高可能性的患者表皮生长因子受体突变。在亚洲人中,EGFR-TKI可能是初诊时伴有MIPC的NSCLC患者的首选治疗方法,无论性别或吸烟状况如何。
致谢
作者在此感谢台北市国立台湾大学附属医院医学研究部的技术支持。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
本研究由98-2314-B-002-117-MY3和98-2628-B-002-087-MY3(台湾台北国家科学委员会)、DOH100-TD-PB-111-TM001(台北行政院卫生部)和100-M1722(台北市台湾大学医院)资助。
权益声明书
没有宣布。
- 收到了2012年1月11日。
- 接受2012年3月27日。
- ©2013人队