摘要
目前尚不清楚维生素D水平是否对慢性阻塞性肺疾病(COPD)的肌肉功能障碍有显著影响。
104例慢性阻塞性肺病患者(平均±SD.25-羟维生素D (25(OH)D), 1,25-二羟维生素D (1,25(OH))2D)和甲状旁腺激素(PTH)水平被测量,并与股四头肌力量和耐力相关。在26名患者和13名对照组中,进行了四头肌活检,并测定了肌源性调节因子(mrf)和纤维特异性肌球蛋白重链(MHC)的mRNA表达。
COPD患者比对照组更虚弱,体力活动更少。两组25(OH)D水平相似(48.5±25.5 nmol·L)-1慢性阻塞性肺病相对55.4±28.3nmol·L-1对照,P = 0.07),但患者的PTH水平显着较高(5.2±2.3 pmol·mL-1相对4.4±2.0 pmol·L-1,p = 0.01)。1,25(OH)D与对照中的强度显着相关,但不具有COPD患者,而不是在COPD(n = 35)或对照(n = 35)受试者中使用重复磁刺激评估的Quaddriceps耐久性。在对照组中,但不是COPD患者,肌肉活组织检查分析显示出25(OH)D和MHCIIA表达之间的负相关(R.2=0.5, p=0.01), mrf4与MHCIIa表达呈正相关(r2=0.5, p=0.009)、myf5和MHCI表达(r2= 0.72,p = 0.004)。
与健康对照组相比,COPD患者的肌肉力量与维生素D水平无关,这可能代表维生素D抵抗。
骨骼肌无力是慢性阻塞性肺疾病(COPD)的重要并发症。大约25%的COPD患者出现明显的虚弱,并与死亡率增加相关[1那2虚弱主要是由于活动减少,但其他因素,包括全身炎症、氧化应激和遗传易感性也有牵连[3.].
许多研究发现了25-羟基维生素D(25(OH)D)之间的关联,以及健康老年人的肌肉力量的措施[4.-6.,补充维生素D可降低跌倒的风险[7.那8.].已显示维生素D受体(VDR)中的多态性以影响正常的肌肉力量[9.那10.]及慢性阻塞性肺病[11.]人口。患有COPD的患者已显示出不充分的维生素D [12.]及减少户外活动时间[13.,两者都会增加维生素D缺乏的风险。janssens.等等。[14.]表明COPD患者的25(OH)D水平低于健康吸烟者,25(OH)D水平随着疾病的严重程度而降低。因此,维生素D可能在COPD中看到的肌肉弱势发展中发挥作用。
VDR敲除小鼠已被证明具有小而不规则的肌纤维,肌源性调节因子(mrf) myf5和肌原蛋白(myogenin)的持久表达[15.].在同一研究中,体外添加1,25-二羟基维生素D (1,25(OH))2D)向成肌细胞显示这些mrf的下调。
当前研究的目的是确定维生素D水平低是否与COPD患者骨骼肌功能受损有关。COPD患者的显著相关性将增加考虑补充策略的可能性。肌肉功能测量采用意志和非意志技术。在一组患者中,研究了维生素D在肌肉中作用的可能的分子机制,重点研究了维生素D与mrf表达和肌肉特异性肌球蛋白重链(MHC)表达之间的相互作用。
对象和方法
研究了广告招募的稳定COPD门诊和控制主体。如果具有显着的合并症,包括不稳定的心血管疾病,恶性肿瘤或限制肌肉骨骼疾病,则被排除在外。所有主题提供了知情的书面同意,该研究由英国伦敦皇家Brompton医院的伦理委员会批准。
获得了前一年中口腔皮质类固醇的加剧率和平均日剂量(添加)的系统史。维生素D摄入量被我们自己开发的标准化召回问卷评估,基于已知的维生素D [16.].耶鲁体育活动调查(YPAS) [17.] St George的呼吸问卷完成。使用COPD患者的疾病特异性的回归方程用Bodystat 1500生物电阻抗装置(Bodystat,Douglas,Mane)测量无脂肪块[18.以及设备内部的控制算法。使用CompactLab系统(Jaeger, Würzburg,德国)对COPD患者进行肺活量测定、容积描记肺容积和气体转移。对照组仅测定肺活量。
104例COPD患者和100例正常人纳入研究。其中,每组35人测量了他们的股四头肌耐力,并对26名患者和13名对照组进行了肌肉活检。有关方法的进一步细节载于补充材料中。
肌肉力量和耐力
如前所述测量了股四头肌最大自发性收缩(QMVC)、握力和嗅吸鼻吸气压力(SNIP),以及对超最大磁股神经刺激的无增强性股四头肌肌力(TwQ) [11.那19.].
使用重复的磁刺激用Magstim Rapid 2刺激器(Designworks,Windsor,UK)和放置在QuadRiceps的主体上的柔性垫圈来测量QuadriCeps耐久性。20.].刺激以30 Hz的频率递送,占空比为0.4(2秒,3秒,3秒)的60列刺激。最初调节刺激剂强度,以产生20%的仰卧QMVC。连续列车产生的衰减用作耐力指标。在COPD和对照组之间比较耐久性曲线,以及基团内的维生素D-Faird and -Undoficity受试者。维生素D不足定义为25(OH)D水平<75nmol·L-1。
血清测量
血清被储存和钙化二钙(25(OH)D),钙质(1,25(OH)的分批分析2d),在研究完成后进行高灵敏度C反应蛋白(HSCRP),白细胞介素(IL)-6,电解质和白蛋白。
肌肉活检
如前所述,肌肉活检样本取自优势腿股外侧肌[20.].使用家务基因人RPLPO用于参考,对MHC1,MHCIIA,MHCIIX,MRF Myogenin,MRF4和MyF5进行实时定量PCR分析。
统计分析
描述性统计数据报告为平均值±SD.或中位数(范围)。用于比较参数数据和非参数数据的Mann-Whitney测试的方法。Spearman等级测试用于相关性。逐步逻辑回归用于建立影响肌肉力量的因素。疾病严重程度在预测的%方面被考虑;气流梗阻(1 s强迫呼气量,一氧化碳肺的转移系数(T.L,有限公司)和气体捕获(残留体积(RV)/总肺容量(TLC))。使用鲁棒差异的回归用于比较COPD和对照组之间的耐久性曲线,并在组内比较维生素D-足够的受试者。p值<0.05被认为是显着的。使用SPSS为Windows版本16.0(SPSS Inc.,Chicago,IL,USA)和Stata发布10.1(Statacorp,TX,USA)的SPSS进行分析。
结果
这些组的年龄和性别匹配良好,但COPD患者较弱,报告的体力活动水平较低(表1).15名患者患有全球慢性阻塞性肺疾病(GOLD) 1期疾病,18名患者患有GOLD 2期疾病,39名患者患有GOLD 3期疾病,32名患者患有GOLD 4期疾病。强的松的中位ADD为2 mg,主要用于急性发作的短时间突发治疗。7例患者服用常规低剂量(<10 mg·d)-1)口服强的松。27%的患者报告在前一年无病情加重,分别有22%、14%、11%和26%的患者有1、2、3或>4病情加重。
维生素D水平在组之间没有显着差异,但COPD组中甲状旁腺激素(PTH)水平较高,25(OH)D和1,25(OH)2D在COPD中显着降低了25(OH)D和1,25(OH)的比例显着降低团体 (表2.).在线补充材料中介绍了维生素D水平和肺功能之间的关系。
肌肉力量
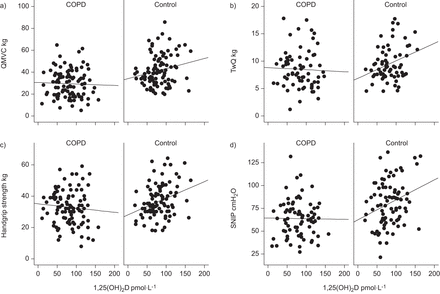
在COPD患者中,25(OH)D,1,25(OH)2D和甲状旁腺激素水平与任何肌肉力量测量无关(图1),或独立或逐步分析,包括潜在的混杂因素。QMVC与性别独立相关,T.L,有限公司(%预测)和白蛋白。手柄强度与性和年龄有关。Snip与性别和RV / TLC相关联(表3).
1,25-二羟基维生素D (1,25(OH))的相关性2D)慢性阻塞性肺疾病(COPD)和对照组肌肉力量的测量。a)股四头肌最大自愿收缩(QMVC): COPD r= -0.04, p=0.73;控制r = 0.2, p = 0.05。b)股四头肌肌力(TwQ): COPD r= -0.04, p=0.76;控制r = 0.30, p = 0.01。c)握力:COPD r= -0.08, p=0.44;控制r = 0.31, p = 0.003。d)嗅吸气压(SNIP): COPD r= -0.01, p=0.91;控制r = 0.28, p = 0.01。
在对照组中,25(OH)D与TWQ显着相关(r = 0.29,p = 0.02),剪切(r = 0.22,p = 0.04)和手柄强度(r = 0.20,p = 0.05),但不是QMVC(r = 0.18,p = 0.07)。1,25(哦)2D与QMVC (r=0.20, p=0.05)、TwQ (r=0.30, p=0.01)、SNIP (r=0.28, p=0.01)和手柄(r=0.31, p=0.003) (图1).调整混淆因子后,25(OH)D与任何肌肉强度的衡量标准没有独立相关。但是,1,25(哦)2D与握力和SNIP独立相关(表4.).COPD患者(N = 35)与对照(n = 35)相比,Quaddriceps耐久性显着降低(Z = 6.7%,95%CI 2.1%-11.3%; p = 0.004)(图2)但在任何一个研究组中,维生素D形不足和 - 易患受试者之间没有差异。
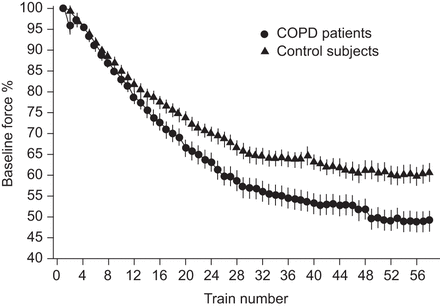
慢性阻塞性肺疾病(COPD)患者和对照组的股四头肌耐力在对重复磁刺激的反应中,COPD患者的力下降得比对照组更快。Z=6.7 (95% ci 2.1-11.3%);p = 0.004。误差条表示扫描电镜。
影响25(OH)D级别的因素
在涉及所有研究对象的逐步多元回归模型中,种族、年龄和每日维生素D摄入量与25(OH)D水平独立相关(r2= 0.11)。模型中未保留的其他因素有研究组、包年数、性别、体重指数、测量时间、白蛋白、IL-6或hsCRP。没有发现炎症介质与任何强度或身体成分之间的联系(图S1)。
54例(52%)COPD患者和55例(55%)对照组服用某种形式的维生素D补充剂。在服用补充剂的COPD受试者中,服用维生素D3补充剂的比例较高(COPD组为46%)相对对照组为18%)。另一项对不服用补充剂的受试者的单独分析显示,COPD患者的膳食维生素D摄入量明显低于对照组(982±611)国际单位在慢性阻塞性肺病相对1287±658国际单位25(OH)D水平显著降低(COPD 41.5±24.6 nmol·L-1相对控制54.8±32.9nmol·L-1,p = 0.03)。在或未服用维生素D补充剂的患者之间没有强度差异。
根据一年中测量的时间分析25(OH)D水平显示COPD和对照组中的不同模式。虽然在11月和2月之间测量的受试者的水平在这两组中相似,但在3月和10月之间测量的受试者的水平在对照组中均明显高,但不在患者中(图3).
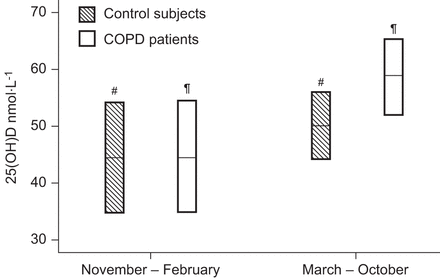
根据一年中测量的慢性阻塞性肺疾病(COPD)和对照组的25-羟基乙多蛋白D(25(OH)D)水平的变化。数据呈现为95%CI。#:均值差5.6,p=0.31;¶:平均差14.2,p=0.03。水平线表示平均值。
肌肉活组织检查分析
对26例COPD患者和13例对照组进行了四头肌mRNA分析。COPD组MHC1 mRNA表达低于对照组(4.19±0.41)相对MHCIIa (COPD 2.98±0.67,对照组2.97±0.43,p=1.00)和MHCIIx (COPD 3.82±0.59,对照组3.78±0.52,p=0.82)表达相似。在COPD组和对照组之间,mrf的mRNA表达没有差异。
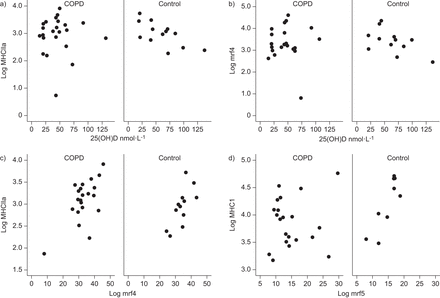
在对照组中,MHCIIa与25(OH)D和1,25(OH)都相关。2D(R.2= 0.47,p = 0.01和r2= 0.35, p = 0.03;而COPD患者MHC表达与维生素D无相关性(图4).在对照组中,25(OH)D与mrf之间存在相关性的趋势如下2=0.38, p=0.08)2=0.32, p=0.06)和myogenin (r .2=0.30, p=0.07), mrf和1,25(OH) mRNA表达2D没有相关。MRFS的mRNA表达和25(OH)D或1,25(OH)之间没有关联2d在copd中。
25-羟基vitamind(25(OH)d),肌源性调节因子(MRF)表达和纤维型表达和纤维型表达在慢性阻塞性肺疾病(COPD)和控制受试者之间:a)25(OH)D和myosin重链(MHC)IIA表达(COPD R.2= 0.00,p = 1.0;控制r2= 0.47,p = 0.01);b)25(OH)D和MRF4表达(COPD r2= 0.00, p = 0.88;控制r2= 0.32,p = 0.06);c)MRF4表达和MHCIIa表达(COPD R.2= 0.00,p = 1.0;控制r2= 0.52, p = 0.009);d) myf5和MHCI表达(COPD r2= 0.01,p = 0.68;控制r2= 0.72,p = 0.004)。
在对照对象中,MRF和纤维型mRNA表达之间发现了许多关联:MRF4与MHCIIA最强烈相关(R.2= 0.52,p = 0.009),而MYF5与MHCI最强烈相关(R.2= 0.72,p = 0.004)。在COPD组中,MRF4或MYF5和任何光纤类型之间没有发现任何关联。在进行活组织检查的亚组中,如在主要研究组中,确认了对照对象的25(OH)D和肌肉强度之间的关联,但不进行COPD受试者(COPD R2=0.07, p=0.22,对照组r2=0.40, p=0.02,用于握力)。在对照组中,MHCIIa表达(而不是MHC1或MHCIIx表达)与股四头肌强度相关,但与COPD受试者(COPD r2= 0.03,p = 0.45和控制r2= 0.36,p = 0.03)。
讨论
本研究的主要发现是,首先,25(OH) D和1,25(OH) D之间没有关系。2D和COPD受试者肌肉力量的测量,尽管在对照组中,1,25(OH)2D与肌肉力量测量独立相关。其次,在两组中,股四头肌耐力与维生素D水平无关。第三,COPD患者25(OH)D/PTH比值明显降低。此外,在肌肉活检亚组中,有两个重要的发现以前没有被证实。在对照组(而非COPD患者)中,25(OH)D与MHCIIa mRNA表达呈负相关,而mrf4和MHCIIa表达与myf5和MHC1表达呈强烈正相关。
研究结果的意义
许多研究支持维生素D和骨骼肌功能之间的联系[4.-7.那9.-11.]但是有关所涉及的机制的数据相对较少。分析来自骨癌的少数活组织检查,已表现出II型肌肉纤维的萎缩,脂肪,纤维化和糖原颗粒渗透[21.].两项研究既是老年女性,都研究了肌肉纤维形态与维生素D补充的变化。S.orensen.等等。[22.]在3-6个月的钙和维生素D类似物1 α-羟基胆钙化醇治疗后,IIa型纤维直径和百分比增加。S.ato.等等。[23.]给了1,000国际单位每天维生素D2ⅱ型纤维直径和百分比均有增加。与野生型对照相比,VDR敲除小鼠所有纤维类型的大小减少了20%,并且显示参与肌细胞生长和分化的mrf异常[15.].1,25(OH)的其他演示行为2骨骼肌中的d包括钙转运的上调[24.和磷脂代谢的调节[25.].维生素D的非基因组或快速效应也有文献记载,包括调节细胞内钙[26.]和激活丝裂原活化蛋白激酶C途径[27.].
维生素D尤其出现在II型纤维中,COPD患者中的Quadriceps表现出IIA型纤维型比例的增加和其横截面积的减少。因此,COPD人口中的维生素D和肌肉力量之间完全缺乏关联是出乎意料的。COPD患者的Quaddriceps耐久性显着降低,但与受对照中维生素D水平影响的强度相比,维生素D在任一组中观察到的耐久性没有影响。这可能是因为维生素D对II型纤维的主要效果,尽管VDR敲除小鼠的研究表明[15.].
只有一项横向研究[28.]研究了接受肺移植的晚期肺病患者的25(OH)D水平和握力,其中有50%患有慢性阻塞性肺病。这项研究没有发现这两个参数之间的关联,但在COPD肌肉中,无力主要发生在运动肌肉中[28.].
对维生素D在COPD中缺乏作用的一种解释是,它被其他过程掩盖了,或者简单地说,与肌肉力量的其他表型调节剂相比,作用的幅度很小。然而,即使我们调整了被认为是导致肌肉萎缩的因素,包括体育活动水平、疾病严重程度和恶化率,仍然没有关系。
另一种假设是,COPD患者对维生素D的作用存在耐药性。尽管25(OH)和1,25(OH)的水平之间没有显著差异2D组中,COPD患者甲状旁腺激素显著增高,25(OH)D/甲状旁腺激素比值显著降低。甲状旁腺激素通过对肾脏、骨骼和维生素D的作用,维持血清钙在正常范围内,并受到1,25(OH)的严格调控。2D.甲状旁腺激素水平随年龄增长而增加。这被认为反映了钙吸收的减少,并且已经假设绝经后的女性在肠道中对1,25(OH)D有抵抗力,尽管这还没有被证实[29.].COPD组的甲状甲状腺素升高表明,尽管25(OH)D水平相似,但肠道对维生素D的抵抗力可能也会增加,钙的吸收也会减少。这一过程可能导致骨吸收增加,并可能解释为什么COPD患者有较高的骨质疏松风险。维生素D抗性的产生有很多潜在的机制。1α-羟化酶(CYP27B1)将25(OH)D转化为1,25(OH)2D,与靶器官中的VDRs结合。然后VDR与视黄酸受体形成异源二聚体,然后才能与DNA结合并产生反应通过基因转录。VDR也存在于细胞质中,并且已被证明具有Nongenomic效应。CYP27B1的活性降低,或减少表达或VDR的不恰当活动可能导致阻力。1,25(哦)的水平2D两组都相似,这表明任何抵抗机制都会涉及VDR及其相互作用。COPD骨骼肌对维生素D途径的潜在影响包括炎症,氧化应激,减少毛细血管性,肌肉缺氧和物理不活跃。值得注意的是,在我们的研究中,我们发现全身炎症和维生素D水平或全身炎症与任何肌肉功能的衡量标准之间没有关系。
慢性阻塞性肺病被认为是一种衰老疾病[30.]并且证据积累了支持这一点,并在COPD患者的肺部演示了衰老标志物[31.[COPD中端粒长度与肺功能之间的阳性关联的发现[32.].维生素D还控制许多与衰老有关的基因[33.[较高的维生素D水平,即使在年龄和其他混淆因素调整后,也与较长的端粒长度相关联34.].肌肉中VDR浓度[35.]和十二指肠[36.[已被证明随着年龄的增长而降低,可能是COPD患者体内浓度的降低导致了对1,25(OH)的相对抗性。2D,这可能是加速在COPD中加速老化的链接。在我们的肌肉样品中,我们无法衡量VDR蛋白水平,因此无法进一步探索这一假设。
两组之间的PTH水平中看到的差异的另一个潜在解释可能是缺镁的存在,因为这会导致低维生素D水平的钝化PTH反应[37.]随后减少骨质营业额。虽然镁主要是细胞内离子,但血清浓度在基团之间没有差异,使得这不太可能是一个重要因素。
肌肉活检亚研究的结果支持维生素D抵抗的存在,因为在正常受试者的分子水平上看到的关联在COPD受试者中不存在。mrf已被证明受1,25(OH)的影响2D.体外,并且在VDR敲除小鼠中持续上调(这在在线补充材料中更完全参考)[15.].MRFS在胚胎发生和细胞培养模型中得到了广泛的研究,它们在骨骼肌发育中发挥了重要作用。MyoD和myf5将干细胞转化为肌源性谱系,而myogenin和mrf4则刺激向多核肌纤维的转变。然而,人们对其在成人肌肉中的作用知之甚少。Mrf4的表达会持续到成年期,而其他MRFS在出生后不久就会减少,随后随着年龄增长和疾病状态而增加。在年轻人和老年人中,MyoD和myogenin mRNA都在抗阻力运动训练后增加,而myf5 mRNA仅在年轻人中增加。
虽然它们在成年肌肉中显然具有持续的作用,但目前的结果表明MRF4和MYF5可能是肌纤维类型的重要调节因素。成年大鼠的一项研究已经证明了高水平的肌肉中的肌肉素mRNA,其主要由具有高水平的MyOD mRNA中的慢纤维组成,这些肌肉在主要由快速纤维组成的那些中。然而,MRF4 mRNA的水平在肌肉之间没有区别,而MYF5 mRNA几乎无法察觉。我们的研究结果得到了MRF4的推动者/报告基因构建的另一个研究支持,该研究已经示出了特异性在快肌纤维中促进MRF4的区域。
研究的局限性
这是一种大的横截面研究,具有良好表型COPD患者和对照组,符合年龄和性别的对照组。然而,与任何横截面研究一样,只能寻找重要的关联,我们无法建立原因和效果关系。人口主要是在英国的白种人生活,结果必须谨慎应用于其他人口。该研究的一个限制可能是使用YPAS作为身体活动的量度而不是直接测量。这是一个召回问卷,因此具有与之相关的固有问题。然而,它是比较人群的有用工具,它已在老年人中验证,已经显示出与最大氧吸收的体力激活分数,并在本研究中的患者和对照之间进行相关[17.].其局限性在于,活检只在一定比例的受试者中进行;然而,亚组中维生素D水平和强度之间的关系与整个人群相匹配,表明它们具有代表性。
结论
尽管水平范围相似,但在正常受试者中观察到的维生素D和肌肉力量之间的关系不存在。我们还展示了在正常科目中某些肌源性调节因子和纤维型表达之间的关联,但不带COPD患者。这些结果令人惊讶,提高了COPD中维生素D抗性的可能性。需要进一步调查VDR表达和维生素D在COPD患者骨骼肌中维生素D后转录作用的进一步分子研究是进一步探索这一假设所必需的。正在进行几项维生素D补充的前瞻性试验,以确定其对COPD中加剧的影响,但可能是对COPD患者的骨骼肌损伤影响较高剂量的补充或甚至无力的维生素D类似物。
致谢
我们要感谢患者和健康的主题,他们参加了这项研究的时间和合作。我们承认皇家Brompton医院和D. Hosking(David Evans Research Center,诺丁汉大学医院,英国诺丁汉,英国)的龙职员实验室工作人员的协助,以便他对稿件有用的评论。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
这项研究由莫尔顿基金会资助,并由英国皇家布朗普顿和哈里菲尔德国民保健服务基金会信托的NIHR呼吸疾病生物医学研究部门和伦敦帝国理工学院(伦敦,英国)支持,后者为M.I. Polkey的工资提供了部分资金。
感兴趣的语句
没有宣布。
- 已收到2012年3月12日。
- 公认2012年4月22日。
- ©2013人队