摘要
我们测试了乙酰唑胺对慢性缺氧时血液力学特性和肺血管阻力(PVR)的影响。
6组大鼠分别给予或不给予乙酰唑胺治疗(疗效:在缺氧暴露10天后治疗;预防:缺氧暴露前40 mg·kg治疗−1·一天−1)和暴露或未暴露于3周的缺氧(高度> 5,500米)。然后,它们用于评估乙酰唑胺对肺动脉压,心输出,血液体积,血液神经和血管生物学参数的作用。
慢性缺氧增加红细胞压积、血粘度和PVR,并降低心输出量。乙酰唑胺治疗缺氧大鼠可降低红细胞压积(治愈降低10%,预防降低11%)、PVR(治愈降低36%,预防降低49%)和右心室肥厚(预防降低-20%),心输出量增加(治愈增加60%,预防增加115%)。乙酰唑胺治疗后血粘度显著降低(-16%),且与PVR相关(r=0.87, p<0.05),提示血粘度可影响肺血流动力学。治疗后肺血管障碍下降(-27%,-45%)表明乙酰唑胺可减少慢性缺氧下肺血管重塑。
乙酰唑胺对红细胞生成、肺循环、血液流变学和心输出量的影响是多因素的,可作为慢性高山病的中肯治疗方法。
人类和大鼠长期暴露于缺氧可导致红细胞增多症和肺动脉高压[1- - - - - -4].红细胞增多症(血红蛋白(Hb)浓度>21 g·dL−1或红细胞压积(Hct)浓度>63%)是蒙氏病或慢性山地病的特征[5].肺动脉高压常与慢性高原病有关[6].这种疾病影响住在海拔3200米以上的5-15%的人口。
最近的研究表明乙酰唑胺,一种碳酸酐酶的抑制剂,能够降低蒙格病的Hct和肺血管阻力(PVR) [3.,4].然而,乙酰唑胺作用于PVR的机制尚不完全清楚。有研究表明,乙酰唑胺治疗3个月后PVR的降低是由于Hct降低后血液粘度的降低[4].根据Poiseuille定律和Hoffman[7]、肺血流动力学和PVR可能受血液黏度的广泛影响。然而,目前还没有关于乙酰唑胺对血液黏度的影响的数据。慢性缺氧时PVR的变化可能与多种机制有关,如肺血管重构[2,8]、血液流变学改变[9,10,缺氧血管收缩[11]或由于Hct升高,红细胞清除更多一氧化氮[12].在各种模型(小鼠、大鼠和豚鼠)中,红细胞增多似乎通过增加血液粘度与肺动脉高压有关[13].血液粘度不仅取决于Hct,还取决于红细胞变形和聚集的能力[14].后者的血液流变学因素可在相当程度上调节肺水平的血流阻力[14- - - - - -16],并可受慢性低氧暴露的影响[10,17].
本研究的目的是提高对慢性缺氧条件下乙酰唑胺治疗后PVR降低的机制的理解,特别强调血液流变学参数(血液粘度、红细胞的聚集-分解和变形性)和肺血管障碍,这与PVR肺血管几何的贡献相对应。我们假设乙酰唑胺可以通过降低低氧肺血管收缩和血液粘度来降低PVR。
方法
动物
所有程序均符合欧洲议会指令2010/63/EU,并获得法国“Ministère del’agriculture”指南(授权号A-93-008-01)的批准。
选取8 ~ 10周龄雄性Wistar大鼠(Janvier, Le Genest Saint-Isle, France),随机分为6组:1)常氧对照组(n=30);2)常氧治疗(n=24);3)常氧预防(n=32);4)缺氧控制(n=28);5)缺氧治疗组28例,6)缺氧预防组32例。两组预防组均在进入低压舱前2天服用乙酰唑胺,而治疗组在缺氧暴露10天后服用乙酰唑胺,此前已有研究表明,低氧暴露可显著增加肺动脉压(PAP) [1].慢性缺氧暴露的大鼠被安置在一个连接气泵的缺氧室21天,空气以380mmhg(海拔5500米)的压力循环。常氧组保持在760毫米汞柱的低压舱外。乙酰唑胺40 mg·kg−1·一天−1;赛诺菲-安万特,巴黎,法国)的饮用水,并记录每天通过测量每个笼子在低压舱每次打开(每天30分钟)的乙酰唑胺饮用量。
血液动力学
缺氧暴露结束时,每组8只大鼠用木酰亚胺-氯胺酮麻醉(腹腔注射木酰亚胺(Rompum;拜耳,伍珀塔尔,德国)10毫克·公斤−1氯胺酮(Clorketam®1000;Vetoquinol, Lure,法国)50 mg·kg−1).在外科实验中,监测麻醉深度的方法是通过失去蹬脱反射,然后监测心跳频率(fC)和平均全身动脉血压的变化。如果需要,静脉内给予额外的麻醉剂量给动物。所有动态程序和生物测量均在45分钟内完成。
在常氧条件下进行血流动力学测量,以评估乙酰唑胺和低氧暴露的慢性效应abinovitchet al。[2].fC,用导管测量平均全身动脉血压和PAP。用热稀释法获得心输出量。
PVR和全身血管阻力(SVR)是用平均动脉血压(肺和全身)除以心输出量来估计的。在本方案中,由于文献中可用的技术不易应用,未对大鼠进行左右耳压测量[18患心力衰竭的风险很高。因此,PVR和SVR的计算没有考虑左右耳压。
从股动脉取血300 μ l,测定动脉血氧饱和度(P啊,一个2)及动脉血二氧化碳张力(P,有限公司2).实验结束时,致死剂量为硫openthal钠(pentothal (CEVA Santé Animale, Libourne, France) 100 mg·kg−1)被注射,心脏被摘除。分离右心室(RV)和包含间隔的左心室(LV+S),称重,液氮冷冻。计算富尔顿比值(RV/(LV+S))来反映右心室肥厚。
血容量测量
每组10只大鼠,分别在缺氧和乙酰唑胺条件下进行血容量变化对比实验。用埃文斯蓝(Sigma, Gillingham, UK)染色法测定血浆体积。简单地,在100 μL生理盐水中注射100 μg染料通过颈静脉导管。导管已灌满生理盐水,染料给药后用200 μL生理盐水冲洗。0、3、5和7分钟后,从动脉导管中取出生理盐水,并将血液样本采集到肝素注射器中。血液被离心以获得血浆样本。在610nm分光光度法测定血浆样品中的Evans ' blue浓度(分光光度计UV-VIS RS 0223;Jenway 6405;Keison Products, Chelmsford, UK),并与已知数量的Evans蓝色染料和供体大鼠血浆样本设计的标准曲线进行比较。考虑到Evans ' blue从血浆腔室逐渐泄漏,我们使用了一个简单的双腔室模型来计算稳态Evans ' blue浓度([EB])。0).血浆体积计算为血浆体积=I海尔哥哥/[EB]0,在那里我海尔哥哥为注射埃文斯蓝的量(100 μg)。然后计算血容量和红细胞体积(RCV):血容量=(血浆volume×100)/(100-Hct), RCV=血容量-血浆体积。
血液流变学、血液学和血管障碍测量
在EDTA管中采集血液后3小时内测量血液流变学参数,并符合最近关于每个亚组12只大鼠血液流变学测量的国际指南[19].剪切速率为36.69 s时的血液粘度−1在37°C时,计算Hct/血液粘度比(定义为血液氧输送效率的血液流变学指标)。RBC伸长指数在37°C和0.95至30 Pa的7个剪切应力下测定。伸长指数值(未显示数据)被绘制成剪应力的函数,半最大变形所需的剪应力和预测的最大伸长指数是通过拟合Lineweaver-Burk曲线确定的[19].将Hct调整至40%后,在37℃测定红细胞聚集指数和防止红细胞聚集的最小剪切率(分解阈值)[19].
血液学分析仪用于评估红细胞、白细胞和血小板计数、平均细胞体积、平均红细胞血红蛋白浓度([Hb])和网织红细胞百分比。
分别用平均PVR和平均SVR除以血液黏度,计算反映几何因素对PVR和SVR贡献的肺血管和全身血管障碍参数[20.].血管障碍的改变可解释为乙酰唑胺和/或缺氧对肺重塑或血管收缩/血管扩张的影响。
统计分析
数据用平均值±表示sd.分布正态性通过Kolmogorov-Smirnov检验进行评估。对环境(常氧和缺氧)和药物(药物对照剂、乙酰唑胺治疗和预防)的影响进行了独立组的方差分析。Newman-Keuls试验被用于因果测试。在适当的时候进行未配对t检验。相关性采用Pearson检验进行评估。对于指数回归,p值经过对数变换线性化后,经过Pearson检验。所有统计分析均使用StatSoft统计软件(StatSoft, Inc., Tulsa, OK, USA)进行。p值<0.05为显著性差异。
后果
心脏形态学数据
与预期一样,慢性缺氧诱发右心室肥厚,预防性治疗乙酰唑胺(表1),通过富尔顿比值以及右心室重量/体重比进行评估。
血液动力学
慢性缺氧后PAP增加,而乙酰唑胺无显著影响(图1一个).我们观察到与对照组相比,只有在预防乙酰唑胺组中使用较低的PAP治疗的主要效果,无论常见常见的还原还是缺氧暴露。
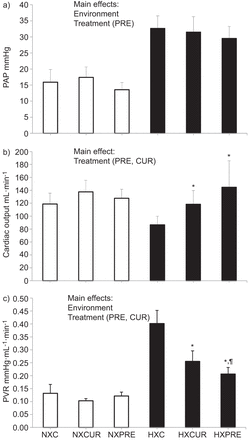
对照组(c)、治疗组(CUR)和预防组(PRE)在常氧(NX)或缺氧(HX) 3周后肺动脉压(PAP)、心输出量(heart output)和肺血管阻力(PVR)的变化。*:与低氧对照组差异显著,p<0.05;¶:与缺氧组比较,差异有统计学意义(p<0.05)。
心输出量没有因缺氧暴露而改变,但乙酰唑胺增加了缺氧大鼠的心输出量与低氧对照大鼠(图1 b).这种增加与卒中量的改善有关,但没有任何变化fC(表1).
低氧对照组PVR升高,乙酰唑胺组PVR降低。低氧预防组的PVR下降幅度大于低氧治疗组(图1 c)与低氧对照组相比,低氧预防组和低氧治疗组的SVR增加,而低氧预防组和低氧治疗组的SVR减少(表1).
血容量
低氧暴露后,与常氧对照组相比,无论采用何种治疗或预防性治疗,红细胞体积均显著增加(表2).低氧对照组暴露于低氧环境后血浆体积明显低于正常对照组。在常氧对照组和低氧治疗组和预防组之间没有发现显著差异,这表明乙酰唑胺治疗使血浆容量恢复到常氧值。
酸碱平衡和血液学参数
慢性缺氧暴露和乙酰唑胺治疗降低了血清碳酸氢盐、碱过量和pH值,在治疗和预防治疗之间没有差异,表明治疗对大鼠(表3).尽管测量是在常氧环境下进行的,但经过驯化的大鼠的血压升高P啊,一个2这与P,有限公司2,提示呼吸机对缺氧的适应。虽然在常氧组和低氧组大鼠之间有相反的趋势,但乙酰唑胺治疗对估计的肺泡-动脉氧压差没有显著影响(p=0.57)。
缺氧使各组Hct、[Hb]、RBC计数、平均细胞体积、网织红细胞百分比升高,血小板计数降低(表3),而乙酰唑胺降低Hct和网织红细胞在预防和治疗缺氧下。虽然乙酰唑胺在缺氧时[Hb]略有下降,但变化没有达到统计学意义(治疗组为-5%,预防组为-7%)。低氧预防治疗后细胞体积略有下降。
血液流变学参数和血管障碍
血液流变学结果见表4.虽然低氧暴露增加了血液粘度,但治疗性乙酰唑胺治疗降低了(-16%),预防性乙酰唑胺治疗倾向于降低血液粘度(-8%,p=0.1).缺氧或治疗均不影响红细胞变形能力和红细胞聚集指数。缺氧可降低红细胞解聚阈值,但乙酰唑胺治疗不影响红细胞解聚阈值。与缺氧对照组相比,缺氧预防组大鼠的Hct/粘度比显著升高。
无论是否使用乙酰唑胺治疗,各组大鼠的PVR均与血液粘度呈指数关系(p=0.015;图2一个).SVR和血液粘度之间的关联接近统计学意义(P = 0.06;图2 b).
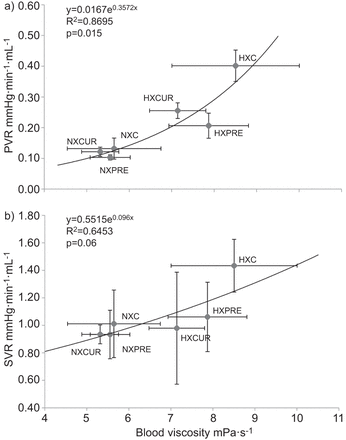
对照组(C)和治疗(CUR)和预防(预)乙酰唑胺治疗组暴露于常氧(NX)或缺氧(HX)3周的大鼠肺血管阻力(PVR)和全身血管阻力(SVR)与血液粘度之间的关系。
缺氧组大鼠肺血管障碍较正常组大鼠增加(图3),但与低氧对照组相比,乙酰唑胺治疗降低,而且乙酰唑胺在预防组中的作用比治疗组更明显。这些发现表明乙酰唑胺对肺血管的直接影响(图3).尽管常氧对照组和低氧对照组之间没有差异(慢性低氧无影响),但治疗和预防低氧组与低氧对照组相比,全身血管障碍也降低了(图3 b).此外,在绘制血管阻力变化时与血管障碍(图4)乙酰唑胺通过作用于肺血管和全身血管障碍而降低PVR和SVR。
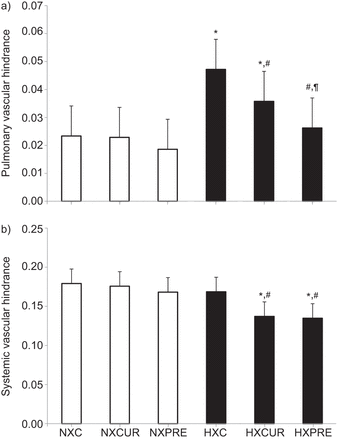
a)正常缺氧(NX)或缺氧(HX)暴露3周的大鼠肺和b)对乙酰唑胺治疗组(C)、治疗组(CUR)和预防组(PRE)进行全身血管障碍计算。*:与相应常氧组差异,p<0.05;#:与缺氧对照组差异,p<0.05;¶:与缺氧组比较,p<0.05。
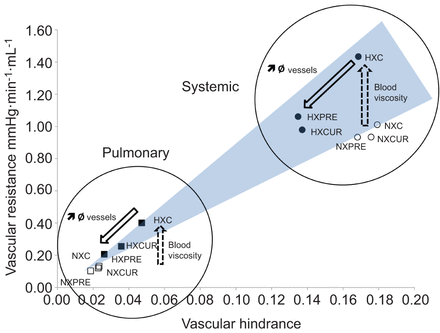
乙酰唑胺治疗组和不治疗组大鼠肺、全身血管阻力和血管障碍的关系。虚线箭头表示由于缺氧,粘度对全身血管阻力的唯一影响。实箭头表示乙酰唑胺对血管直径的影响。Ø:直径;NX: normoxia;HX:缺氧;C:控制;坏蛋:治疗;PRE:预防性乙酰唑胺治疗组。
讨论
我们的结果首次表明,在慢性缺氧暴露后使用乙酰唑胺,无论是预防还是治疗,都能有效地降低Hct,通过血浆体积的恢复;2)血粘度;3) PVR和SVR;4)右室肥厚(仅在预防性治疗后)。血液粘度或肺/全身血管障碍与PVR/SVR之间的关系提示乙酰唑胺对血液动力学的有益影响涉及血液流变学和肺/全身血管系统的适应。
观察到的血清碳酸氢盐和碱过量的下降表明,尽管在饮水中给予该治疗,大鼠在常氧和缺氧条件下都能很好地服用。由于饮水量通常在缺氧暴露开始时减少,预防组在缺氧前2天开始乙酰唑胺治疗,以获得足够剂量的乙酰唑胺。在治疗后的大鼠中,治疗是在缺氧暴露10天后开始的,因为此前有报道称,从第10天到第21天,肺动脉高压和Hb浓度保持不变[1,8].在乙酰唑胺治疗的第一天后,我们观察到大鼠的饮水量显著增加,这表明乙酰唑胺在治疗过程中也起到了很好的作用。正如先前在人类中显示的那样,乙酰唑胺治疗在预防组和治疗组中都轻微降低了Hct [3.].
正如我们的研究所证实的,慢性缺氧会导致血浆容量下降[21]以及红细胞体积增加引起的总血容量增加[22].由于乙酰唑胺具有利尿作用,可望在缺氧时进一步减少血浆体积,通过刺激通气和血氧作用,可能导致肾促红细胞生成素释放减少,从而抵消乙酰唑胺引起的Hct降低[3.,4].令人惊讶的是,用乙酰唑胺治疗的低氧大鼠血浆容量恢复到常氧值,与低氧对照大鼠相比,虽然没有显著增加,但略有增加。在长期用乙酰唑胺治疗并暴露于缺氧的大鼠中,利尿作用似乎并不持续。因此,可以认为乙酰唑胺治疗的缺氧大鼠Hct的下降并不完全是由于红细胞生成量的下降(网状红细胞百分比的下降),也可能是血浆体积上升的结果。这可以解释为维持血容量在正常值的生理适应。缺氧引起的血浆体积减少可能是由于众所周知的缺氧对肾素醛固酮系统的钝化作用[21和其他复杂的机制,如外周动脉化学接受[23,24].乙酰唑胺抑制钝化作用的机制尚不明确。在乙酰唑胺作用下增加通气和动脉氧合可减少急性缺氧时对利尿的缺氧刺激[23].
慢性缺氧引起的PVR增加可能与以下几个因素有关,如血液流变学改变[10]、缺氧血管收缩或肺血管的肌肉化[2,8].我们的数据不支持RBC在缺氧下PVR增加中的聚集和可变形性的作用。在缺氧下降低RBC分解阈值的确切原因是未知的,但可以推测血小板计数的减少在这一发现中发挥了作用[25].无论缺氧下红细胞解聚阈值变化的机制如何,其降低并不能补偿缺氧下Hct和血液粘度的增加导致PVR的增加。
虽然血粘度对缺氧下PVR的作用尚不清楚[26],R.ichaletet al。[4]先前的研究表明,乙酰唑胺治疗后PVR降低的部分原因可能是Hct和血液粘度降低[7].我们的结果支持乙酰唑胺降低PVR(在缺氧条件下)与1)降低血液粘度(在缺氧预防组-8%,在缺氧治疗组-16%)和2)降低血管障碍(在缺氧预防组-45%,在缺氧治疗组-35%)有关。我们的研究发现,血液粘度与PVR之间存在很强的相关性,这加强了血液粘度对PVR的重要作用。然而,乙酰唑胺治疗的大鼠的血管几何形状的适应也需要考虑,因为血管障碍的减少主要反映了肺血管重构的减少,在较小程度上反映了肺血管张力的变化。肺血管张力的变化可能很小,因为我们的测量是在常氧状态下进行的,因此限制了低氧肺血管收缩现象。
先前在狗身上进行的一项研究表明,乙酰唑胺可能钝化动物急性严重缺氧时的肺血管收缩,而不依赖于动脉氧分压的降低[27].另一项研究发现,乙酰唑胺可通过在急性缺氧时平滑肌细胞内钙的减少而作用于肺循环[28,29].然而,乙酰唑胺对低氧肺血管收缩的作用在人类中仍在讨论中,如Faoro等.[30.在10天的适应后(海拔3700 - 4700米),乙酰唑胺对海平面原体的急性治疗未能降低它,这表明乙酰唑胺对重构的影响可能比肺血管舒张更大。在本研究中,PAP的所有测量均在常氧条件下进行。因此,乙酰唑胺作用下低氧大鼠PVR的降低可能主要是由于肺血管重塑降低和血液高粘度降低,而不是急性肺血管舒张(无花果3),4])。这些结果支持了乙酰唑胺在预防组和治疗组中分别部分预防和纠正肺重塑,导致PVR下降的假设。观察到的肺血管障碍降低支持这一假设。反过来,PVR的降低可能导致右心室后负荷的下降,这可能是心输出量改善的原因。对乙酰唑胺作用下血管重构的分子机制的进一步研究显然是必要的。然而,我们的研究的一个局限性是PVR(以及SVR)是估计的,而不是由左心房压力校正的。由于乙酰唑胺低氧大鼠的血容量有增加的趋势,我们有理由认为乙酰唑胺组的左耳压较大,可能导致PVR的低估。第二个限制是所有的测量都是在正常情况下进行的。我们无法测量慢性乙酰唑胺治疗对低氧肺血管收缩的直接影响,以及低碳酸血症对肺动脉压力的可能影响。进一步的研究必须考虑到这些局限性。
缺氧组与未缺氧组之间的血容量缺乏统计学差异,这表明乙酰唑胺对心脏前负荷没有影响,因此不影响心输出量。然而,尽管没有统计学意义,但在慢性缺氧后,预防性治疗组的平均血容量比对照组高31%。事实上,可以推测,乙酰唑胺治疗后,心脏的前负荷在生理上增加了(在预防条件下比在治疗条件下更多),这可能通过弗兰克-斯塔林效应参与了每搏量和心输出量的增加。此外,与缺氧对照组相比,乙酰唑胺低氧处理大鼠的心输出量增加可能与PVR降低引起的右心室后负荷下降引起的卒中量增加有关。类似地,在继发性肺动脉高压患者中,西地那非治疗增加了心输出量,主要是通过降低右心室后负荷[3.].此外,由于乙酰唑胺增加通气和改善肺泡氧张力(和P啊,一个2),可减少低氧肺血管收缩,从而限制慢性缺氧时肺动脉重塑和PVR的增加。乙酰唑胺也有可能通过改善通气/灌注匹配来提高肺气体交换效率。预防性乙酰唑胺对缺氧大鼠Hct/血粘度比的提高也表明,血液流变学的氧气运输效率和组织氧合效率得到有效提高,限制了缺氧应激。
如前所述,PVR的降低直接影响右室重量,在预防治疗的大鼠中减缓右室肥厚[2].治疗组大鼠PVR的降低不会导致Fulton比率的显著变化。我们有理由认为肺重塑需要几天的时间[8,因此,在我们的低氧暴露模型(21天)中,会影响右心室后负荷。虽然有报道称慢性高山病可能导致心力衰竭,但我们的结果表明乙酰唑胺对右心有效。
虽然乙酰唑胺对PVR起作用,但我们的结果表明,它并不是一种特殊的作用,因为该药物也降低了SVR。虽然不总是观察到,但一些研究已经描述了暴露于缺氧的人类和大鼠SVR的增加[1,31].这种增加的部分原因是适应鼠的Hct较高[31,但其他因素也被认为与此有关,如肾上腺素能介导的血管收缩张力增加和/或体循环中的血管重塑[31]我们的结果支持血液粘度的作用,因为血液粘度和SVR之间的相关性几乎是显著的。然而,缺氧增加了SVR,而没有增加任何血管障碍(无花果3),4];常氧控制与低氧对照组)。因此,在缺氧条件下,肺循环比体循环更容易受到重构机制的影响。乙酰唑胺治疗在常氧状态下没有效果,但降低了缺氧大鼠的全身血管障碍,导致SVR恢复到基线常氧值。这个表述与P的结果是一致的ickkerset al。[32他发现乙酰唑胺对全身血管系统也有一定的影响。
值得注意的是,与急性高剂量乙酰唑胺注射液相比,慢性乙酰唑胺摄入对肺血管系统和高血压的影响较小[27或更具体的治疗,如西地那非或波生坦。事实上,这两种药物可以防止急性缺氧时肺血管收缩剂的反应,以及慢性暴露后肺动脉高压、右心肥大和肺动脉重塑的发展[8,33].
总之,我们目前的实验研究表明,乙酰唑胺预防和治疗慢性高山病都是有效的,通过改善肺血管的几何形状来调节PVR。此外,乙酰唑胺可增加心输出量,减少右心室肥厚,因此可降低心力衰竭的长期风险。乙酰唑胺对多个系统有影响,如红细胞生成、血液粘度、肺循环、通气和心脏功能,因此从生理病理学的角度来看,它是一种有趣的治疗慢性高山病的方法。
致谢
我们感谢M.S. Chambris和S. Varela(巴黎第13大学)在动物护理方面的工作。我们还要感谢我们的药剂师M. Micoulaud。
脚注
利益陈述书
没有人申报。
- 收到了2011年12月9日。
- 接受2012年2月13日。
- ©2012人队