摘要
细胞外基质(ECM)成分在气道结构中起重要作用。我们假设慢性阻塞性肺疾病(COPD)患者的ECM肺成分不同于吸烟和不吸烟的无气流阻塞的受试者。
我们测定了26例COPD患者、26例非COPD吸烟者和16例非吸烟对照组大、小气道和肺实质不同腔室中弹性纤维、i型、-III型和-IV型胶原蛋白、versan、decorin、biglycan、lumican、纤连蛋白和腱蛋白的分数区。
在所有肺区中,非阻塞性肺病患者的弹性纤维分数面积均高于COPD患者和非吸烟对照组。COPD患者大、小气道和非梗阻吸烟者小气道中i型胶原蛋白分数区均低于非吸烟者。与非吸烟者相比,COPD患者在气道实质中有较低的纤维连接蛋白分数区,在小气道中有较高的纤维连接蛋白分数区,在大、小气道室中有较高的腱蛋白分数区。在COPD患者中,弹性纤维和纤维连接蛋白与肺功能参数之间存在显著相关性。
主要ECM成分的改变广泛存在于COPD患者的所有肺室中,并可能导致持续的气流阻塞。
慢性阻塞性肺疾病(COPD)是全世界死亡和发病率的主要原因。它的负担仍然被低估,因为慢性阻塞性肺病在高收入和低收入国家诊断不足和治疗不足,主要是在疾病的轻度阶段[1- - - - - -3.].吸烟是COPD发病最重要的危险因素。有人提出,慢性香烟引起的炎症与易感吸烟者肺部结构变化的发展有关,这有助于进行性气流限制[4,5].
肺细胞外基质(ECM)的主要成分是胶原蛋白、弹性纤维、蛋白多糖、纤维连接蛋白和腱蛋白[6,7].先前的研究报告了弹性蛋白的减少[8- - - - - -10]和蛋白多糖[11], COPD患者肺泡中总胶原蛋白含量增加[12].很少有研究评估气管和肺实质不同水平的ECM组成[13,14].
胶原蛋白是肺间质中最丰富的组成部分,特别是纤原性i型和iii型胶原蛋白,对维持肺结构很重要。iv型胶原是基底膜的主要成分,也是肺中含量最多的非纤原性胶原[15,16].
蛋白聚糖是由蛋白质核心和糖胺聚糖侧链组成的大分子,参与维持胶原原纤维的组装、水分平衡以及细胞粘附和迁移[17,18].目前对COPD患者肺中蛋白多糖沉积的模式知之甚少。到目前为止,已有研究描述了远端肺内蛋白和装饰蛋白的改变[10,11].
肌腱素和纤维连接蛋白在持续的组织损伤中发生改变,调节重要的细胞特性和炎症细胞的趋化性[19].目前很少有研究分析COPD患者中腱蛋白和纤连蛋白的表达[13,20.,21],但没有研究涉及所有肺间室中的这些蛋白质。
我们推测,COPD患者大气道、小气道和肺实质中ECM的组成不同,肺功能正常的吸烟者和非吸烟者之间也不同。此外,我们假设这些差异有助于COPD的肺功能损害。
因此,我们的目的是量化COPD患者所有肺室中几种ECM成分(弹性纤维,i型,-III和-IV型胶原蛋白,versan, decorin, biglycan, lumican,纤连蛋白和腱素)的组成,与吸烟和肺功能有关。
方法
这项研究得到了São保罗大学医学院和A.C. Camargo医院(均为São保罗,巴西)、莱顿大学医学中心(莱顿,荷兰)和巴勒莫大学(巴勒莫,意大利)的审查委员会的批准。所有受试者均提供书面知情同意书。
主题
我们分析了2001年至2007年间68例因原发性或转移性肺肿瘤而接受肺切除手术的患者的肺组织。
信息包括人口统计数据、病史和吸烟史、药物和术前肺功能从患者的医院图表中获得。患者诊断为哮喘、支气管扩张、感染性疾病α1-抗胰蛋白酶缺乏或间质性肺病不包括在内。
患者分为以下几类:1)不吸烟(NS, n=16);不吸烟,用力呼气量在1秒(FEV1)≥80%预测和FEV1/用力肺活量(FVC)≥70%。2)非阻塞性吸烟者(NOS, n=26):目前和/或戒烟(戒烟≥1个月),肺功能正常(FEV1≥80% pred和FEV1/ FVC≥70%)。3) COPD (n=26):目前和/或戒烟(戒烟≥1个月)合并COPD (FEV1/ FVC < 70%)。15例COPD患者(5例全球慢性阻塞性肺疾病倡议(GOLD) I期,轻度,9例II期,中度,1例III期,重度,[1]),且与支气管扩张剂使用前相比均改善<12%。
组织处理
在大多数病例中,可获得远离肿瘤的2 ~ 4块外周实质和1 ~ 2块中央气道。一般来说,由于肿瘤靠近或手术边界,从中心区域获得的组织较少。碎片在10%缓冲福尔马林中固定24小时,处理后石蜡包埋。4 μm厚切片用苏木精-伊红染色进行初步分析。我们排除了表现为纤维化疾病、肿瘤组织和狭窄后肺炎的病例。
组织化学
为了鉴别弹性纤维,使用了Weigert的间苯二酚-紫红素氧化技术[22].
免疫组织化学
抗原检索和初抗见在线补充资料的表1S。免疫组化技术的细节在在线补充材料中描述。
形态分析
在横切面上切开两个大(上皮基底膜周长> 6mm)气道和三个小(≤6mm)气道,分析所有受试者的10个细支气管周围段(肺泡附着部位)和10个远端肺泡段(肺泡间隔距离任何小气道边界至少1×100场)[23].
将气道壁细分为内层,包括上皮细胞与内平滑肌边界之间的区域、平滑肌层与外层之间的区域,位于外平滑肌边界与气道外界限之间,即。肺泡实质(图1在网上的补充资料中)。
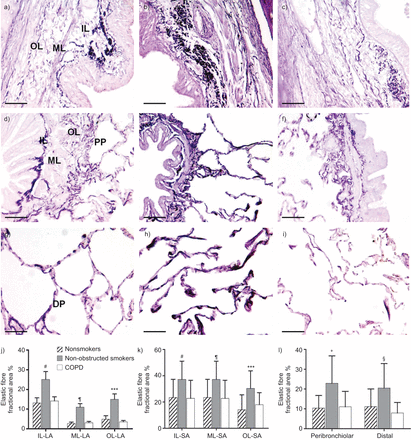
非吸烟者(a、d和g)、非阻塞性吸烟者(b、e和h)和慢性阻塞性肺病(COPD)受试者(c、f和i)的a - c)大气道(LA)、d - f)小气道(SA)和细支气管周围实质(PP)和g - i)远端实质(DP)的弹性纤维分数区。比例尺=50 μm。j-l) LA、SA、PP和DP中弹性纤维的分数区。IL:内层;ML:肌层;OL:外层。数据以均数±表示sd.* * *: p < 0.001;#: p < 0.03;¶: p < 0.0001;+: p < 0.004;§: p<0.02,与非吸烟者和COPD受试者相关。
在大气道中,iv型胶原和腱蛋白主要染色于支气管上皮层的上皮下区和血管壁。为了避免包括血管中存在的iv型胶原蛋白和腱蛋白,我们只分析了大气道中的上皮下区域。这些被定义为上皮以下12 μm区域。我们进一步分析了大气道的肌层、小气道的内肌层和肌层以及远端和细支气管周围的实质。对于大气道,我们用400倍的放大镜测量了10个上皮下区域。
使用image - pro Plus 4.1 for Windows软件(Media Cybernetics, Silver Spring, MD, USA)通过图像分析确定每个隔间的分数区域。阳性染色区域的测量如前所述[24].染色强度通过平均色密度(每个活检组织的加权平均值)进行分析,并表示为强度值(白色=0;黑色= 255)。详细信息在在线补充材料中描述。
统计分析
采用SPSS 15.0软件(SPSS, Chicago, IL, USA)进行统计分析。数据以均数±表示sd或中位数(四分位范围(IQR)),取决于数据分布。为了比较NS、NOS和COPD组之间的数据,酌情使用单向方差分析或Kruskal-Wallis检验。Bonferroni调整用于多个分析试验。我们进行了全因子一般线性模型,以评估各组、性别、年龄和中心对不同肺室中ECM成分分数区域的影响;大、小气道内、外、肌层合并,支气管周围/远端实质一起分析。一般线性模型的结果仅显示在单变量分析中组间有显著差异的ECM成分。一般线性模型分析的完整数据在在线补充资料[25].
未配对t检验或曼-惠特尼检验用于比较吸烟者和戒烟者之间的差异。对ECM组分的分数面积进行了较大的比较与小气道和支气管周围与远端实质用配对t检验。形态学与临床数据之间的关联采用Pearson或Spearman系数检验。p值为0.05被认为是显著的。
结果
主题
文中给出了这些群的特征表1.COPD组在年龄和吸烟史方面与NOS组相似,但正如预期的那样,肺功能低于其他两组。均值±sdFEV的1/FVC在COPD组为58.3±9.8%,NOS组为77.5±6.5%,NS组为83.4±7.6% (p≤0.0001)。FEV1COPD患者FVC比值低于正常值下限(69.6±1.7)[26].8名COPD患者,其他两组患者在手术时均未接受类固醇治疗。
NS患者明显小于NOS和COPD患者(p≤0.007)。NS组女性多于男性。
形态测量学
根据所研究的蛋白质,测量了46-67条(平均58条)大气道和137-157条小气道(平均147条)。共测量了578个大型气道和1465个小型气道。NS、NOS和COPD患者大气道周长平均值分别为11.8±4.6 mm、7.4±1.5 mm和11.3±5.3 mm (p=0.39)。NS、NOS和COPD患者的小气道周长分别为1.9±0.8 mm、2.1±1.0 mm和2.0±1.4 mm (p=0.64)。NS、NOS和COPD患者的支气管周围实质总长度分别为12.8 mm、12.2 mm和12.9 mm (p=0.363)。对于远端实质,NS、NOS和COPD的总长度分别为17.4 mm、15.7 mm和17.3 mm (p=0.084)。
弹性纤维
与COPD和NS组相比,NOS组大、小气道内层(p<0.03)、肌肉层(p<0.0001)和外层(p<0.001)以及细支气管周围(p<0.004)和远端实质(p<0.02)弹性纤维的分数面积更高。NS与COPD之间无显著差异(图1).数据载于表2.
在大气道(p=0.051和p=0.017)和小气道(p=0.001和p=0.038)中有显著的群体和中心效应,而在年龄和性别上无显著影响。组(p=0.001)和性别(p=0.012)有显著影响,但实质的中心和年龄没有影响(表2S在线补充资料)。
免疫组织化学分析
ECM蛋白的免疫反应性在COPD患者、NOS和NS的肺组织中显示出相似的染色模式。完整的免疫组化数据在表2.
i型胶原蛋白
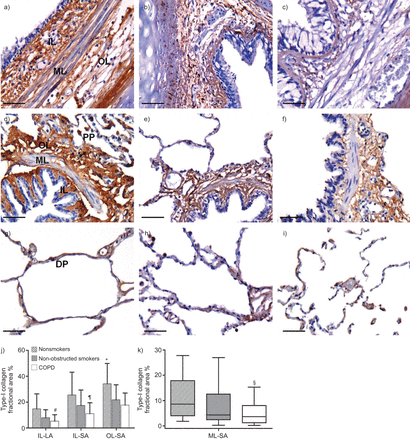
COPD患者大气道内层、小气道内层及肌层i型胶原的分数面积较正常人低(p=0.01, p=0.004, p=0.03)。在小气道外层,与NS对照组相比,COPD患者和NOS中的i型胶原蛋白较低(p≤0.01)(图2).
非吸烟者(a、d、g)、非阻塞性吸烟者(b、e、h)和慢性阻塞性肺疾病(COPD)受试者(c、f、i)的a - c)大气道(LA)、d - f)小气道(SA)和细支气管周围实质(PP)及g - i)远端实质(DP)中的i型胶原分型区。标尺=50 μm。j, k) LA和SA中i型胶原的部分区域。IL:内层;OL:外层;ML:肌肉层。数据以均数±表示sd或中位数(四分位范围)。#:与不吸烟对照组相比,p=0.01;¶:与不吸烟者相比p=0.004;+:与非阻塞性肺病患者和COPD患者相比,p≤0.01;§: p=0.03。
当所有层合并时,组、中心、年龄和性别对大小气道无显著影响(表3S在线补充资料)。
iii型和iv型胶原蛋白
COPD、NOS和NS在大、小气道和支气管周围/远端实质中无差异。免疫组化分析的结果描述在表2一般线性模型在在线补充资料的表4S和表5S中描述。
Versican
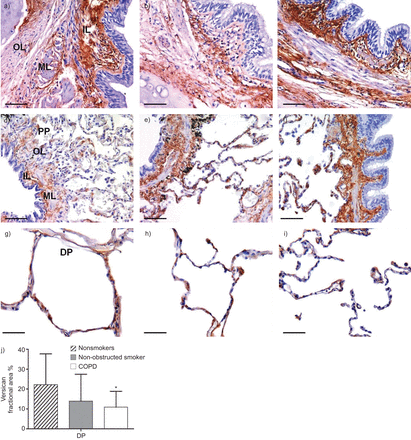
COPD患者仅远端实质的分数区较NS患者低(p<0.05) (图3).大气道、小气道和细支气管周围实质内的交叉分数区组间无差异。
非吸烟者(a、d和g)、非阻塞性吸烟者(b、e和h)和慢性阻塞性肺疾病(COPD)受试者(c、f和i)远端实质(DP)中a - c)大气道、d - f)小气道和细支气管周围实质(PP)及g - i的纵向分数区。比例尺=50 μm。j)远端实质内异位小区。IL:内层;OL:外层;ML:肌肉层。数据以均数±表示sd.*:与不吸烟者相比p<0.05。
各组、中心、年龄和性别对脑实质水平无显著影响(表6S在线补充资料)。
Decorin, biglycan和lumican
COPD、NOS和NS在任何大或小气道层或支气管周围/远端实质中均无差异。免疫组化分析的结果描述在表2一般线性模型见在线补充资料中的表7S、8S和9S。
纤连蛋白
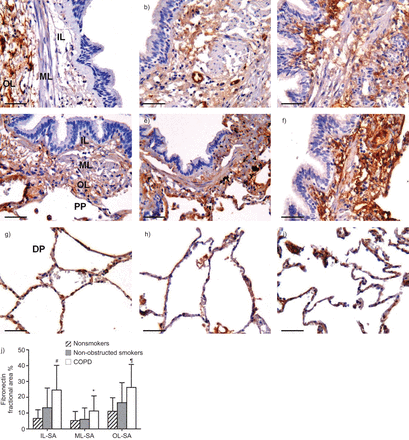
COPD组小气道内层、肌层和外层纤维连接蛋白分数区均高于NS组和NOS组(p<0.02, p<0.05和p<0.04) (图4).在大气道和肺实质中,各组间纤维连接蛋白分数区无差异。
非吸烟者(a、d和g)、非阻塞性吸烟者(b、e和h)和慢性阻塞性肺疾病(COPD)受试者(c、f和i)的a - c)大气道、d - f)小气道(SA)和细支气管周围实质(PP)及g - i)远端实质(DP)中的纤连蛋白分数区。比例尺=50 μm。j) SA内层(IL)、肌肉层(ML)和外层(OL)的纤维连接蛋白分数区。数据以均数±表示sd.*: p < 0.05;#: p < 0.02;¶: p<0.04,与非吸烟者和非阻塞性吸烟者相关。
各组、中心、年龄和性别对小气道水平无显著影响(表10S在线补充资料)。
Tenascin
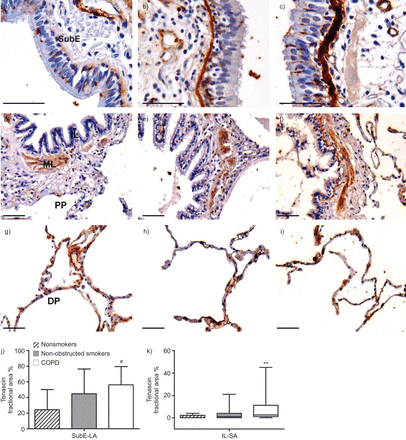
COPD组大气道上皮下区和小气道内层的腱素分数区高于NS对照组(p<0.02)与p < 0.01) (图5).大、小气道肌层和肺实质中腱蛋白分数区在各组间无差异。
非吸烟者(a、d、g)、非阻塞性吸烟者(b、e、h)和慢性阻塞性肺疾病(COPD)受试者(c、f、i)的a - c)大气道(LA)、d - f)小气道(SA)和细支气管周围实质(PP)及g - i)远端实质(DP)中的腱素分数区。标尺=50 μm。j, k)皮下区(SubE)和(LA)和SA的内层(IL)的腱蛋白分数区。ML:肌肉层。数据以均数±表示sd.* *: p < 0.01;#: p<0.02,相对于不吸烟者。
各组、中心、年龄和性别对气道水平无显著影响(表11S在线补充资料)。
大与小航空公司/支气管旁与远端软组织
ECM分数区差异较大与小气道,细支气管周围和远端肺泡间隔表2.
平均色密度
ECM蛋白平均色密度的结果与分数区域的结果相似(数据未显示)。
Clinical-morphological相关性
在COPD组中,FEV与FEV呈负相关1大气道外层(r= -0.66, p=0.009)和小气道肌肉层(r= -0.48, p=0.03)的% pred和弹性纤维分数面积;和FEV之间1/FVC和小气道肌层纤维连接蛋白分数区(r= -0.39 p=0.05) (图2 s在线补充材料)。
仅分析NOS组时,年龄与大气道外层弹性纤维分数面积相关(r=0.74, p=0.038)。pack-yrs与远端实质弹性纤维分数区呈负相关(r= -0.59, p=0.026)。FEV与FEV之间的纤维连接蛋白分数区也呈负相关1小气道内层(r= -0.50, p=0.018)和外层(r= -0.47, p=0.027)图3年代在线补充材料)。NS组的临床参数与ECM组成无相关性。
在COPD患者中,小气道和肺实质之间的弹性纤维分数区具有显著相关性(r=0.77, p<0.0001)。小气道与大气道间的分数区呈正相关(r=0.61, p<0.02),小气道与肺实质间的分数区呈正相关(r=0.72, p<0.0001)。我们还发现小气道和肺实质之间的纤维连接蛋白分数区存在显著相关性(r=0.72, p<0.0001)。大气道内腱素分数区与肺实质正相关(r=0.61, p<0.02)。
当前的与抽过烟
戒烟者戒烟的中位时间(IQR)为6.0(2.25-10)年。目前吸烟者与戒烟者相比,ECM组成无显著差异,不考虑阻塞(数据未显示)。
讨论
在本研究中,我们描述了COPD患者大、小气道和肺泡实质中ECM成分的变化,与吸烟或不吸烟的无气流阻塞的受试者相比。与COPD患者和NS受试者相比,NOS中弹性纤维的分数区域更高。COPD大、小气道及远端实质内分流区i型胶原表达较NS低。COPD患者小气道和大气道(腱素)纤维连接蛋白和腱素的分数区较高。这些结果不受吸烟状况或吸烟年限的影响。我们的结果表明,COPD在大气道和小气道的ECM组成中都有复杂的改变。
弹性纤维损伤是COPD病理生理学中的一个经典概念,其原因可能是吸烟引起的弹性酶/抗弹性酶失衡[27].B缺乏et al。[14]表明COPD患者远端肺弹性纤维比吸烟者少。我们的发现补充了本研究,因为我们发现COPD患者的大、小气道和肺实质中的弹性纤维分数区与NOS相比较低。令人意外的是,当COPD患者与NS比较时,没有发现差异。
我们如何解释这些发现呢?Desleeet al。[28]表明在严重COPD患者中弹性蛋白基因表达增加,而弹性纤维密度或桥氨酸含量没有显著增加。这些作者认为,严重的COPD患者可能对弹性纤维的修复无效。我们的发现与这些观察结果一致,并提示非COPD的吸烟者可能能够增加弹性蛋白表达,作为对吸烟相关损伤的反应,而COPD患者可能不会出现这种增加。有趣的是,Cantoret al。[29的研究表明,在老鼠身上暴露3个月的香烟会导致呼吸道弹性纤维增生。人类在童年以后就不能充分地在组织中合成弹性蛋白了[30.].在本研究中,我们没有评估弹性纤维的完整性/质量,但在NOS和COPD患者中都发生弹性纤维破坏[31,32].因此,吸烟者的弹性纤维可能也没有完全发挥功能。
目前气道弹性纤维含量与FEV的负相关关系1与之前的数据一致[28].这些数据表明,在气道弹性纤维含量最低的患者中,气流限制和/或气道塌陷不太常见。人们可能会推测,降低弹性纤维含量会降低气道壁顺应性,从而增加气道壁刚度,这确实在COPD中观察到[33]甚至哮喘[34].因此,在COPD存在的情况下,气道弹性纤维含量降低甚至可能代表一种对抗气流限制的保护机制。值得注意的是,在对COPD患者和无症状吸烟者的联合分析中,据报道气道弹性纤维含量与呼吸计值呈正相关[14].后者在当前的分析中通过纳入无症状吸烟者得到了证实(数据未显示),并表明在无COPD的情况下气道弹性纤维的丧失也可能对肺功能有害,类似于肺气肿中发生的实质弹性纤维的丧失[9].
胶原蛋白在COPD中的研究结果是相互矛盾的。而有研究显示COPD患者肺泡胶原蛋白增加[12,35],其他COPD与对照组之间无差异[11].很少有研究关注呼吸道中的胶原蛋白亚型。Hogget al。[36]表明重度COPD细支气管中总胶原蛋白的减少与i型/-III型胶原蛋白比例的减少有关。Gosselinket al。[37]发现i型胶原蛋白α1 (COL1A1)和iii型胶原蛋白α1 (COL3A1)基因表达降低与FEV下降相关1分别在细支气管周围的肺组织和小气道中。他们认为,小气道的增厚与纤维发生相关基因的表达无关。
在本研究中,我们发现COPD患者中i型胶原蛋白分数区较少。我们推测,结构蛋白的丢失导致气道刚度降低,使其更容易受到正常呼气时施加的外力的影响,有利于崩溃。此外,我们发现NOS组小气道外层i型胶原含量较NS组低。这一水平的i型胶原蛋白结构改变可能导致无COPD吸烟者的气道-实质解耦[38].
葡聚糖是肺中蛋白聚糖透明质家族的丰富成员[18].我们描述了COPD患者远端实质的小分数区与NS相比。相反,在轻/中度COPD患者中,Merrileeset al。[10通过半定量分析,COPD患者的肺泡染色与吸烟对照组相比有所增加。这些差异结果的原因尚不清楚,但可能与两项研究中使用的不同分析方法有关。
Decorin、biglycan和lumican是与纤原性胶原相互作用的小蛋白聚糖,参与维持细胞外环境[39- - - - - -41].在体外研究表明,COPD患者的成纤维细胞暴露于香烟烟雾或不同细胞因子时,蛋白多糖的生成异常,转化生长因子(TGF)-β Smad通路的表达改变[42,43].在本研究中,与NOS和NS对照组相比,轻/中度COPD中decorin、biglycan和lumican的表达没有差异。范年代traatenet al。[11结果显示,重度肺气肿患者细支气管周围区decorin和biglycan染色明显低于轻度肺气肿患者。后来,Noordhoeket al。[44]的研究结果表明,在基础情况下,重症肺气肿患者肺组织中分离的成纤维细胞产生的装饰蛋白含量较高,TGF-β刺激后,与轻度肺气肿患者的成纤维细胞相比,其分泌的装饰蛋白含量下调更为明显。结合我们的研究结果,蛋白聚糖的改变似乎在严重的慢性阻塞性肺病中更为明显。
腱素和纤维连接蛋白在肺发育过程中起着重要的形态调节作用。在成人生活中,这两种蛋白质在组织损伤和炎症后发生改变,调节细胞粘附、迁移和分化[7].先前的研究表明,COPD患者和吸烟者大气道中的腱蛋白表达发生改变[20.,45].我们的数据扩展了这些观察结果,显示COPD患者大气道和小气道中肌腱蛋白表达较高。COPD患者纤维连接蛋白也较高,主要是在小气道水平。有趣的是,腱素和纤维连接蛋白诱导基质金属蛋白酶的表达和活性[7],导致组织损伤的持续。慢性阻塞性肺病患者纤维连接蛋白与肺功能的负相关强化了这些假设。
我们的研究有局限性。我们缺乏严重的COPD组,这将有助于更全面地描述这种疾病的ECM组成。另一个限制是NS组的年龄较小,但多变量分析显示年龄在数据中没有显著影响。有趣的是,对几种蛋白质观察到中心效应,这表明种族/环境因素可能影响肺中的ECM组成,并导致COPD的不同表型。
虽然分析了远离肿瘤的肺组织,但我们不能排除ECM中观察到的变化受到恶性肿瘤的影响。由于所有患者都有恶性肿瘤,不太可能只在COPD组发生相互作用。部分COPD患者在支气管扩张剂后未评估肺功能;然而,这些老年人是或曾经是重度吸烟者,并且没有哮喘、肺纤维化或支气管扩张史。
由于来自大气道的支气管活检正被用于COPD的研究目的[46],一个重要的问题是疾病模式在中心是否相似与远端肺。COPD患者的弹性纤维、i型胶原蛋白和腱蛋白在大小气道中观察到类似的ECM重塑模式。然而,COPD患者的ECM组成模式在小气道和实质之间发现了更显著的相关性。
总之,我们发现,主要ECM元素,弹性纤维,胶原蛋白,纤维连接蛋白和腱蛋白的改变在轻/中度COPD患者的所有肺区室中普遍存在。慢性阻塞性肺病中ECM成分的改变可能导致持续性组织损伤,并可能在该病的气流阻塞特征中起作用。
致谢
我们感谢K.Y.M. Kimoto和das Clfínicas医院(São Paulo大学医学院,São Paulo,巴西)和A.C. Camargo医院(São Paulo)胸外科的胸外科医生协助收集肺组织。我们也感谢A. James(西澳大学,克劳利,澳大利亚)对这篇手稿的建设性意见。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
这项研究得到了Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), Conselho Nacional de Desenvolvimento Científico e Tecnológico (CPNq;Brasília,巴西)和Laboratório de Investigação Médica 05 (LIM05-HCFMUSP;São圣保罗大学医学院,São巴西圣保罗)。
权益声明书
P.S.海姆斯特拉、P.J.斯特克和K.F.拉贝的兴趣声明见www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2011年11月4日
- 接受2012年3月15日。
- ©2012人队