欧洲呼吸188bet官网地址学会(ERS)研究研讨会题为“慢性阻塞性肺病的身体活动、营养状况和全身炎症”,由“临床生理学和运动”ERS科学小组4.01组织,汇集了国际专家讨论慢性阻塞性肺病(COPD)中身体活动、营养状况和炎症的几个重要方面,包括病理和病理生理学、测量、以及临床和治疗意义。以下是2011年11月11日至12日在意大利佛罗伦萨举行的为期两天的会议的简要总结,以及主要结论和观点。
慢性阻塞性肺病无疑是一种与肺部异常炎症反应相关的疾病,但越来越多的证据表明,它也与全身性炎症有关[1- - - - - -4],特别是在疾病恶化期间[5对心血管系统、新陈代谢和骨骼肌的影响[6,7]。可能与全身性炎症相关的全身性后果包括:心血管疾病、肥胖、高血压、2型糖尿病、抑郁、失调、营养不良、骨骼肌萎缩和功能障碍、缺乏运动、骨质疏松、贫血和骨髓功能障碍[8- - - - - -20.]。在过去的十年中,COPD患者合并症与全身性炎症的关系已经被广泛研究。这是因为在临床上见到的大多数COPD患者(约70%)都伴有一种或多种合并症[7]。考虑到慢性呼吸系统疾病、肥胖、心血管和代谢疾病的流行比例,以及它们有共同的风险因素,如衰老、吸烟、体育活动水平低和西方致胖饮食,慢性呼吸系统疾病、肥胖、心血管和代谢疾病之间的临床关联并不令人惊讶。人们不太了解的是,所有这些疾病都能独立预测心血管风险,慢性呼吸系统疾病、心血管疾病和代谢性疾病之间的联系很可能不仅仅是常见疾病之间的简单联系[21]。事实上,目前的证据虽然有限,但表明慢性呼吸、心血管和代谢疾病之间可能存在协同作用,当它们结合在一起时,它们可能相互作用,促进:1)自然进化的恶化,2)功能能力受损,3)呼吸困难的恶化,4)健康相关生活质量的降低,5)死亡率的增加[1]。一些作者建议用“复杂慢性疾病”来描述这种情况[1]。这可能是指患有多种疾病的患者,也可能是指大多数慢性疾病(如。慢性阻塞性肺病(COPD)和糖尿病(糖尿病)不是反映一种表型,而是在不同疾病阶段具有不同表型的复杂疾病。这一概念的含义是,只孤立地治疗一种慢性疾病,而忽视了对其他伴随慢性疾病的关注,可能导致健康效益达不到最佳水平。重要的是,预计未来几年“复杂慢性疾病”的流行率将出现前所未有的增长[1]。图1描述了COPD中不同程度的损害。
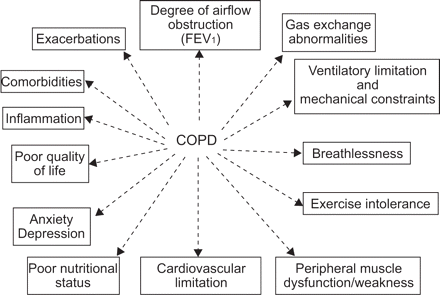
慢性阻塞性肺疾病(COPD)的不同程度损害。FEV1: 1 s内用力呼气量。
当然,提出一种统一的机制来促进与COPD相关的合并症的发展是很诱人的。其中一个可能的机制是全身性炎症,这可能是由促炎介质从肺部“溢出”到体循环引起的[6]。然而,以下几点对COPD的全身性是不利的,我们应该承认:1)全身性炎症在COPD患者中的分布是不均匀的[22];2)其在较长时间内的稳定性尚未得到研究[23];3)全身性炎症、COPD的严重程度、合并症和死亡率是否密切相关目前尚不清楚[24];4)一些证据表明,合并症似乎与年龄有关,而与疾病严重程度无关[24]。到目前为止,这个问题仍然没有答案。
不管copd -全身性炎症相关的合并症的性质,一个有趣的问题是合并症是否可能与康复反应有关[7,25]。最近,一项回顾性队列研究调查了这个问题。作者发现,Charlson指数以及代谢性疾病和心脏病的存在都降低了康复的可能性(优势比从0.57-0.72不等)[7]。心血管合并症对康复反应的负面影响在另一项研究中得到证实[25]。相比之下,康复有望对肺部康复患者经常出现的大多数合并症产生有益的影响[26]。目前,这种关系仍存在争议。
肢体肌肉功能障碍是COPD的另一主要表现[20.]。肌肉功能障碍的特征是肌肉力量丧失和耐力受损,后者与周围肌肉疲劳增加呈负相关[27- - - - - -30.]。这些功能障碍与肌肉的各种病理生理变化有关,即生物能量改变(氧化能力差)[31]、纤维类型再分配(由第一类纤维转为第二类纤维)[32,33],毛细血管化改变[33],氧化应激[34- - - - - -38]和肌肉萎缩[38- - - - - -41影响慢性阻塞性肺病患者亚群。导致这些病理生理变化的致病机制是多因素的。系统性炎症和氧化/亚硝化应激已被描述为COPD肌肉功能障碍的致病机制[42,43]。肌肉水平局部炎症标志物的存在不太清楚,但这是一个有争议的问题[36,44- - - - - -48]。因此,慢性阻塞性肺病是一种具有肺外表现的肺部疾病,其中骨骼肌功能障碍是一个独立的预后因素,在一定程度上是造成这些患者运动耐受不良的原因[28- - - - - -30.,40,41,43]。运动训练是一种旨在通过改善呼吸、心血管、代谢和外周肌肉功能来恢复运动耐受性的策略。运动训练改善慢性阻塞性肺病患者全身性炎症的能力尚不清楚。我们知道运动可以引发慢性阻塞性肺病患者的炎症反应和氧化应激[49- - - - - -52]。非损伤性(中等强度和短时间)运动通过刺激白细胞介素(IL)-6、IL-10和IL-1ra而抑制肿瘤坏死因子(TNF)-α,从而增加循环炎症细胞和细胞因子的水平[53- - - - - -55]。这些细胞因子通过调节葡萄糖代谢动员能量底物,可能调节肌肉重塑,也可能减弱或抑制炎症反应(“抗炎”作用)。然而,有害的(高强度和长时间)运动通过刺激细胞因子(IL-1β和TNF-α)的释放引发最初的炎症反应,这些细胞因子在受损肌肉的降解中起作用[53- - - - - -55]。随后是再生和修复的后期阶段,释放抗炎细胞因子(IL-10, IL-1ra和TNF-R),这些细胞因子调节肌肉重构,以应对运动引起的损伤。由此推论,对于健康受试者而言,绝对意义上的“非伤害性”运动对于慢性阻塞性肺病患者而言,可能是相对强度的(“伤害性”运动)[50]。事实上,对于相同强度的运动,COPD患者的乳酸生成增加[56]。即使有害的运动似乎可以激活健康人的再生,COPD患者也可能容易受到永久性肌肉损伤[57]。事实上,肌肉收缩引起的炎症反应的损伤期和修复期的大小和持续时间受个体特征的影响[58,59]。在慢性阻塞性肺病患者中,全身性炎症、衰老、以前缺乏锻炼(即。久坐不动)和恶化都可能与肌肉收缩的不同炎症反应有关。老年人的肌肉在运动后更容易受伤[58- - - - - -60]。然而,一些研究报告,与年龄匹配的对照组相比,COPD患者对运动的炎症反应异常[56,57他指出,老龄化只是一个潜在的促成因素。因此,慢性阻塞性肺病患者反复的运动可能是有害的。运动训练不能逆转全身性炎症,并会损害肌肉水平的氧化还原状态[42,57,61,62]。这种情况在肌肉萎缩和低体重指数的COPD患者亚群中更为明显[36,42,56,63]。这些患者可能会经历较小的“治疗范围”或训练安全区域,以获得有效但更安全的运动处方,或从额外的药物或生理(如。营养)干预措施。
尽管如此,运动训练已被证明对约70%的COPD患者在运动耐量和生活质量方面是有益的,至少部分是通过改善周围肌肉功能[52,64,65]。但其余30%的COPD患者从肺部康复/运动训练中获益较少或根本没有获益[66] ?在得出一些患者对肺康复无反应的结论之前,首先要考虑的问题是无反应的定义。这不是一个微不足道的问题,因为一些患者的疾病可能在某些方面有所改善(如。生活质量或症状)而在其他方面没有明显改善(如。运动公差)。有证据表明,接受运动训练的COPD患者呼吸困难强度有相当小的下降,无论他们是否表现出运动耐受性的改善[67]。我们是否应该得出这样的结论:这样的病人对康复没有反应?另一个需要考虑的问题是我们用来量化肺部康复影响的测试模式的反应性。例如,一些患者在恒定工作速率耐力骑行测试中可能表现出运动耐受性的改善,而在6分钟步行测试中却没有[68]。从这些观察结果可以明显看出,在宣布患者不能从肺部康复中获益之前,应谨慎行事。话虽如此,但必须承认,COPD患者对肺康复的反应程度差异很大,有些患者几乎没有或根本没有获益。在健康个体中也有类似的观察结果,这一现象与遗传因素有关[69- - - - - -71]。因此,对训练反应的高度个体差异并非COPD所独有。同样有趣的是,与健康受试者相比,COPD患者对运动训练的骨骼肌反应的性质可能不同[72]。对运动训练缺乏反应也可能与不能忍受足够的训练强度和/或持续时间和/或对训练干预的依从性差有关。例如,与强度较低或时间较短的计划相比,高强度或持续时间较长的计划所引起的反应较大[73,74]。在运动训练后出现明显的收缩性疲劳的患者也显示出更明显的训练效果[75]。一些肌肉萎缩明显的慢性阻塞性肺病患者(恶病质患者)似乎更容易受到肌肉水平氧化应激和炎症的影响[51,62,63,76]。这个问题很重要,因为肌肉萎缩发生在约35%的适合肺部康复的严重COPD患者中[77也有20%的门诊病人出现中度气流阻塞[78],并预示着死亡率的增加[40,41]。此外,有研究表明,有几种机制损害了病毒性COPD患者的肌肉重塑,如抑制肌肉生成、增加蛋白质降解和减少蛋白质合成[76,79]。虽然运动训练/肺康复在恶病质COPD患者中产生的外周肌纤维表型适应/重塑比非恶病质COPD患者少,但与非恶病质COPD患者相比,恶病质COPD患者能够增加运动能力[80]。我们很容易推测,在病毒性慢阻肺患者中,训练对外周肌纤维重塑的有限影响可能是由于运动训练同时激活了肥大(胰岛素样生长因子1和机械生长因子)和萎缩(泛素蛋白酶体)信号通路[80]。然而,这确实需要在未来的研究中得到证实。此外,应该强调的是,训练强度和持续时间也可能在运动训练对cachectic COPD的迟钝反应中起关键作用。
很明显,从临床角度来看,预测单个COPD患者运动训练的有效性和反应程度仍然具有挑战性。运动限制的初始机制似乎影响肺部康复的运动结果[81]。最近的信息表明,在运动训练中出现股四头肌收缩性疲劳的COPD患者在功能性运动能力和与健康相关的生活质量方面表现出更大的训练效果[75]。对运动训练有反应的慢性阻塞性肺病患者的典型临床表现是,他们的运动耐受性差主要与骨骼肌薄弱有关(即。疲劳)而不是呼吸限制/约束[66,81]。因此,由此得出的推论是,“非疲劳者”从康复中获得的好处应该少于“疲劳者”。然而,这并不完全正确,因为最近的研究表明,即使在“非疲劳者”中,康复后的运动耐受力也有所提高[75]。情况非常复杂,可能涉及其他几个因素,如用力呼吸困难、呼吸限制/约束、动态肺过度膨胀和缺乏动力。目前正在研究提高肺部康复反应率的策略。第一步是优化药物治疗[82]。氧(83], heliox [84]、无创通气[85]、间歇训练[86]、单腿运动[87]和营养支持作为运动训练的辅助手段[88,89]是药物和非药物干预的例子。
未来需要解决几个未解决的问题:1)从研究角度和临床角度定义无反应;2)目前尚不清楚在运动训练后表现出全身炎症介质水平降低或局部肌肉TNF-α和IL-6表达降低的非病毒性COPD患者(至少40%)外周肌肉中发生了什么;3)病毒性慢阻肺患者康复后运动能力提高的机制尚不清楚,尽管周围肌纤维的表型适应比非病毒性慢阻肺患者少,但其潜在生理学仍有待进一步了解;4)病毒性慢阻肺患者运动训练反应中呼吸受限和用力性呼吸困难的潜在调节作用尚不清楚,需要进一步探讨;5)运动训练已被证明可以逆转一些与去条件化相关的代谢异常,并改善运动耐受性;但是,需要优化培训方案;6)什么是最好的干预方法:单独补充营养或合成代谢补充剂或与运动相结合;7)营养补充品:蛋白质含量高(占总热量的20%),或碳水化合物多于脂肪,或富含抗氧化剂?8)合成代谢剂、生长素(促氧特性)、N-3多不饱和脂肪酸的作用,以及最近过氧化物酶体增殖物激活受体的参与;9)在特定的患者中,如病毒性慢性阻塞性肺病患者,一种有希望的方法是将适当增加的热量摄入(直到体重恢复)与肌肉训练相结合; and 10) the involvement of other organs (如。脂肪组织)和全身炎症中的身体成分(变化)。
尽管如此,即使考虑到无应答者的比例,肺康复仍然是一种非常有效、安全和有效的干预措施,可以改善COPD患者的生活质量、呼吸困难和运动耐受性。
动态恶性通货膨胀、肺部炎症和慢性阻塞性肺病急性加重之间复杂的相互作用尚未完全阐明。恶性通货膨胀是否会导致慢性阻塞性肺病的炎症后果,以及恶性通货膨胀如何反过来恶化。
静止时(静态恶性通货膨胀)和运动时(动态恶性通货膨胀)发生的恶性通货膨胀和加重是COPD的两个关键特征。它们的存在深刻地影响了疾病的临床表现,因为它们与呼吸困难有关[90],运动不耐受[90],负能量,平衡/体重下降,用力呼气量在1 s内下降较快[91,92]和生活质量差[93]。因此,更好地了解慢性阻塞性肺病这三个特征之间的相互作用似乎对帮助开发更有效的治疗干预措施很重要。恶性通货膨胀和恶化可以被认为是相互独立的:恶性通货膨胀通常被认为是纯粹的机械事件,而恶化则被描述为炎症现象,其特征是气道和全身炎症的恶化[94,95]。慢性阻塞性肺疾病中呼吸系统的机械紊乱是否会导致炎症状态,最近有讨论[96]。支持这一理论的最具说服力的证据来自重症监护和急性呼吸窘迫综合征领域,表明肺过度膨胀可能与体循环中肺释放的促炎细胞因子有关[97]。相反,据报道,旨在最小化过度膨胀的机械通气策略可以减少全身促炎细胞因子反应[98]。根据这些数据,我们很容易推测类似的全身性炎症反应也可能与COPD中动态恶性通货膨胀的发生有关。然而,只有很少的证据支持这一概念。例如,我们知道运动可能与慢性阻塞性肺病患者体循环中炎症标志物的增加有关,特别是在存在恶病质的情况下[50,51]。然而,尚不确定这种免疫反应是来自肺的扩张还是来自肢体肌肉的收缩和/或炎症细胞的激活。沿着这条线,应该注意的是,健康受试者也表现出与运动相关的免疫反应,尽管这些个体在运动期间的肺体积保持稳定甚至减少。这使得很难将COPD的免疫反应仅仅归因于动态恶性通货膨胀的存在。
关于过度膨胀对慢性阻塞性肺病炎症的潜在影响的证据只是间接的,并且可能相互矛盾。单独吸入皮质类固醇对COPD相关气道炎症的影响并不大[99但据报道与全身炎症的减少有关[One hundred.,101]以及最近的肺部收缩效果[102]。这似乎证明了COPD患者肺部过度扩张的潜在炎症作用。相反,肥胖的慢性阻塞性肺病患者与瘦弱的患者相比,肺容量更低[103]同时表现出更大程度的全身炎症[104不支持恶性通货膨胀是这种疾病产生系统性炎症反应的主要因素的观点。事实上,与肺容量减少明显相关的肥胖是慢性阻塞性肺病全身性炎症水平的一个强有力的预测指标。
目前的证据还不能确定COPD患者肺过度扩张与全身性炎症之间的潜在关系。与此同时,最常见的炎症事件的恶化也与呼吸系统内的机械紊乱有关,包括恶性通货膨胀的恶化[105,106]。考虑到急性加重目前是基于呼吸困难恶化来定义的,这些调节呼吸困难感知的机械紊乱是定义和识别急性加重的核心。因此,可以设想这是一个恶性循环,恶化促进肺部过度膨胀进一步恶化,而过度膨胀反过来又可能促进更多的炎症和肺功能恶化[96]。
本次研究研讨会的出发点是众所周知的慢性阻塞性肺病患者缺乏身体活动,多年来人们一直将其归咎于外周肌肉功能和呼吸功能异常,这反映在肺力学和气体交换上。主要的首要问题是,是否部分责任也在于全身性炎症,如果是,如何归咎于全身性炎症。
一些证据确实表明,慢性阻塞性肺病与全身性炎症有关,这可能导致心血管系统、代谢和骨骼肌的后果(合并症?)然而,这些来自形态学、生化和生理指标的证据最近才开始深入研究,其本身就有些难以解释,因此,尽管这些合并症明显存在,但它们是否与COPD的系统性后果有关本身(促炎介质从肺部“溢出”到体循环)或仅仅导致衰老(COPD患者通常是老年人)或独立于合病条件的临床COPD表型,目前尚不清楚。
部分问题还在于,我们仍然不完全清楚运动是否具有抗炎或促炎作用,以及局部和/或全身炎症是否对肌肉收缩性(疲劳)有有害影响与非疲劳者),是否会导致肌肉萎缩(恶病质)与非恶病质)以及它是否对COPD患者康复期间运动训练的反应有临床意义(响应者)与无)。部分问题还来自于什么是最合适的运动测试(骑自行车)与走)107,模式(增量)与恒定工作速率)[108],强度和持续时间[108]以及比较COPD和合并症患者运动的最合适的对照对象。
该小组的共识是,对COPD患者的适当评估需要一种综合的方法,将所有潜在的系统性表现考虑到多维图像中。在这种背景下,了解慢性呼吸、心血管和代谢疾病之间相互作用的性质和程度是21世纪的一项重要医学挑战,如果不能解决这一新的现实,只会助长这一现象的发展,并造成无与伦比的不良健康后果。总之,本次研讨会提出了广泛的研究方向(表1),以便更好地了解身体活动、营养状况与COPD患者肺部和全身性炎症之间的关系。希望这些将导致药理学和非药理学的进步,不仅可以提高生活质量,而且可以延长它面对目前令人失望的功能结果,从少数可用的治疗方法。
致谢
ERS研究研讨会教员的成员如下:P. Laveneziana(联合主席;巴黎,法国),P.帕朗热(联合主席;M. Decramer(比利时鲁汶)、L. Puente-Maestú(西班牙马德里)、F. Maltais(加拿大魁北克)、R. Rabinovich(英国爱丁堡)、I. Vogiatzis(希腊雅典)、T. Troosters(比利时鲁汶)、H.R. Gosker(荷兰马斯特里赫特)、A. Schols(荷兰马斯特里赫特)、G. Scano(意大利佛罗伦萨)和E. Barreiro(西班牙巴塞罗那)。
参与者(ERS研究研讨学院的52 + 2名ERS科学活动助理如下:A. Neder(巴西)、A. Bellocq(法国)、R. Garrod(法国)、A. Huertas(法国)、L. Laviolette(法国)、V. Andrianopoulos(希腊)、Z. Louvaris(希腊)、S. Stavroula(希腊)、A. Aliverti(意大利)、E. Clini(意大利)、G. Mileti(意大利)、K. Wadell(瑞典)、S. Ward(英国)、B. Marinov(保加利亚)、A. Chambellan(法国)、F. Costes(法国)、E. Kortianou(希腊)、I. Nasis(希腊)、M. Vasilopoulou(希腊)、S. Devi Perumal(印度)、G. Fiorenzano(意大利)、D. Savi(意大利)、A. Chwist-Nowak(波兰)、D.L. Ardelean(罗马尼亚)、B. Nadezda(俄罗斯)、P. Joppa(斯洛伐克)、R. Zwick(奥地利)、P. Gagnon(加拿大)、B. Lemire(加拿大)、F. Ribeiro(加拿大)、R. de Paula Vieira(德国)、P. Roussi(希腊)、E. Bernardi(意大利)、B. Binazzi(意大利)、M. Brunori(意大利)、C. Coli(意大利)、R. Duranti(意大利)、F. Gigliotti(意大利)、G. Innocenti Bruni(意大利)、B. Lanini(意大利)、I. Presi(意大利)、I. Romagnoli(意大利)、W. Altenburg(荷兰)、T.E. Eriksen(挪威)、M. Emtner(瑞典)、J. Hartman(荷兰)、P. Klijn(荷兰)、D. Inal-Ince(土耳其)、D. Yilmaz(土耳其)、P. Collins(英国)、E. Gagliardi(意大利)、V. Rebeaud和L. Monnot (ERS科学活动助理,瑞士)。
脚注
支持声明
该研究研讨会由ERS赞助,由勃林格殷格翰公司(意大利)和辉瑞公司(意大利)提供无限制的资金支持。
利益声明书
对本研究感兴趣的声明可在www.www.qdcxjkg.com/site/misc/statements.xhtml
- ©2012人队















