文摘
治疗急性肺损伤(ALI)在重症监护医学仍然是一个尚未解决的问题。激活和招募中性粒细胞被视为阿里的发展的重要机制。吡格列酮拥有强大的多效性的抗炎作用,在阿里,我们探索了它的影响。
C57Bl / 6小鼠暴露于aerosolised脂多糖(lps)(μg·500毫升−1)和肺泡间质和血管内中性粒细胞4 h后评估。肺渗透率变化评价荧光素isothiocyanate-dextran间隙和支气管肺泡灌洗液中蛋白质含量。在体外,人类使用piolitazone孤立的中性粒细胞(10μM 1或3 h),然后激活N甲酰-l-methionyl -l-leucyl -l苯丙氨酸。中性粒细胞激活、附着力、发布和活性氧(ROS)的形成和吞噬作用是测量。
吡格列酮治疗之前或之后诱导ALI显著减少肺泡(分别减少了73%和67%)和间质嗜中性粒细胞涌入(分别减少了55%和63%)和降低肺通透性改变(分别减少了64%和58%)表明吡格列酮治疗ALI的保护作用。此外,吡格列酮显著降低脱粒和中性粒细胞粘附在不影响ROS形成和释放或细菌的吞噬作用。
吡格列酮可以降低招聘和激活中性粒细胞从而防止LPS-induced阿里。我们的研究结果暗示吡格列酮治疗的潜在作用阿里的管理。
急性肺损伤(ALI)是一种危及生命的疾病的年龄调整患病率每年每100000人86.2 (1]。尽管在重症监护医学创新,阿里的死亡率仍高达40%。阿里的特点是alveolar-capillary障碍导致的渗透率增加肺部水肿和富含蛋白质的液体因此导致动脉氧化损伤。脓毒症是阿里发展的一个主要原因,其中革兰氏阴性细菌均占据主导地位。脂多糖(LPS)吸入模仿人类的革兰氏阴性阿里,诱导中性粒细胞招募,肺部水肿,最后损害的气体交换2]。招募中性粒细胞是阿里的发展的一个关键事件1,3),导致等离子体氧化渗漏和恶化。中性粒细胞的重要性在阿里支持研究肺损伤是废除了损耗的中性粒细胞(4,5]。neutrophil-dependent阿里的大部分是由颗粒蛋白释放激活中性粒细胞。例如,azurocidin和α-defensins隐含直接改变磁导率的变化(6,7),而中性蛋白酶的来源,如中性粒细胞弹性蛋白酶,已经提出重要的表面活性剂的降解蛋白质,上皮细胞凋亡和凝固8,9]。此外,中性粒细胞产生大量的活性氧(ROS)和活性氮物种。除了他们重要的抗菌效应函数,neutrophil-derived氧化剂促进有害的促炎效应,因此在阿里neutrophil-dependent组织损伤的主要原因(3]。
过氧物酶体proliferator-activated受体(PPAR)被称为转录因子属于核激素受体超家族。配体依赖性转录因子PPARs是,包含三个亚型(α、β和γ)被独特的基因编码。除了它们的重要性在脂类和碳水化合物代谢的规定,PPARs,尤其是PPAR-α和PPAR-γ,收到关注的强有力的抗炎作用[10]。先前的研究已经表明,PPAR-γ配体减少炎性细胞因子基因的表达和炎性细胞因子的生产(11,12]。因此,PPAR-α和PPAR-γ受体激动剂可能有助于治疗急性炎症性疾病,如阿里(13]。在这种背景下,几项研究已经证明PPAR-γ受体激动剂的有益作用的模型过敏性气道炎症和bleomycin-induced阿里14,15]。
虽然之前在体外和在活的有机体内研究揭示了吡格列酮的抗炎作用,较少的已知影响吡格列酮在阿里的中性粒细胞。招募中性粒细胞,释放颗粒蛋白和一代的ROS的中性粒细胞在阿里和显示关键事件可能是一个合适的潜在的治疗目标。因此,我们地址吡格列酮治疗的效果neutrophil-dependent阿里的典范。
方法
动物
8-week-old雄性C57Bl / 6小鼠获得Janvier SAS (Le Genest圣岛,法国)。中性粒细胞减少腹腔内注射的Ly6G-specific单克隆抗体1 a8(100μg /鼠标前12 h和0 h有限合伙人吸入;BioXcell、西黎巴嫩,美国NH)。小鼠完整的白细胞计数与吡格列酮治疗(2μg / g(体重)或氯化钠0.9%,腹腔内注射LPS吸入前12 h和0 h支持1 h有限合伙人吸入后,分别。所有的实验都经当地伦理当局批准。
小鼠模型的阿里
Aerosolised有限合伙人的肠炎沙门氏菌(Sigma-Aldrich有限公司,圣路易斯,密苏里州,美国)溶解在0.9%盐水(μg·500毫升−1)是利用诱导肺中性粒细胞浸润。六个老鼠暴露同时aerosolised有限合伙人在一个定制的盒子(22厘米直径10厘米)连接到一个空气nebuliser (MicroAir;欧姆龙医疗、弗农山、美国IL) 30分钟。八个控制小鼠盐气溶胶暴露。嗜中性粒细胞计数在支气管肺泡灌洗液(BALF)和肺组织(间质和肺血管)评估4 h后吸入。30分钟前安乐死,5μL anti-mouse-Ly-6G (Gr-1)异硫氰酸荧光素(FITC) (Gr1一起;美国圣地亚哥eBioscience CA)和100μl FITC-dextran·毫升(30毫克−1FITC-dextran, 70 kDa;Sigma-Aldrich有限公司)通过尾静脉注射血管内中性粒细胞的标签。老鼠anesthetised的腹腔内注射氯胺酮(125毫克/公斤体重;Sanofi-Cefa GmbH,杜塞尔多夫,德国)和甲苯噻嗪(每公斤体重12.5毫克;凤凰科学、圣约瑟夫,密苏里州,美国)。气管是解剖和插管(PortexFineBore聚乙烯管材,0.28毫米内径/外径0.61毫米;美国史密斯医疗国际,基恩,NH)。5×0.5毫升PBS注入和撤回。此后,胸腔被打开了中线切口和肺血管是冲洗与0.5毫米15毫升冰冷的PBS EDTA切下后静脉静脉促进放血。肺被移除,剁碎和消化liberase(1:20, 25毫克liberase RI·毫升−1水;罗氏公司,德国曼海姆)。消化肺细胞通过过滤器(70μm;Miltenyi研究GmbH, Bergisch格拉德巴赫,德国)和由此产生的单细胞悬液在300 g离心5分钟。丸resuspended在1毫升汉克的平衡盐溶液0.3更易·L−1EDTA和0.1%牛血清白蛋白(BSA)。BALF离心5分钟在300 g(图S1)。
流式细胞术
细胞颗粒被贴上PerCP-Cy5.5 anti-mouse Ly-6G、PE anti-mouse CD115, APC-Cy7 anti-mouse CD45和APC anti-mouse F4/80 (eBioscience)。中性粒细胞被确定典型的外观在向前散射散射和CD45 + CD115 -和PerCP-Gr1 +细胞(图S2)。在肺内,FITC-Gr1抗体被用来区分间质中性粒细胞(CD45 + CD115, PerCP-Gr + FITC-Gr1)和血管内中性粒细胞(CD45 + CD115, PerCP-Gr1 + FITC-Gr1 +)。流式细胞术研究使用BD流式细胞仪进行第二章(美国加利福尼亚州圣何塞,正欲)和数据分析使用FlowJo软件(美国或树明星,亚什兰)。
肺通透性
FITC-dextran被用来评估血管渗漏。100年μL FITC-dextran·毫升(30毫克−1)是由尾静脉注射安乐死和染料外渗前30分钟是用来评估血管通透性的变化。100的荧光μL BALF上层清液(氟BALF)和50μL血清(氟血清)测量和渗透率成交量μL表示:
BALF的蛋白质浓度
BALF的蛋白质含量上层的评估使用Bio-Rad蛋白质测定方法的基础上,布拉德福德(Bio-Rad实验室GmbH,慕尼黑,德国)。在595纳米测量吸光度进行标(无限®200专业版;瑞士Mannedorf Tecan集团有限公司)。
组织学和电镜
实验完成后,对肺的一部分在福尔马林固定,嵌入在石蜡和梅耶的苏木精和伊红染色组织学检查。肺的另一部分是准备扫描电镜如前所述5]。
中性粒细胞隔离
从健康的捐赠者人类中性粒细胞(男性年龄在25 - 35岁,没有药物)被孤立是前面描述的(16]。中性粒细胞与吡格列酮10μM孵化1或3 h。
脱粒
与吡格列酮孵化后,中性粒细胞激活通过添加10毫米N甲酰-l-methionyl -l-leucyl -l苯丙氨酸(fMLP;Sigma-Aldrich有限公司)和upregulation CD11b和CD29使用BD流式细胞仪测量30分钟后第二章。
流室
我们涂培养皿与纤连蛋白或细胞间粘附分子(ICAM) 1(1μg·毫升−1+ 10% BSA)层流室。中性粒细胞与吡格列酮治疗(10μM 1或3 h)。与fMLP激活后,中性粒细胞在1达因·厘米灌注−2纤连蛋白或ICAM-1和牢牢地附着中性粒细胞量化4分钟后在多个字段(至少六个字段×100放大)。
吞噬作用
荧光大肠杆菌和opsonising试剂(分子探针,尤金,或者美国)被重组的制造商。免疫球蛋白(Ig) G opsonisation实现根据制造商的指示。补充opsonisation被孵化获得的细菌与新鲜的人类血清37°C 1 h。Opsonised粒子被清洗和播种到中性粒细胞,也一直与吡格列酮10μM孵化1或3 h。荧光与BD流式细胞仪测定30分钟后第二章。
活性氧
ROS是探测到dihydrodichlorofluoresceindiacetate贴现;分子探针)如前所述17]。基本上,细胞profluorescent孵育,亲脂性的H2-DCF-DA,这可以通过细胞膜扩散。反应和细胞内活性氧导致荧光分子DCF(最大发射∼530海里),因此,DCF荧光可以作为测量细胞内ROS水平。荧光强度与流式细胞仪量化30分钟后第二章。同样,细胞外活性氧测定单线态氧传感器绿色试剂(欧洲分子探针,莱顿、荷兰)推荐的制造商。
统计数据
所有数据都表示为±sd。进行了统计计算使用GraphPad棱镜5 (GraphPad软件公司,圣地亚哥、钙、美国)。未配对t, Mann-Whitney测试或测试与克鲁斯卡尔-沃利斯事后邓恩测试使用。
结果
吡格列酮保护neutrophil-dependent阿里
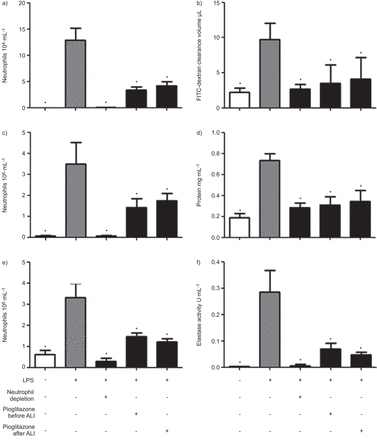
在C57Bl / 6小鼠暴露于aerosolised脂多糖,我们观察到中性粒细胞招聘、等离子体泄漏,肺(超)结构,弹性蛋白酶BALF中活动。有限合伙人治疗血管内的数量增加,间质和肺泡中性粒细胞通过流式细胞术分析(图S2)肺匀浆和BALF (图1)。此外,蛋白质浓度,以及荧光右旋糖酐的间隙,增加了有限合伙人的BALF治疗,从而表明增强型等离子体泄漏和水肿的形成。此外,neutrophil-derived弹性蛋白酶的活性,在阿里蛋白酶重要,高架在LPS-treated动物(图1)。中性粒细胞减少破坏肺泡液体射流和结构性变化,证实了先前描述的重要性在阿里中性粒细胞(图1)。测试这个模型的吡格列酮的潜在作用neutrophil-mediated阿里,老鼠用吡格列酮治疗前有限合伙人曝光。在这些实验中,我们发现,吡格列酮降低了招聘的中性粒细胞在血管内,有限合伙人吸入后肺间质和肺泡腔室(图1)和预防增强肺血管渗漏表示通过蛋白质含量降低BALF和FITC-dextran余隙容积(图1)。此外,吡格列酮治疗1 h阿里感应后表现出类似的效果(图1)。肺LPS暴露后的组织学和超微结构分析显示肺泡间隔增厚,炎性细胞的聚集间质和肺泡,并富含蛋白质的液体流入到肺泡空间相比控制小鼠暴露于aerosolised生理盐水。吡格列酮之前(图2)和(数据未显示)有限合伙人吸入后废除这样的组织学改变,进一步支持neutrophil-mediated阿里的保护作用。
吡格列酮可以降低脂多糖(LPS)全身急性肺损伤(ALI)的中性粒细胞招募的干扰。老鼠与有限合伙人的挑战通过吸入和牺牲4 h后。此外,耗尽了中性粒细胞抗体注射或老鼠piogliatzone处理(2μg / g体重),前12 h和1 h或1 h有限合伙人曝光后表示。量化的)肺泡c)间质和e)在小鼠血管内中性粒细胞作为表示。肺灌洗和b)荧光素isothiocynate (FITC)右旋糖酐间隙,d)蛋白质浓度和f)弹性蛋白酶活动评估支气管肺泡灌洗液的老鼠视为表示。控制n = 8,有限合伙人n = 10,有限合伙人+中性粒细胞减少n = 9,吡格列酮n = 8。*:与LPS-treated动物相比p < 0.05。
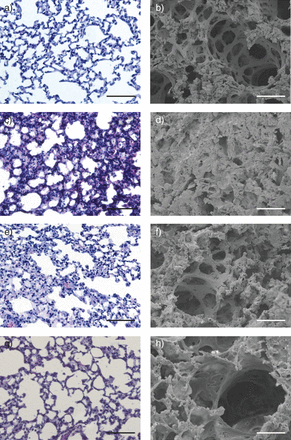
全身的吡格列酮可以防止脂多糖(LPS)肺组织结构变化。a、c、e和g)代表组织学和b, d, f和h)的扫描电子显微镜图像从小鼠肺治疗如下:a和b)控制;c和d)有限合伙人;e和f)吡格列酮在有限合伙人;g和h)有限合伙人后吡格列酮。为每个组(n = 5。a、c、e和g) = 250μm规模酒吧。b, d, f和h) = 50μm规模酒吧。
吡格列酮可降低中性粒细胞粘附ICAM-1和纤连蛋白
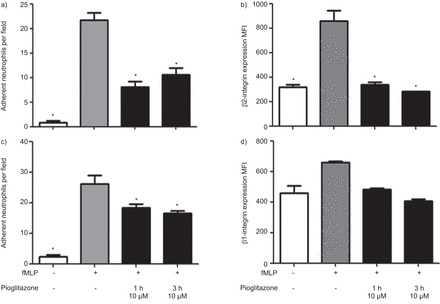
我们的在活的有机体内突出中性粒细胞招募的直接还原的数据与吡格列酮治疗。进一步证实这个想法,我们分析了吡格列酮对灌注孤立的人类中性粒细胞粘附的影响在固定ICAM-1 (图3)。中性粒细胞与吡格列酮治疗1 h和3 h 10μM ICAM-1严重减少粘连。对中性粒细胞恪守ICAM-1β2-integrins的upregulation分泌囊泡是一个先决条件。这样的转变是由促分泌素,如细菌肽fMLP墙。因此,我们分析了吡格列酮对fMLP-inducedβ2-integrin upregulation中性粒细胞。经过活化的中性粒细胞与fMLPβ2-integrin的表达明显升高(图3)。吡格列酮(10μM 1或3 h)显著降低β2-integrins fMLP-induced表达式(图3),从而提供了一个解释降低粘附ICAM-1后吡格列酮治疗。
吡格列酮影响中性粒细胞粘附细胞间粘附分子(ICAM) 1、纤粘连蛋白。孤立的人类中性粒细胞与吡格列酮预处理(10μM, 1和3 h),然后激活N甲酰-l-methionyl -l-leucyl -l苯丙氨酸(fMLP)。一)中性粒细胞被灌注固定重组ICAM-1 1达因·厘米−2枚举和贴壁细胞的数量。n = 8 - 10。b)平均荧光强度(MFI) surface-expressedβ2-integrin以流式细胞术染色后直接共轭抗体。n = 3 - 6。c)中性粒细胞被灌注固定纤连蛋白1达因·厘米−2枚举和贴壁细胞的数量。n = 8 - 10。d)的MFI surface-expressedβ1-integrins以流式细胞术染色后直接共轭抗体。n = 3 - 6。*:fMLP组相比p < 0.05。
作为血管外的运动的中性粒细胞β1-integrins是至关重要的,我们测试了吡格列酮的影响在β1-integrin upregulation和中性粒细胞粘附β1整合蛋白底物纤连蛋白。流室实验显示显著降低中性粒细胞的粘附纤连蛋白与吡格列酮预处理后(10μM) 1或3 h (图3)。治疗与fMLP导致中性粒细胞的趋势增加纤连蛋白配体的表面表达α5β1-integrin,预处理的效果完全逆转与吡格列酮(图3)。
吡格列酮并不影响中性粒细胞抗菌活性
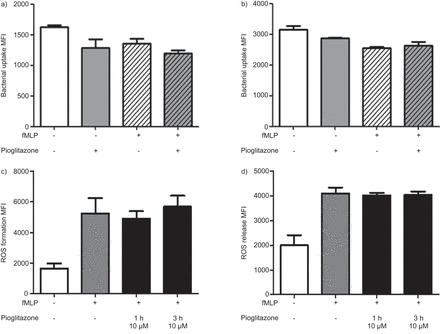
除了他们的贡献阿里,中性粒细胞在细菌感染显示重要的抗菌效应功能。分析如果吡格列酮的有益的抗炎效果不影响这些功能,我们测试了pioglitazone-treated中性粒细胞吞噬细菌的能力。IgG-opsonised吞噬作用(图4)或complement-opsonised (图4 b)FITC-labelled大肠杆菌被流式细胞术进行评估。而细菌吸收补充opsonisation后中性粒细胞增加免疫球蛋白g opsonisation相比,吡格列酮不会大幅改变细菌吸收。
吡格列酮并不影响中性粒细胞抗菌活性。细菌的荧光免疫球蛋白G - b) complement-opsonised大肠杆菌通过流式细胞仪或休息时,中性粒细胞的激活。中性粒细胞激活了N甲酰-l-methionyl -l-leucyl -l与吡格列酮苯丙氨酸(fMLP)和预处理。n = 4。孤立的人类中性粒细胞与吡格列酮预处理(10μM, 1和3 h)。c),中性粒细胞被贴上敏感染料2′,7′二乙酸-dichlorodihydrofluorescein和活性氧(ROS)生成记录fMLP刺激后通过流式细胞术。数据显示平均荧光强度(MFI) fMLP曝光后30分钟。n = 6。d)中性粒细胞与单线态氧贴上绿色标记的细胞外释放活性氧。数据显示MFI fMLP曝光后30分钟。n = 6。数据意味着±sd。
进一步粘附和迁移,中性粒细胞释放活性氧导致阿里。然而,ROS也显示中性粒细胞中重要的抗菌功能。因此,我们调查了吡格列酮对活性氧的影响形成和释放的孤立的人类fMLP引起的中性粒细胞。从健康的捐赠者隔离后中性粒细胞,中性粒细胞孵化了吡格列酮(10μM) 1或3 h . fMLP明显诱导活性氧的形成和释放。然而,吡格列酮预处理未能影响ROS生成(图4摄氏度)和(图4 d吡格列酮),从而暗示不损害中性粒细胞抗菌活性和吡格列酮的保护作用并不源于对活性氧释放的影响。
讨论
尽管在重症监护医学创新,阿里革兰氏阴性细菌引起的仍然是一个重大的挑战。在我们的研究中,我们将演示有益阿里的吡格列酮治疗的减少水肿形成和嗜中性粒细胞浸润,两者都是阿里的关键事件在开发过程中。
PPAR-α和-γ受体激动剂开发dyslipidaemia和2型糖尿病的治疗。然而,最近的研究显示额外的有利影响动脉粥样硬化和炎症性疾病,由稳定内皮功能的部分解释18,19]。PPAR-α受体激动剂的保护作用中的fibrate类LPS-induced肺损伤曾成立(20.]。与记录PPAR-γ控制中性粒细胞迁移的重要性(21),我们调查glitazones的影响,这可能会直接降低中性粒细胞的激活和招聘,一个过程,重要的是会导致组织损伤在阿里3]。因此,我们分析了吡格列酮对中性粒细胞活性的影响。中性粒细胞浸润的重要性LPS-induced阿里证实在中性粒细胞粘附模型或迁移受损。在这种情况下,这是表明缺乏CXCR2或β的封锁2整合蛋白保护从阿里22,23]。在我们的研究中,吡格列酮预防血管内中性粒细胞粘附和肺浸润。这是一个解决在体外试验在缺乏其他细胞但在基质的存在通常参与中性粒细胞粘附和迁移,我们得出这样的结论在活的有机体内影响可能在很大程度上,与直接干扰β1-integrins和β2-integrins的表面表达。我们的结果与之前的研究相一致,显示了单核细胞粘附于内皮细胞表明吡格列酮的保护作用在急性炎症(24]。有趣的是,在我们的研究中,我们发现了类似的吡格列酮治疗后效果有限合伙人吸入治疗前相比,有限合伙人吸入。这是有趣的,这种模式的治疗可能依赖于迅速发生抗炎活动。一个可能的解释可能是内皮细胞粘附分子的表达(25,26]。特别是减少表达P-selectin glitazones治疗后可能为中性粒细胞减少招聘提供一个解释26]。此外,减少氧化应激(27和减少脂质介质的释放28)在回应glitazones可能提供替代解释减少中性粒细胞肺浸润LPS吸入后开始治疗时。
快速upregulationβ2-integrins中性粒细胞通常动员的结果的预成型的颗粒。β2-integrins局部分泌囊泡,一个隔间出院时neutrophil-endothelial交互建立。分泌小泡也富含azurocidin [29日),相关的蛋白质以前neutrophil-mediated渗透率变化(5,30.,31日]。因此,减少表面后β2-integrins fMLP刺激不仅解释了粘附能力下降,但也可能指向受损释放颗粒与阿里相关的蛋白质。与此一致的是,我们发现降低BALF弹性蛋白酶活动从老鼠用吡格列酮治疗。弹性蛋白酶加剧阿里通过增加内皮和上皮通透性(32,33(表面活性剂),蛋白水解乳沟蛋白质34和诱导细胞凋亡35]。的在活的有机体内中性粒细胞弹性蛋白酶在阿里的重要性的研究进一步证实了使用elastase-deficient老鼠(36)或使用特定抑制剂(37]。尽管活性氧的释放是一个重要的抗菌机制,生产过剩的活性氧会导致组织损伤在脓毒症和阿里38]。在动物模型的阿里,neutrophil-derived活性氧引起肺损伤,如通过组织学检查和渗透率测量(39,40]。此外,它已被证明,ROS能破坏内皮细胞间紧密连接的粘着斑激酶的磷酸化(41]。因此,不足或封锁还原型烟酰胺腺嘌呤二核苷酸磷酸氧化酶防止阿里(38,42,43]。然而,在我们的研究中,吡格列酮未能影响活性氧释放。因此,吡格列酮的保护作用主要来自于减少中性粒细胞脱粒,附着力和招聘。
迁移后,中性粒细胞在细菌不可替代的间隙,其中大部分是由吞噬作用和细胞内的细菌杀死44]。数据从我们的研究表明,吡格列酮不影响细菌吸收和间隙,所评估的ROS形成实验。因此,这些数据表明,吡格列酮可能不会损害间隙在细菌感染,因此,进一步支持它的临床适用性。然而,进一步在活的有机体内研究评价吡格列酮对细菌的影响所需的间隙在更广泛的环境。
结论
吡格列酮变弱的招聘和激活的中性粒细胞在阿里的典范,因此,显示有利影响。此外,吡格列酮治疗后出现阿里是有效治疗ALI发病之前,暗示潜在角色glitazones在阿里的管理。
确认
作者希望承认x Balaj, Roubrocks和s·温克勒(,分子心血管研究所(IMCAR),亚琛工业,亚琛,德国)为他们的优秀的技术援助。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明
本研究支持的德意志Forschungsgemeinschaft德国心脏基金会、Else-Kroner-Fresenius基金会和b·布劳恩基金会。
感兴趣的语句
没有宣布。
- 收到了2011年5月29日。
- 接受2011年11月24日。
- ©2012人队