编辑:
多种亚型一氧化氮(NO)合成酶在人气道和血管内皮细胞中组成性表达,不断产生NO。NO在调节肺功能方面发挥着重要作用,包括调节肺血管阻力、气道口径和宿主防御。NO的产生和通过液相反应消耗可以在呼出的空气中检测和监测,这为评估健康和炎症性肺部疾病(特别是哮喘)中NO代谢动力学提供了一个重要窗口1。
一系列具有里程碑意义的研究发现,囊性纤维化(CF)患者肺NO相对缺乏,囊性纤维化是一种严重的慢性炎症性肺部疾病,研究普遍显示呼出NO减少2,3.。然而,对于无缺陷的解剖定位和机制,以及其与CF疾病进展的关系仍存在争议。通过使用不同呼气流速下的呼气NO分析,间接研究试图根据基本模型将NO产生区分为支气管和肺泡腔4- - - - - -7。然而,在这些患者中,没有证据表明NO直接注入肺泡的命运。我们的目的是通过评估气管插管肺移植患者终末期CF中内源性呼出NO和静脉注射硝酸甘油(GTN)肺微血管代谢产生呼出NO的动力来探讨这些问题。8。
如前所述,使用实时、计算机控制和集成系统(Logan Research Ltd 2000和3000系列,英国罗彻斯特)对下气道中的NO浓度进行呼吸-呼吸潮汐测量[8],详细情况见在线补充资料。
目的探讨7例终末期CF患者下气道气相NO浓度(平均年龄26岁;对5男2女)行全麻醉气管插管及机械通气诱导肺移植患者进行研究。CF患者与常规心内直视手术行冠状动脉搭桥术(CABG;4例)术前呼吸功能检查及胸片常规评价肺功能正常(平均年龄56岁)。研究得到医院伦理委员会的批准,并得到患者的书面同意。
在麻醉诱导后、移植患者在肺切除前、CABG患者在体外循环前进行基线测量,以评估内源性一氧化氮的产生和释放到气相。在血流动力学稳定的患者中,如前面所述,将250 μg GTN滴入中心静脉导管,记录呼出NO和动脉血压的变化8还有网上的补充资料。
在CF患者中发现几乎无法检测到的NO水平,在30秒内输出为7.6±6ppb。这与常规心内直视手术患者形成对比(30秒内91.4±21 ppb;图1)。代表性的轨迹显示在图1A和C的在线补充材料。
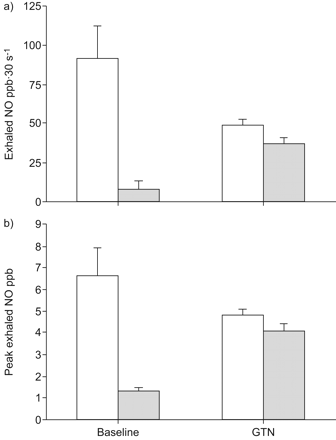
)曲线下的面积超过30 s和b)峰值呼出一氧化氮(NO)的内源性气相(基线)和呼出不应对250 -μg丸的硝酸甘油静脉管理(GTN)控制患者心内直视手术对冠状动脉旁路移植或终末期肺移植和囊性纤维化。GTN值代表基线上的变化。
在CF患者中,250 μg GTN bolgs的气相NO明显高于基线水平(36.7±6 ppb),这与常规心内直视手术对照组患者的气相NO水平(48.7±4 ppb;图1)。有代表性的gtn诱导的呼出NO的痕迹出现在图1B和D的在线补充材料。
这些发现为目前关于成人CF中NO交换动力学的争论提供了新的见解。尽管该疾病具有慢性炎症性质,但据报道呼出NO不变或较低,取决于疾病的严重程度2,4- - - - - -7。我们的研究调查通风接受肺移植的患者呼出没有清楚地演示了一个深刻的减少内源性气相没有孤立的降低航空公司的终末期CF患者。这个结论必须考虑两种方法论问题潮汐的测量没有呼出和高的潜在影响内源性二氧化碳(有限公司2)呼气时没有。然而,我们的对照组和CF患者的GTN实验使用了相同的方法。关于公司2在美国,我们还没有看到变化的内源性一氧化碳的主要影响2在3-6%之间(未发表的观察),但潜在的影响甚至更高端的潮汐CO2在CF患者不能排除。未发表的终末期肺动脉高压观察显示呼出NO保存较好,这也表明CF中内源性呼出NO的减少可能是独特的,不太可能是终末期肺疾病的结果本身。
CF相对无缺陷的确切机制尚不清楚。最近的研究使用了扩展的NO交换分析,得出了矛盾的结果,显示CF儿童和成人中没有改变、增加或减少支气管流量和/或肺泡NO浓度4- - - - - -7。新出现的共识表明,成人CF中NO缺乏的主要机制可能与支气管炎症增加和相关的NO合酶表达缺陷、活性和NO产生或产生的NO降解增加有关2,3.,6,9。后者可能涉及细菌机制、液相反应的催化和化学消耗以及通过高粘性黏液层的过程6,9。
本研究通过研究外源性硝酸甘油肺微血管代谢引起的NO通量,扩展了目前对肺泡NO交换机制的认识。我们的在活的有机体内对病人的研究似乎证实了体外观察Hennoet al。10关于硝普钠对CF肺动脉孤立血管环内皮独立舒张的保护作用。我们初步结果扩展这些研究微脉管系统和气道尤其是终末期的保留能力,这一举动隔间CF肺微血管构筑GTN和释放没有转化为增加消费的肺泡和航空公司没有证据在肺泡液体或气相。这与内源性NO释放的显著减少以及一些患者终末期CF相关的肺血管功能障碍的可能性有关7,10。综上所述,这些数据为CF中NO通路失调的支气管上皮和粘膜消耗假说提供了强有力的支持。此外,这些数据也提示CF气道可能是通过亚硝基血管扩张剂的肺代谢来治疗NO暴露的靶点。
脚注
感兴趣的语句
没有宣布
- ©2010人队















