文摘
的一个主要治疗策略在囊性纤维化旨在发展中调节器的囊性纤维化跨膜电导调节(雌性生殖道)通道。我们最近发现的甲基乙二醛α-aminoazaheterocycle加合物,作为一个新家庭的雌性生殖道抑制剂。在结构活性关系研究中,我们已经确定GPact-11a,复合能力,而不是抑制激活雌性生殖道。
在这里,我们现在在雌性生殖道GPact-11a活动使用的效果在体外(碘流出,荧光成像和膜片箝记录),体外(短路电流测量)和在活的有机体内(唾液分泌)实验。
GPact-11a我们报告:1)是雌性生殖道的活化剂在几个气道上皮细胞系;2)激活获救F508del-CFTR鼻、气管、支气管,胰腺癌细胞系和人类CF纤毛上皮细胞,刚从肺样本分离;3)刺激体外氯化结肠分泌和增加在活的有机体内的唾液分泌雌性生殖道+ / +但不是雌性生殖道−−/老鼠;和4)雌性生殖道的选择性,因为其效果是由雌性生殖道抑制异烟肼-172年,glyh - 101,格列本脲和GPinh-5a。
最后,这项工作识别选择性激活的野生型和F508del-CFTR获救。这个无毒、水溶性代理代表一个好的候选人,单独或结合F508del-CFTR校正器,雌性生殖道调制器在囊性纤维化的发展。
囊性纤维化跨膜电导调节(雌性生殖道蛋白质是cAMP-dependent ATP-gated氯通道,在顶端表面局部的,中介Cl- - - - - -transepithelial在航空运输,肠和其他液体运输组织1- - - - - -4。有缺陷的雌性生殖道的函数负责囊性纤维化(CF),最常见的一种,致命的人类常染色体隐性障碍的白种人。CF的主要临床问题反复肺感染,导致进行性肺恶化。超过1500的突变雌性生殖道已确定导致CF表型,∼90%的CF患者在一个或两个F508del突变雌性生殖道等位基因。的删除F508诱发走私,gating-defect雌性生殖道的蛋白质导致受损的频道活动即使出席了细胞的质膜5。
在发展中chloride-channel增强治疗CF,假设恢复Cl- - - - - -渗透率将正确的底层细胞缺陷导致肺部疾病。因此,寻找试剂修改雌性生殖道的活动是一个活跃的研究领域之一,主要治疗策略在CF。许多药理代理人能够加强cAMP-dependent雌性生殖道功能已确定6,7并称为“电位器”(例如染料木黄酮,vx - 770, alkylxanthines)。此外,一些种类的电位器,尽管在野生型CFTR (wt)检测非常有效的疗效有限F508del-CFTR突变体,如forskolin(移频键控),β2-adrenergic或A2B-adenosine受体受体激动剂6,8,9,其中一些缺乏选择性6,10和低亲和力11,12。另一类雌性生殖道调节器,称为雌性生殖道的“催化剂”,被选中的基础上他们的力量(低微摩尔的submicromolar范围)和他们的能力,诱导CFTR-dependent电致Cl- - - - - -运输的方式独立的阵营。
在先前的研究中,我们描述了一个新家庭的雌性生殖道抑制剂:甲基乙二醛的α-aminoazaheterocycle加合物;其中,核苷5(称为“GPinh-5a”;图1一个)是一种非常有效的雌性生殖道抑制剂13,14。这里,后结构活性研究中,我们确定了methylglyoxal-9-propyladenine加合物(图1 b5),一个模拟一个命名GPact-11a(格勒诺布尔普瓦捷雌性生殖道activator-11a),选择性,水溶性和wt和突变F508del-CFTR无毒催化剂。
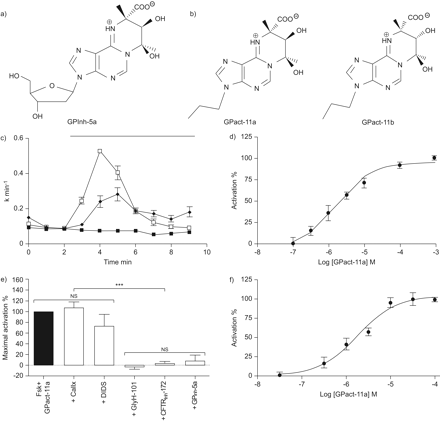
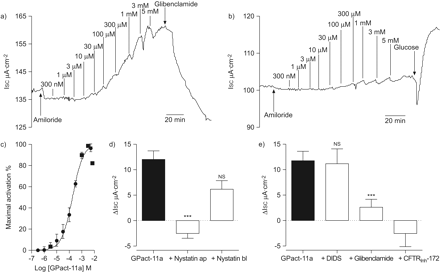
a、b)构造演化的甲基乙二醛α-aminoazaheterocycle囊性纤维化跨膜电导调节(雌性生殖道)抑制剂,GPinh-5a (a), CFTR methylglyoxal-9-propyladenine检测激活:GPact-11 (b),同分异构体的混合物,主要的对映体的混合物11一个和小11 b。c)典型碘射流实验显示由GPact-11a势差现象(100μM;□)和抑制GPinh-5a(1μM;▪)forskolin(移频键控、1μM)诱导反应wt-CFTR中国仓鼠卵巢(CHO)细胞(♦:移频键控)。上面的单杠跟踪表示药物的存在。d) GPact-11a的量效曲线存在移频键控(1μM) wt-CFTR CHO细胞。e)的影响glyh - 101(10μM),雌性生殖道异烟肼-172(10μM), GPinh-5a(200点),是(4 41-diisothiocyanatostilbene-2 21-disulfonic酸);100μM)和芳烃(杯;100 nM)移频键控(1μM) + GPact-11a(100μM)反应。f) GPact-11a的量效曲线存在Calu-3移频键控(1μM)的细胞。数据意味着±扫描电镜;为每个条件n = 4。ns:不重要的。* * *:p < 0.001。
材料和方法
化学
所有原料都是商用research-grade化学品和使用前未经纯化。被分析薄层色谱监测反应的荧光指示剂UV254 Macherey-Nagel (Duren,德国)。1H和13C核磁共振(NMR)谱记录在一个力量皇冠(美国麦迪逊,WI) 400(400和100 MHz)。化学变化是在ppm的残余信号相对于溶剂,和信号描述为单线态(s),广泛的单线态(bs),紧身上衣(d)、三联体(t)的紧身上衣,紧身上衣(dd),四方(q),多重态(m);耦合常数在赫兹报道。methyglyoxal商用集中水溶液(40%;1.5毫升,9.0更易)、9-propyladenine(480毫克,1.8更易)和水(5毫升)补充道。氩是刷新通过解决方案和混合加热50°C 17 h。蒸发压力降低后,残留的色谱仪使用C18反相(10 g)淋洗与h2O H,然后2O-methanol(甲醇)(95:5)给GPact-11a(24%)和GPact-11b (17%)。
GPact-11同分异构体的化学性质
GPact-11a。熔点:152 - 154°C;1H NMR (400 MHz, D2O): 8.84 (1 h, s, CH基于“增大化现实”技术),8.20 (1 h, s, CH基于“增大化现实”技术),4.53 (1 h, s, CH), 4.20 (2 h tJ= 7.0赫兹,CH2),1.87 - -1.81 (2 h, m, CH2),1.75 (3 h, s, CH3),1.67 (3 h, s, CH3),0.85 (3 h, t,J= 7.0赫兹,CH3);13C NMR (100 MHz, D2O): 176.6(羧基),146.8 (C四世),145.1 (CH基于“增大化现实”技术),142.7 (CH基于“增大化现实”技术),117.6 (C四世),89.2 (C四世),70.6 (CH)、63.3 (C四世),46.1 (CH2),25.7 (CH3),22.8 (CH2),22.2 (CH3),10.2 (CH3);lrm (FAB[+],甘油):m / z 322 ([m + H]+);元素分析计算出C14H19N5O41/3 H2H O: C 51.37, 6.06, 21.39 N,发现C 51.34, 5.98 H, 21.24 N。
GPact-11b。议员:102°C;1H NMR (400 MHz, D2O pH = 7,磷酸盐缓冲剂):8.72 (1 h, s, CH), 8.23 (1 h, s, CH) 4.21 (3 h, m, CH2和CH), 1.86 (5 h, m, CH2和CH3),1.74 (3 h, s, CH3),0.84 (3 h, t,J= 7.0赫兹,CH3),13C NMR (50 MHz, D2O, pH = 7,磷酸盐缓冲剂)176.1(首席运营官),146.5 (C四世),144.2 (CH基于“增大化现实”技术),144.0 (CH基于“增大化现实”技术),117.5 (C四世),74.1 (CH)、60.7 (C四世),45.5 (CH2),26.0 (CH3),24.4 (CH20 (CH), 18日3),9.6 (CH3),,8经(EI) calc. C14H19N5O4(M + H):+322.1515,322.1507,发现[M + Na]+344.1335,发现344.1343。
其他化学物质
3 - ((3-trifluoromethyl)苯基]5 - [(4-carboxyphenyl)亚甲基]2-thioxo-4-thiazolidinone(雌性生殖道异烟肼-172)和N(2-naphthalenyl) ((3 5-dibromo-2 4-dihydroxyphenyl)亚甲基)甘氨酸酰肼(glyh - 101)来自VWR国际(Fontenay-sous-Bois、法国)。GPinh-5a合成如前所述13。Miglustat从多伦多研究化学物质(多伦多,加拿大)。所有其他化学物质来自σ(圣路易斯,密苏里州,美国)。所有化学药剂都溶解在DMSO,除了GPact-11a, GPinh-5a,阿米洛利,miglustat和glyh - 101,溶解在H2啊,与异丙肾上腺素溶解在0.9%氯化钠。
细胞培养
细胞系培养如前所述:中国仓鼠卵巢(CHO), Calu-3,期刊/ CF1515,CF-KM4 MM3916,NuLi CuFi-117和CFPAC-118。HEK293细胞培养和瞬变转染pEGFP-CFTR wt或F508del已经描述19,20.。
新人类纤毛上皮细胞分离
这项研究是我们当地的机构伦理委员会批准。人类肺组织获得七个病人:三non-CF男性,平均年龄61岁,non-CF女性年龄在65岁,F508del / F508del-CFTR男性年龄在37岁,F508del / R1066C女性年龄在26岁和F508del / H1085R-CFTR女性年龄在23岁。叶切除术后,肺样本,远离恶性病变,很快被切割。切除后结缔组织、软骨和平滑肌组织,上皮组织是剪小段。单一的上皮细胞是机械分离通过支气管组织多次通过fire-polished巴斯德吸量管。分离人类上皮细胞纤毛被镀到文化菜6 h在培养基(杜尔贝科修改鹰介质/ HAM-F12胰岛素μg·5毫升−1transferin 7.5μg·毫升−1氢化可的松10−6米,内皮细胞生长补充2μg·毫升−1ng,上皮生长因子25毫升−1T3 3.10−5米,l谷氨酰胺200毫米,青霉素和链霉素100μg·毫升−1)。
动物
Wt (雌性生殖道+ / +),雌性生殖道淘汰赛(雌性生殖道−−/)雌性老鼠(C57Bl / 6 129 - cftrtm1unc)获得CDTA (中心分布,Typage et Archivage动物、奥尔良、法国),研究了3岁和4周之间。为了防止致命的肠梗阻,老鼠与movicol®(30 g·L−1)的饮用水。
CFTR功能分析的检测活动在体外
雌性生殖道Cl- - - - - -频道活动被碘化验(125年我)流出21或由单细胞荧光成像技术,利用potential-sensitive探测器,双(1,3-diethylthiobarbituric酸)trimethine oxonol (DiSBAC2(3);分子探针,尤金,或者美国)22。碘化流出曲线被绘制的速度构造125年我与时间。所有的比较都是基于时间依赖率极大值(k =最高利率,分钟−1)不含点用于建立基线(k peak-k基底,分钟−1)。荧光成像的结果给出了转换数据获取信号变化百分比(Fx)相对于时间之外的刺激,根据方程:Fx = ((Ft-F0) / F0)×100英尺和F0荧光值在时间t时的刺激,分别。直方图表示的值对应的水平稳定的每种药物引起的荧光变化。雌性生殖道Cl- - - - - -电流测量broken-patch,全细胞膜片箝技术的配置20.。
营浓度测量
细胞内营是评估营高温超导免疫(美国微孔、Billerca MA)按照制造商的指令进行操作。发光测量与TopCount NXT(美国PerkinElmer沃尔瑟姆,MA)微型板块读者。
短路电流测量
顶端膜Cl- - - - - -当前测定小鼠结肠上皮细胞已经描述15或之后两极化的协议23使用以下浴的解决方案:使用serosal-to-mucosal梯度顶端,107毫米K-gluconate, NaHCO 4.5毫米氯化钾,25毫米31毫米MgSO4,1.8毫米Na2HPO40.2毫米,不2阿宝45.75毫米Ca-gluconate 12毫米d葡萄糖;NaHCO基底外侧111.5毫米氯化钾25毫米31毫米MgSO4,1.8毫米Na2HPO40.2毫米,不2阿宝4,1.25毫米CaCl212毫米d葡萄糖23。
数据分析
数据意味着±扫描电镜,其中n是指孤立的细胞的数量(单细胞测量),细胞群(碘射流和营地测量)和n的动物数量。数据集和一个未配对t检验进行比较。所有图表绘制GraphPad Prism 5.0为Windows (GraphPad软件、圣地亚哥、钙、美国)。假定值< 0.05被视为具有统计学意义。
结果
GPact-11a wt-CFTR活动的影响
我们首先检查的影响GPact-11a CHO细胞稳定表达wt-CFTR与我们的机器人使用碘流出测量细胞主要筛选试验。这个试验允许雌性生殖道通道激活或抑制的快速检测。腺苷酸环化酶激活移频键控(图1 c碘化)刺激流出wt-CFTR CHO细胞(相对率= k峰- k基底= 0.44±0.01分钟−1,n = 4;图1 c)。这种射流被GPinh-5a抑制(图1 c)。在实验中给出图1 c,GPact-11a强Fsk-induced反应的相对速度0.38±0.02分钟−1(n = 4)。由GPact-11a雌性生殖道的刺激,在随后移频键控的存在剂量依赖性关系描述half-maximal有效浓度(EC50)2.1±1.3μM (n = 4;图1 d)。进行了类似的实验与小异构体GPact-11b导致电子商务502.9±0.9μM(数据没有显示,n = 4)。CFTR GPact-11a完全被检测的影响异烟肼-172年,glyh - 101和GPinh-5a三个选择性雌性生殖道抑制剂13,26,27但并不是受了影响,芳烃,两个non-CFTR抑制剂28(图1 e)。我们扩展我们的研究来评估GPact-11a的影响在人类的肺上皮细胞内源性wt-CFTR Calu-3行,并发现一个欧共体501.8±1.3μM移频键控(图1 f)。
GPact-11a wt-CFTR氯通道的激活
然后我们探讨wt-CFTR CHO细胞营水平以应对几个GPact-11a浓度。图2一个表明GPact-11a对基底细胞没有影响营水平。然而,因为我们测量一个低水平的营地和移频键控,我们希望证实这些结果在人类气管气道上皮细胞系(MM39)内生wt-CFTR表达。图2 b显示了营地的强劲增长水平刺激移频键控但证实GPact-11a没有影响信号通路。
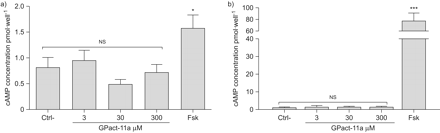
GPact-11a对营地的影响水平wt-cystic囊性纤维化跨膜电导调节)的中国仓鼠卵巢(CHO)和b) MM39细胞系。Forskolin(移频键控;10μM)作为积极的控制。按Ctrl -:未经处理的细胞。n = 6 wt-CFTR CHO细胞和n = 12 MM39细胞。ns:不重要的。*:p < 0.05;* * *:p < 0.001。
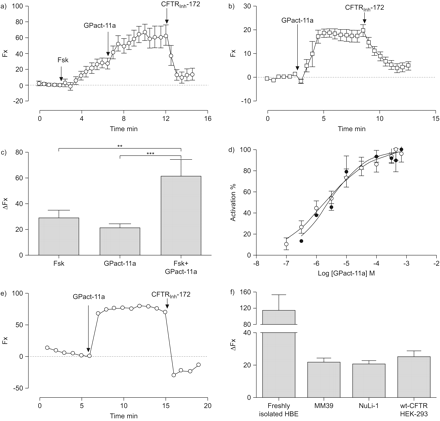
我们在雌性生殖道GPact-11a活动的影响相比,在移频键控的存在与否,使用单细胞荧光成像技术应用于MM39。正如预期的那样,我们观察到,移频键控增加了记录荧光信号。信号被进一步增加了GPact-11a和完全抑制雌性生殖道异烟肼-172 (图3)。有趣的是,如图所示图3 b,GPact-11a增加了记录荧光信号没有移频键控和这种效应被雌性生殖道抑制异烟肼-172年。图3 c总结结果通过刺激移频键控或GPact-11a而产生的响应的振幅co-application GPact-11a +移频键控。这些结果表明添加剂和不是一个协同效应表明移频键控和GPact-11a两种不同机制的行动。我们确定的量效效果GPact-11a,移频键控的存在与否,并计算出一个电子商务502.8±0.1μMμM和2.1±0.1,分别为(图3 d)。我们确定GPact-11a对人类的影响纤毛上皮细胞刚从肺样本中分离(新孤立HBE;图3 f)。在这些细胞中,GPact-11a诱导荧光被雌性生殖道的强劲增长异烟肼-172 (图3 e)。最后,GPact-11a激活wt-CFTR HEK293细胞表达EGFP-wt-CFTR暂时性的蛋白质,在气管(MM39)和支气管(NuLi)细胞系和新鲜孤立HBE细胞(图3 f)。重要的是,雌性生殖道反应HBE倍高于细胞系。
功能评价的GPact-11a wt-cystic囊性纤维化跨膜电导调节(雌性生殖道)双(1,3-diethylthiobarbituric酸)trimethine oxonol化验。a、b)时间课程的相对荧光(Fx)显示的效果forskolin(移频键控),GPact-11a和雌性生殖道异烟肼-172年MM39细胞。c)直方图显示的附加效果移频键控和GPact-11a MM39细胞。为每个条件a - c n = 12。d)的量效曲线GPact-11a MM39细胞存在(○)或缺失(•)的移频键控(1μM)。数据点报告的正常化的相对荧光收集实验共有30个细胞中分离出来。e)外汇显示时间进程的影响GPact-11a新鲜分离人类支气管纤毛上皮细胞(HBE细胞)。f)直方图的影响总结GPact-11a HEK293细胞获得暂时性的表达EGFP-wt-CFTR蛋白(n = 52),在MM39 (n = 83)和NuLi (n = 12)细胞系和新鲜孤立HBE细胞(n = 14获得四个病人)。浓度移频键控1μM GPact-11a 300μM CFTR (d除外)和检测异烟肼-172年10μM。
我们使用全细胞膜片钳技术记录雌性生殖道瞬变电流在HEK293细胞表达EGFP-wt-CFTR蛋白质。与GPact-11a刺激后,全细胞电流线性增加,逆转-40 mV (图4和b)确认其Cl- - - - - -大自然。这Cl- - - - - -目前雌性生殖道的抑制了细胞外灌注异烟肼-172 (图4)。
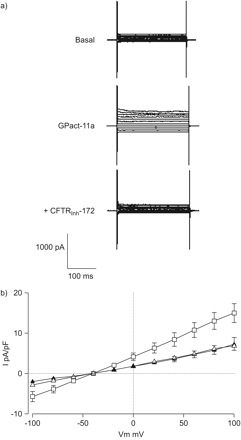
膜片钳实验与wt-CFTR HEK293细胞转染。)代表完整的细胞Cl的痕迹- - - - - -电流引起的潜在控股-40 mV系列的测试电位从-100年到100年mV在20 mV增量。b)相应的电流(I)由细胞电容电压(Vm)关系正常化:基底(▴;n = 7);GPact-11a (□;300μM, n = 7);CFTR GPact-11a +检测异烟肼−172 (▵;10μM, n = 7)。
GPact-11a获救的活化剂F508del-CFTR氯通道
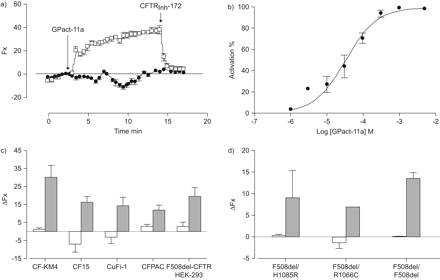
我们由单细胞荧光成像,GPact-11a的效果对人类CF气管腺上皮细胞从内部表达F508del-CFTR (CF-KM4细胞)。有缺陷的贩卖miglustat F508del-CFTR的特点是可以纠正的22,29日。荧光的急剧增加,抑制雌性生殖道异烟肼-172 (图5)或glyh - 101(数据未显示),记录添加GPact-11a后miglustat-corrected CF-KM4细胞。相反,对未经处理的CF-KM4细胞(GPact-11a没有影响图5),确认GPact-11a雌性生殖道的选择性。在miglustat-corrected CF-KM4细胞,GPact-11a诱导荧光与EC的浓度升高5034.3±1.8μM (图5 b)。互补的研究进行一些人类上皮细胞系表达F508del-CFTR内生或瞬变时在图5中c。之后,再次拯救F508del-CFTR miglustat等离子体膜,GPact-11a激活F508del-CFTR在HEK293细胞表达EGFP-F508del-CFTR暂时性的蛋白质和鼻(CF15),气管(CF-KM4),支气管(CuFi)和胰腺(CFPAC) CF细胞系(图5度)。最后,我们评估了GPact-11a对纤毛上皮细胞刚从人类肺部分离不同的CF基因型。突变R1066C是在雌性生殖道的第二个跨膜域错义突变30.并导致严重的CF表型。R1066C-CFTR蛋白质是不正确处理,不像F508del-CFTR,不能纠正该缺陷降低温度或butyrate-treated细胞31日。突变H1085R是严重和罕见的错义突变被梅西埃et al。32。H1085R-CFTR蛋白质提供了一个贩卖F508del-CFTR校正器可以纠正的缺陷33。图5 d表明,在miglustat-pretreated细胞从3 CF患者不同的基因型,GPact-11a诱导荧光的强劲增长。
功能评价的GPact-11a F508del-cystic囊性纤维化跨膜电导调节(雌性生殖道)双(1,3-diethylthiobarbituric酸)trimethine oxonol化验。)时间课程的相对荧光(Fx)显示GPact-11a和雌性生殖道的作用异烟肼-172年治疗CF-KM4细胞(•)或在CF-KM4纠正miglustat (□)。为每个条件n = 12。b)量效曲线GPact-11a miglustat CF-KM4细胞之前纠正。数据报告的正常化的相对荧光收集的三个独立的实验共有30个细胞。c) GPact-11a对F508del-CFTR细胞系的影响治疗(□)或修正(▓)miglustat (8 < n < 127)。GPact-11a d)效应对人类支气管纤毛上皮细胞细胞刚从肺囊性纤维化不同基因型分离(F508del / F508del-CFTR (n = 4), F508del / R1066C (n = 7)和F508del / H1085R-CFTR (n = 9))。CFTR浓度检测异烟肼300年-172年10μM GPact-11aμM (b除外),细胞培养miglustat 100μM 2 h(除了CFPAC: 100μM, 24 h)。
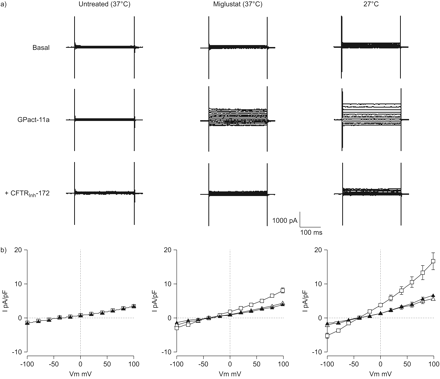
在HEK293细胞全细胞膜片箝记录电流瞬变表达EGFP-F508del-CFTR蛋白(图6)。而GPact-11a没有影响这些细胞培养在37°C(留下痕迹;图6和b),一个线性non-voltage-dependent Cl- - - - - -当前记录细胞治疗miglustat(中间的痕迹;图6和b)或低温培养(正确的痕迹;图6和b)。F508del-CFTR Cl- - - - - -电流激活GPact-11a被雌性生殖道抑制异烟肼-172 (图6和b)。
全细胞膜片箝记录与F508del-cystic囊性纤维化跨膜电导调节(雌性生殖道HEK293细胞治疗(n = 5),纠正了miglustat(100μM;4 h, n = 5)或培养27°C (24 h, n = 5))代表全细胞Cl的痕迹- - - - - -电流引起从-100年到100年mV, 20 mV的步骤。b)相应的电流(I)细胞电容电压(Vm)关系正常化。浓度GPact-11a 300μM和雌性生殖道异烟肼-172年10μM。▴:基底;□:GPact-11a;CFTR▵: +检测异烟肼-172年。
体外评价GPact-11a
我们确定的影响GPact-11a transepithelial离子运输在短路电流(Isc)条件雌性生殖道+ / +和雌性生殖道−−/小鼠结肠上皮细胞。在这些条件下,雌性生殖道+ / +组织有一个意味着transepithelial阻力(Rte),40.1±1.5Ω·厘米2意思是自发的sc42.1±2.7μA·厘米−2(n = 88)。为雌性生殖道−−/组织,Rte和我sc分别为34.4±2.5Ω·厘米吗2和-2.7±2.9μA·厘米−2分别(n = 24)。所有实验在100年存在μM阿米洛利抑制Na休息+当前的活动设定的上皮钠通道(钠)。transepithelial Cl的贡献- - - - - -运输(我Cl)研究了两极化的基底外侧膜包含高钾浓度的解决方案23。这个过程允许测量顶端离子电导的变化,避免污染在目前的反应,例如,charybdotoxin-sensitive顶端K+渠道23。后两极化,平均Rte和我sc在雌性生殖道+ / +结肠分别为40.2±1.4Ω·厘米2和147±7μA·厘米−2分别(n = 12)。添加两边GPact-11a浓度增加雌性生殖道+ / +结肠上皮细胞诱导剂量依赖性的我sc与电子商务50175.6±1.1μM (n = 3;图7和c)。它是由格列本脲抑制(图7)。相反,应用程序在相同的实验条件GPact-11a没有影响雌性生殖道−−/结肠上皮细胞(图7 b)。添加葡萄糖增加了我sc显示组织的生存能力(图7 b)。
我们室短路电流(我的录音sc在老鼠升结肠。a)的典型例子的影响双方GPact-11a添加浓度增加雌性生殖道+ / +小鼠结肠。阿米洛利(100μM添加粘膜一侧)被用来抑制残留上皮钠活动和格列本脲(500μM添加两边)被用来抑制囊性纤维化跨膜电导调节(雌性生殖道)。b)典型的例子显示了增加GPact-11a添加浓度对双方的影响雌性生殖道−−/小鼠结肠。葡萄糖(40毫米添加两边)被用来验证组织的反应性。跟踪是代表三个独立的实验。c) GPact-11a效应的剂量反应曲线雌性生殖道+ / +小鼠结肠(n = 3), d) GPact-11a-induced我scpermeabilisation后制霉菌素(200μg·毫升−130 min)说,在顶端基底(美联社,n = 5)或(提单,n = 4)膜。e)的影响做了(4 41-diisothiocyanatostilbene-2 21-disulfonic酸);500μM, n = 4)、格列本脲(500μM, n = 18)和雌性生殖道异烟肼-172(100μM, n = 5) GPact-11a-induced我sc。实验前应做pre-incubated 10分钟。ns:不重要的。* * *:p < 0.001。
进行了进一步的实验没有两极化的协议确定GPact-11a的特异性。首先,我们permeabilised顶端或基底膜μg·200毫升−1制霉菌素的30分钟,然后我来衡量sc。所示图7 d,用制霉菌素permeabilising顶端膜阻止了GPact-11a基底效应(n = 5)而permeabilisation GPact-11a我没有显著的影响sc反应(n = 4)。其次,雌性生殖道+ / +结肠上皮细胞,我的高度sc由GPact-11a被雌性生殖道抑制异烟肼-172年,格列本脲但不是受到了(图7 e)。最后,我们发现,这个协议,没有GPact-11a效果雌性生殖道−−/结肠上皮细胞(n = 4,数据未显示)。
在活的有机体内评价GPact-11a
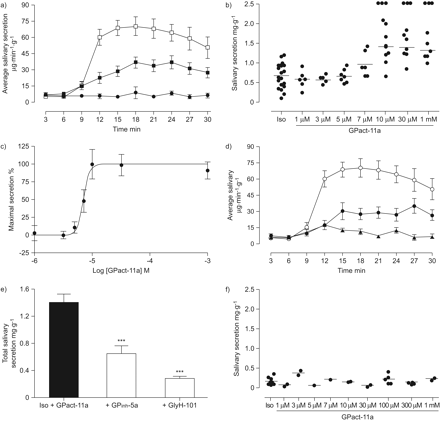
评估在活的有机体内GPact-11a影响雌性生殖道+ / +和雌性生殖道−−/老鼠,我们使用非侵入式测量技术的唾液分泌25。首先,我们确定了分泌唾液分泌的能力雌性生殖道+ / +老鼠通过刺激唾液腺GPact-11a孤单。GPact-11a本身并没有提高唾液分泌(n = 3;图8)。相反,异丙肾上腺素刺激唾液分泌平均36.9±5.2μg·分钟−1·g−1(n = 19;图8)。GPact-11a强isoprenaline-induced分泌(70.2±9.0μg·分钟−1·g−1,n = 7;图8)。图8 b总结GPact-11a浓度的增加和获得的结果表明,GPact-11a,异丙肾上腺素的存在,引起唾液分泌存在剂量依赖的相关性雌性生殖道+ / +老鼠与一个电子商务507.1±1.1μM (5 < n < 8;图8 c)。异丙肾上腺素/ GPact-11a-induced唾液分泌抑制GPinh-5a和glyh - 101 (图8 d和e)。最后,我们没有发现异丙肾上腺素和GPact-11a唾液的分泌雌性生殖道−−/老鼠(图8 f)。
在活的有机体内GPact-11a的评价。平均唾液分泌雌性生殖道+ / +引起的小鼠GPact-11a (•;30μM, n = 3), GPact-11a(30μM)与异丙肾上腺素(10μM, n = 7)(□)或异丙肾上腺素(▪;10μM, n = 19)。b)总唾液分泌雌性生殖道+ / +由异丙肾上腺素(Iso;10μM),有或没有GPact-11a浓度增加。GPact-11a c)相应的剂量反应曲线。d)平均总唾液分泌唾液分泌和e)雌性生殖道+ / +引起的小鼠GPact-11a(30μM)与异丙肾上腺素(10μM, n = 7)(○)和由两个雌性生殖道抑制剂抑制:GPinh-5a (•;20点,n = 11)和glyh - 101 (▴;10μM, n = 4)。f)总唾液分泌雌性生殖道−−/由异丙肾上腺素(Iso;10μM),有或没有GPact-11a浓度增加。
讨论
在目前的研究中,我们报告的发现methylglyoxal-9-propyladenine加合物命名GPact-11a,选择性,水溶性和wt和F508del-CFTR无毒催化剂。最重要的我们目前调查的结果是:1)GPact-11a是一种新型活化剂的雌性生殖道氯通道在人类呼吸道上皮细胞系;2)GPact-11a激活获救F508del-CFTR鼻、气管、支气管和人类CF胰腺上皮细胞;3)GPact-11a wt-CFTR的活化剂和拯救F508del-CFTR人类纤毛上皮细胞刚从CF和non-CF肺样本分离;4)体外氯化,GPact-11a刺激结肠分泌雌性生殖道+ / +老鼠;5)在活的有机体内,它增加唾液分泌雌性生殖道+ / +老鼠;6)GPact-11a雌性生殖道的选择性,因为,在我们的实验条件,我们所建立的雌性生殖道抑制剂抑制GPact-11a的影响雌性生殖道异烟肼-172年,glyh - 101,格列本脲或GPinh-5a。此外,我们没有观察到任何non-CFTR通道的激活在未修正的F508del-CFTR细胞雌性生殖道−−/老鼠。
结构性因素对雌性生殖道激活
在GPact-11a的化学结构(图1 b),可以区分三个主要元素:1)嘌呤芳香杂环化合物组成的融合嘧啶和咪唑环;2)一个疏水性丙基侧链连接到一个氮原子的嘌呤;和3)形成的亲水环与9-propyladenine甲基乙二醛的缩合反应。后者环可能包括的主要药效团因为9-propyladenine不是活跃在雌性生殖道频道(数据没有显示)。催化剂的结构GPact-11a接近抑制剂GPinh-5a的结构。在这两种结构,第一和第三个元素存在。这个观察显示一个潜在的共同目标包括亲水结合位点药效基因(即。第三个元素)。GPact-11a 9-propyl疏水性取代基的取代了9 - (2-deoxyribos-1-yl)取代基在GPinh-5a亲水。这个替换产生的转变从一个激活抑制剂。GPinh-5a和GPact-11a都是两性离子在生理的pH值,携带羧酸盐功能和质子化了的亚氨基的集团,两个属性解释他们的高水溶性。
与前文所述的催化剂相比,可以提到一些相似之处。黄嘌呤催化剂是嘌呤取代基杂环化合物与疏水代替附加到一个氮原子嘌呤(甲基环己基、环戊二烯基、异丙基)6。疏水性取代基与氮原子也出现在pyrrolo [2, 3 b]吡嗪(丁基RP107和RP108)15和唑酮催化剂(乙1-EBIO和DCEBIO)6。这些催化剂是由两个融合搭载和5环嘌呤GPact-11a杂环。一些benzoquinolizinium活化剂也呈现出疏水侧链,丁在产甲烷- 91和产甲烷- 104,与芳杂环由三个融合搭载戒指6。
对新一代的雌性生殖道活化剂
与其他离子通道相比,压敏电阻器等渠道或neurotransmitter-activated通道34- - - - - -36,雌性生殖道药理学仍处于起步阶段。没有选择性的配体、催化剂或抑制剂已被批准用于临床使用。第一代的雌性生殖道调节器最初确定调查后细胞内信号通路。例如,雌性生殖道可以激活剂,提高细胞营地或稳定CFTR磷酸化检测(磷酸酶抑制剂)6。然而,两个受体信号通路(β2肾上腺素能受体,2 b腺苷受体)有效地激活wt-CFTR通过刺激腺苷酸环化酶,提高细胞的营地9,11,37,38,但不能激活F508del-CFTR人类呼吸道上皮细胞。近年来,一系列的化合物显示活动在体外被描述。雌性生殖道开器包括类黄酮、黄嘌呤39,40,benzoquinoliziniums6或荧光素衍生品41。然而其中一些化合物缺乏选择性和亲和力较低。雌性生殖道激活需要高度的营地和随之而来的监管域(域)的磷酸化蛋白激酶6,34。雌性生殖道活化剂可以直接在雌性生殖道蛋白质,或间接通过抑制磷酸二酯酶(从而提高营)或抑制磷酸酶(CFTR从而增加检测磷酸化)6,34。间接影响预计不会对CF药物治疗是有用的,基本的缺陷是内在的雌性生殖道蛋白质和上游调控通路。在这项研究中,我们确定了GPact-11a选择性和cAMP-independent活化剂wt F508del-CFTR获救。因此,GPact-11a的作用机制仍然未知,GPact-11a代表了一个有趣的和潜在候选人的发展未来的药理治疗CF因其水溶解度和没有毒性。
一个校正器+ CF bi-therapy的催化剂?
F508del-CFTR活化剂预计不会是有效的,除非他们有关联的校正器F508del mistrafficking。虽然单个化合物两种类型的活动是可取的,bi-therapy涉及校正器+一个活化剂可以考虑。我们相信activator GPact-11a就是这样一个有价值的候选人。的水溶性和明显没有毒性GPact-11a使这个代理非常有吸引力。虽然需要一个完整的临床前安全性研究,我们初步的在活的有机体内实验中我们没有观察到严重副作用或死亡率的老鼠。药理剂是一个先决条件的选择性工业和/或临床前进一步发展。GPact-11a似乎是选择性的雌性生殖道上皮细胞,因为我们没有观察到任何类型的离子通道的激活未修正的F508del-CFTR细胞和结肠癌的雌性生殖道−−/老鼠。此外,在我们的模型与CFTR功能检测的影响GPact-11a系统完善的雌性生殖道抑制剂所抑制。
总之,激活表面F508del-CFTR需要组合疗法包括代理为拯救F508del-CFTR加工、耦合策略恢复F508del-CFTR功能/监管在质膜上。这种bi-therapy可能包括,例如,miglustat GPact-11a和将被认为是在我们的未来的研究作为一个潜在的治疗在CF。
确认
作者要感谢g·卡布里尼,Glokner-Pagel和m .莫顿提供NuLi CuFi-1, CFPAC,分别和MM39 CF-KM4细胞系。我们感谢p . Corbi和p . Bonnette访问non-cystic纤维化和人类肺囊性纤维化样本,分别。
脚注
支持声明
从Mucovie j·伯特兰得到了奖学金。b Boucherle和a .坯支持的人数从Vaincre la mucoviscidose (VLM)和法国的研究,分别。l . Dannhoffer支持的博士后奖学金VLM和p . Melin-Heschel VLM格兰特。
感兴趣的语句
没有宣布。
- 收到了2009年7月31日。
- 接受2010年1月12日。
- ©2010人队