文摘
17号染色体单核苷酸多态性(SNPs)授予对方篮里早发性哮喘的风险增加。目的是研究17个snp对方篮里是否修改早期呼吸道感染和哮喘之间的关联。
关联分析是在499名儿童进行的(268年与哮喘、平均年龄11岁)从流行病学研究哮喘的遗传和环境(EGEA)。12-yr后续数据被用来评估持续或间歇性的哮喘年轻成年。呼吸道感染前2年的年龄是回顾性评估。
12 17单核苷酸多态性研究对方篮里,优势比(或)感染之间的联系和早发性哮喘发病年龄(≤4岁)在运营商的风险更高的基因型(-6.36或3.42)比非携带者(或1.84 - -2.44;假定值为五个SNPs)交互0.02 - -0.04。风险基因型也增加了感染之间的联系和儿童哮喘,融汇在成年期(-7.16或4.84非运营商和1.74 - -2.25;假定值为10个snp)交互0.008 - -0.05。在孩子17对方篮里风险基因型和环境烟草烟雾(ETS)暴晒,感染和哮喘之间的联系进一步加强。
17温度系数的遗传变异和早期ETS暴露提高早期呼吸道感染和早发性哮喘之间的关系和儿童哮喘,融汇在成年。
早期患儿下呼吸道感染,这主要是由病毒引起,如呼吸道合胞体病毒(RSV)或鼻病毒,反复喘息和儿童哮喘的风险增加1- - - - - -4。尚不清楚呼吸道感染与一个倾向是一种标记识别婴儿开发哮喘,或是否感染哮喘的《盗梦空间》是有因果联系5,6。肺发展早期生活是一个关键时期,它被认为病毒感染会增加哮喘的风险通过影响免疫反应的发展或改变肺功能4,7,8。然而,丹麦的双胞胎对最近的一项研究发现没有证据支持一个因果的感染作用6。
只有少数的婴儿毛细支气管炎等呼吸道病毒感染发展喘息和哮喘复发,这表明遗传和环境因素可能影响哮喘和感染之间的关系9。例如,接触环境烟草烟雾(ETS)可能扮演这样一个角色10。单核苷酸多态性(snp)在先天免疫和其他免疫反应基因,已经被证明与RSV的严重性细支气管炎11,12然而,缺乏调查研究遗传因素影响毛细支气管炎和哮喘之间的关系9。
全基因组关联研究(GWAS) 17号染色体上显示单核苷酸多态性之间的关联温度系数和儿童哮喘13几项研究已经复制14- - - - - -17。在流行病学研究哮喘的遗传和环境(EGEA)已经表明,赋予的风险增加17温度系数变异仅限于早发性哮喘,并进一步提高了早期生活ETS暴露16。后者发现最近在白复制对象18。目前还不清楚这些基因变异如何影响哮喘的风险。有趣的是,17个温度系数的一个基因的表达,ORMDL3,被发现强烈刺激与polyinosine-polycytidylic酸诱导的肺成纤维细胞,表明ORMDL3可能在病毒性呼吸道感染中发挥作用14。因此,17个温度系数变异之间的相互作用和早期生活事件似乎发挥重要作用的发展早发性哮喘。然而,不知道这些影响后持续的童年。
本研究的目的是为了测试以下两个假设:1)早期呼吸道感染和哮喘之间的关系,特别是早发性哮喘、基因变异影响的17个温度系数;和2)17温度系数的修改影响变异在感染和早发性哮喘之间的关系进一步增加了ETS暴露在早期的生活。此外,我们测试了两个额外的哮喘表型相同的假设:儿童哮喘持续或间歇性的在年轻的成年。
方法
研究人口和设计
EGEA结合病例对照研究和家庭的研究。详细设计和协议已报告19。哮喘病人渊源者(7岁- 70岁)是从六个胸部诊所招募五个法国城市在1991年和1995年之间(EGEA1)。哮喘渊源者的家属都包括,通过包括渊源者的父母和兄弟姐妹或包括渊源者的配偶和孩子。此外,以人群为基础的控制被招募。
在目前的研究中,儿童协会进行了分析(年龄≤16岁)从EGEA家庭和控制样品。在EGEA1注册的604个孩子,我们使用的数据来自499名儿童(268患有哮喘,231没有哮喘)基因型对方篮里17日完整信息,哮喘和呼吸道感染的发病年龄(图E1补充材料)。12-yr后续EGEA1最近进行的(EGEA2;2003 - 2007年)20.。活动的哮喘EGEA2获得236年(88%)在EGEA1 268儿童患有哮喘。
所有的参与者或他们的父母给书面知情同意。
基因分型
基因分型结果被描述16。在目前的研究中,我们调查了11个snp位于35.23和35.34 Mb 17号染色体上的温度系数与哮喘相关显著(p < 0.01) EGEA家庭16。我们还包括一个额外的SNP, rs7216389,因为它是研究最多的17个温度系数变异复制初始GWAS研究后续13。12个单核苷酸多态性在强大的连锁不平衡(LD),与成对LD系数D '在0.87和1.0之间16。
健康结果和风险变量
入选标准使用在渊源者EGEA1定义哮喘,哮喘的定义,描述了在亲戚或以人群为基础的控制19,21。早发性哮喘被定义为≤4岁哮喘的发作16。self-completed问卷被用来评估哮喘患儿是否在第一次调查还活跃在EGEA2哮喘,这被定义为有哮喘发作或使用哮喘药物治疗在过去的12个月。在EGEA1受试者患有哮喘,持久和弛张在成年早期哮喘的定义根据活动在EGEA2哮喘(yes / no)。受试者没有哮喘在EGEA1参照群体的分析。
呼吸道感染的早期生活是基于父母在EGEA1报告,并定义为一个积极回答“你的孩子有支气管炎、细支气管炎在2岁之前?”。ETS暴露在生命早期(≤2岁年龄)被定义为前面描述的16。
统计分析
优势比(或)和95%可信区间估计了感染和哮喘之间的联系通过使用广义估计方程方法分对数链接函数考虑家庭兄弟姐妹之间的依赖。血亲关系被定义为集群单元。或根据年龄和性别进行调整。测试是否感染哮喘协会受到17温度系数的遗传变异,我们介绍了感染效应,苏格兰民族党效应,一个SNP x感染模型中的术语而调整年龄和性别。17个snp对方篮里,我们假定一个隐性遗传模型(风险等位基因纯合子基因型与其他基因型)提供最适合17对方篮里轨迹之间的联系和早发性哮喘发现之前16。苏格兰民族党x感染交互测试通过使用普遍分数测试,采用卡方分布有一个自由度。我们用δβ统计识别影响我们观察和评估不包括这些观测结果的影响。实证测试假定值的SNP和感染之间的相互作用也由模拟计算(即。标记基因型模拟的零假设下没有SNP x感染交互通过观察到的标记等位基因频率和LD模式在单核苷酸多态性和保持观察表型EGEA儿童)中的数据。对于每个SNP,假定值估计1000年的比例为交互模拟导致检验统计量大于或等于一个观察。最后,我们还测试了感染和哮喘之间的关系是否修改17温度系数变异和接触ETS在早期生活中,使用一个类似的策略。
结果
描述性的特点
研究对象的特点有或没有在招聘(EGEA1)在哮喘表1。正如所料,客观地测量标记的哮喘,如特异反应性、总免疫球蛋白E (Ig),外周血嗜酸性粒细胞,用力呼气量在1 s (FEV1)与诊断哮喘和支气管高反应性显著相关(p < 0.05)。研究对象的平均年龄在第二个调查(EGEA2)为22.4年(四分位范围20.0 - -24.2年)。167名儿童的早发性哮喘、84年持续哮喘、62弛张哮喘和21在第二个调查数据遗失了。101名儿童晚发性哮喘患者中,有44人持续哮喘、46弛张哮喘和11有缺失的数据在第二个调查。
早期感染
早期呼吸道感染和哮喘表型显著相关,但大多数与早发性哮喘和哮喘弛张在成年早期(表2)。或更改后略微调整了年龄和性别。进一步调整ETS或特异反应性改变不了关联。呼吸道感染和哮喘之间的关联出现在男孩比女孩强:感染之间的联系和早发性哮喘的或者是男孩的3.70(2.17 - -6.32)和2.29(1.14 - -4.59)的女孩,但没有显著差异(p = 0.43)。没有关联的17个snp对方篮里和早期呼吸道感染(p > 0.1,数据未显示)。还有17个snp对方篮里之间没有关联和感染时,分层分析在儿童哮喘(或在0.85和1.57之间;p > 0.1)或没有哮喘(或在0.59和0.84之间;p > 0.1)。
17对方篮里基因型对协会的影响感染哮喘
呼吸道感染和早发性哮喘之间的关系是在运营商的风险基因型为每个12 17温度系数的遗传变异(或介于3.42和6.36之间,根据基因变异)比非携带者(或在1.84和2.44之间)(表3)。统计上显著的感染和17观察对方篮里基因型之间的相互作用五个snp (p = 0.02 - -0.04;表3)。相比之下,感染和哮喘之间的关联与发病年龄≥5年根据基因型之间没有显著性差异;或观察到运营商的风险基因型的0.7倍,1.7倍或在非携带者(假定值0.29和0.93之间的交互等;数据未显示)。
然后我们检查在儿童哮喘患儿的或一般在成年早期哮喘(持续或间歇性的哮喘与没有在儿童哮喘)。或感染和儿童哮喘之间的关系,宽容别人的儿童在成年后高2.1 -3.7倍与风险基因型比儿童nonrisk基因型(或介于4.84和7.16之间在非运营商和在1.74和2.25之间;假定值互动10个snp) 0.008 - -0.05 (表4)。感染和儿童哮喘之间的关系持续到成年早期没有明显修改17对方篮里snp(或不同的0.9 - -1.9倍,互动假定值从0.18 - -0.91;数据未显示)。
δβ统计不确定的人有强烈的影响效应估计所示表3和4。我们估计模型的参数又没有十大最具影响力的观察。交互的假定值< 0.05表3仍然达到了显著性水平,除了rs8076131 (p = 0.07);和交互作用的假定值< 0.05表4仍然达到了显著性水平,除了rs903281 (p = 0.08), rs4795405 (p = 0.07)和rs4794820 (p = 0.11)。
ETS暴露
我们进一步研究了影响的17个基因型和对方篮里ETS暴露在生命早期呼吸道感染和哮喘之间的关系。图1显示感染之间的联系和早发性哮喘或弛张哮喘在rs8069176根据ETS暴露和风险基因型;苏格兰民族党显示最重要的基因-环境相互作用。感染和早发性哮喘和弛张哮喘之间的关系与rs8069176 ETS暴露对象之间很强的GG基因型(早发性哮喘或9.98(3.56 - -27.97),在成人哮喘弛张热或10.68 (3.58 - -31.82))。或感染和早发性哮喘之间的关系明显不同的孩子暴露在ETS和孩子不是ETS暴露,但只在运营商的风险基因型(交互感染x ETS;p = 0.03儿童携带rs8069176 GG)。其他11个snp显示类似的模式,具有很强的感染之间的联系和早发性哮喘儿童暴露在ETS和携带的风险基因型(ORs介于4.65之间为rs9303277 CC(1.62 - -13.34)和10.04 (3.63 - -27.69)rs2305480 GG),和其他孩子弱关联(数据没有显示)。
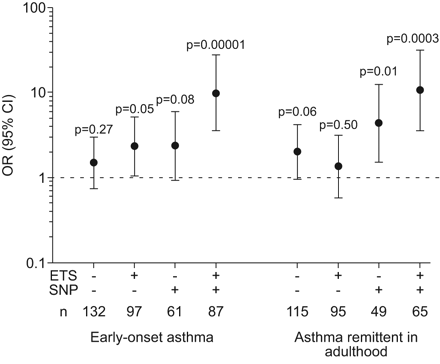
哮喘协会(早发性哮喘和哮喘弛张在成年期)和呼吸道感染早期,根据环境烟草烟雾(ETS)暴露在生命早期(是的:+,:-)和rs8069176基因型(单核苷酸多态性(SNP): +: GG;-:AG) + AA)。
模型的参数估计没有十大最具影响力的观察导致轻微下降,感染和早发性哮喘之间关联的证据:在ETS-exposed科目rs8069176 GG基因型,或为9.18 (3.06 - -27.6)。
讨论
这项研究表明,17个风险基因型增加对方篮里早期呼吸道感染和哮喘之间的正相关,这是局限于早发性哮喘和哮喘,融汇在成年早期。感染和早发性哮喘之间的关系(或弛张哮喘)是进一步提高当孩子有17个风险变异受到对方篮里ETS在早期的生活。目前的研究支持早期的发现显示早期的生活事件的重要性在17温度系数变异和哮喘之间的关系16。
感染和哮喘
儿童下呼吸道感染可能识别已存在的生理或免疫异常,也可能提供一个第一触发开始喘息婴儿容易开发哮喘。否则,有人建议,病毒性呼吸道感染和哮喘可能有因果联系。有一些因果关系的证据,包括最近实验小鼠模型的研究结果表明,先天免疫激活的病毒性呼吸道感染可导致慢性气道炎症性疾病的发展7,8,22。婴儿与17个对方篮里风险变异可能造成肺损伤呼吸道病毒感染的反应不同,这可能会增加他们对开发反复喘息或哮喘的易感性。然而,我们不能得出结论的因果关系之间的联系早期呼吸道感染和哮喘,如果我们假设感染和哮喘之间的因果关联,解释了我们的发现可能是17温度系数变异增加了开发哮喘的风险与潜在风险因素互动早期占据喘息。17温度系数变异之间的基因基因或基因-环境相互作用和常见的呼吸道感染和哮喘的风险因素(如先天免疫基因变异)可能影响哮喘的风险。
大感兴趣的基因组区域
研究了17个对方篮里基因的功能在很大程度上是未知的,尤其是哮喘。之间的关系ORMDL3、病毒感染和哮喘是由副大臣et al。14他发现ORMDL3表达强烈诱导病毒刺激的实验模型。最近的一项研究报道,ORMDL3促进内质网介导的炎症反应23。在这12个snp研究,属于一个ORMDL3而其他的基因间(三个单核苷酸多态性)或属于其他基因,IKZF3(SNP),参与淋巴细胞发展的规定,ZPBP2,或者带pellucida-binding蛋白2 (SNP),和GSDML(6个snp),编码一个gasdermin蛋白质与皮肤上皮屏障功能和分化24。这些17对方篮里snp与转录水平密切相关ORMDL313,发现最近,有文字记录的水平GSDML,这表明两ORMDL3和GSDMLcoregulated了顺式代理的遗传变异25。因此,我们的流行病学观察符合生物的发现表明,遗传变异行为在一个大的基因组区域,发挥了作用在至少三个基因(转录活动ZPBP2,GSDML和ORMDL3)25。
肺功能和特异反应性
17个snp对方篮里,FEV之间的联系1不是EGEA和其他人群,但在这些人群肺功能没有在童年早期测量吗15,16。有充分的证据表明,减少气道大小的一个危险因素在病毒感染早期的喘息4。因此,它可能也会猜测17温度系数变异修改之间的联系减少肺功能在婴儿期和早发性哮喘。在功能余气量降低最大流量(V′马克斯,FRC)在第一年的生活是与瞬态有关,但不持久,早期的喘息,强烈的表型与病毒感染有关,在图森儿童呼吸系统的研究26。然而,它也表明,减少的值V′马克斯,FRC1月与持续喘息儿童在11岁的年龄从珀斯学习27。EGEA渊源者被招募在年龄≥7年,因此,我们的研究不能直接与出生队列研究图森、珀斯等研究26- - - - - -28在学校,在哮喘患儿年龄在EGEA包括更频繁。
特异反应性和早期呼吸道病毒感染都是独立与随后的哮喘有关,和特异反应性和呼吸道感染与强风险增加有关开发哮喘29日。大多数研究表明,17个snp对方篮里都不是与特异反应性或全部IgE,但可能是过敏性哮喘15- - - - - -17。然而,由于强烈的特异反应性之间的联系和哮喘儿童EGEA(几乎90%的哮喘儿童特应性),我们不能对过敏性哮喘和nonatopic进行单独分析。
持久和弛张哮喘在成年早期
EGEA的纵向设计提供了一个独特的机会来研究儿童哮喘的持久化到成年早期。这项研究没有足够的统计能力,进行单独的分析根据主体间发病年龄与持续或间歇性的哮喘;然而,大多数儿童哮喘(62%)有一个第一次哮喘发作年龄≤4岁。17的修改影响温度系数变异感染和哮喘之间的关系是最为明显的哮喘汇出在成年早期,表明17的功能作用温度系数变异可能局限于早期的生活事件,这可能是在以后的年龄长大。
ETS,早期的事件和表观遗传学
我们研究是否ETS暴露在生命早期进一步修改的呼吸道感染和哮喘之间的关联,但这导致了相对较小的子组。早期生活ETS暴露的额外修改效果,然而,似是而非,因为ETS暴露可以影响孩子的肺功能和免疫系统。ETS的小孩在子宫内或在生命早期表现出小而清晰的赤字在肺功能,并有明显的剂量依赖性关系的证据吸烟的母亲和儿童的肺功能30.。它也表明,暴露在ETS在生命早期会影响信号通过先天免疫受体,这可能与感染的易感性增加ETS暴露了婴儿31日。此外,在小鼠模型,香烟的烟雾被证明影响抗病毒促炎症过程10。Verlaanet al。25建议环境触发器和常见的17个温度系数变异可能影响表观遗传状态通过将平衡支持的一个染色质构象导致基因表达的变化。非常早期的窗口与ETS的表达和互动都支持这一假说的表观遗传变异的作用。
限制
子群分析导致相对小数量的科目,尤其是当考虑到ETS暴露。我们不能排除假阴性结果由于电力不足。虽然结果不被删除的有影响力的学科研究样本,解释应该谨慎和复制需要确认我们的观察。我们研究的另一个主要的限制是病毒性呼吸道感染回顾性评估问卷。我们没有客观数据确认自我幼年时期呼吸道感染病毒,尽管它是行之有效的,大多数的襁褓中的呼吸道疾病是由病毒感染引起的32。哮喘患儿的父母可能是更有可能召回呼吸道感染发作期间的前两年孩子的生活比没有哮喘的儿童的父母。尽管回忆偏倚可能导致感染和哮喘之间的关系的高估,它无法解释17温度系数的修改影响变异在这个协会。我们无法评估严重性的角色,也没有特定的病毒感染,如鼻病毒或RSV细支气管炎。最近,门诊气喘病与鼻病毒感染被证实是一个更强有力的后续预测因子哮喘与RSV比喘息1。是感兴趣的不仅复制我们的发现在未来的研究中,也以不同的方式探索17温度系数变异是否交互与鼻病毒或RSV细支气管炎。防止假阳性结果由于潜在的混杂因素或数据分层,假定值测试17个snp对方篮里的交互感染被模拟和计算导致这里显示相同的结果。我们没有Bonferroni调整到正确的申请多个测试,因为它是太保守了高水平的LD的12单核苷酸多态性分析。此外,进一步的单体型分析导致这里显示相同的结果。
总之,本研究显示了17个温度系数变异的重要作用,早期呼吸道感染和早期接触ETS早发性哮喘。我们的纵向数据也表明,17温度系数变异修改协会早期呼吸道感染和哮喘表型不持续到成年。因此,我们的结果增加了证据表明表达的相关窗口17温度系数变异是在生命早期。
确认
作者要感谢EGEA合作组:协调:F考夫曼;F Demenais(遗传学);我销(临床方面)。呼吸病学:M Korobaeff (Egea1), F巴斯坦·努克可荣获(Egea1) (Inserm U 700年,巴黎,法国);我Annesi-Maesano (Inserm U 707年,法国巴黎);F•考夫曼N Le Moual R Nadif,议员Oryszczyn (Inserm U 780、瑟、法国);V Siroux (Inserm U 823年法国格勒诺布尔)。遗传学:J法因戈尔德(Inserm U 393年,法国巴黎);E Bouzigon F Demenais MH Dizier (Inserm U 946年,法国巴黎);我直觉,米莱斯罗普(CNG,埃夫里市,法国)。 Clinical centres: I Pin, C Pison (Grenoble, France); D Ecochard (Egea1), F Gormand, Y Pacheco (Lyon, France); D Charpin (Egea1), D Vervloet (Marseille, France); J Bousquet (Montpellier, France); A Lockhart (Egea1)(Cochin, Paris, France), R Matran (Marseille, France); E Paty, P Scheinmann (Necker, Paris, France); A Grimfeld, J Just (Trousseau, Paris). Data and quality management: J Hochez (Egea1) (Inserm ex-U155, Paris); N Le Moual, C Ravault (Inserm U 780, Villejuif); N Chateigner (Inserm U 794, Evry); J Ferran (Grenoble, France).
作者感谢所有那些参与的设置学习和考试所涉及的各个方面。作者感谢三CIC-Inserm内克尔,格勒诺布尔和马赛人支持这项研究,受试者在第二个调查研究。感谢所有的人参加,并没有他们研究是不可能的。
脚注
↵可以从本文的补充材料www.www.qdcxjkg.com
支持声明
这项研究得到了法国高等教育与科研、大学巴黎Diderot-Paris 7,赠款从法国机构环境和职业健康安全(格兰特afsset - 4月- se - 2004),法国国家研究机构(赠款ANR 05 - s - 020 - 02/05 - 9 - 97和ANR 06-CEBS),默克公司大幅& Dohme (MSD),医院的临床研究计划(PHRC)巴黎,加布里埃尔,一个多学科研究来识别基因和环境引起的哮喘欧洲共同体(合同n 01896°集成项目激光冲徊化- 2004 1.2.5 - 1后基因组方法了解哮喘的分子偏见旨在预防或治疗控制)。L.A.M. Smit支持欧洲变态反应学和临床学院欧洲网络(EAACI-GA Immunology-Global过敏和哮喘2LEN)交换奖学金奖。
感兴趣的语句
一份声明中对这项研究可以发现www.www.qdcxjkg.com/misc/statements.dtl
- 收到了2009年9月30日。
- 接受2009年12月8日。
- ©2010人队















