文摘
特发性肺纤维化(IPF)是一种毁灭性的条件是有许多癌症的预后比。
最近的特发性间质性肺炎的分类重新定义了诊断标准确定IPF诊断所必需的。目前作者相信这种定义是不正确的,是依靠微妙的组织学差异的定义单独的疾病类别。
进一步问题影响IPF的研究观点的分化两种致病的假设。一个主张至高无上的炎症触发启动纤维化,另建议纤维化时由于慢性上皮损伤和修复的失败由于异常epithelial-mesenchymal交互。目前作者相信这个分裂是阻碍IPF和扭曲的理解研究重点。
相反,它认为,在多个通路异常参与伤口愈合,炎症导致特发性肺纤维化的发展,并建议一个新的理由的临床分类及发病机理可能更有效率在推动在未来寻找新的治疗方法。
特发性肺纤维化(IPF)是一种毁灭性的,进步的肺纤维化的条件中位数2.8 - -4.2岁的生存,并没有有效的治疗方法1,2。持续的科学和临床研究是至关重要的如果IPF发病机制的理解和有效的治疗方法。然而,有两个争议目前阻碍更好地理解IPF的努力。首先,2002年美国胸科学会(ATS) /欧洲呼吸学会(ERS)共识文件特发性间质性肺炎的分类(188bet官网地址表1所示⇓),目前的作者认为不正确,改变了IPF诊断标准诊断所必需的1。其次,两个相互竞争的致病假说是扭曲研究重点。在本文中,这两个问题得到解决和可能的解决方案建议。
IPF是什么?
ATS /人分类将IPF定义为“一个特定的形成原因不明的慢性fibrosing间质性肺炎,局限于通常的肺癌和与组织学实体相关的间质性肺炎”1。因此通常的间质性肺炎(摘要)和IPF现在被视为同义术语。新的分类的最有争议的方面是采用非特异性组织学病变的特发性间质性肺炎(NSIP)作为一种独特的疾病。与其他的特发性间质性肺炎,然而,NSIP并不表现出临床表型区别与摘要/ IPF。目前作者认为强调微妙的组织学差异摘要NSIP和使用这些定义单独的临床实体是不正确的,是阻碍试图更好地了解肺纤维化疾病的发病机理。
有强有力的证据表明,不同的疾病定义目的可能导致相同的组织学图片。结缔组织疾病、过敏性肺炎、石棉肺结节病可能导致摘要的组织学病变进展1。结缔组织疾病、过敏性肺炎、药物引起的肺部疾病,急性呼吸窘迫综合征和解决某些情况下的隐原性组织肺炎可能都产生一个组织学NSIP的照片1,3。成纤维细胞的焦点,摘要的基本特性,也发生在NSIP虽然没有那么频繁。此外,摘要和NSIP经常发现影响同一个人当肺活检样本取自不同站点IPF患者4。
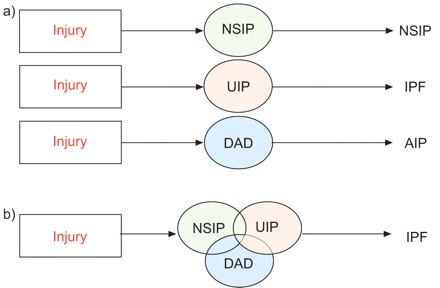
总的来说,患者的预后NSIP活检患者优于摘要(中位数生存33与56个月)5。然而,组织学不是唯一决定因素疾病的结果。Latsiet al。5显示,死亡率在前两年之后的诊断主要是与肺功能损害的严重程度和组织学诊断。此外,摘要患者活检,但不定或NSIP出现在高分辨率计算机断层扫描(HRCT)有更好的预后比摘要和一个典型的IPF HRCT上6。另一个最近的观察是,在IPF疾病进展,而不是总是被逐渐进步,经常发生通过一系列快速的逐步恶化7。这些明显的IPF急性加重的特色是在活检的出现弥漫性肺泡损伤,急性间质性肺炎的组织学病变7。这种共存的组织学和疾病行为模式挑战传统思维对这些条件的分离和不相关的性质(图1所示⇓)。
)当前提出的范式的分类系统是一个单独的损伤导致单独的组织学病变,因此单独的疾病。b)目前提出同样的损伤可能会导致一个或结合组织学病变,当共享一个共同的临床表型,代表单一疾病特发性肺纤维化(IPF)。NSIP:非特异性间质性肺炎;摘要:通常的间质性肺炎;爸爸:弥漫性肺泡损害;航:急性间质性肺炎。
家族IPF可能表现为不同成员的摘要或NSIP同样影响家庭。最近的一项研究的基因表达分析在摘要和NSIP家族或家庭之外的来源发现,只有零星的摘要之间微小的基因表达变化和零星NSIP病例,但更大的家族,分家例之间的变化8。在早期的研究中,塞尔曼说et al。9摘要显示显著的基因表达谱差异和过敏性肺炎,但发现病例的NSIP概要文件的摘要。这些数据提供了令人信服的证据,一个单一的疾病实体可能导致一系列的组织学异常负责。
重叠的组织实体,HRCT外观和肺功能的影响对疾病结果,基因表达谱和缺乏NSIP临床表型的强烈反对限制IPF的组织学诊断的摘要。目前作者认为特发性摘要和特发性NSIP,共享一个共同的临床表型,形成一个谱系疾病共同的发病机制。这是他们认为特发性间质性肺炎的分类,在未来,目标是归类的基础上疾病共同的发病的机制。基因表达分析提供了诱人的前景提供了一个新的IPF诊断的金标准。然而,鉴于目前缺乏一个明确的黄金标准测试,分类应结合临床,放射和病理方面的疾病表现和行为。依靠这种分类方法相结合,是希望所有点疾病的表型连续代表IPF可以承认,一些持续成功至关重要的临床和基础科学研究到这个毁灭性的疾病。
进展IPF的发病机制的理解
自1980年代中期以来,已经取得了显著的成就,在IPF的发病机制的理解。首次发病的假设形状主要由概念由伤口模型的研究。人们相信,在纤维化,夸张和不受控制的愈合反应发生时,关键的启动特性的炎性细胞pro-fibrotic产品的大量涌入和释放10。这种观点导致了信仰,纤维化可以预防通过抑制炎症反应,这理由仍然支撑着继续使用糖皮质激素和咪唑硫嘌呤IPF的一线治疗1。最近,论点,炎症细胞纤维化已受到密切关注。越来越多的研究人员现在认为,纤维化收益独立于炎症的事件。相反,他们认为,纤维化发展的后果异常上皮和epithelial-mesenchymal应对慢性肺泡上皮损伤11。
IPF:多种原因和多种途径?
哺乳动物防御机制进化多个分子途径和机制的细化和吸收伤口。进化的过程中创造了相当大的基因多效性,以及冗余,在细胞信号和伤口愈合通路。目前作者相信IPF的发展由于异常发生在多个生物学途径影响炎症和创伤修复。进化适应的结果,主要异常可以弥补单一关键分子招募否则冗余机制。通常只有当错误发生在多个路径保护机制是克服和疾病的发展。的想法最好被击中多次阐明恶性肿瘤,它已经表明,体细胞突变序列的关键需要致癌基因在恶性肿瘤的发展12。即使在best-characterised恶性肿瘤,序列的突变,导致同一疾病不同个体间13。此外,在许多不同的癌症,这种变化影响的响应特定的抗癌药物14。
现在清楚的是,两个人对IPF的易感性和疾病模式的行为和发展都与病人基因型15。一些调查人员进行广泛搜索纤维化基因。一系列的多态性对IPF的易感性有关,和疾病严重程度和进展15。此外,初步证据表明,体细胞基因突变在IPF的发展过程中发挥作用16,17。
IPF的触发启动纤维化的发展仍然是未知的。然而,有越来越多的证据表明,一个广泛的潜在的有害因素可能发挥作用在IPF的发生和发展18,19。过多的IPF患者大量吸烟1。氧化应激、环境污染和粉尘都牵扯IPF的潜在原因18。IPF患者病毒性呼吸道感染的研究表明过去感染的患病率增加19。此外,有一些迹象表明IPF患者遭受感染的特定亚型病毒尤其与体细胞突变的感应19。
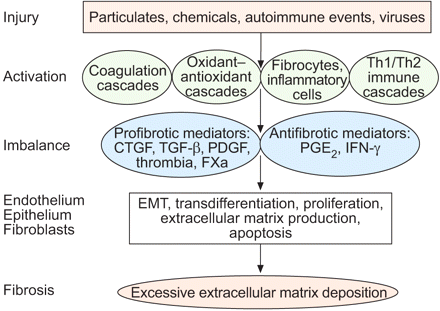
受伤后,当前提出multiple-pathway机制在起作用的发病机理IPF(图2所示⇓)。一系列的分子异常会导致纤维化现在特征。凝血级联,抗氧化途径,细胞凋亡,炎性细胞因子,血管生成和血管重塑,生长因子、表面活性剂和矩阵监管因素都与纤维化动物模型20.- - - - - -23。此外,这些串联启动行为和形态的变化多种细胞类型,包括上皮细胞、成纤维细胞、内皮细胞、居住和迁徙的炎症细胞,,最近被描述,循环纤维母细胞祖细胞(纤维细胞)20.- - - - - -25。这些关键路径的相对作用的证据,不同的细胞纤维化的发病机制之间的相互作用在人类逐渐形成20.- - - - - -25。
特发性肺纤维化的发病机制的新模型:损伤激活多个炎症、细胞信号和修复途径。激活这些pro -级联产生了不平衡和antifibrotic介质。反过来,这些介质激活多种细胞类型,导致细胞功能的变化,和最终的相互作用导致进行性纤维化。Th:辅助细胞;CTGF:结缔组织生长因子;TGF-β:转变增长factor-β;PDGF:血小板源生长因子;Xa FXa:因素;PG:前列腺素;IFN-γ:interferon-γ; EMT: epithelial–mesenchymal transition.
在其他复杂疾病一样,目前的作者相信这些关键通路的异常平衡影响个体之间可能会有所不同。这可以解释的范围临床、放射和病理表型IPF的观察。当前IPF思维倾向于关注个体介质纤维化或单通道与纤维发生有关。这个模型的局限性已经反映在令人失望的试验针对个别疾病的治疗途径26,27。持续的坚持这种方法可能会影响未来的治疗方法和治疗策略的发展。目前作者认为采用multiple-pathway理解IPF发病机理的模型将有利于未来的研究方法更适合这种复杂疾病的理解。此外,如果multiple-pathway假说是正确的,似乎最有效的治疗方法是同时针对多个纤维化通路。这种治疗方法类似于用于治疗许多癌症。此外,与许多癌症个性化治疗的基础上,每个病人的主要致病的途径成为可能的深入了解异常的平衡,导致肺纤维化。
结论
特发性肺纤维化是一种毁灭性的疾病。清晰的分类是特发性肺纤维化的障碍缺乏黄金标准的测试。未来尝试分类特发性间质性肺炎应该考虑疾病的临床和放射学表现,而不是仅仅依靠微妙的组织学差异为基础的定义单独的疾病实体。了解疾病的全谱环绕的特发性肺纤维化会有助于更好的了解其发病机制。然而,教条坚持单一途径是特发性肺纤维化的发病机制的关键是未来成功的障碍研究特发性肺纤维化,并有可能阻碍正在寻找治疗方法。multiple-pathway疾病发病机理模型更好的解释了当前可用的证据和提供了一个理由采用一种方法治疗,同时目标多个纤维化瀑布。
- 收到了2007年6月11日。
- 接受2007年7月16日。
- ©人期刊有限公司