抽象的
肺动脉高压的发病机制包括血管平滑肌细胞膜去偏振和随后的钙流入。通常,在这种条件下激活钙门控钾通道并使膜上搅拌。但是,在肺动脉高压下,它们下调。作者假设这些渠道的药理学增强会降低肺动脉高血压。
硫酸盐(DHEA-S,0.1mg·mL-1),最近表征的钙门控钾通道的活化剂,给予饮用水大鼠。
肺动脉血压,增加4周的缺氧(15±0.2至29.4±2.5mmHg),在用DHEA-S处理的大鼠中选择性地减弱了DHEA-S的持续时间(23.9±0.9mmHg)和大鼠的大鼠只有在肺动脉高压完全发育(缺氧的最后2周)后才会鉴于DHEA-S; 24.4±1.4 mmHg)。DHEA-S还减少了与肺动脉高压相关的肺血管重塑和右心室肥厚。心脏指数和全身性动脉血压在组中没有差异。
作者得出结论,用钙门控钾通道的活化剂处理,硫酸氢酮酮酮硫酸盐,已知是人体良好的耐受性,降低了大鼠的缺氧肺动脉高压。
该研究得到了捷克共和国的拨款机构的支持,授予NOS。306/97/0854,305 / 97 / S070和305/00/1432。
尽管肺动脉高压治疗干预的可能性最近有所扩大,但它们仍然具有重要的局限性,特别是效果特别不令人满意,严重的副作用和高成本1-7.。因此,需要对慢性肺动脉高压的有效,安全和易于使用的治疗遗体。
肺动脉高压的机制包括血管收缩和血管壁改造1。通过细胞内钙(CA)浓度([Ca.2+]一世)8.那9.,这反过来又受到膜势的主要管辖10.。在抗性肺动脉中,肌细胞的静息膜电位主要由电压门控钾(K)通道提供控制10.那11.。相反,CA门K(k加利福尼亚州)在休息条件下相对不活跃,但在细胞刺激时开放(IE。去极化和增加[CA.2+]一世)10.-13.。它们的开放复制细胞膜,因此用作负反馈限制降荡的阳性反馈10.那12.那13.。
因此,作者假设K的药理学增强加利福尼亚州渠道活动可以抑制肺动脉高压的发育。为了测试这一假设,最近表征的水溶性硫酸盐酯加利福尼亚州通道活化剂(DehydroepianDrosterone(DHEA)14.那15.)被使用,因为它被人类妥善了16.-18.。利用了大鼠肺动脉高压肺高血压良好的慢性缺氧模型。
方法
根据赫尔辛基公约和欧洲共同体和国家卫生研究院使用实验动物进行实验19.-21.。所有程序均由作者机构的动物研究委员会批准。
通过慢性暴露于缺氧(常乳10%氧,4周),在三组成年男性Wistar SPF大鼠中引发了肺动脉高压。22.。将它们与两组进行比较,没有肺动脉高血压(IE。保持在诺诺比亚(表1)⇓)。所有大鼠都是从捷克共和国的Anlab,布拉格,称重250克。
为了测试DHEA硫酸盐(DHEA-S)以防止肺动脉高压的发展,一组缺氧暴露的所有4周治疗DHEA-S(“预防性”给药,HD4)。为了看看DHEA-S是否可以逆转已经建立的肺动脉高压,当肺高血压完全开发时,另一组从缺氧暴露的第3周开始时给予DHEA-S 2周22.(“治疗”施用,组HD2)。剩余的缺氧大鼠没有接受任何治疗(H组)。为了排除DHEA-S对正常,健康的肺循环的不利影响,将一组常氧大鼠赋予DHEA-S 4周(ND4组),而剩余的常氧大鼠没有治疗(N组)。任何群体都没有死亡率。DHEA-S(Sigma-Aldrich,布拉格,捷克共和国)在饮用水中进行(0.1毫克·mL-1)。平均每日DHEA-S摄入量为9.0-9.7μg·g体重-1。
完成缺氧暴露和DHEA-S治疗后,大鼠用硫喷妥设计(40 mg·kg体·重量)麻醉-1那I.P.)。全身动脉血压(SAP;通过颈动脉插管)和肺动脉血压(PAP;通过颈静脉和右心室引入的导管)22.在大鼠自发呼吸室空气时测量。获得稳定值后,将大鼠通过气管造口气通风,在60呼吸·min-1和峰值吸气压力为6-8 cmh2O.胸腔切断后,用超声波流量计(T106 + 2.5 mm SS系列流量介绍,带有J-反射器的血液流动术后;跨音系统,伊萨卡,NY,USA)作为心输出的估计23.。该值相对于体重称为心脏指数。
取样左心室血液中的血细胞比容测定后,将心脏移除,右心室与左心室加隔膜重量比(RV / LV + S)被确定为与肺动脉高压相关的右心室肥大的量度。为了评估肺脉管系统的形态改造肺动脉高压,在甲醛固定肺的载玻片上计算厚壁厚围伏(≤300μm)(%TWPV)的百分比22.。
结果显示为平均值±SEM。使用一个因素分析的差异进行评估群体之间的差异,然后是Fisher的受受保护的最小差异后HOC.测试。p值为<0.05被认为是显着的。
结果
在暴露于慢性缺氧的结束时,大鼠的体重低于生活在室内空气中的同一年龄的大鼠。DHEA-S治疗对体重没有影响(表2⇓)。
正如预期的那样,慢性暴露于缺氧引发的肺动脉高血压:H组在N群中显着高于N组(图1A⇓)。重要的是,在用DHEA-S(HD4和HD2)处理的慢性缺氧基团中,PAP显着降低,所述慢性低氧基团比未处理的缺氧基团(H)仍然高于常见常见基团(N和ND4)(图。1A⇓)。在诺莫莫血症中,DHEA-S对PAP没有影响。
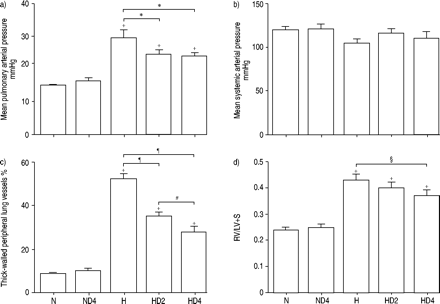
脱氢硫代酮酮酮酮(DHEA-S)选择性地减少大鼠慢性缺氧肺动脉高压。慢性缺氧诱导的肺动脉血压(a)的增加,厚壁外周肺血管(c)的百分比和左心室和左心室加隔膜重量比(RV / LV + S; d)都被DHEA减少- 治疗。通过慢性缺氧或DHEA-S不妨碍全身动脉血压(B)。n:21%氧气(o2)一直没有DHEA-S;ND4:21%O2所有的时间,DHEA-S在测量前的最后4周;h:10%o24周,没有DHEA-S;HD2:10%O24周,DHEA-S后2周的缺氧暴露;HD4:10%O24周,DHEA-S所有4周的缺氧暴露。数据显示为平均值±SEM。§:P <0.05;*:P <0.01;#:P <0.005;¶:P <0.0001;+:P <0.0005缺氧基团不同于常氧基团。
DHEA-S对肺循环的选择性,因为没有改变SAP(图1B⇑)。DHEA-S通过DHEA-S的减少不介绍心输出或血细胞比容的任何改变,因为缺氧群体都没有不同(表2⇑)。DHEA-S在常氧中的胃科减少了令人惊讶的减少(ND4相对n,表2⇑)被注意到,作者没有解释,特别是随着DHEA-S对慢性缺氧没有这样的作用。作者不知道在人类摄取DHEA或DHEA-S中报道的减少的血细胞比容。在常氧的DHEA-S治疗没有改变心脏输出和SAP(表2⇑和图。1B.⇑)。
与慢性缺氧肺动脉高压相关的周围肺血管的增厚在该研究中显而易见为H的高%TWPV与N和ND4组相比。DHEA-S以依赖于治疗持续时间的方式显着降低了这种增加(图1C⇑)。
慢性缺氧肺动脉高压与右心室肥大有关:H组右心室壁和RV / LV + S的重量显着高于N组(图1D⇑,表2⇑)。从缺氧曝光开始的DHEA-S管理限制了右心室肥厚的发育,如HD4组中的下RV / LV + S所示于HD4组的研发(图1D⇑)。此外,HD4和N组之间右心室壁的重量没有显着差异(表2⇑)。然而,HD2和H组在右心室重量或RV / LV + S中没有不同(表2⇑, 无花果。1D⇑)。左心室加隔膜重量不受DHEA-S的影响(表2⇑)。
讨论
结果表明,DHEA-S的预防性和治疗应用选择性地减少了通过慢性暴露于缺氧的大鼠引发的肺动脉高血压。这种发现可能是临床兴趣,因为人类长期DHEA或DHEA-S摄取的相当大的经验证明其安全性16.-18.。
DHEA(3β-羟基-5-和rosten-17-One)及其硫酸化形式是定量最丰富的哺乳动物类固醇,包括人类24.。它们是由肾上腺皮质刺激肾上腺皮质分泌的25.。虽然他们已知超过半个以上,但他们的生理作用和行动机制仍然仍然不足24.-26.。DHEA是生物活性雄激素和雌激素的前体,但不考虑其多种抗癌,抗静电,抗糖尿病,抗肥胖和免疫保护作用24.-26.。这些动作未通过特定的细胞内受体介导。DHEA作用的提出机制包括用于一些效应(特别是免疫保护),抗氧化性能的抗荧光皮质激活24.-26.而且,最近,激活k加利福尼亚州渠道14.。后两种机制中的每一个能够通过本研究观察到的DHEA-S来降低肺动脉高压。在这种情况下,抗荧光皮质激素效应不太可能在这种情况下发挥作用,因为肾上腺切除术不影响慢性缺氧肺动脉高血压的发育27.。
DHEA-S最初在本研究中进行了测试,以查看对K的影响加利福尼亚州频道激活。而K.加利福尼亚州在静止条件下,通道几乎没有活性抗肺动脉,它们在膜去偏振上打开并增加[CA.2+]一世10.-13.。在这种情况下,k加利福尼亚州通道开口倒装细胞膜,从而用作限制去极化程度和随后的Ca流入,血管收缩和增殖的伺服机构10.那12.那13.。虽然肺血管平滑肌肉去偏振并增加[CA.2+]一世存在于肺动脉高血压中28.-33.,,,,,,,,K加利福尼亚州渠道活动预计会上升,实际上已经反复显示减少31.那33.,可能是由于通道蛋白表达的下调。这个k的原因和机制加利福尼亚州通道下调是未知的,但它可能有助于持续的去偏振和增加[CA2+]一世肺动脉高压。因此,药理学k可能很可能加利福尼亚州DHEA-S补偿慢性缺氧诱导损失的频道刺激加利福尼亚州通道限制血管平滑肌膜去偏振的能力。值得注意的是,一氧化氮,可用于几种形式的肺动脉高压的临床管理,也通过激活k导致肺血管舒张加利福尼亚州渠道34.。
DHEA-S也可以减少肺动脉高压通过其抗氧化能力。氧化应激在肺动脉高压机制中似乎很重要35.。用抗氧化剂治疗大鼠,N- 在慢性缺氧期间,在慢性缺氧期间患有类似程度的血糖胞嘧啶,如目前的DHEA-S所见类似的程度36.。
对本研究的意外观察是治疗(2周)DHEA-S对罂粟和右心室肥大的影响之间的解剖。在HD2组中,PAP显着低于未处理的缺氧大鼠,而RV / LV + S不是。随着右心室肥大被认为是由于PAP升高导致的后载增加的结果37.,在减少PAP后,右心室肥厚可能存在右心室肥厚的时间不足。
总之,通过慢性暴露于缺氧,钙门钾通道活化剂和抗氧化剂,脱氢钠酮酮酮酮酮硫酸盐,降低了大鼠肺动脉高血压。在这方面,如果从缺氧暴露的开始或从中间暴露开始时,脱氢硫代酮酮酮硫酸盐同样有效,当肺动脉高压完全发育肺动脉高压时。作为脱氢硫代酮酮硫酸盐,众所周知,人类耐受,它可能证明对至少某种类型的慢性肺动脉高压的临床管理有益。
- 已收到2002年9月12日。
- 公认2002年11月20日。
- ©ers Journals Ltd