抽象的gydF4y2Ba
作者最近证实了亚甲基蓝(MB),一氧化氮(NO)通路的抑制剂,减少了内毒素血症羊肺毛细血管压力、肺淋巴流量和蛋白质清除的增加。在本研究中,作者检测了MB是否通过一氧化氮途径以外的机制影响肺血流动力学和血管外肺水(EVLW)的积累。gydF4y2Ba
十六件清醒,慢性仪表绵羊随机接受静脉注射MB 10 mg·kggydF4y2Ba−1gydF4y2Ba或等渗盐水。三十分钟后,所有绵羊都接受了静脉注射的gydF4y2Ba大肠杆菌gydF4y2Ba内毒素1μg·kggydF4y2Ba−1gydF4y2Ba20分钟,静脉输注MB 2.5 mg·kggydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba或等渗盐水6小时。gydF4y2Ba
MB显着减弱内毒素诱导的肺动脉高压和右心室破坏,降低了EVLW的积累。此外,MB降低了血浆血栓素B中的增量gydF4y2Ba2gydF4y2Ba和6-keto-prostaglandin FgydF4y2Ba1α.gydF4y2Ba,消除了发热反应。然而,MB对循环中性粒细胞、血清透明质酸和替代补体途径的总溶血活性的变化没有影响。gydF4y2Ba
作者得出结论,在绵羊中,亚甲基蓝通过抑制花生四烯酸的环加氧酶产物,至少在一定程度上减轻了内毒素诱导的肺动脉高压和水肿。这是亚甲基蓝的一种新效应gydF4y2Ba在活的有机体内gydF4y2Ba.gydF4y2Ba
- 内毒素gydF4y2Ba
- 肺血管外的水gydF4y2Ba
- 亚甲蓝gydF4y2Ba
- 肺循环gydF4y2Ba
- 6-keto-prostaglandin fgydF4y2Ba1α.gydF4y2Ba
- 血栓滤蛋B.gydF4y2Ba2gydF4y2Ba
本研究部分由挪威研究委员会(Grant 120473/730),雅典急性医学基金会和部门基金支持。gydF4y2Ba
急性肺损伤(ALI)是一种肺部表现的全身性炎症过程,通常与脓毒症有关。肺水肿是由肺微血管压力和通透性增强引起的,是ALI的病理生理特征gydF4y2Ba1gydF4y2Ba.各种介质在Ali中涉及,例如内毒素,细胞因子,籽糖苷,补体,细胞外基质的降解片段,以及氧自由基gydF4y2Ba1gydF4y2Ba- - - - - -gydF4y2Ba4gydF4y2Ba.越来越多的证据也表明,一氧化氮(NO)在发病机制中起着重要作用gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.gydF4y2Ba
NO是一种由l-精氨酸合成的自由基,由NO合成酶家族(NOS)合成。在正常肺中,一氧化氮由两种结构性一氧化氮合酶亚型(内皮和神经元一氧化氮合酶)产生,这两种一氧化氮合酶亚型定位于肺血管内皮细胞、气道上皮细胞和非肾上腺素能、非胆碱能神经纤维gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.内皮细胞NO扩散到相邻的平滑肌细胞并激活可溶性鸟苷酸环化酶,生成环状鸟苷3’-5’单磷酸(cGMP)。反过来,cGMP引起平滑肌松弛,从而调节肺血管和支气管张力gydF4y2Ba5gydF4y2Ba- - - - - -gydF4y2Ba8gydF4y2Ba.神经元没有介导神经递质,也可以调节支气管扩张gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.一氧化氮合酶的第三种亚型,即诱导型一氧化氮合酶,在许多类型的细胞中表达和活性上调,包括巨噬细胞、中性粒细胞、成纤维细胞、血管平滑肌和气道上皮细胞对内毒素和促炎细胞因子的反应gydF4y2Ba5gydF4y2Ba- - - - - -gydF4y2Ba7gydF4y2Ba,gydF4y2Ba9gydF4y2Ba.根据损伤的严重程度,该亚型可能产生过量的NO,导致肺微血管损伤和肺血管收缩缺氧损伤,并伴有外周循环衰竭。NO的有害作用在很大程度上是由于增强cGMP的产生、激活环氧化酶(COX)、改变补体途径、产生活性氧和活性氮以及诱导细胞凋亡gydF4y2Ba5gydF4y2Ba- - - - - -gydF4y2Ba7gydF4y2Ba,gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba11.gydF4y2Ba.gydF4y2Ba
抑制可诱导的一氧化氮合酶(NOS)活性已被发现可以减弱实验性ALI的形态学特征,并改善动脉氧合gydF4y2Ba11.gydF4y2Ba.然而,有报道称,在使用非选择性NOS抑制剂后,肺血管张力进一步增加,甚至肺水肿加重gydF4y2Ba12.gydF4y2Ba.最近,作者证实了内毒素性羊亚甲基蓝(MB)是一氧化氮合酶和可溶性鸟苷酸环化酶的非选择性抑制剂gydF4y2Ba8gydF4y2Ba,gydF4y2Ba13.gydF4y2Ba,通过肺淋巴流量和蛋白清除评估,显著降低了肺液过滤的增加。MB的作用与降低肺毛细血管压力和通透性-表面积产物有关。此外,MB改善了气体交换,并阻止了肺淋巴和血浆cGMP的增加,以及血浆亚硝酸盐和硝酸盐gydF4y2Ba14.gydF4y2Ba,gydF4y2Ba15.gydF4y2Ba.本研究的目的是进一步探讨MB是否会影响肺血管动力学并防止其他机制除了抑制无途径之外的其他机制的含蓄血管肺水(EVLW)。gydF4y2Ba
材料和方法gydF4y2Ba
动物的准备gydF4y2Ba
本研究经挪威实验动物委员会批准。两性的十六岁的绵羊,体重37.6±1.6千克(平均±SEM),用氟烷0.8-1.25%(Astrazeneca,Cheshire,Cheshire,英国)。一种医疗级导管(131162-24; Kebo Lab,Stockholm,Sweden)被植入到左心房中gydF4y2Ba通过gydF4y2Ba在第四次肋间空间中的左胸传道术。此外,还将5-FR介绍者(CP-07511-P; Arrow International,Reading,Pa,USA)插入左常见的颈动脉和8.5-F介绍者(CC-350B; Baxter Healthcare,Irvine,CA,美国)被置于左外部颈静脉。手术后,使动物恢复1周。gydF4y2Ba
测量和样品gydF4y2Ba
实验当天,将醒着的羊放入实验笼中。4-Fr光纤热敏电阻导管(PV2024L;推手医疗系统,慕尼黑,德国)是先进的胸主动脉。7-Fr定向热稀释导管(131HF7;(Baxter Healthcare)被引入肺动脉。导管连接到压力传感器(transac III;Abbott Critical Care Systems,北芝加哥,IL,美国),并持续用肝素10 IU·kg生理盐水冲洗gydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba(Nycomed Pharma,Oslo,挪威)。在565A患者数据监视器(Kone,Espoo,Finland)上显示了心率,平均动脉压(MAP),平均肺动脉压(PAP),肺动脉闭塞压力(PAOP),肺动脉闭塞压力(PAOP)和平均左心房压力(LAP)。压力被记录在79个多指(草图,昆西,MA,USA)上,常设动物的前腿肩部的零参考水平。有效的肺毛细管压力(gydF4y2BaPgydF4y2BacgydF4y2Ba)根据Holloway技术衍生自PAOP跟踪gydF4y2Ba等等。gydF4y2Ba16.gydF4y2Ba.gydF4y2Ba
体表面积计算为BWgydF4y2Ba0.67gydF4y2Ba×0.084,其中BW为kg体重。通过热染料稀释技术确定心脏指数(CI),EVLW,肺血容量指数(PBVI)和右心室喷射级分(RVEF),如冷Z-021(脉动医疗系统)评估。吲哚菁绿冰冷溶液的5-mL荧光溶液的稀释曲线(0.5mg·mlgydF4y2Ba−1gydF4y2Ba(在5%葡萄糖)(斥力医疗系统)注入右心房显示,并立即检查。排除慢洗脱曲线,每个变量都计算为5次成功测量的平均值。此外,采用光纤热敏电阻导管测量体温。计算系统血管阻力指数(SVRI)为:gydF4y2Ba 和肺血管阻力指数(PVRI)为:gydF4y2Ba
和肺血管阻力指数(PVRI)为:gydF4y2Ba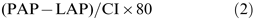 使用Evans Blue和血细胞计数计数静脉血白细胞,并且使用用May-Grünwald-Giemsa染色的载玻片涂片测定白细胞差分计数。收集肺动脉血液的样品,进入凝块活化剂管(Vacutainer 367789; Becton Dickinson,Meylan Cedex,法国)和含有乙二胺四乙酸(EDTA; Sigma Chemical Co.,St Louis,Mo,Mo,USA的管)的管和0.04米吲哚美辛。采样后立即,血液以4°C离心(2,000×gydF4y2BaggydF4y2Ba10分钟)。将血清和等离子体样品储存在-70℃直至分析。gydF4y2Ba
使用Evans Blue和血细胞计数计数静脉血白细胞,并且使用用May-Grünwald-Giemsa染色的载玻片涂片测定白细胞差分计数。收集肺动脉血液的样品,进入凝块活化剂管(Vacutainer 367789; Becton Dickinson,Meylan Cedex,法国)和含有乙二胺四乙酸(EDTA; Sigma Chemical Co.,St Louis,Mo,Mo,USA的管)的管和0.04米吲哚美辛。采样后立即,血液以4°C离心(2,000×gydF4y2BaggydF4y2Ba10分钟)。将血清和等离子体样品储存在-70℃直至分析。gydF4y2Ba
协议gydF4y2Ba
在稳定的基线血流动力学测量2-2.5 h后,记录−0.5 h时的值。随后,动物被随机分配给静脉注射MB 10 mg·kggydF4y2Ba−1gydF4y2Ba(Nycomed Pharma)(MB组),或相应体积的等渗盐水(对照组)。从时间开始0小时,gydF4y2Ba大肠杆菌gydF4y2BaO26:B6内毒素1μg·kggydF4y2Ba−1gydF4y2Ba(Sigma Chemical Co.)溶解在30ml等渗盐水中静脉注入20分钟。MB组另外收集了MB 2.5 mg·kg的输注gydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba对照组给予相应体积的等渗生理盐水,持续6 h。末次测定后,用硫喷妥钠100 mg·kg处死gydF4y2Ba−1gydF4y2Ba(雅培实验室,北芝加哥,美国,美国)。gydF4y2Ba
生物化学分析gydF4y2Ba
血凝素(Tx) B的浓度gydF4y2Ba2gydF4y2Ba6-酮前列腺素(PG) FgydF4y2Ba1α.gydF4y2Ba,溶质代谢物的血栓素agydF4y2Ba2gydF4y2Ba和前列腺素(PGIgydF4y2Ba2gydF4y2Ba)分别由酶免疫测定(Biotrak RPN220和RPN221; Amersham International,Buckinghamshire,英国)测定。通过辐射测定(10-9294-01; Pharmacia和Upjohn诊断,乌普萨拉,瑞典)测量血清透明质酸浓度。通过在含有0.1%明胶(Sigma Chemical Co.)和7mM EDTA的含有0.1%的明胶(Sigma Chemical Co.)和7mM EDTA的37℃下,通过将羊血清稀释1:15稀释1:15,在37°C下用2%洗涤的兔红细胞孵育,含有0.1%的兔红细胞,测量替代补体途径的总溶血活性。在96微型井板。将板离心并将上清液除去在另一个板上,并在410nm处读取光密度。结果称为含有100%裂解活性的正常人血清的标准曲线。绵羊替代的溶血活性非常接近人的价值〜100%。gydF4y2Ba
统计分析gydF4y2Ba
数据表示为平均值±SEM。对于每个变量,检查正常性。通过双向方差分析评估数据。如果F值统计学意义,则使用不配对的双尾T-试验或配对T检验来分别评估基团与基数之间的差异朝向基线值。概率值<0.05被认为是显着的。gydF4y2Ba
结果gydF4y2Ba
血液动力学gydF4y2Ba
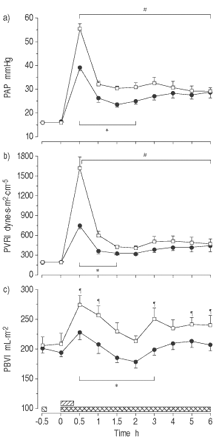
MB显着抑制了内毒素的血液动力学响应(图1gydF4y2Ba⇓gydF4y2Ba和表1gydF4y2Ba⇓gydF4y2Ba).与对照相比,MB将PAP的增量降低至0.5至2小时,并在PVRI和PAOP以0.5至1.5小时的〜60%(P <0.05)。此外,MB减少了增加gydF4y2BaPgydF4y2BacgydF4y2Ba在整个实验中,约50% (p<0.05)。对照组4 ~ 5 h LAP较基线水平略有升高(p<0.05)。PBVI在0.5 ~ 1 h、3 h和5 ~ 6 h均呈上升趋势(p<0.05)。在MB组,LAP和PBVI与基线相比保持不变,后者显示0.5和3 h组间差异(p<0.05)。同时,MB在0.5 ~ 3 h和5 h时降低了RVEF (p<0.05)。MB也能抵消MAP和CI的下降(p<0.05),但SVRI组间无差异。gydF4y2Ba
亚甲基蓝(Mb)对清醒,内臭绵羊肺血管动力学的影响(平均值±SEM,N = 8只动物/组)。a)平均肺动脉压(PAP);b)肺血管阻力指数(PVRI);c)肺血容量指数(PBVI)。□:内毒素(ET)对照组;•:MB / ET组。在这两个群体中,gydF4y2Ba大肠杆菌gydF4y2BaET1μg·kggydF4y2Ba−1gydF4y2Ba注射时间:0小时(0秒)。MB组给予MB 10 mg·kggydF4y2Ba−1gydF4y2BaET(┘)之前0.5小时,然后输注MB 2.5 mg·kggydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba从ET开始(gydF4y2Ba ).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组支架内各时间点与组内基线相比p<0.05;gydF4y2Ba¶gydF4y2Ba:在对照组中,来自Intragrous基线的P <0.05。gydF4y2Ba
).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组支架内各时间点与组内基线相比p<0.05;gydF4y2Ba¶gydF4y2Ba:在对照组中,来自Intragrous基线的P <0.05。gydF4y2Ba
亚甲基蓝于血流动力学对唤醒,内臭绵羊的影响gydF4y2Ba
肺血管外含水量gydF4y2Ba
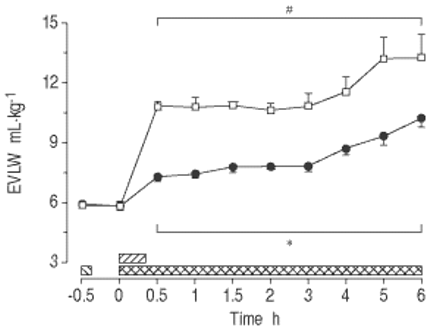
对照组的EVLW增加了2倍以上(p<0.001;图2gydF4y2Ba⇓gydF4y2Ba).相比之下,MB在整个研究中减少了30-50%的EVLW的积累(P <0.05)。gydF4y2Ba
亚甲基蓝(Mb)对清醒,内臭绵的血管肺水(EVLW)含量的影响(平均值±SEM,N = 8只动物/组)。□:内毒素(ET)对照组;•:MB / ET组。在这两个群体中,gydF4y2Ba大肠杆菌gydF4y2BaET1μg·kggydF4y2Ba−1gydF4y2Ba注射时间:0小时(0秒)。MB组给予MB 10 mg·kggydF4y2Ba−1gydF4y2BaET(┘)之前0.5小时,然后输注MB 2.5 mg·kggydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba从ET开始(gydF4y2Ba ).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组中支架内所有个体时间点与组内基线相比p<0.05。gydF4y2Ba
).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组中支架内所有个体时间点与组内基线相比p<0.05。gydF4y2Ba
Cyclo-oxygenase产品gydF4y2Ba
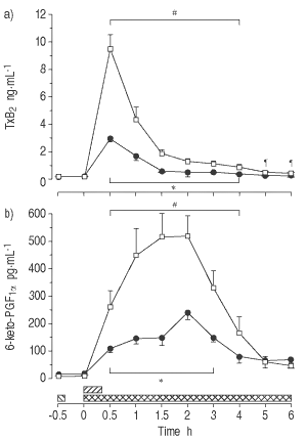
在对照组中,等离子体TXBgydF4y2Ba2gydF4y2Ba在0.5 h时达到高于基线85倍的峰值,与血浆6-酮- pgf的增加平行gydF4y2Ba1α.gydF4y2Ba,2小时达到75倍(P <0.01;图3gydF4y2Ba⇓gydF4y2Ba).此后,TxBgydF4y2Ba2gydF4y2Ba和6-keto-PGFgydF4y2Ba1α.gydF4y2Ba逐渐下降,尽管在整个实验和4小时的情况下显示Intragrous差异(P <0.05)。与控件相比,MB在TXB中降低了峰值增量gydF4y2Ba2gydF4y2Ba通过70%和6-keto-pgfgydF4y2Ba1α.gydF4y2Ba在4和3 h时,组间差异仍然存在(p<0.05)。gydF4y2Ba
亚甲基蓝(Mb)对A)血栓素B等血浆浓度的影响gydF4y2Ba2gydF4y2Ba(TXB.gydF4y2Ba2gydF4y2Bab) 6-酮前列腺素FgydF4y2Ba1α.gydF4y2Ba(6-keto-PGFgydF4y2Ba1α.gydF4y2Ba)在清醒中,内毒素绵羊(平均值±SEM,n = 8只动物/组)。□:内毒素(ET)对照组;•:MB / ET组。在这两个群体中,gydF4y2Ba大肠杆菌gydF4y2BaET1μg·kggydF4y2Ba−1gydF4y2Ba注射时间:0小时(0秒)。MB组给予MB 10 mg·kggydF4y2Ba−1gydF4y2BaET(┘)之前0.5小时,然后输注MB 2.5 mg·kggydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba从ET开始(gydF4y2Ba ).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组支架内各时间点与组内基线相比p<0.05;gydF4y2Ba¶gydF4y2Ba:在对照组中,来自Intragrous基线的P <0.05。gydF4y2Ba
).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组支架内各时间点与组内基线相比p<0.05;gydF4y2Ba¶gydF4y2Ba:在对照组中,来自Intragrous基线的P <0.05。gydF4y2Ba
体温和实验室变量gydF4y2Ba
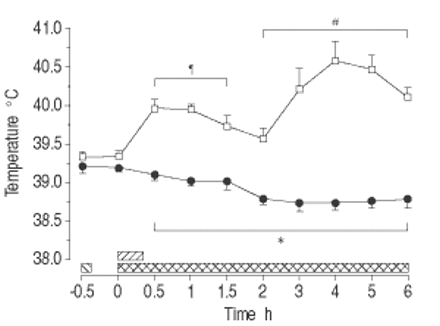
MB废除内毒素诱导的发热响应(P <0.001;图4gydF4y2Ba⇓gydF4y2Ba).在这两组中,循环中性粒细胞计数迅速下降至25倍,而血清透明质素均逐渐增加(P <0.01),而无杂项差异(表2gydF4y2Ba⇓gydF4y2Ba).替代补体途径的总溶血活性的变化是温和的,尽管观察到一些统计上显著的差异。在对照组中,替代补体途径的总溶血活性在0.5 h时略有增加,然后在1.5 ~ 3 h低于基线水平时下降(p<0.05)。MB组在2 h和4 ~ 6 h出现微弱下降,5 h组间差异有统计学意义(p<0.05;表2gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
亚甲基蓝(MB)对清醒内毒素血症绵羊体温的影响(平均±扫描电镜,n=8只/组)。□:内毒素(ET)对照组;•:MB / ET组。在这两个群体中,gydF4y2Ba大肠杆菌gydF4y2BaET1μg·kggydF4y2Ba−1gydF4y2Ba注射时间:0小时(0秒)。MB组给予MB 10 mg·kggydF4y2Ba−1gydF4y2BaET(┘)之前0.5小时,然后输注MB 2.5 mg·kggydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba从ET开始(gydF4y2Ba ).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组支架内各时间点与组内基线相比p<0.05;gydF4y2Ba¶gydF4y2Ba:与对照组组内基线相比,支架内所有个体时间点p<0.05。gydF4y2Ba
).*:在支架内的所有单个时间点之间的组之间P <0.05;gydF4y2Ba#gydF4y2Ba:两组支架内各时间点与组内基线相比p<0.05;gydF4y2Ba¶gydF4y2Ba:与对照组组内基线相比,支架内所有个体时间点p<0.05。gydF4y2Ba
亚甲基蓝于实验室变量在清醒,内臭绵羊中的影响gydF4y2Ba
讨论gydF4y2Ba
本研究表明,在内泌毒性绵羊中,MB以减毒的肺动脉高压和增加的rvef,减少了EVLW的积累。MB的这些效果与COX产品TXB的抑制相关gydF4y2Ba2gydF4y2Ba和6-keto-PGFgydF4y2Ba1α.gydF4y2Ba以及对内毒素的发热反应。gydF4y2Ba
人Ali的大多数病理特征可以通过生身细菌或内毒素的系统性输注来模仿。绵羊对内毒素特别敏感,并患有肺动脉高压,右心室破坏和肺液过滤增加gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba17.gydF4y2Ba,gydF4y2Ba18.gydF4y2Ba.在本研究的对照组中,作为EVLW评估的肺水肿,在暴露于内毒素时迅速上升,然后对实验的其余部分逐渐增加。相比之下,用MB处理的动物显着降低EVLW的积累。在组之间差异的单一致病因子是肺动量的血管收缩。虽然MB只会减少PAP和PVRI中的早期相位增量,gydF4y2BaPgydF4y2BacgydF4y2Ba在整个研究中是对照组的一半。这些发现证实了作者最近在内毒素血症绵羊中观察到的预处理后持续滴注MB减少了PAP、pvid - 19和pvid - 19的增加gydF4y2BaPgydF4y2BacgydF4y2Ba14.gydF4y2Ba,gydF4y2Ba15.gydF4y2Ba.因此,我们认为MB后EVLW的降低至少部分是由于肺微血管压降低的结果。然而,MB可以通过降低肺微血管通透性和/或表面积来降低EVLWgydF4y2Ba14.gydF4y2Ba.本观察到MB阻止了PBVI的增加gydF4y2BaPgydF4y2BacgydF4y2Ba暴露于内毒素后,支持后一种假设。此外,在内毒性晚期的后期,MB可以增强肺淋巴的泵送,最有可能通过减少淋巴血管中过量的CGMP产生gydF4y2Ba14.gydF4y2Ba.这种效果也可能导致本研究中EVLW的较少积累。gydF4y2Ba
除了降低肺动脉高压和水肿,MB减轻了内毒素暴露后RVEF的下降。后一种影响很可能是由于心脏后负荷降低所致。反过来,右心室功能的改善可能有助于更好地维持CIgydF4y2Ba18.gydF4y2Ba因此,由于SVRI保持不变,因此地图。改善血液力学的另一种可能的机制可以是MB抵消了内毒素诱导的心肌收缩性降低,这是由CGMP介导的gydF4y2Ba19.gydF4y2Ba.gydF4y2Ba
内毒素和NO激活花生四烯酸的COX通路,导致TxA的合成gydF4y2Ba2gydF4y2Ba,pgi.gydF4y2Ba2gydF4y2Ba等前列腺素gydF4y2Ba2gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba.TXAgydF4y2Ba2gydF4y2Ba是早期肺动脉混凝土和支气管混凝土的主要介体。此外,TXAgydF4y2Ba2gydF4y2Ba刺激血小板聚集和中性粒细胞粘附,并可能提高肺微血管通透性。相比之下,PGIgydF4y2Ba2gydF4y2Ba产生相反的生理效应。因为酸gydF4y2Ba2gydF4y2Ba和PGIgydF4y2Ba2gydF4y2Ba快速水解,通过测定其生物学 - 活性代谢物,TXB来测量它们的活性gydF4y2Ba2gydF4y2Ba和6-keto-PGFgydF4y2Ba1α.gydF4y2Ba分别gydF4y2Ba2gydF4y2Ba.gydF4y2Ba
在本实验中,内毒素引起了血浆TXB的快速增加gydF4y2Ba2gydF4y2Ba随后随后随后与血浆6-keto-pgf逐渐增加的平行下降gydF4y2Ba1α.gydF4y2Ba.这种前列腺释放模式与内毒性绵羊的先前观察结果一致gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba18.gydF4y2Ba.有趣的是,作者发现MB明显降低了TXB的血浆浓度gydF4y2Ba2gydF4y2Ba和6-keto-PGFgydF4y2Ba1α.gydF4y2Ba.早期的研究还表明,MB可以拮抗花生素酸和Bradykinin诱导的TXA的产生gydF4y2Ba2gydF4y2Ba和PGIgydF4y2Ba2gydF4y2Ba通过抑制可溶性胍基环化酶的机制,在人血小板和猪主动脉内皮细胞中gydF4y2Ba21.gydF4y2Ba,gydF4y2Ba22.gydF4y2Ba.然而,本研究是第一个证明MB抑制内毒素诱导的COX产品的全身释放的gydF4y2Ba在活的有机体内gydF4y2Ba.迄今为止,这种效果背后的确切机制仍然不清楚。前列腺的减少的系统释放可能是由对受体偶联机构的干扰导致控制膜磷脂的释放的受体耦合机构,通过氧化铁血管部分的COX和末端PG合成酶的量和/或活性的变化酶或细胞外分泌减少gydF4y2Ba2gydF4y2Ba,gydF4y2Ba22.gydF4y2Ba.此外,一些NOS抑制剂,如NgydF4y2BaGgydF4y2Ba据报道,-硝基-精氨酸甲酯和氨基胍也能减少COX产物的生成,从而表明NO和COX通路之间的相互作用gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba11.gydF4y2Ba.因此,MB抑制TXAgydF4y2Ba2gydF4y2Ba最有可能对观察到肺动脉高压和EVLW的减少以及改善的rvef。这与许多研究表明TXA的抑制剂一致gydF4y2Ba2gydF4y2BaTXA的合成和拮抗剂gydF4y2Ba2gydF4y2Ba受体在实验ALI中衰减肺动量血管收缩,水肿形成和右心室衰竭gydF4y2Ba17.gydF4y2Ba,gydF4y2Ba18.gydF4y2Ba,gydF4y2Ba23.gydF4y2Ba,gydF4y2Ba24.gydF4y2Ba.此外,其他脂质介质如白三烯和血小板活化因子也在ALI中大量释放,有助于肺部微血管压力和渗透性变化gydF4y2Ba2gydF4y2Ba,gydF4y2Ba25.gydF4y2Ba.因此,需要阐明MB对这些介质的可能影响。gydF4y2Ba
作者观察到MB对血流动力学和EVLW的有利影响是在排除发烧的同时发生的。后一种作用可能是由于抑制PGE的合成gydF4y2Ba2gydF4y2Ba,调节发热反应。有证据表明MB可以抵消白细胞介素(IL)-1β诱导的PGE的产生gydF4y2Ba2gydF4y2Ba在培养的人气道上皮细胞中gydF4y2Ba10.gydF4y2Ba.另一种解释可能是Mb的有益效果至少部分地从减少贡献发热反应和内皮损伤的反应性氧物种的形成gydF4y2Ba26.gydF4y2Ba.然而,后一种假设在本研究中并没有被特别提到。gydF4y2Ba
透明质酸,一种肺细胞外基质的糖胺基聚糖组成部分,是正常间质性建筑和组织水合的重要调节因素gydF4y2Ba27.gydF4y2Ba.Hyaluronan的增加浓度存在于支气管肺泡灌洗液和来自败血症诱导的Ali患者的血清中存在gydF4y2Ba4gydF4y2Ba.反过来,透明质酸降解片段可能上调炎症细胞中可诱导的NOS表达,促进肺部炎症的传播gydF4y2Ba28.gydF4y2Ba.在本调查中,作者发现内毒素增加了血清透明质酸浓度。后者可能反映了肺部过度的透明质植物流出,同意先前的化粪池绵羊的研究gydF4y2Ba29.gydF4y2Ba.然而,MB对透明质酸的变化没有影响,表明肺部流体过滤没有受该机制的影响。gydF4y2Ba
对内毒素的肺部血液动力学反应显然在反刍动物中比其他物种更突出。这被认为主要是由于存在常驻肺血管内巨噬细胞。内毒素引发肺巨噬细胞,用于增加NO和促炎细胞因子的产生,例如肿瘤坏死因子-α和IL-1β。反过来,后一种细胞因子刺激肺毛细血管内中性粒细胞招生和保留,随后的肺部损伤gydF4y2Ba1gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba9gydF4y2Ba.在绵羊内卵血症中,已显示低外周白细胞计数与肺液过滤和低氧血症增加相关gydF4y2Ba17.gydF4y2Ba,gydF4y2Ba18.gydF4y2Ba.在本研究中,作者发现MB没有改变循环中性粒细胞计数的内毒素诱导的降低。这可能意味着MB对肺部中的中性粒细胞没有影响。然而,已显示腹膜内施用的MB对大鼠进行肠穿孔后降低肺中性粒细胞螯合和肺泡损伤gydF4y2Ba30.gydF4y2Ba.所用物种与模型之间的差异可以解释研究之间的差异。gydF4y2Ba
互补的活化刺激多核白细胞,可以在自己的权利中诱导瞬时肺损伤gydF4y2Ba1gydF4y2Ba,gydF4y2Ba4gydF4y2Ba.由于检测绵羊补体激活产物的方法是不可用的,作为补体激活的一个指标,我们测量了替代补体途径的总溶血活性。作者发现补体的溶血活性只有微小的变化,不受MB的影响。因此,补体激活不有助于在这个模型中观察到的病理生理变化。这与作者最近的研究结果是一致的gydF4y2Ba体外gydF4y2Ba观察到内毒素,以对应于本研究中使用的剂量的剂量,与整个细菌相比,难以激活补体(T.E.Mollnes,个人通信)。gydF4y2Ba
综上所述,亚甲蓝可以保护内毒素诱导的绵羊急性肺损伤,表现为减轻肺动脉高压和水肿,改善右心室功能。本文作者认为,这些作用很可能是由于除了抑制一氧化氮途径外,还抑制花生四烯酸的环加氧酶产物。亚甲基蓝会影响前列腺素的释放gydF4y2Ba在活的有机体内gydF4y2Ba驳斥该染料仅作为一氧化氮合酶和可溶性胍基环化酶的阻断。需要进一步的实验以阐明一氧化氮途径和环氧氧酶产品如亚甲基蓝的合并抑制剂是否有益于脓毒症相关的急性肺损伤。gydF4y2Ba
致谢gydF4y2Ba
作者感谢L.K. Eliassen和G. Bergseth提供的技术援助,感谢R. Wolstenholme提供的数字准备,感谢P. McCourt提供的语言建议。gydF4y2Ba
- 已收到gydF4y2Ba2001年6月27日。gydF4y2Ba
- 接受gydF4y2Ba2002年5月31日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba