摘要gydF4y2Ba
机械通气可以挽救病人的生命,但也会给肺带来额外的压力。丝裂原活化蛋白激酶(MAPK)代表一个蛋白激酶家族,在许多不同形式的压力下被磷酸化和激活。gydF4y2Ba
本研究采用Western blot分析高压通气对MAPK细胞外信号相关激酶(ERK)-1/2、c-Jun氨基末端激酶(JNK)和p38激酶激活的影响,以及对MAPK激活的转录因子c-Jun的影响。ets样蛋白(Elk)-1和激活转录因子(ATF)-2。gydF4y2Ba
在成年大鼠中,高压通气(45/10峰值吸气压/ cmH呼气末正压)gydF4y2Ba2gydF4y2BaO)处理30或60分钟不影响动脉氧合,但导致ERK-1/2、JNK、c-Jun、Elk-1和ATF-2磷酸化增强,与正常通气(13/3)大鼠相比。ERK-1/2和JNK的激活定位于类似肺泡型细胞的细胞。此外,高压通气增强了NF-κB抑制剂的磷酸化和NF-κB转录因子的核转位。在离体灌注小鼠肺中,MAPK/ERK激酶抑制剂U0126可抑制通气诱导的ERK-1/2和Elk-1的激活,但对通气诱导的细胞因子释放无影响。gydF4y2Ba
目前的作者得出结论,机械通气触发特定的信号通路,如丝裂原活化蛋白激酶和核因子-κB通路,这可能有助于肺部炎症和增殖。gydF4y2Ba
这项研究得到了德国科学基金会(Deutsche Forschungsgemeinschaft Grant DFG Uh 88/2-4)和国际临床导向研究基金会(IFCOR)的资助。gydF4y2Ba
机械通气是一种挽救生命的治疗方法,但如果在经肺压力升高的情况下进行,则会对肺施加额外的压力。根据施加的物理力的程度,这种压力可能通过机械转导导致肺细胞的激活,推测是由肺泡过度膨胀引起的gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba或膜破裂和组织破坏gydF4y2Ba3.gydF4y2Ba.为了支持通气可以激活特定信号通路的观点,作者最近证明了转录因子核因子(NF)-κB的激活和促炎介质的释放,在无明显组织损伤的情况下gydF4y2Ba4gydF4y2Ba- - - - - -gydF4y2Ba6gydF4y2Ba.gydF4y2Ba
除了NF-κB外,应激激活信号级联的可能候选通路是丝裂原活化蛋白激酶(MAPK)依赖通路,它可以被辐照、渗透胁迫、生长因子或菌株激活gydF4y2Ba1gydF4y2Ba,gydF4y2Ba7gydF4y2Ba.MAPK是一个以脯氨酸为靶点的丝氨酸-苏氨酸激酶家族,可将环境刺激转导到细胞核。哺乳动物至少表达四组明显调控的MAPK:细胞外信号相关激酶(ERK)-1和2,c-Jun氨基末端激酶(JNK 1, 2和3),也被称为应激激活蛋白激酶,p38激酶和ERK-5gydF4y2Ba8gydF4y2Ba.MAPK的一个主要功能是激活转录因子,如ETS-like protein-1 (Elk-1)、c-Jun、c-Fos和活化转录因子(ATF)-2,这些因子控制着多种基因,其中许多基因参与了炎症和增殖的调控。例如,c-Jun家族的成员,与c-Fos和ATF-2一起,形成被称为激活蛋白(AP)-1的homo-或异源二聚体,激活许多不同的促炎基因gydF4y2Ba9gydF4y2Ba.Elk-1与血清反应因子(SRF)协同作用,并与c-Fos和早期生长反应(egr)-1等多种基因启动子区域的血清反应元件(SRE)结合,触发其基因表达gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba.然而,在ERK-2磷酸化后,Elk-1也可能激活独立于SRF和SRE的基因,如肿瘤坏死因子(TNF)和趋化因子9E3/cCAF(趋化和血管生成因子)所示。gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba.ATF-2可以与C-Jun结合,并激活C-Jun,TNF和E-Selectin的基因gydF4y2Ba9gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba14gydF4y2Ba.gydF4y2Ba
因此,MAPK可被各种形式的细胞外应激激活,并可能在细胞对高压力通气的反应中发挥重要作用。然而,高膨胀压通气对MAPK的影响尚不清楚。为此,用正常和高峰值吸气压力(PIP)通气大鼠,并应用呼气末正压(PEEP)使肺损伤最小化。gydF4y2Ba15gydF4y2Ba,gydF4y2Ba16gydF4y2Ba.Western blot和免疫组织化学分析MAPK的激活情况。为了研究MAPK激活的一些后果,我们分析了已知由MAPK控制的转录因子的激活。此外,为了证明这些转录因子是由MAPK控制的,我们用灌流的小鼠肺来研究MAPK/ERK激酶(MEK)抑制剂U0126对ERK-1和Elk-1磷酸化和细胞因子释放的影响。最后,在完整动物的灌注小鼠肺中证实先前的发现gydF4y2Ba4gydF4y2Ba, NF-κB在大鼠中的活化gydF4y2Ba体内gydF4y2Ba被调查。gydF4y2Ba
材料和方法gydF4y2Ba
动物gydF4y2Ba
这项研究得到了荷兰鹿特丹伊拉斯谟大学动物委员会的批准。雄性Sprague-Dawley大鼠(体重220-330 g)来自Harlan (CPB, Zeist,荷兰),雌性BALB/C小鼠(20-23 g)来自德国Borstel研究中心繁殖室。按照美国国立卫生研究院(NIH)的指导方针对动物进行护理和处理。gydF4y2Ba
通风的老鼠gydF4y2Ba体内gydF4y2Ba
制备技术已在前面介绍过gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba.简单地,用65%的二氧化氮/35%的氧气和2%的异氟烷麻醉动物。随后,将无菌聚乙烯导管插入颈动脉,抽取动脉血样并监测血压。随后,一个无菌金属套管被插入气管。这些手术结束后,停止气体麻醉,并以60mg·kg继续麻醉gydF4y2Ba−1gydF4y2Ba戊巴比妥钠gydF4y2Bai.p。gydF4y2Ba(戊巴比妥钠;Algin, masassluis,荷兰)。随后用潘库溴铵2 mg·kg诱导肌肉松弛gydF4y2Ba−1gydF4y2Ba,gydF4y2Ba坜gydF4y2Ba(巴夫龙;在压力恒定的时间循环模式下,吸气氧分数为1.0,使用Servo Ventilator 300(西门子Elema, Solna,瑞典)进行通风。gydF4y2Ba
大鼠(每组4只)机械通气,每次30次·mingydF4y2Ba−1gydF4y2Ba具有常压(13/3; PIP / PEEP在CMH中gydF4y2Ba2gydF4y2BaO)或高压(45/10)30或60分钟。在研究结束时,从动脉血中提取肝素化的血液,然后用过量的戊巴比妥杀死动物。不通风的对照组在气管切开术后立即处死,方法相同。打开胸腔,收集无菌肺,立即冷冻保存。免疫组化:打开胸腔,整块切除肺,灌注HOPE液gydF4y2Ba18gydF4y2Ba,gydF4y2Ba19gydF4y2Ba.然后肺部膨胀10 cmhgydF4y2Ba2gydF4y2BaO,钳住气管,将肺置于4°C HOPE溶液中保存,待进一步分析。gydF4y2Ba
免疫组织化学gydF4y2Ba
希望固定,如前所述制备石蜡包埋的标本gydF4y2Ba18gydF4y2Ba,gydF4y2Ba19gydF4y2Ba.取4µm厚的切片,置于Superfrost+玻片上(041300;Menzel-Gläser Braunschweig,德国),并像其他地方描述的那样去划分gydF4y2Ba18gydF4y2Ba,gydF4y2Ba19gydF4y2Ba.除了阳性参考切片,阴性对照也包括在每个染色系列中,以确保结果均匀。样品经25% H预处理gydF4y2Ba2gydF4y2BaOgydF4y2Ba2gydF4y2Ba室温下保存30分钟。gydF4y2Ba
然后应用一抗,每一抗用1/100稀释的磷酸盐缓冲盐水(PBS)在室温下1小时。PBS冲洗2次(每次1分钟)。二抗(驴抗兔,偶联碱性磷酸酶,抗小鼠吸收)(44311;(Dianova, Hamburg, Germany))在环境温度下,用1/100的稀释液在PBS中浸泡30分钟。PBS冲洗2次(每次1分钟)。gydF4y2Ba
然后根据制造商的方案(k0624;Dako斯特鲁普、丹麦)。显色反应在10分钟内完成。用梅耶尔氏血进行复染。使用Kayser的甘油明胶安装载玻片并拍照。gydF4y2Ba
离体灌注小鼠肺制剂gydF4y2Ba
小鼠肺的制备和灌注基本如最近所述gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba.简单地说,肺以非再循环的方式以1ml·min的恒定流量经肺动脉灌注gydF4y2Ba−1gydF4y2Ba导致肺动脉压力为2-3厘米gydF4y2Ba2gydF4y2BaO.作者使用Roswell Park Memorial Institute (RPMI)无酚红缓冲液(37°C)作为灌注介质。采用负压(−10/−3 cmH)室内空气通气gydF4y2Ba2gydF4y2BaO) 90次·分钟gydF4y2Ba−1gydF4y2Ba在控制条件下,产生的潮气量(gydF4y2BaVgydF4y2BaTgydF4y2Ba)〜200μl。用差压传感器(DP 45-24;有效的,Northridge,CA,USA)测量人造胸腔室压力,并且通过连接到差压传感器的杂草型气动谱管测量气流速率(DP 45-15;有效期)。通过压力传感器(IsoTec Healthdyne,Irvine,Ca,USA)连续监测动脉压,该压力传感器连接到肺动脉中的套管结束。所有数据都传输到计算机并用普罗族软件(Hugo Sachs Elektronik,3月Hugstetten,德国)分析。gydF4y2BaVgydF4y2BaTgydF4y2Ba通过对流量积分得到,并应用公式对数据进行分析:gydF4y2Ba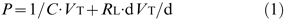 在哪里gydF4y2BaPgydF4y2Ba室的压力,gydF4y2BaCgydF4y2Ba是肺顺应性gydF4y2BaRgydF4y2BalgydF4y2Ba是肺阻力。gydF4y2Ba
在哪里gydF4y2BaPgydF4y2Ba室的压力,gydF4y2BaCgydF4y2Ba是肺顺应性gydF4y2BaRgydF4y2BalgydF4y2Ba是肺阻力。gydF4y2Ba
Western印迹分析gydF4y2Ba
在液氮的持续存在下,用杵和臼将冰冻的肺制成粉末。将肺粉溶解并匀浆于缓冲液(50 mM Tris-Cl, pH 6.8, 150 mM NaCl, 1% Triton X-100)中,缓冲液中含有PefaBloc (1 mM),抑蛋白(1µg·mL)gydF4y2Ba−1gydF4y2Ba),胃蛋白酶(1μg·mlgydF4y2Ba−1gydF4y2Ba)、白细胞介素(1µg·mL .gydF4y2Ba−1gydF4y2Ba)、NaF (1 mM)、NaF (1 mMgydF4y2Ba3.gydF4y2Bavo.gydF4y2Ba4gydF4y2Ba(1 mM)和β-甘油磷酸(1 mM)。冷冻20 min后,将细胞碎片打成球,16000 × 15min收集裂解液gydF4y2BaggydF4y2Ba.总蛋白质含量采用市售试验(Pierce, Rockford, IL, USA)测定。gydF4y2Ba
等量蛋白质(60µg·槽)gydF4y2Ba−1gydF4y2Ba)经十二烷基硫酸钠(SDS)-聚丙烯酰胺凝胶电泳后,转移到硝基纤维素转移膜(Schleicher & Schuell, Dassel, Germany),然后用一抗(New England Biolabs (NEB),法兰克福,德国)和辣根过氧化物酶偶联二抗(NEB)进行免疫印迹。结合抗体与LumiGLO化学发光底物的检测按生产厂家(NEB)进行。采用OPTIMAS 6.2软件(OPTIMAS Corporation, Bothel, WA, USA)进行密度分析。gydF4y2Ba
免疫沉淀反应gydF4y2Ba
整除的小鼠肺粉末溶解在500µl冷裂解缓冲(10毫米三pH值7.4,150毫米氯化钠,特里同x - 100 1%, 1毫米乙二胺四乙酸(EDTA), 1毫米ethyleneglycol-bis -(β-aminothylether) - N, N, N ', N ' -tetraacetic酸(EGTA) pH值8.0,0.2毫米NagydF4y2Ba3.gydF4y2Bavo.gydF4y2Ba4gydF4y2Ba, 0.2 mM PefaBloc, 1% NP-40),在4°C通过端-端旋转持续搅拌30分钟。为了分散较大的团聚体,将原裂解液超声化为3×5 s(布兰森超声公司,丹伯里,CT,美国)。离心收集最终裂解液(16000 ×)gydF4y2BaggydF4y2Ba, 4°C, 15分钟)。总蛋白质含量采用市售试验(Pierce, Rockford, IL, USA)测定。在2×免疫沉淀缓冲液(20 mM Tris pH 7.4, 300 mM NaCl, 2 mM EDTA, 2 mM EGTA pH 8.0, 0.4 mM Na)中沉淀第一抗体5µg和总蛋白500µggydF4y2Ba3.gydF4y2Bavo.gydF4y2Ba4gydF4y2Ba(0.4 mM PefaBloc, 1% NP-40)在4°C通过端-端旋转孵育过夜。免疫复合物采用Protein G Plus琼脂糖(Santa Cruz Biotechnology, Inc., Santa Cruz, CA, USA)在4°C下持续搅拌1小时,离心4分钟(16000 ×gydF4y2BaggydF4y2Ba4°C)。用1×免疫沉淀缓冲液(10 mM Tris pH 7.4, 150 mM NaCl, 1 mM EDTA, 1 mM EGTA pH 8.0, 0.2 mM Na)洗涤3次gydF4y2Ba3.gydF4y2Bavo.gydF4y2Ba4gydF4y2Ba, 0.2 mM PefaBloc, 0.5% NP-40)。沉淀在电泳样品resuspended缓冲区(62.5毫米三pH值6.8,2% SDS、5%甘油、0.006%溴酚蓝,2%β巯基乙醇),煮5分钟,离心机,上层清液装上一个SDS-polyacrylamine凝胶电泳(页面),电泳和涂抹描述为西方墨点法。gydF4y2Ba
电泳迁移迁移试验gydF4y2Ba
核萃取物的制备和电泳迁移率的测定如前所述gydF4y2Ba4gydF4y2Ba.gydF4y2Ba
统计分析gydF4y2Ba
印迹中条带的强度被量化,并表示为来自不通风对照动物的值的比率。对所有数据进行对数转换,并通过配对单侧t检验分析13/3和45/10之间的差异(同时分析来自同一凝胶的数据)。假设p<0.05时具有统计学意义。gydF4y2Ba
结果gydF4y2Ba
通气13/3 cmHgydF4y2Ba2gydF4y2BaO (PIP/PEEP)或45/10 cmHgydF4y2Ba2gydF4y2Bao导致18毫升·kg的潮数gydF4y2Ba−1gydF4y2Ba和48毫升·kggydF4y2Ba−1gydF4y2Ba分别gydF4y2Ba21gydF4y2Ba.60分钟的通风,45/10 CMHgydF4y2Ba2gydF4y2BaO耐受良好,血氧合正常(表1)gydF4y2Ba⇓gydF4y2Ba).正如预期的那样,在这些条件下,平均动脉压降低了。通气和不通气动物的血清转氨酶和肌酐水平没有差异(表1)gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
氧合,平均动脉压,血清酶和血清肌酐gydF4y2Ba
促丝糖型活化蛋白激酶gydF4y2Ba
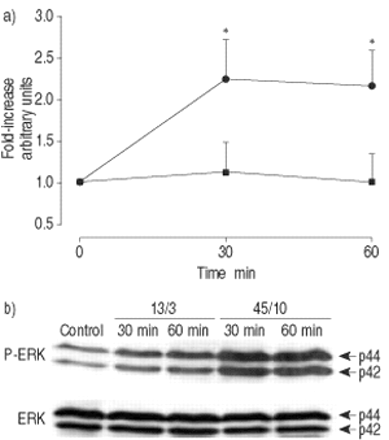
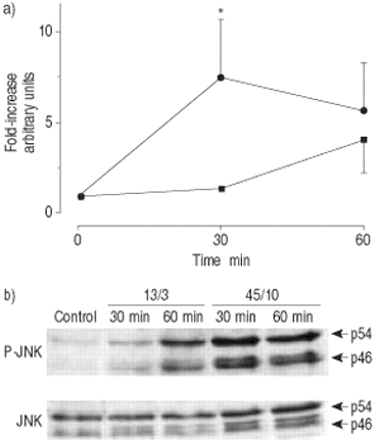
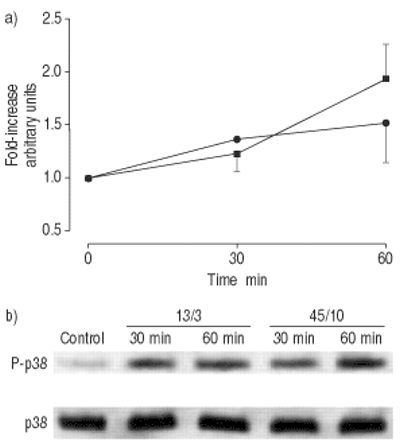
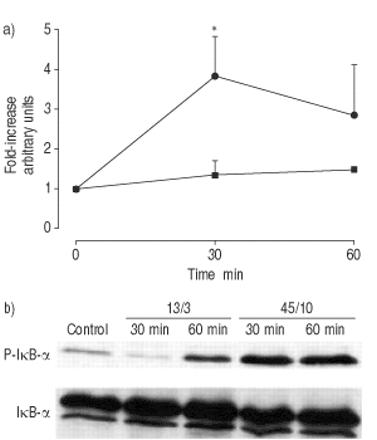
天然未磷酸化形式的ERK-1/2和JNK的表达在不同条件下没有差异(图1)。1和2gydF4y2Ba⇓gydF4y2Ba⇓gydF4y2Ba).大鼠13/ 3cmh通气30或60 mingydF4y2Ba2gydF4y2BaO对ERK-1/2磷酸化无影响,而45/10 cmH通气则无影响gydF4y2Ba2gydF4y2BaO使ERK-1/2磷酸化增加了两倍(图1)gydF4y2Ba⇓gydF4y2Ba).ERK-1和ERK-2的磷酸化没有差异。在分析的两种JNK亚型中,p54(图2)gydF4y2Ba⇓gydF4y2Ba)显示出比p46更一致的结果,而p46则显示出与p54相同的模式。13/3 cmH通气后JNK磷酸化未见增强gydF4y2Ba2gydF4y2BaO在通气30min后升高约4倍,提示通气本身可能是jnk活化的刺激因子。45/10 cmH换气gydF4y2Ba2gydF4y2BaO导致JNK在30分钟后激活7倍。在所有条件下,天然p38激酶的含量都相似。两种通气模式均可增加p38的磷酸化水平,但45/10 cmH通气均可增加p38的磷酸化水平gydF4y2Ba2gydF4y2BaO与13/3 cmH通气无差异gydF4y2Ba2gydF4y2BaO(图。3gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
肺匀浆中细胞外信号相关激酶(ERK)-1/2磷酸化的时间进程大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10,•)持续30或60分钟。b)用免疫印迹法分析ERK,使用针对ERK磷酸化(P)或未磷酸化形式的特异性抗体。a)密度值显示为不通风对照组的fold增加,代表4只动物的平均值±sem (p44和p42的平均值(p42和p44分别代表ERK-1和ERK-2))。*: p < 0.05gydF4y2Ba与gydF4y2Ba13/3。gydF4y2Ba
肺匀浆中c-Jun氨基末端激酶(JNK)磷酸化的时间进程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO,▪)或高压(45/10,•)30或60分钟。b)通过免疫印迹分析JNK,使用针对JNK磷酸化(P)或未磷酸化形式的特异性抗体。a)密度测量值显示为在不通风的对照组中,fold的增加,代表4只动物的平均值±sem。常压通气30 min后,折射率较基线增加1.40±0.31。*:显著(p<0.05)大于13/3。p54和p46代表JNK亚型。gydF4y2Ba
肺匀浆中p38磷酸化的时间进程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10;•)30或60分钟。b)使用磷酸特异性p38抗体,采用免疫印迹法分析P-p38。a)密度数据值显示为不通风对照组的fold增加,代表4只动物的平均值±sem。用45/10 cmH换气30分钟后gydF4y2Ba2gydF4y2BaO,较基线增加1.36±0.05。gydF4y2Ba
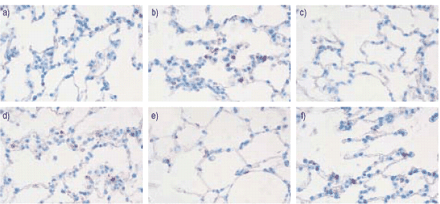
采用免疫组化方法鉴定过度膨胀导致MAPK磷酸化的细胞类型。由于在初步实验中,用于Western blot的抗体似乎与经典的福尔马林固定不起作用,因此采用了新的HOPE固定技术,这是一种相对于传统固定具有较少变性的方法gydF4y2Ba19gydF4y2Ba.使用这种方法,可获得ERK、JNK和p38磷酸化(P)形式的特异性抗体的阳性染色(图4)gydF4y2Ba⇓gydF4y2Ba).P-ERK和P-JNK仅在13/3 cmH通气60 min时微弱检测到gydF4y2Ba2gydF4y2BaO(无花果。4 a和cgydF4y2Ba⇓gydF4y2Ba),但在大小、形状和位置与II型肺泡上皮细胞相似的细胞中,信号明显增加(图)。4 b和dgydF4y2Ba⇓gydF4y2Ba).P-ERK和P-JNK偶见于45/10 cmH通气的肺内皮细胞gydF4y2Ba2gydF4y2BaO.在通气30分钟后也有类似的观察(数据未显示)。然而,在这两个时间点,P-ERK或P-JNK阳性细胞的分布是异质性的,并没有在所有II型细胞中观察到激活。P-p38也主要在类似肺泡上皮II型细胞的细胞中检测到,但在13/3 cmH通气的肺中没有差异gydF4y2Ba2gydF4y2BaO或45/10 cmHgydF4y2Ba2gydF4y2BaO(无花果。4 e和fgydF4y2Ba⇓gydF4y2Ba).同样,P-p38只在II型细胞的一部分中发现。对于所有的MAPK,不能排除肺泡上皮I型细胞活化的可能性。gydF4y2Ba
大鼠肺中丝裂原活化蛋白激酶的活化gydF4y2Ba体内gydF4y2Ba.大鼠机械通气(13/3;峰值吸气压力/呼气末正压cmHgydF4y2Ba2gydF4y2BaO;A)、c)、e))或高压(45/10;B), d), f)。细胞外信号相关激酶(ERK) (a)和b)、c- jun氨基末端激酶(JNK) (c)和d)和p38 (e)和f)磷酸化抗体免疫组化染色(红色)显示,过度膨胀激活ERK和JNK主要存在于肺泡上皮II型细胞中。gydF4y2Ba
丝裂原活化蛋白激酶活化的转录因子gydF4y2Ba
为了研究ERK和JNK激活的一些细胞内后果,我们研究了转录因子c-Jun、Elk-1和ATF-2的激活。c-Jun属于对各种刺激反应迅速形成的直接早期基因。与此一致,通风45/10 cmHgydF4y2Ba2gydF4y2BaO增加了两者的表达量(图5)gydF4y2Ba⇓gydF4y2Ba)和磷酸化(图6gydF4y2Ba⇓gydF4y2Ba本地c-Jun。另外,以45/10 cmH换气gydF4y2Ba2gydF4y2BaO诱导Elk-1的磷酸化增加了6倍(图7)gydF4y2Ba⇓gydF4y2Ba)和ATF-2的磷酸化几乎增加了3倍(图8)gydF4y2Ba⇓gydF4y2Ba).在Elk-1和ATF-2的表达上没有发现差异。gydF4y2Ba
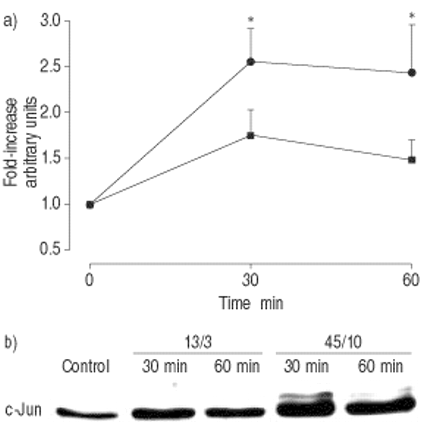
c-Jun在肺匀浆中表达的时间进程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10,•)持续30或60分钟。b)使用特异性c-Jun抗体,用免疫印迹法分析c-Jun。a)密度测量值显示为在不通风的对照组中,fold的增加,代表4只动物的平均值±sem。*:显著(p<0.05)大于13/3。gydF4y2Ba
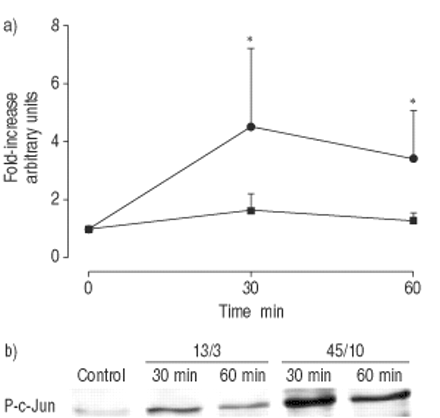
肺匀浆中C-Jun磷酸化的时间过程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10,•)持续30或60分钟。b)使用磷酸化c-Jun抗体,通过免疫印迹法分析磷酸化(P) c-Jun。a)密度测量值显示为在不通风的对照组中,fold的增加,代表4只动物的平均值±sem。*:显著(p<0.05)大于13/3。gydF4y2Ba
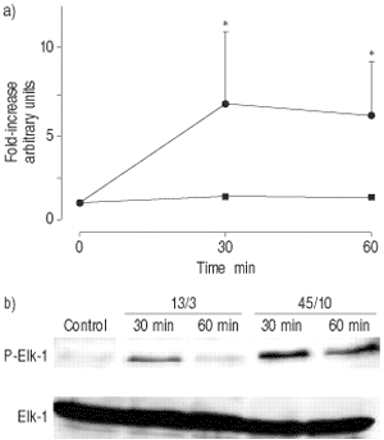
肺匀浆中ets样蛋白-1 (Elk)-1磷酸化的时间进程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10,•)持续30或60分钟。b)通过免疫印迹分析Elk-1,使用针对磷酸化或未磷酸化形式的特异性抗体。a)密度测量值显示为在不通风的对照组中,fold的增加,代表4只动物的平均值±sem。常压通气30 min和60 min后,fold增加量分别为1.38±0.21和1.30±0.11。*:显著(p<0.05)大于13/3。gydF4y2Ba
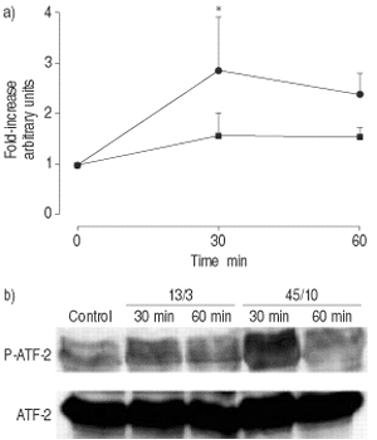
肺匀浆中活化转录因子-2磷酸化的时间进程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10,•)持续30或60分钟。b)使用针对ATF-2磷酸化(P)或未磷酸化形式的特异性抗体,通过免疫印迹分析ATF-2。a)密度值显示为不通风对照组的fold增加,代表4只动物的平均值±sem。*:显著(p<0.05)大于13/3。gydF4y2Ba
核因子-κBgydF4y2Ba
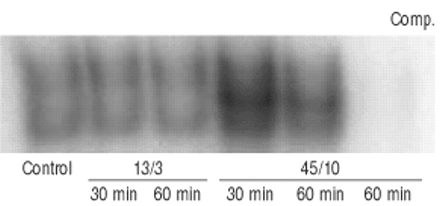
45/10 cmH换气gydF4y2Ba2gydF4y2BaO迅速增加了NF-κB抑制剂(IκB-α)的磷酸化(图9)gydF4y2Ba⇓gydF4y2Ba).已知磷酸化导致IκB-α的降解,这反过来促进NF-κB的核易位。与此相一致,45/10 cmH通气大鼠核提取物中NF-κB含量增加gydF4y2Ba2gydF4y2BaO(图10所示gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
肺匀浆核因子-κB(IκB-α)磷酸化抑制剂的时间过程。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO;▪)或高压(45/10,•)持续30或60分钟。b)使用磷酸化或未磷酸化IκB-α的特异性抗体,通过免疫印迹分析IκB-α。密度测量数据。数值显示为在不通风的对照组上增加的倍数,代表4只动物的平均±扫描电镜。*:显著(p<0.05)大于13/3。gydF4y2Ba
大鼠肺过度膨胀导致核因子-κB易位。大鼠留下(对照,时间点0),或者用常压机械通风(13/3;峰值吸气压力/正端呼气压力在CMH中gydF4y2Ba2gydF4y2BaO)或高压(45/10)30或60分钟。电迁移率移位法测定NF-κB转运。在未标记的(“冷”)寡核苷酸(Comp.)存在下NF-κB带被消除。gydF4y2Ba
ERK-1/2,ELK-1和细胞因子释放在分离的灌注小鼠肺中gydF4y2Ba
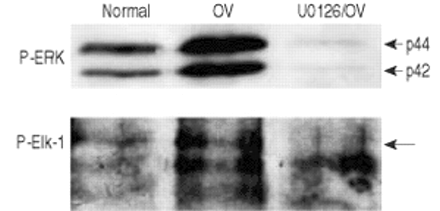
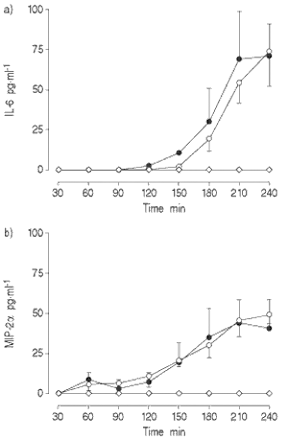
最后,对通气诱导的MAPK激活的一些后果进行了研究。为此,我们使用了离体灌注小鼠肺模型,该模型能够精确控制通气和灌注,并且可以排除血细胞或神经衰弱等混杂因素gydF4y2Ba6gydF4y2Ba.肺以−10/−3或−25/−3 cmH通气gydF4y2Ba2gydF4y2BaO,潮汐量分别为9和32毫升·公斤gydF4y2Ba−1gydF4y2Ba,如前所述gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.作为观察gydF4y2Ba体内gydF4y2Ba,在灌流小鼠肺中,压力升高通气60 min可导致ERK-1/2磷酸化增强(图11)gydF4y2Ba⇓gydF4y2Ba)和JNK(2.8±1.4倍,n=3,均值±sd)。经选择性mek抑制剂U0126预处理后,ERK的激活被完全消除,而JNK的激活未被显示(数据未显示)(图11)gydF4y2Ba⇓gydF4y2Ba).U0126也能阻止Elk-1的磷酸化(图11)gydF4y2Ba⇓gydF4y2Ba).然而,U0126预处理对通气诱导的白细胞介素(IL)-6和巨噬细胞炎症蛋白(MIP)-2释放到灌注液中没有影响(图12)gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
细胞外信号相关激酶(ERK)-1和ets样蛋白(Elk)-1在正常压力下通气60min的离体灌注小鼠肺中的激活(−10/−3;cmH吸气末压/呼气末正压gydF4y2Ba2gydF4y2BaO)或高压(−25/−3,通气过度)。10分钟后再灌注10µM U0126。使用ERK-1磷酸化(P)形式的特异性抗体,通过免疫印迹分析ERK-1。使用针对Elk-1磷酸化形式的特异性抗体进行免疫沉淀分析。P-Elk-1带用箭头表示。其他乐队的身份尚不清楚。本文给出了三个独立实验中具有代表性的免疫印迹。gydF4y2Ba
通气诱导离体灌注小鼠肺灌注液中白细胞介素(IL)-6和巨噬细胞炎症蛋白(MIP)-2α水平的变化肺通气60分钟,正常压力(−10/−3;cmH吸气末压/呼气末正压gydF4y2Ba2gydF4y2BaO),然后常压通气180分钟(♦,n=3),−25/−3 cmHgydF4y2Ba2gydF4y2BaO(〇,n=5),或用−25/−3 cmH通风gydF4y2Ba2gydF4y2BaO + 10 μ M U0126预处理(•,n=3)。数据意味着±sem。gydF4y2Ba
讨论gydF4y2Ba
已知MAPK在各种压力下会迅速被激活。本研究表明,对于高膨胀压力通气引起的机械应力也是如此。MAPK在过度膨胀反应中被激活的主要细胞类型似乎是肺泡II型细胞,尽管不能排除I型细胞。过度膨胀不仅激活了MAPKgydF4y2Ba体内gydF4y2Ba这表明,这种现象并非继发于白细胞内流或神经调节。转录因子ATF-2、Elk-1和c-Jun的磷酸化和/或表达提供了证据,表明MAPK有效地激活了它们通常已知的靶点,在这里我们特别针对Elk-1进行了论证。然而,研究结果也表明,ERK通路并不参与通气诱导的促炎细胞因子和趋化因子(IL-6, MIP-2)的释放,这使得MAPK激活的最终生理后果尚不清楚。鉴于众所周知MAPK对细胞增殖的贡献gydF4y2Ba22gydF4y2Ba,作者推测,它们在II型细胞中的优先激活可能会影响在长期通气个体中观察到的II型细胞增生gydF4y2Ba23gydF4y2Ba.这也提出了一个问题,通气诱导的MAPK激活是否可能与急性呼吸窘迫综合征(ARDS)的纤维增生期有关,特别是与这些患者中常见的II型细胞增生有关gydF4y2Ba24gydF4y2Ba.因此,在未来的研究中,研究MAPK在后期的表达也很重要。gydF4y2Ba
大鼠以13/3 cmH通气gydF4y2Ba2gydF4y2BaO或45/10 cmHgydF4y2Ba2gydF4y2Ba选择这些通气模式是为了尽量减少呼气末肺泡塌陷和随后的表面活性物质功能障碍gydF4y2Ba18gydF4y2Ba.先前的研究表明,当动物以45 cmH的PIP通气时gydF4y2Ba2gydF4y2BaO,应用呼气末正压10 cmH可减轻肺损伤gydF4y2Ba2gydF4y2BaOgydF4y2Ba15gydF4y2Ba,gydF4y2Ba16gydF4y2Ba,尽管PIP高达45 cmHgydF4y2Ba2gydF4y2BaO, PEEP并不能完全防止肺损伤,特别是在后期的时间点。然而,在45/10 cmH通气时,作为肺功能测量的氧合和作为肺外器官损伤指标的血清转氨酶活性和肌酐水平没有差异gydF4y2Ba2gydF4y2Ba与13/3 cmH通气相比gydF4y2Ba2gydF4y2BaO(见表1)gydF4y2Ba⇑gydF4y2Ba).由此,本文作者得出结论:在前60分钟,以45/10 cmH通气gydF4y2Ba2gydF4y2BaO没有造成严重的肺损伤(组织学数据也支持这一点),因此在这些条件下MAPK的激活可能是由特定的机械转导机制解释的,而不是由可能来自受损细胞的非特异性过程gydF4y2Ba3.gydF4y2Ba.gydF4y2Ba
目前,不知道如何将通风引起的应变和应力转化为生物信号,但是假设由细胞感测的初始信号是可延伸的假设是合理的。这是由于机械拉伸已经显示出在心肌细胞中激活ERK和JNK的事实gydF4y2Ba25gydF4y2Ba系膜细胞gydF4y2Ba26gydF4y2Ba,黑色素细胞gydF4y2Ba27gydF4y2Ba,肺内皮细胞gydF4y2Ba28gydF4y2Ba和L929细胞gydF4y2Ba29gydF4y2Ba.ERK-1/2 (p42/p44)在H441肺上皮细胞延伸20%的10分钟内被激活gydF4y2Ba30.gydF4y2Ba.在A549细胞中,15%的菌株在30 min内激活应激激活蛋白激酶JNK,在较晚的时间点(2 h)激活p38激酶,而ERK-1/2未激活gydF4y2Ba31gydF4y2Ba.后者的结果与II型细胞中通气诱导的ERK激活形成对比gydF4y2Ba体内gydF4y2Ba(图4 bgydF4y2Ba⇑gydF4y2Ba),并表明A549细胞的拉伸只能部分地提供全完整器官中肺泡上皮II细胞中的情况的模型。gydF4y2Ba
据作者所知,到目前为止,只有一项研究确定了特定的细胞类型对过度膨胀有反应gydF4y2Ba体内gydF4y2Ba32gydF4y2Ba.通过使用gydF4y2Ba原位gydF4y2Ba杂交,达gydF4y2Ba等gydF4y2Ba.gydF4y2Ba32gydF4y2Ba在20 mL·kg通气大鼠肺泡巨噬细胞、肺泡上皮细胞和内皮细胞中显示细胞外基质金属蛋白诱导剂(EMMPRIN)、明胶酶A和明胶酶B的激活gydF4y2Ba−1gydF4y2Ba4小时无PEEPgydF4y2Ba32gydF4y2Ba.在本研究中,在这些细胞中发现了过度膨胀激活MAPK,特别是在肺泡上皮II型细胞中,偶尔在内皮细胞中。然而,由于缺乏选择性的II型细胞反染色,目前的数据并没有完全排除MAPK在其他细胞类型如I型细胞中的激活。之前的研究已经表明II型细胞可以对拉伸做出反应,特别是那些显示表面活性剂释放的研究gydF4y2Ba33gydF4y2Ba和来自拉伸的肺泡上皮细胞的IL-8gydF4y2Ba34gydF4y2Ba.II型细胞对伸展反应的间接证据早在20年前就已经有了,当时研究表明,即使是一次深呼吸就足以释放肺表面活性物质gydF4y2Ba35gydF4y2Ba.目前尚不清楚MAPK是否有助于通气诱导的表面活性剂释放或IL-8的产生。然而,由于MIP-2被认为是IL-8的小鼠类似物,本研究在U0126处理下的阴性结果表明,ERK也可能不会促进IL-8从拉伸的II型细胞中释放出来。gydF4y2Ba
与JNK和ERK-1/2相比,p38激酶没有被过度膨胀激活,这表明通气诱导的信号级联具有一定的特异性。过度膨胀导致p38不被激活的一个可能的解释可能是最近的观察,即p38激酶对拉伸反应的激活与JNK和ERK-1/2的调节不同gydF4y2Ba29gydF4y2Ba.然而,不能排除p38在60分钟后被激活的可能性,正如在应变的A549细胞中观察到的那样gydF4y2Ba31gydF4y2Ba.有趣的是,在所有通风肺部都注意到P38的磷酸化,表明机械通气过程可能足以激活P38。报告了MIP-2 [36和未发表的数据]的类似发现。在这些条件下P38和MIP-2之间是否存在链接仍有待建立,但已知P38有助于脂多糖诱导的肺部MIP-2生产gydF4y2Ba37gydF4y2Ba.gydF4y2Ba
MAPK的一个主要作用途径是通过激活转录因子,因此Elk-1、c-Jun和ATF-2的过度膨胀磷酸化是可以预期的。通过对mek抑制剂U0126的实验gydF4y2Ba38.gydF4y2Ba,目前的作者得出结论,在对过度膨胀的反应中,Elk-1主要是由ERK激活的。有趣的是,已知Elk-1可调节c-Fos转录,在采用损伤通气策略通气的离体大鼠肺中发现该转录上调gydF4y2Ba39.gydF4y2Ba.许多即时早期反应基因的启动子区一致存在Elk-1结合元件(gydF4y2Ba如。gydF4y2BaC-FOS,MAPK磷酸酶-1,EGR-1)gydF4y2Ba13gydF4y2Ba提示该通路可能在通气应激反应中起重要作用。gydF4y2Ba
天然未磷酸化的c-Jun表达因过度膨胀而增加。这可能是由于c-Jun启动子结合c-Jun:ATF-2异二聚体,经JNK磷酸化后,导致c-Jun转录增强和随后的c-Jun的产生gydF4y2Ba9gydF4y2Ba.c-Jun表达增强可能是P-c-Jun表达增加的部分原因。c-Jun可能形成同源二聚体,也可能与c-Fos一起形成属于AP-1转录因子家族的异源二聚体,其转录活性通过JNK磷酸化c-Jun上的Ser63和Ser73进一步增强gydF4y2Ba9gydF4y2Ba.因此,本研究的发现表明,在过度结束期间形成和激活AP-1。因为AP-1也可以由C-Jun同源体形成,所以U0126影响通气诱导的细胞因子释放的失败不会排除AP-1在该过程中的参与。AP-1是众所周知的,用于控制许多促炎基因,例如IL-2,IL-5,粒细胞巨噬细胞群刺激因子,干扰素(IFN)-γ和基质金属蛋白酶gydF4y2Ba9gydF4y2Ba.显然,AP-1和其他转录因子(如egr-1)在非生理性高膨胀压力通气中的作用值得进一步研究。gydF4y2Ba
除了MAPK途径外,本研究还显示了NF-κB在高压通气大鼠中的激活。在通气或拉伸反应中,NF-κB的核转位已经在细胞培养的实验中得到证实gydF4y2Ba40gydF4y2Ba在离体灌注的小鼠肺中gydF4y2Ba4gydF4y2Ba, 但不是gydF4y2Ba体内gydF4y2Ba.本研究也为NF-κB的活化与i -κB -α的磷酸化提供了证据。众所周知,这种磷酸化会导致IκB-α的泛素化和随后的降解,这是NF-κB进入细胞核的前提条件。NF-κB控制着许多促炎基因,在小鼠肺中,作者最近表明,只有在启动子中具有NF-κB共识序列的介质在过度膨胀反应中被释放gydF4y2Ba4gydF4y2Ba.综上所述,通气可能有助于NF-κB的活化,正如ARDS患者中观察到的那样gydF4y2Ba41.gydF4y2Ba.gydF4y2Ba
综上所述,本研究表明,高膨胀压力通气激活肺泡上皮II型细胞的细胞外信号相关激酶-1/2和c-Jun氨基末端激酶,以及多种转录因子(et -like protein-1, c-Jun, activated transcription factor-2,核因子-κB)。这些发现表明,过度膨胀引发特定的信号通路,导致协调良好的细胞反应。作者认为,这些信号通路可能与慢性通气患者的细胞增殖和炎症有关。gydF4y2Ba
致谢gydF4y2Ba
作者要感谢S. Hallmann, K. Viertmann, H. Kühl(德国博尔斯特尔研究中心)和S. Krabbendam(鹿特丹伊拉斯谟大学)提供的专家技术援助,以及L. Visser-Isles(伊拉斯谟大学)提供的英语编辑工作。gydF4y2Ba
- 收到了gydF4y2Ba2001年9月11日。gydF4y2Ba
- 接受gydF4y2Ba2002年5月1日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba