摘要
慢性阻塞性肺疾病(COPD)患者表现为肺血管低氧收缩受损,可能导致气体交换异常,可能与肺动脉内皮功能障碍有关。本研究的目的是探讨PA对低氧刺激的反应在体外内皮源性一氧化氮(NO)在这一反应中的作用。
对25例肺切除术患者的肺动脉进行了研究。将患者分为对照组、COPD+常氧血症(COPDN)和COPD+低氧血症(COPDH).缺氧血管收缩(HV)在刺激或抑制内皮细胞释放NO前后和外源性NO存在时进行评估。
与其他组比较,COPD组HV降低H.HV的大小与动脉血氧张力有关。低氧刺激在刺激内皮细胞释放NO后引起更大的收缩,而它的抑制实际上消除了HV。外源性NO完全抑制HV。内皮依赖性血管扩张剂引起的最大舒张与HV的大小相关。
综上所述,慢性阻塞性肺疾病和低氧血症患者的肺动脉对低氧刺激的反应受损,内皮细胞释放的一氧化氮调节了低氧血管收缩。慢性阻塞性肺疾病中肺动脉对缺氧的反应减弱可能是导致气体交换异常的原因之一。
本研究得到了来自Investigación Sanitaria Fondo的99/0188和00/0922赠款的支持,以及来自Española de Neumología y Cirugía Torácica的separate -2000赠款的支持。V.I. Peinado获得了Comissió Interdepartamental de Recerca i Innovació Tecnològica和Fundació Clínic per a la Recerca Biomèdica的支持。S. Santos是来自Española de Neumología y Cirugía Torácica (SEPAR)的研究奖学金获得者。
低氧肺血管收缩(HPV)是调节通气灌注比的有效机制(V”一个/问’)的匹配,在调节动脉氧分压(PO2)用于许多呼吸系统疾病,包括慢性阻塞性肺疾病(COPD)。事实上,在这种情况下,对HPV的抑制减弱V”一个/问的关系,正如血液流向通风不良的肺泡单元所显示的[l, 2]。先前的研究表明,轻度COPD和中度低氧血症患者可能表现出血管对低氧刺激的反应减弱3.以及100%的氧气4提示肺血管的反应性改变对启发O2浓度。尽管慢性阻塞性肺疾病中这种反应性改变的致病机制还不完全清楚,但在之前的一项研究中,目前的作者表明,它与肺肌肉小动脉正常结构的变化有关2.
内皮源性一氧化氮(NO)在调节肺循环血管张力和血管重构中起着重要作用。对COPD患者离体肺动脉进行的研究表明,重度COPD患者存在内皮功能障碍5和温和6疾病。在后一项研究中,在非低氧血症的轻度COPD患者中,甚至在肺功能正常的吸烟者中,都已经出现了内皮功能障碍和肺动脉结构紊乱。因此,作者认为动脉低氧血症可能在这些血管改变的早期发病机制中起次要作用,它们更有可能与烟草烟雾制品的直接影响有关6.因此,作者假设内皮功能的损害发生在COPD病程早期,它改变了对缺氧刺激的反应,从而促进进一步的气体交换改变。
慢性阻塞性肺疾病患者对低氧刺激反应的评估在活的有机体内是困难的,因为经常并发低氧血症。在体外肺动脉环暴露于缺氧的研究,只在一系列呼吸系统疾病不明的患者中进行7- - - - - -9.据目前作者所知,目前还没有关于COPD患者肺动脉对缺氧刺激反应的研究在体外.因此,本研究的目的有两个方面:第一,描述肺动脉对缺氧刺激的反应在体外伴有或不伴有低氧血症的COPD患者;二是通过特异性评估内皮源性NO的作用,研究缺氧血管收缩(HV)与内皮功能之间的关系。
材料与方法
主题
25例患者(2例女性,23例男性)因局部肺癌而接受肺叶切除术或肺切除术。所有患者均无肺动脉高压的临床证据。术前几天进行了肺功能测试(强迫肺活量测定、身体容积描记术测定的静态肺容积和一氧化碳扩散能力)和动脉血气测量(23例患者)。该研究得到了Clínic医院伦理研究委员会(西班牙巴塞罗那)的批准。
根据强迫肺活量测定和动脉血气测定结果将患者分为三组。1)控制。肺功能正常及动脉血氧张力正常的病人(P啊,一个2)在正常范围内(>10.64 kPa (80 mmHg))。2) COPD+常氧血症(COPDN).1秒用力呼气量(FEV)1) <80%预测值和FEV1/用力肺活量(FVC) <70% pred)和P啊,一个2>10.64 kPa (80 mmHg)。3) COPD+低氧血症(COPDH).有气流阻塞及动脉低氧血症的病人(P啊,一个2<10.64 kPa (80 mmHg))。一般特征及肺功能数据见表1⇓.
肺动脉环的制备
动脉环的处理如前所述6.简单地说,将切除的肺标本置于冷的Krebs-Henseleit’s (KH)缓冲液中(含(单位mM) 118 NaCl, 24 NaHCO)3., 11.1葡萄糖,4.7 KCl, 1.2 KH2阿宝4, 1.2 MgSO4, 2.5 acl2)和21%的O气体2/5%二氧化碳(pH值7.35-7.45)。将外径为1.8 ~ 2.3 mm的动脉段仔细切除,去掉可见的脂肪和结缔组织,切成约3mm长的环形。每个患者的4个环悬浮在20毫升的器官浴室(Panlab, Barcelona, Spain)中,充满KH缓冲液,持续用21%的O充气25% CO2,并保持在37°C的外部水浴由循环加热器加热。等距张力的变化被记录在每个环的力传感器(Panlab)连接到计算机图表驱动器记录器。每个环施加1.75 g的静止张力。平衡≥90分钟后,所有环用吲哚美辛(1×10−5M),以抑制花生四烯酸的环氧合酶产物的合成,花生四烯酸在整个实验过程中都存在。O2通过浸泡氧电极(氧计,781型;Strathkelvin Instruments, Bearsden, UK)在其中一个室中。动脉环在常氧和低氧条件下进行研究。在常氧条件下,KH与21%的O气体2/ 5%股份有限公司2/74%(氮)N2气体混合物,产生了PO2在37°C的动脉环附近的器官浴室,20.1±0.3 kPa(151±2 mmHg)。用5%的CO泡KH可诱导缺氧条件2/ 95% N2气体的混合,从而导致PO21 - 2分钟后降至0.53±0.1 kPa(4±1 mmHg)。
对缺氧刺激的反应
平衡后,所有环预收缩去甲肾上腺素(NA) (1×10−71×10−6M)以获得稳定的张力平台。收缩稳定后,迅速诱导缺氧10分钟,记录血管张力的变化。暴露于缺氧后,重新建立常氧条件,用KH冲洗环,并让其平衡60分钟。
一氧化氮与低氧刺激反应的相互作用
为了确定内皮来源的NO在缺氧反应中的潜在作用,我们分三步研究了动脉环。在第一步,环最初与NA (1×10−71×10−6M),收缩稳定后,用单剂量以下no依赖性血管扩张剂对两个环进行检测:二磷酸腺苷(ADP) (1×10−6M)和组胺(1×10−7M),每环一个。第三环用浓度为1×10的NO供体硝普钠(SNP)进行测定−81×10−7M。第二步,当每个血管扩张剂达到最大舒张时,环暴露于缺氧10分钟,然后重新建立常氧条件。第三步,评估NO合成抑制的效果。为此,NG‐单甲基‐1‐精氨酸(l‐NAME) (1×10−3M)加入到浴室内存在的血管扩张剂(组胺或ADP)中,并在10分钟后重复低氧刺激。在实验结束时,将所有环冲洗干净,用KCl (60 mM)进行最大收缩,以建立最大收缩响应。此外,为了排除实验过程中操作对内皮细胞造成损伤的可能性,我们在实验结束后用抗因子8相关抗原染色,对部分动脉的内皮细胞的显微镜外观进行了评价。
在NA预收缩环中暴露于缺氧后,四种不同剂量的SNP浓度范围从1×10−111×10−7在12名患者(每个患者4个环,每个环一个剂量)中进行了M的测定,然后再次暴露在缺氧中。SNP治疗后对缺氧的反应以先前反应的百分比表示。为了检查NO对缺氧反应的直接影响,在四个动脉环中进行了第二组实验,在浴液中加入浓度为50 ppm NO的NO气体,用化学发光分析仪(CLD 700 AL;生态物理学,Hombrechtikon, Switzerland),然后暴露于缺氧刺激。所有药物均购自Sigma化学公司(美国密苏里州圣路易斯)。
测量
HV被评估为暴露于缺氧后所达到的最大张力与缺氧刺激前所记录的张力之间的差异。缺氧引起的张力变化用KCl引起的最大收缩的百分比表示。通过测量每种血管扩张剂(ADP和组胺)引起的张力降低来确定每个肺动脉环的舒张,并以最大收缩与KCl的百分比表示。
统计分析
所有数据均以均值±sd表示。组间比较采用方差分析(ANOVA)。当重大的,事后采用Newman-Keuls检验进行两两比较。用配对t检验比较NA预收缩环与血管扩张剂孵育前后的缺氧反应。变量之间的关系采用Pearson相关检验进行评估。在适当的时候对变量进行对数变换。在所有情况下p‐value <0.05被认为是显著的。
结果
对照组由两名不吸烟者和五名吸烟者组成。慢性阻塞性肺病患者为重度吸烟者,表现为中度的气流阻塞(表1)⇑).
血管对缺氧的反应
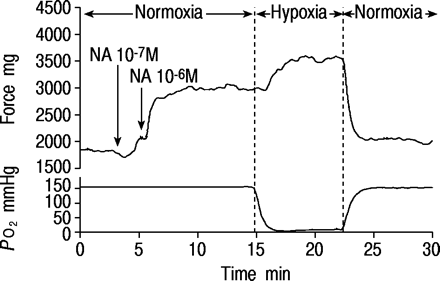
离体肺动脉环对低氧刺激的代表性反应如图1所示⇓.钠预收缩后,暴露于缺氧引起强烈收缩,从a开始PO2在20-30 mmHg的器官浴中,虽然要获得最大的和可重复的反应,aPO2要求<1.33 kPa (10 mmHg)。暴露后3-5分钟内收缩至缺氧达到峰值,并保持稳定≥5分钟(图1)⇓).长时间暴露会导致一些环的色调缓慢而逐渐地下降。正常氧条件的恢复完全消除了缺氧引起的收缩。在本研究中观察到的对低氧刺激的反应模式与较小直径的肺动脉相似7.表2总结了三组患者对缺氧反应的结果⇓.与其他两组相比,低氧血症COPD患者低氧刺激产生的张力变化明显较低。正常血氧血症的COPD患者与对照组之间对低氧刺激的反应无差异。对缺氧反应的程度在体外与动脉有显著相关性PO2(r=0.62, p<0.01)⇓).
与去甲肾上腺素(NA)预收缩并暴露于缺氧(95%氮)的离体肺动脉环的代表性反应。PO2:器官浴介质中氧气的分压。1 mmHg=0.133 kPa。
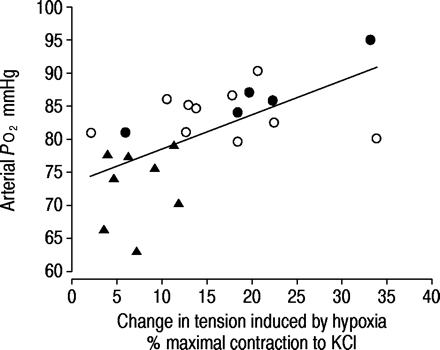
缺氧刺激引起的张力变化的关系在体外在肺动脉环和动脉分压氧(PO2).•:控制;〇:慢性阻塞性肺疾病(COPD)+常氧血症;低血氧症▴:慢性阻塞性肺病+。r = 0.62, p < 0.01。1 mmHg=0.133 kPa。
诱导内源性一氧化氮释放后的低氧血管收缩
最大收缩到NA (1×10−6M)在三组中相似。与先前的观察一致6, ADP引起的弛豫(1×10−6M)明显低于对照组(31±14)与KCl最大收缩22±8%,对照组和COPD患者;p = 0.05)。见表2⇑低氧血症的COPD患者对no依赖性血管扩张剂反应最低。的确,内皮功能,通过ADP或组胺诱导的血管舒张程度评估,与低氧刺激反应的程度相关(ADP: r=0.59, p<0.01;组胺:r=0.46, p<0.05)(图3)⇓).当低氧刺激应用于经no依赖性血管扩张剂(组胺或ADP)预处理的动脉环时,张力的变化比单独缺氧时更大(p<0.01)(图4a)⇓,表2⇑),尽管获得的最大张力是相似的。与其他两组相比,低氧COPD患者的动脉环在诱导NO释放后也显示出收缩到缺氧的幅度减小(表2)⇑).
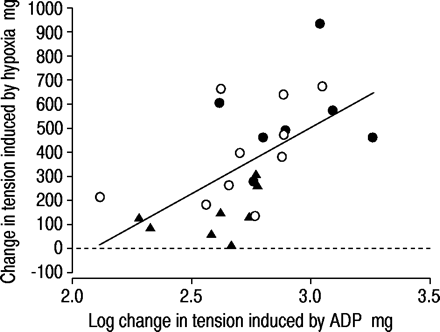
通过二磷酸腺苷(ADP)诱导的最大舒张(log转换)评估内皮功能与肺动脉环对缺氧刺激的反应之间的关系。•:控制;〇:慢性阻塞性肺疾病(COPD)+常氧血症;低血氧症▴:慢性阻塞性肺病+。r = 0.59, p < 0.01。
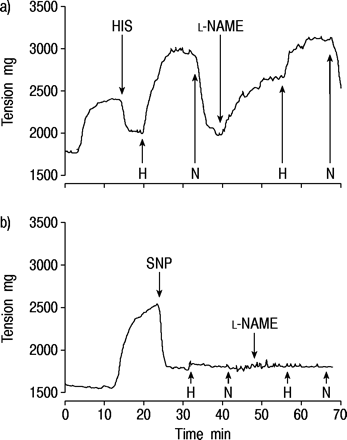
内皮源性一氧化氮(NO)对肺动脉缺氧收缩的影响。实验过程分三步进行。在第一步中,去甲肾上腺素收缩后,用a)组胺(HIS;1×10−7M)或b) NO供体硝普钠(SNP;1×10−8米)。在第二步中,为实现组胺最大放松时,动脉环被暴露于低氧(H) 10分钟,然后常氧条件下被重新建立。第三步,N抑制NO合成G单甲l精氨酸应承担应承担的设备(l量名称;1×10−3M), 10分钟后,重复低氧刺激。张力的变化被测量为暴露于H后获得的最大张力与缺氧刺激之前记录的张力之间的差值。N: normoxia。
讨论
现在的结果在体外研究表明,与对照组和正常低氧血症的COPD患者相比,中度COPD和轻度低氧血症患者的肺动脉对低氧刺激的反应降低。这种减少与内皮依赖性弛豫的下降有关。此外,对低氧刺激的反应在体外与动脉粥样硬化显著相关PO2值。
一般认为疾病状态与肺泡减少有关PO2持续HV和血管重构是肺动脉高压的主要机制。由于这个原因,对缺氧的反应减弱在体外在本研究中发现的低氧血症慢性阻塞性肺疾病患者可能存在争议。然而,研究慢性阻塞性肺病患者行显示广泛的变异个体反应的肺循环变化启发O2浓度2,3.,10.一般来说,终末期COPD患者对O的血管反应较低2呼吸比病情较轻的患者要少4,11.总的来说,这些临床发现和目前的研究结果与COPD患者亚组中血管对低氧刺激反应性降低一致,特别是那些有更大的气体交换障碍的患者。
在慢性阻塞性肺疾病中,对低氧刺激的反应降低可能对肺气体交换产生不利影响,低氧血症主要是由于缺氧引起的V”一个/问的不平衡12,13.血管调节的障碍V”一个/ Q '配对可使动脉氧合恶化。这一假设似乎被肺动脉环对缺氧反应的显著相关性所证实在体外动脉PO2(图2⇑),即对缺氧的反应越低在体外越低P啊,一个2.这一发现与麦克默里的结果一致et al。14在慢性缺氧大鼠中显示急性缺氧的升压反应降低。但需要注意的是,本研究中的COPD患者仅存在中度的气流阻塞,并无肺动脉高压的临床证据。即使在大多数低氧血症患者中P啊,一个2>9.31 kPa (70 mmHg)。因此,这些结果提示,在气流阻塞程度较轻的情况下,肺动脉对缺氧的反应性可能发生改变,并可能在气体交换障碍中起致病作用。
肺内皮细胞是众所周知的血管张力调节剂。它在缺氧反应中的作用已被许多作者所认识15,16尽管在许多方面存在争议。在这项研究中,内皮依赖性舒张较好的患者对缺氧反应较强(图3)⇑).这一观察结果提示NO通路可能部分参与了HPV的调控。事实上,在经诱导内皮释放NO的药物预处理的动脉中,缺氧引起的张力变化是最大的(图4a⇑).这似乎不是收缩前动脉张力降低的结果,因为先前使用SNP松弛的血管在暴露于缺氧时并不收缩(图4b)⇑).此外,在经内皮依赖性血管扩张剂预处理的动脉环中,抑制内皮型一氧化氮合酶(eNOS)和l‐NAME会在常氧状态下引起张力的强烈增加,而在应用低氧刺激时,几乎没有额外的收缩(表2)⇑).总之,这些发现与HPV在某种程度上与抑制内源性血管扩张剂有关,而不是与合成和释放血管收缩剂有关7,17,18.缺氧可能引起NO有效性的降低,尽管这种抑制的机制还不确定。因为分子O2是eNOS生成NO和l -瓜氨酸所必需的,可想而知,缺氧可能是NO合成的速率限制因素。然而,其他机制应该有助于HV,因为在本系列中,目前的作者发现尽管eNOS刺激,一些动脉的HV减少或消失。
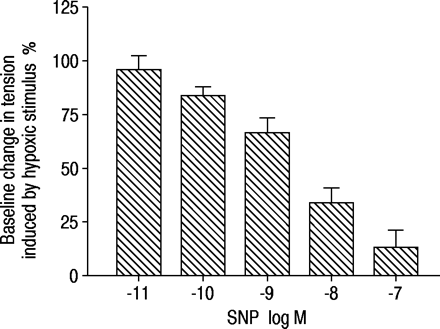
HV也被外源性NO消除,这与Ohe先前记录的实验数据一致et al。9以及健康受试者的临床研究19慢性阻塞性肺病患者12.作者发现,内皮独立的血管扩张剂的存在,如SNP或NO气体直接泡在器官浴室,是有效的低氧收缩拮抗剂。对于SNP,抑制作用是剂量依赖性的(图5)⇑).推测,过量的外源性NO直接作用于可溶性鸟苷酸环化酶,克服了缺氧对平滑肌细胞的影响。在灌流兔肺中,魏斯曼et al。20.表明no依赖的鸟苷酸环化酶活性在减弱血管收缩剂对缺氧的反应中具有重要作用,而no独立的鸟苷酸环化酶刺激并不能改变HV。外源性NO对HV的抑制作用并不排除HV可能是由内源性NO的可利用性降低引起的概念,因为外源性NO可以对其内源性合成产生负反馈21.有证据表明,在长时间吸入NO后灌注的肺中,对缺氧引起的高血压的血管反应性改变,这表明NO本身直接抑制eNOS活性22.
一些COPD患者对缺氧反应降低的机制尚不清楚。一般认为,慢性低氧血症在改变肺血管内皮no依赖性血管舒张中起着关键的致病作用23- - - - - -25.然而,这一观点受到了挑战,因为研究发现,在肺功能正常的吸烟者和轻度慢性阻塞性肺疾病的非低氧血症患者中,至少部分可以观察到肺动脉的结构异常和内皮功能障碍6,12,26.这表明烟草烟雾成分可能在改变肺循环中起直接作用6,27.目前的作者最近发现吸烟者的肺动脉中eNOS的表达减少28.推测慢性阻塞性肺疾病(COPD)肺动脉高压自然史的初始事件可能是香烟烟雾制品对肺内皮的损害,随后eNOS表达下调,内皮功能受损。根据目前的调查,HV也可能在这个阶段受损。这种情况可能会进一步恶化V”一个/问的配合并促进动脉低氧血症的发展。在这种情况下,持续暴露于中度低氧血症可能最终导致肺血管重构,这可能进一步放大烟草烟雾制品的初始影响。
综上所述,本研究结果显示,在慢性阻塞性肺疾病患者的肺动脉中,内皮源性一氧化氮合酶依赖性舒张与缺氧性血管收缩似乎是相关现象。这些发现还表明,慢性阻塞性肺疾病的低氧反应降低可降低血管收缩的有效性,改变肺循环对不同氧浓度的适应性,从而促进动脉低氧血症的发展。
- 收到了2002年1月17日。
- 接受2002年3月12日。
- ©ERS期刊有限公司