抽象的
活化的多形核中性粒细胞在急性呼吸窘迫综合征(ARDS)中的作用通过细胞外释放反应性细胞产物,如弹性蛋白酶。表面活性剂对ARDS患者肺功能恢复有重要作用。其免疫调节特性的意义与此效应尚未阐明。本研究的目的是确定表面活性剂给药对急性呼吸窘迫综合征婴儿的抗炎作用。
在2岁女性中ARDS的急性期间,用α复合的PMN衍生的弹性蛋白酶水平1-Protease抑制剂(E-α1在同时获得的动脉和中央静脉血液样品中测量PI)。结果与冷却施用表面活性剂的气管坏死因子-α(TNF-α)和白细胞介素-6(IL-6)相关的结果(Alveofact®60mg·kg·体重−1).
在现在的情况下,首次更高的E-α1动脉血PI浓度为4.51 mg·L−1)高于中心静脉血(2.28 mg·L−1).给药后,这些浓度和动静脉差异降低,说明在ARDS期间,大部分PMN脱颗粒发生在肺血管床,并被表面活性剂抑制。同时,TNF - α和IL - 6血浆浓度在数小时内降低,肺功能恢复。
外源性表面活性剂对多形核中性粒细胞活化的局部抑制,可能在给药后肺功能的早期改善中起关键作用。
急性呼吸窘迫综合征(ARDS)作为脑膜炎球菌败血症的并发症,使死亡率增加>50%1.多形核中性粒细胞(PMNs)作为原发性免疫反应的效应细胞,在ARDS的发病中起主导作用2,3..当被内毒素激活时,这些细胞被隔离在肺循环系统中。细胞外蛋白酶、炎症介质和活性氧代谢产物的释放导致肺泡毛细血管屏障的解体,导致肺水肿的形成和肺表面活性物质的失活4.端周膜表面活性剂更换成功用于治疗所产生的呼吸窘迫5,6.潜在的全身炎症反应是可检测的通过血管内增加PMN脱粒产物,例如弹性蛋酶7,如果没有与α络合1-蛋白酶抑制剂,可引起组织损伤和血清蛋白和凝血因子的降解8.血浆弹性蛋白酶/α浓度1- 抑制剂复合物(E-α1PI)9和非pmn来源的促炎细胞因子,如肿瘤坏死因子- α (TNF - α)10地理和白介素6 (IL 6)11,被证明与疾病的严重程度相关。作者自己在体外结果使他们认为,表面活性剂治疗ARDS的关键作用可能与抑制PMN的活化有关12.然而,这尚未在患者中进行研究。因此,在动脉和中枢静脉血样品中,在脑膜炎球菌脓毒症诱导的ARDS的过程中同时服用,E-α水平1作为PMN激活的指示,并确定并评估与表面活性剂治疗和需氧量相关的PMN活化的指示剂,如TNF-α和IL-6的临炎细胞因子。
案例报告
一名2岁零9个月的女性被送往Lübeck医科大学的儿科重症监护室,在短暂的发烧和感冒症状后,她的冷漠和呕吐迅速增加。她之前从未接受过任何治疗。周围脉搏不明显,心率125次·min−1.此时,孩子对痛苦刺激的反应仅是无特定的;她的呼吸迅速和浅。中央体温升高,但周边的凉爽皮肤已经显示出多个Petechiae和Ecchymoses。Glasgow脑膜炎球菌败血症预后得分,有15个可能的15分,表示预期致命结果13.
录取实验室分析
下列值是从通量的动脉血液分析中获得:pH7.15;动脉二氧化碳张力5.68 KPA;动脉氧气张力(PA,O.22.88 kPa);基底过量−14 mM;乳酸3.4毫米;葡萄糖1.78毫米;粒细胞12900个细胞·µL−1,其中17%为未成熟前体;thrombocytes 165000个细胞·µL−1;纤维蛋白原138 mg·dL−1;纤维蛋白原降解产物>8 mg·L−1;国际标准化凝血酶原比3.1;部分血栓形成时间77.5秒;天冬氨酸氨基转移酶13 u·l−1;丙氨酸氨基转移酶7 U·L.−1;γ谷氨酰转移酶8 U·L−1;乳酸脱氢酶266 U·L.−1;145毫米钠;钾4.55毫米;钙1.36毫米;氯化物100毫米;TNF-α1.56 ng·mL−1(酶联免疫吸附试验);IL 6 9.59µg·毫升−1(生物测定);C-反应蛋白(CRP)18 mg·L.−1;和e-α1pi 1.85 mg·l−1.在脑脊髓液中获得以下值:蛋白质0.82g·l−1;葡萄糖96 mg·dL−1;乳酸2.5毫米;白细胞1365个−1,其中63%是PMNS。血液和脑脊液培养均导致生长脑膜炎奈瑟氏菌B组。
课程
入院后立即给氧,插入中心静脉导管和动脉导管,患儿插管和通气。首次采血后,给予地塞米松(0.6 mg·kg·体重)−1·天−1在四种不同剂量)和抗生素治疗开始使用头孢噻肟(200 mg·kg·体质量−1·天−1四种单剂量)和青霉素(500 mg·kg·体重−1·天−1六次单独注射)。输注0.9%氯化钠、儿茶酚胺和新鲜冷冻血浆可恢复循环。通气需求增加,呼吸窘迫迅速加重(图1)⇓).入场后八小时(峰值吸气压力40 CMH2O,呼气末正压8 cmH2O,平均气道压力(MAP) 18 cmH2O,吸气氧分数(F我,o.2)1.0,PA,O.2/F我,o.211.2 KPA,氧合指数(oi; 100 f我,o.2地图/PA,O.2) 21),气管内给予表面活性剂(Alveofact®;勃林格殷格翰(Boehringer Ingelheim Corp., Ingelheim, Germany)总剂量为60 mg·kg·体重−1.表面活性剂施用后两小时,肺功能显然有所改善(PA,O.2/F我,o.216.1 kPa, OI 16), 12 h后进一步恢复(PA,O.2/F我,o.223.9 KPA,OI 8)。孩子们在治疗的第九一天拔管。
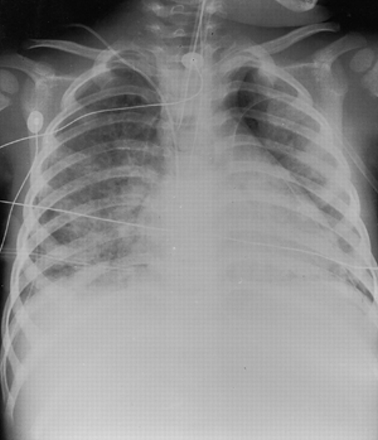
一位2岁女性的胸部射线照相,脓毒症诱导的急性呼吸窘迫综合征在表面活性剂施用前。
至于化学浓度的变化,虽然,最初,CRP浓度只是适度提高,E‐α1PI浓度在1.85 mg·L时已经出现了病理升高−1(参考范围80-230μg·l−1TNF-α(1.56 ng·ml−1)和IL‐6(9.59µg·mL .−1)已经达到了最大的血浆浓度(图2⇓).入院五小时后,静脉E-α1PI浓度从最大4.18毫克·宽减少−12.29 mg·L−13 h后,动脉E‐α1PI浓度仍然从4.27 mg·l增加−1最大水平为4.51 mg·l−1.此时,表面活性剂的施用导致与肺功能e-α的减少相关的肺功能立即改善1PI差异,在2小时内约为最大值的四分之一,在治疗过程中进一步降低(表1)⇓).这些变化也伴随着动脉E-α的清晰减少1血浆中PI、IL - 6和TNF - α的浓度。从最初的12900个细胞·µL开始,循环pmn的数量增加−1到17,500个细胞·μl−1表面活性剂治疗时,在整个治疗过程中保持稳定。CRP浓度持续升高至348 mg·L−1在48小时内。尽管局部硝酸甘油和肝素抗凝血局部促进循环和优化外周灌注(100 u·kg−1·24小时−1),明显的皮肤坏死,愈合后留下疤痕。尽管预后不佳,这孩子还是活了下来。然而,恢复很差,包括严重的缺氧/缺血性脑病,明显的痉挛和缺乏交互反应。
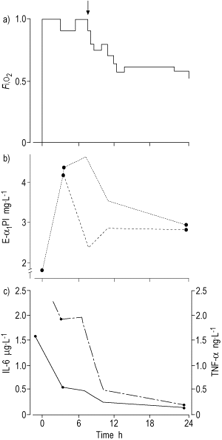
时间过程:a)吸气氧气分数(f我,o.2);b)动脉(Ⅵ)和中枢静脉( - - )弹性蛋白酶/α1- 抑制剂复合物(E-α1π)血浆浓度;c) 2岁女性急性呼吸窘迫综合征患者气管内表面活性剂(垂直箭头)给药后动脉肿瘤坏死因子- α (TNF - α)(- - - -)和白细胞介素- 6 (IL - 6)(-)血浆浓度。
讨论
目前,ARDS仍是脑膜炎球菌感染性休克最致命的并发症1.已知存在于临床症状的严重程度之间存在的相关性,促炎细胞因子和死亡率的血浆浓度导致了目前案件中致命结果的期望1,11.与之前报道的病例一样,该患者在入院时TNF - α和IL - 6浓度已经达到最大值11.此外,可以在E‐α快速增加的基础上记录PMN的激活1PI浓度并与临床和放射学同时呼吸窘迫相关。
如前所述,支气管肺泡灌洗液的细胞学和生化分析提供了PMNS和高浓度的细胞产物的证据1.Zimmermann也报道了ARDS中PMN活化的肺部位et al。14,谁证明了在体外动脉pmn的活化程度大于中心静脉pmn。在目前的病例中,肺也可以被确定为PMN最大激活的部位通过动静脉E‐α的测定1pi差异是由于体内肺PMN脱粒。为了目前的作者的知识,没有报告描述了E-α浓度浓度的这种动脉差异1PI是迄今为止肺PMN脱颗粒的指标。尽管气管内注射天然表面活性剂已被证明是治疗ARDS的有效成分5,6,因为它的生物物理特性15,通过该物质的许多生物抗炎作用的部分仍然必须阐明该物质的许多生物抗炎作用。抑制淋巴细胞和单核细胞功能16,以及抑制细胞因子诱导的PMN活化6通过表面活性剂,尚未在患者研究中进行检查。
在此描述的情况下,首次进行肺功能的变化,弹性蛋白酶的肺释放和与表面活性剂治疗相关的细胞因子浓度可以根据疾病过程的概要记录进行记录。
动脉弹性蛋白酶/α迅速下降1- 抑制剂复合物浓度和消除其在表面活性剂施用后循环细胞因子浓度的降低结合的消除其动静脉差异,强烈表明肺的多核性核心粒细胞活化的抑制。这些变化及其与肺功能改善的对应关系可能表明表面活性剂的抗炎性质参与了该物质的急性效应。即使与肺泡空间的细胞相互作用,例如巨噬细胞,粒细胞和肺细胞,是由于表面活性剂的局部施用,关于急性呼吸窘迫综合征在肺泡屏障的损伤,额外的可能性表面活性剂组分对间质和血管内细胞的肺泡作用不能排除出来。表面活性剂的给药似乎不仅影响多骨核心子粒细胞的激活,而且影响其他炎症细胞的响应,这些细胞导致肿瘤坏死因子-α和白细胞介素-6浓度的增加。由于肿瘤坏死因子-α和白细胞介素-6是目前正在开发的细胞因子阻断策略的目标物质之一17,表面活性剂给药可以在与此类疗法结合使用时提供进一步的选择。需要进一步的研究来解决关于本案例中观察到的效果是否与其他表面活性剂制剂类似的问题,其中表面活性剂的组分参与这些效果,特别是表面活性剂蛋白的局部减少浓度可能在这些浓度中起允许的作用。作用,以及是否可以通过改性剂量和剂量方案来优化所需的效果。
- 已收到2001年7月6日。
- 接受2001年9月7日。
- ©ers Journals Ltd














