抽象的
生理适应急性缺氧涉及各种专用细胞的氧气感测,包括颈动脉型I细胞,肺部神经头脑体细胞,肺动脉肌细胞和胎儿肾上腺素细胞。
缺氧通过关闭特定钾通道并触发细胞反应来诱导去极化。分子生物学策略最近允许鉴定k+在这些特化细胞中表达的通道亚单位。
几个电压门+当在异源表达表达时,缺氧时,包含六个跨膜段和单个孔结构段和单个孔结构段(KV1.2,KV1.5,KV2.1,KV3.1,KV3.3,KV4.2和KV9.3)。系统。另外,背景k+通道亚基任务-1,其包含四个跨膜段和两个孔隙域,也参与了外周化学感受器中的氧和酸感测。
目前,识别氧气传感器的工作正在取得进展。调节β亚基可能在氧对Kv通道亚基的调制中起重要作用。
这项工作得到了国家科学研究中心(CNRS)的支持。
对环境缺氧的快速反应是呼吸率的反射。该反射在位于颈动脉分叉的颈动脉体中引发1那2.减少动脉氧气张力(P.A,O.2),第一类化学感受器颈动脉体细胞释放神经递质,激活窦神经的传入感觉纤维,刺激脑干呼吸中枢,刺激通气反射性增加。类似地,神经上皮体细胞,是由位于气道粘膜内的含有胺和肽的细胞组成的神经簇,是缺氧刺激的转导器,在呼吸调节中发挥气道化学受体的作用3.-5..在围产期内,在建立交感神经内的内容之前,缺氧另外触发来自肾上腺素斑铬细胞的儿茶酚胺释放6..这种“非神经源性”机制对于新生儿生存缺氧应激的能力至关重要,并调节呼吸系统以及心血管和代谢反应。除了释放神经递质和对呼吸的刺激,缺氧也对肺循环产生了深刻的适应性影响7.那8..缺氧诱导的阻力性肺动脉平滑肌(PASM)血管收缩,导致无氧血液向肺通气较好的区域重新分配。胎儿的低氧张力环境也有助于胎儿高肺血管阻力。从胎儿右心室喷出的血液通过开放的动脉导管绕过肺循环9.那10..在出生时,氧气张力的增加产生了肺动脉抗性的快速下降,而引起了导管的闭合纱。虽然缺氧肺动脉血管收割机在匹配通风和灌注方面满足了必要的生理功能,但它也有助于慢性阻塞性肺病患者的肺动脉高血压的发展,患有高海拔高度的人们7..
这些专业细胞共享常见的一种机制,该机制将缺氧刺激转化为细胞反应:氧敏感钾通道的闭合1那2那7.那8..缺氧去极化了氧敏感细胞,增加了兴奋性,激发了电压门控的开口2+频道,增加细胞内CA2+,并触发细胞反应,包括神经递质释放和肌细胞收缩。
鉴定氧敏感k的分子组分,已经取得了最近的进展+频道。首先,哺乳动物K的分子多样性+将描述通道α和β亚基。其次,氧敏感k的表达+将详细介绍颈动体,神经上皮体,PCAM以及克隆细胞系中的颈部,神经头脑体,PC12和H-146中的频道亚基。最后,参与这些K的调节的分子机制+将讨论氧的通道亚基。
钾通道α亚基的分子多样性
K.+通道是形成离子孔的α亚基的多聚体。在哺乳动物中,克隆了>70α亚基,形成最大的离子通道族11.(fig. 1⇓).K.+根据膜拓扑结构,通道可分为三个不同的结构类。最大组包括具有六个跨膜段和单个孔结构域(P)的亚基。P域是所有K之间的保守区域+从细菌到人的渠道,并确定k+离子选择性12..氨基和羧基末端都在细胞内。6个跨膜段和1个p域通道组成电压门控(Kv)和钙激活(SK, Slo) K+通道(图1所示⇓).功能通道是相同亚基(同源体)或不同亚基(异多聚体)的四聚体(图2⇓).组装结构域T1是胞囊肌氨基末端的一部分14.那15..异多聚物在功能上不同于同质多聚物,有助于增加复杂性11..一些KV通道(KV1.4,KV3.3和KV3.4)的特征在于快速的电压依赖性灭活。通道的细胞质氨基末端可以被视为带正电荷的球,这通过封闭孔隙打开后引起通道的快速关闭(图2⇓).
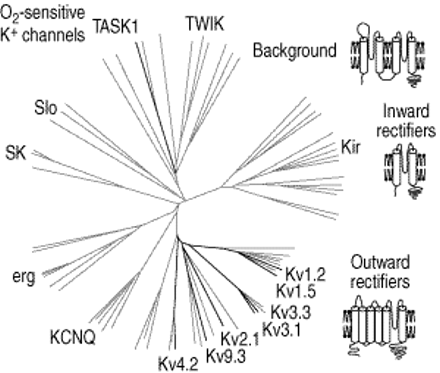
钾的系统发育树(k+)通道α亚基。提出的亚基参与氧气(o2)-Sensing用黑色表示。
第二个结构家庭包括k+具有两个跨膜段和一个p域的通道(图1⇑).再一次,四个亚基结合形成一个功能通道。内向整流器(IRK),三磷酸腺苷(ATP)依赖K+通道(KATP)和G蛋白受调节的K.+频道(girk)属于这个结构类11.那16..
最后一个结构家庭是由k制成的+具有四个跨膜段和两个p域的通道17.(fig. 1⇑).已经提出了这些亚基来二聚体。这些基因编码背景k+这些通道对拉伸、脂肪酸、麻醉、内外pH值敏感,并受到G蛋白偶联膜受体的正或负调控17..
钾通道β亚基的分子多样性
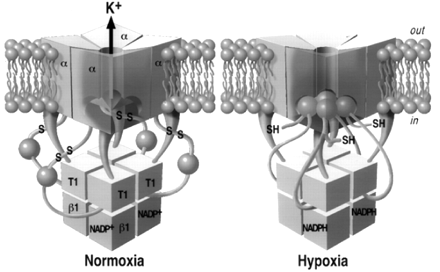
β亚基调控K的生物合成和门控+α亚基渠道。已经识别出三个主要的调控Kvβ亚基(Kv β1-3)18..KVβ亚基与α亚基的氨基末端相互作用14.那19.(图2⇑).四个β亚基与四个α亚基相互作用以形成功能通道。同样,不同β亚基的异统称性关联有助于提高KV通道的复杂性。KVβ1和KVβ3的氨基末端类似于KV1.4,KV3.3和KV3.4α亚基的灭活球。KVβ1或KVβ3亚基的共表达具有缺乏灭活球的KV1.x亚基的kV1.x亚基产生了快速的灭活k+通道18..最近通过X射线晶体学解决了KVβ2的3D结构19..每个亚基是氧化还原酶酶,其活性位点在其活性位点中具有烟酰胺酰胺辅因子。α-β复合物用四个T1结构域取向,形成面向跨膜孔的环,面向细胞质的四个β亚基14.(图2⇑).跨膜孔通过T1(4)β(4)β(4)复合物(悬挂式缆车)上方通过横向,带负电的开口与细胞质连通13.那19.(图2⇑).电压依赖性钾的失活肽+通道(一些KVα和KVβ的带正电荷的氨基末端)通过进入这些开口来达到其行动部位(图2⇑).β亚基包括两个跨膜片段调节钙依赖的Slo通道的活性。
颈动脉I型体和嗜铬细胞瘤PC-12细胞氧敏感钾通道的亚基组成
颈动脉体的主要感觉细胞应对缺氧和酸中毒,并用去极化发起电活动,钙入口和神经精神分泌2那20.-25..在大鼠I型细胞中,参与介导这些反应的关键离子电流是氧和酸敏感背景K+当前的26.那20.那21..该电流显示基线活动,没有电压和时间依赖性,并分享克隆K的所有生物物理和药理性质+频道任务-1,四个跨膜段的成员和两个P-域系列26.-30.(fig. 1⇑).TASK-1对铯、四乙基铵和4-氨基吡啶不敏感,但被钡、奎宁、奎尼丁和锌阻断。TASK-1可通过吸入全麻(包括氟烷)打开,但可通过布比卡因等局部麻醉剂阻断28.那29..任务-1的关键特征是其对外部pH的高敏感性,在pH 7.3下具有半抑制27..原位杂交和逆转录酶 - 聚合物链反应(RT-PCR)分析(未发布数据)表明任务-1信使核糖核酸(mRNA)在I型颈动脉体细胞中丰富26..由于其基线活动,任务-1设置静止膜电位,从而控制细胞兴奋性。在大鼠型癌细胞型颈动脉体细胞中,缺氧关闭任务-1类似的通道,而在内外贴片配置中没有效果26..切除时氧敏感性的损失表明,可能需要一些细胞源信使或辅助因子赋予或维持任务-1的氧敏感性26..当在转染的细胞或卵宫卵母细胞中表达时,缺氧(未发布数据)没有显着改变任务-1。最近,内源性大麻素Anandamide(AA的酰胺),磷脂酶D的产物已被证明是任务-1的直接和选择性阻滞剂31.测定Aandamide或相关分子在颈动脉体细胞中任务-1的缺氧抑制中的功能作用将是有趣的。
缺氧通过抑制几种类型的钾通道来启动颈动脉体的神经分子反应20.那23.那25..除了大鼠I型电池中的背景任务电流外,瞬态向外k+缺氧对兔I型细胞电流也有可逆性抑制作用25..最近使用使用腺病毒基因转移的主要负策略阐明阐明Shal(Kv4.x)亚基在兔型I颈动脉体细胞缺氧去极化中的功能作用25.(fig. 1⇑).kV1.x主导负负面没有效果,尽管Kv4.x主导负极完全抑制了瞬态向外电流,去极化细胞并消除了缺氧诱导的去极化25..在HEK293细胞中表达时,Kv4.2对缺氧或氧化还原刺激不敏感32.然而,用KVβ1.2的KV4.2的共表达形成K.+缺氧可逆地抑制的渠道32.这项工作表明,在兔型I颈动态化学感受器细胞中,与KVβ亚基相关的Shal亚基可以编码氧敏感的瞬态向外k+通道25.(图2⇑).在外面切除的蛋白组织中类似地观察到kV4.2 /kVβ1.2的缺氧抑制表明急性缺氧通过膜限定途径作用32.这些数据表明,Kv4.2/Kvβ1.2蛋白或具有固有的氧敏感,或有一个密切相关但独特的氧敏感元件在宿主细胞的膜上内源性表达。每个β亚基是一个氧化还原酶,其活性部位有一个烟酰胺辅助因子18..辅助因子可以在其还原,烟酰胺腺苷二核苷酸二核苷酸(NADPH)或氧化(NADP+)形式。k的Gating构象状态+通道可偶联到β亚基活性位点18.(图2⇑).因此,β亚基可以用作调节KV4.2通道的活性的细胞内氧化还原装置。作为一氧化碳(CO)还原KV4.2 /KVβ1.2的缺氧抑制,可另外参与血管氧传感器(至少在HEK细胞中)32.
颈动脉体I型细胞和嗜铬细胞PC12细胞均来源于神经嵴,在低氧分压下主要合成多巴胺作为神经递质反应(P.O.2) 状况33那34.缺氧通过抑制电压门控缓慢灭活k来诱导PC12细胞的去极化+频道。RT-PCR分析显示,KV1.2,KV1.3与KV2.1,KV3.1和KV3.2通道基因一起在PC12细胞中表达33那34(fig. 1⇑).振动筛α亚基KV1.2的表达,但没有其他k+通道基因,PC12细胞的增加暴露于延长缺氧(18小时)33.此外,与在常氧中维持的细胞相比,慢性缺氧中维持在慢性缺氧中的细胞变得更加敏感33.Charybdotoxin是Kv1.2的阻滞剂,抑制氧敏感k+电流在PC12细胞中34.此外,抗KV1.2抗体的细胞内给药完全消除了该电流,而抗KV2.1抗体无效34.最后,缺氧抑制KV1.2当在卵脓卵母细胞中表达时,尽管它未能影响KV2.134.这些结果表明,与KV2.1不同,KV1.2编码氧敏感电压门控缓慢失活k+PC12细胞中的通道[34-33]。
氧敏感k的亚基组成+神经头脑体内和小细胞肺癌H-146细胞的通道
肺神经上皮小体由广泛分布于气道粘膜的神经支配的含胺和肽的细胞簇组成3.那4.那5..这些细胞在功能上类似于I型颈动脉体细胞,并表现为肺化学感应感。催眠抑制作用+通道诱导细胞去极化和神经递质释放5..
神经头脑体细胞在其血浆膜上表达氧合蛋白质NADPH氧化酶5..缺氧影响氧化酶的功能通过底物氧的可用性降低,导致氧反应性中间体的产生降低,包括H.2O.2.Kv1.4、Kv3.3和Kv3.4在外施H后失去快速失活2O.2并在内出配置中切除贴片时3.那35那36那37(图2⇑).当减少药剂(减少的谷胱甘肽或二硫代噻唑醇)或在减少细胞的细胞内介质中挤压贴剂时,这种效果是可逆的。这些通道的氨基末端中的半胱氨酸氧化负责灭活的损害,随之而来的电流幅度增加36.这种调节可能是基于在失活的球结构域和蛋白质的另一部分之间快速和可逆的二硫化物桥的形成36(图2⇑).H2O.2-敏感通道Kv3.3a与NADPH氧化酶(gp91)的膜组分共表达Phox.和p22Phox.)在胎兔和新生儿肺的神经上皮体细胞3..神经头脑体细胞暴露于过氧化氢导致k的增加+信道振幅3..NADPH氧化酶作为神经头脑体细胞氧传感器的关键作用在GP91中证明了Phox.敲除老鼠4..缺氧不能抑制K+氧化酶缺陷小鼠中的通道4..然而,NADPH氧化酶不是普遍的氧传感器,作为k的缺氧抑制+PASM细胞中的通道在氧化酶敲除动物中不妨碍38.
小细胞肺癌细胞系H-146来自与神经头脑体细胞相同的前体池39.H-146细胞表达氧敏感k+频道。这些通道对4-氨基吡啶有抗性,但被奎尼丁完全阻断39.该药理类似于任务-1的药理学(图1⇑).RT-PCR分析显示,如颈动脉体型细胞所述,H-146细胞中任务-1的丰富表达26.那39.然而,氧敏K+H-146细胞中的电流对外部酸中毒不敏感,任务-1的标志27.那39.任务-1可能的异络层关联与另一个酸不敏感的两个p域k+因此可以涉及通道亚单元。然而,四种跨膜段K的异络层关联k+频道亚基仍有待证明。
肺动脉肌细胞氧敏感Kv通道的亚基组成
缺氧肺动脉血管收缩至少部分地是由于在皮疹细胞中闭合了电压门控Charybdotoxin抗性和4-氨基吡啶敏感的kV通道7.那8..利用简并聚合酶链反应(PCR)技术在大鼠PA环中鉴定了电压门控Shaker和Shab亚家族的Kv1.2、Kv2.1和Kv9.3 α亚基40(fig. 1⇑).在培养的怀孕细胞中另外发现KV1.3的较弱表达40.排除Kv1.2和Kv1.3作为候选氧敏钾+通道组分,因为它们都被Charybdotoxin阻塞。KV2.1是一种缓慢灭活的Charybdotoxin抗性和4-氨基吡啶敏感的电压门控K.+通道40那41.作为同性恋者,KV9.3不表达功能电流40.然而,Kv9.3与Kv2.1结合形成异多终子。重要的是,Kv9.3将Kv2.1的激活阈值从~ - 20 mV转移到~ - 50 mV,这是PA肌细胞静息膜电位的范围40.因此,kV2.1 / kV9.3异多聚体可以有助于设置这些细胞的静止膜电位。在单通道级别,KV9.3增加了8至14 ps的kV2.1的电导(生理k+坡度)40.随后通过蛋白质印迹分析在大鼠和卵巢Pa肌细胞中证明KV2.1的表达42-44.有趣的是,KV2.1沟道活动的增加是在绵延肺脉管系统中成熟的缺氧肺血管收缩的增加42.KV2.1同源体和KV2.1 / KV9.3异多聚体缺氧时缺氧抑制,当在COS和L细胞中表达时40那45.细胞内给药抗KV2.1抗体抑制全细胞k+电流和去极化大鼠皮疹细胞43.抗KV2.1还提升静止张力,并在膜渗透大鼠PA环中递减4-氨基吡啶诱导的血管收缩43.kv2.1 / kV9.3的缺氧抑制在皮疹细胞的静息膜电位范围内,这可能因此可以显着促成缺氧肺动脉血管收缩43那40.KV2.1和KV2.1 / KV9.3通道由细胞内ATP在切除的内涂层中刺激40.ATP对Kv通道活性的调节可能是线粒体呼吸与细胞电发生的联系。缺氧时细胞内ATP浓度下降可能导致Kv2.1/Kv9.3电流幅值降低,从而导致PASM细胞去极化收缩40.此外,线粒体脱象以及脱氧葡萄糖,抑制PA肌细胞kV电流46-47.
RT-PCR,Northern印迹以及Western印迹分析证实了PASM细胞中Kv1.2,Kv2.1和Kv9.3的表达,进一步揭示了Kv1.1,Kv1.4,Kv1.5,Kv1的存在。6对于β亚基的α亚基和KVβ1.1,KVβ2和KVβ344(fig. 1⇑).但是,在帕特尔的研究中et al。40,PCR使用特异性引物未检测到KV1.540.低互氧核糖核酸(cDNA)模板浓度以及弱引物效率可能解释这种差异。然而,应该考虑到KV1.5在PA内皮细胞中高度表达,并且细胞污染可能导致PASM细胞中KV1.5表达的高估48那43.与KV1.5不同,KV1.2与KV1.5不同,在L细胞中表达时,缺氧被缺氧抑制45.然而,KV1.2在PASM细胞静止膜电位的范围内不活跃45.正如之前在Kv2.1和Kv9.3中观察到的,Kv1.2和Kv1.5的共同表达产生了一个异源抗树毒的K+在相关的生理潜力下活跃的通道,其被缺氧可逆地抑制45.这些结果表明异多聚体KV2.1 / KV9.3和KV1.2 / KV1.5可以编码氧敏感k+Pa myocytes的频道45那40.
与抗KV2.1不同,抗KV1.5抗体的细胞内施用既不是引起的去极化也不升高大鼠基础肺动脉调43.这表明,Kv2.1主要受缺氧抑制,而由Kv2.1阻滞(可能与Kv9.3有关)引起的缺氧去极化将膜电位转移到Kv1.5(可能与Kv1.2有关)活跃的范围43.kv1.2 / kV1.5的缺氧抑制可以扩增去极化43那45.
慢性缺氧导致k减少+信道电流幅度和Pa肌细胞的去极化,肺动脉压的稳步增加,压力响应急性缺氧的响应减少,最终与肌细胞的肥大和增殖进行重塑49那50.慢性缺氧下调kv1.1,kV1.2,kV1.5,kV2.1,kV4.3和kV9.3 mRNA和/或蛋白表达在培养的大鼠PASM细胞中,而不影响KVβ1-3亚基的mRNA水平50那51.β亚基的不变转录可能会增加与β亚基相关的α亚基的分数,从而通过促进失活来减少kV电流50.这些数据表明,慢性缺氧期间的KV通道转录的调制可能导致肺血管收缩和高血压49那50.
最近,显示Kv3.1b在兔子皮中以及PC12细胞中表达52(fig. 1⇑).Kv3.1b在L929细胞中表达时,可被缺氧可逆地抑制52.缺氧抑制仍然存在于切除的斑块中,提示一种膜界机制。Kv3.1b在缺氧肺动脉血管收缩中的作用尚不清楚,因为电压激活阈值超出了兔PASM细胞静息时所遇到的膜电位范围52.与另一KVα或β亚基的关联可能会使激活阈值移位,如KV2.1 / KV9.3和KV1.2 / KV1.5的情况下所观察到52那45那40.
结论和观点
在过去的4年内,几个氧敏感k+已经鉴定了通道亚基:KV1.2(PC12,PA),KV1.5(PA),KV2.1(PA),KV3.1(PA,PC12),KV3.3(神经头脑体,H-146),KV4.2(颈体),KV9.3(PA)和任务-1(颈动脉H-146)3.那25.那26.那32那33那34那39那40那43那45那52.这些通道在存在氧气存在下是开放的,但通过缺氧可逆地关闭。有趣的是,在兔和人类导管颤动,缺氧打开,而氧气可逆地关闭电压门K+通道导致出生时肌细胞的去极化和收缩9.那10..
KV1.2,KV1.5,KV2.1和KV3.1在PA和导管均匀肌肉细胞中表达9.那40那43那44.因此,相同的αkV通道亚基可以根据宿主细胞通过氧气差异调节。例如,KV2.1的缺氧敏感性在cDNA转染的L细胞中始终报告,仅在转染的COS细胞的子集中观察,而在mRNA注入的外爪卵卵卵细胞中不存在34那40那45.这些结果表明,在特殊的细胞中差异表达的调节蛋白可能需要赋予或维持差分氧敏感性。在神经头脑体细胞中,现在清楚的是,NADPH氧化酶是通过氧化还原的氧化氧调节来调节KV3.3的氧气传感器,其快速氨基终端依赖性灭活4..在颈动脉体细胞中,作为活性氧化还原酶的KVβ1.2蛋白也是KV4.2的缺氧调节所需的32.
发现构成氧敏感钾通道的分子组分及其氧气传感器可能有助于了解对重要疾病的理解,包括肺动脉高血压和持久性导管血管。
致谢
作者感谢M. Lazdunski为持续的支持和实验室的所有成员在本研究时的帮助下。G. Jarron,M.Jodar,V.Lopez和F. Aguila认可出于出色的技术援助。
- 已收到2001年1月9日。
- 公认2001年3月7日。
- ©ers Journals Ltd