抽象
间质性肺疾病(也称为弥漫性浸润性肺病)是已知的或未知的原因实质肺部疾病的一组异质性。这些病症通常与呼吸困难,弥漫性肺浸润,和受损的气体交换相关联。大多数间质性肺病的是原因不明的。间质性肺病的已知原因包括有机和无机粉尘吸入以及气体或烟雾,药物,辐射,和感染。
本文总结的是已与福朋间质性肺疾病的临床,放射学和组织病理学特征。这些病症包括脱屑性间质性肺炎,呼吸性细支气管炎相关性间质性肺病,肺朗格汉斯细胞组织细胞增生症和特发性肺纤维化。现有证据表明,脱屑性间质性肺炎,呼吸性细支气管炎伴间质性肺疾病,肺郎格罕组织细胞增生症的大多数病例是由吸烟在易感个体引起的。戒烟应该是在初始治疗方法与这些间质性肺病吸烟者主要成分。此外,吸烟似乎是特发性肺纤维化发展的危险因素。
这种审查是由梅奥基金会的资助支持。
吸烟对个人和社会都是非常昂贵的。一半的吸烟者最终会被他们的习惯杀死1。吸烟仍然是美国过早死亡和发病的最可预防的原因和发达世界1,2。香烟烟雾超过4000度的化合物的复杂混合物,并导致多种人类肺部和全身效应1-3。吸烟是肺癌,这又是癌症死亡的美国男性和女性的首要原因的主要原因1,2。此外,吸烟是患慢性阻塞性肺疾病(COPD)的主要危险因素。据估计,所有吸烟者的10-15%的开发临床显著气流阻塞1。近来,吸烟已经被牵连导致间质性肺疾病。
肺间质性疾病(ILDs)或弥漫性肺浸润性疾病是一类由已知或未知原因引起的肺部疾病,其典型特征为呼吸困难、弥漫性肺实质浸润、限制性肺功能障碍和气体交换障碍4-8。最常见的ILD包括特发性肺纤维化(IPF),结节病,尘肺,并与结缔组织疾病相关的那些4-8。最近已经认识到吸烟有关的几个间质性肺病,包括脱屑性间质性肺炎(DIP),呼吸性细支气管炎伴间质性肺病(RBILD),肺郎格罕组织细胞增生症(PLCH),以及IPF的发展。在这篇文章中,作者将审查这些肺部疾病的临床,影像和病理特点以及他们的吸烟的关系。
方法
笔者搜索发布1966年至1999年的医学主题词(目)条款吸烟与肺癌,肺疾病,间质性肺疾病,支气管炎文学MEDLINE数据库,朗格汉斯细胞增生症和肺纤维化在不同的搜索中使用,并研究每个搜索过程中发现合并。限分别只有英语语言设置。作者通过手动搜索检索到的文章的参考文献确定的其他相关研究。对于包括在本次审查研究的首要标准是基于对他们的相关性来参与护理的患者肺部疾病临床医生,以及它们的质量,作者的判断。
脱屑性间质性肺炎
DIP目前归类为特发性间质性肺炎的一个形式9。The most striking histopathologic finding in DIP (fig. 1⇓)是均匀地分散肺泡空间内的巨噬细胞色素的数量增加的情况下6,9。在低放大率下,从一个领域到另一个领域的整体外观是相对一致的。弥漫性纤维化和轻度间质性炎症使肺泡间隔增厚到不同程度。蜂窝变化,如果存在,是最小的,和整体架构保持,虽然一些肺气肿的变化是常见的。
吸烟相关间质性肺病的组织学特征。一个)脱屑性间质性肺炎(DIP)示出了肺组织散射的生发中心的相对漫参与低功耗视图。到右侧时,midly萎陷肺组织显得有些固体,而空域是在左更加明显,并且示出了由巨噬细胞的一个突出填充。B)DIP的大功率视图,示出在标记的肺泡巨噬细胞和肺泡温和间隔增厚和纤维化增加。示出帧内肺泡巨噬细胞的一个突出的集合C)呼吸性细支气管炎相关性间质性肺病(RBILD的低功耗视图),其上的细支气管和肺泡管中心。d)RBILD的大功率视图,示出在标记的肺泡巨噬细胞和肺泡温和间隔增厚和纤维化增加。E)示出了中央粉红纤维化和星状字符肺朗格汉斯细胞增生症(PLCH)示出了两个病变(低级中心),其示出了中央气蚀,而另一个的(到第一的右侧)的低功率图。周围的肺组织显示了肺气肿变化和附加的病变(最右边)。主动的细胞病变(左中心)以及肺LCH(右中心)的老愈合损伤的存在的情况并不少见。f)对PLCH示出具有其独特的折叠和微妙的核大量朗格汉斯细胞大功率图。 A pigmented alveolar macrophage with its oval nucleus and denser tan cytoplasm is also present (right centre). g) Low-power view of usual interstitial pneumonia showing patchy fibrosis which is more prominent in the subpleural regions (lower). Focal honeycomb change is present (left lower). Note the presence of some entirely normal lung tissue (upper). h) Low-power view showing numerous vague nodular lesions involving the lung parenchyma. One of these (upper centre) is a lesion of Langerhans' cell histiocytosis, whereas the others represent respiratory bronchiolitis. Numerically, the latter were much more numerous and most likely accounted for this patient's clinical signs and symptoms (即RBILD)。在这种情况下,相同的附加字段表明由巨噬细胞与空域填充大的区域,典型的DIP。
The average age at onset of symptoms for patients with DIP (table 1⇓)is ∼40 yrs10,11. 在儿童中发生是罕见的,但DIP是这个年龄组间质性肺病中较常见的一种,在那里它可能是一种与吸烟无关的不同疾病12,13。大多数研究指出男性居多,与受影响的近两倍经常名女性9-11。呼吸困难和咳嗽是最常见的主诉,发病通常是隐匿的。60%的患者可听到吸气爆裂声10,11以及发生在患者的近一半杵状指10,11。
在两个最大的案例系列,大约患者的DIP熏90%或有抽烟10,11。DIP有时可能与系统性疾病或感染,以及职业/环境因素和药物的暴露有关10-22。例如,该系列中的40例DIP报道卡林顿等。10,5(12.5%)有结缔组织疾病,包括异烟肼诱导的狼疮综合征的一个案件。只有“特发性”的情况下,没有相关的障碍将被目前接受为DIP。此外,局灶性巨噬细胞聚集,称为“DIP样反应”,在一些设置可以被看作是一个偶然的病变23,24。
X线,肺容积减小出现,除非有共存阻塞性气道疾病,例如在与肺气肿吸烟者10,11。大约四分之一的患者存在双基底混浊,外观模糊,呈毛玻璃样。虽然这种影像学表现在早期报道中被认为是DIP的一个特征特征,但后续的研究更多地显示了一种非特异性的线性或网状结节间质模式9。具有减小的扩散能力限制的缺陷肺功能测试通常发现,但异常通常不太明显高于普通型间质性肺炎的情况下观察到9,10。
高分辨率计算机断层扫描(HRCT)的主要发现(图2)⇓)是存在磨砂玻璃衰减的区域25,26。这些通常有胸膜下肺区的优势。纤维化的衰减暗示的不规则线条出现在患者的一半和蜂窝状不是通常存在25-28。
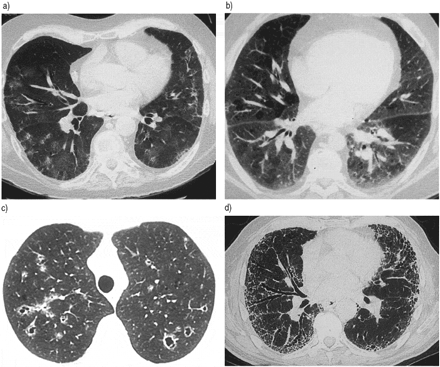
高分辨率计算机断层扫描(HRCT)与吸烟有关的间质性肺病的放射特性。a)一种59年生的男性,与外围优势毛玻璃衰减的脱屑性间质性肺炎表示片状区域HRCT。b)一种51年生的男性,呼吸性细支气管炎相关性间质性肺病表示漫整个两肺毛玻璃衰减的斑片状区域HRCT。c)一种33年生女性肺朗格汉斯细胞的组织细胞增生症HRCT表示多发性结节和厚壁囊肿。有保肺底(未示出图)。d)一个72年生的雄性与特发性肺纤维化(普通型间质性肺炎)表示胸膜下网状密度和具有相关联的牵引支气管扩张蜂窝状的HRCT。
如果不及时治疗,对患者的DIP三分之二有恶化的临床证据10。然而,自发改善可以看到和在7(21.9%)中观察到的32名未经治疗的患者与由卡林顿报道DIP等。10。改善是否与戒烟有关尚不清楚。治疗时,DIP患者通常接受长期的皮质类固醇治疗。大多数DIP患者在接受皮质类固醇治疗后病情保持稳定或有所改善,完全康复是可能的10,11,27,28。糖皮质激素治疗的反应并不一致的患者大约四分之一可能会继续,尽管治疗DIP恶化10,11,28。细胞等免疫抑制剂的作用仍然不确定。在由卡林顿报道的病例系列等。10,11的40例(27.5%)12岁的平均存活后死亡。晚期复发29还有复发的肺移植已报告30.,31。这些报告不指定吸烟是否是DIP的复发因素。上述疗法的角色需要相对于戒烟的效果进行重新评估。
呼吸性细支气管炎相关性间质性肺病
毛细支气管炎是临床上用来描述各种小气道炎症性疾病的总称32. 细支气管疾病可由吸烟、感染、吸入、吸入环境因素、药物和潜在的系统性疾病(包括结缔组织疾病和移植排斥反应)引起。Niewehner描述了呼吸性细支气管炎等。33作为一个偶然的尸检发现,主要是年轻男性吸烟者。这种疾病是目前公认的极其常见于吸烟者,术语“吸烟者的支气管炎”,是描述性的合适32。呼吸性细支气管炎通常无症状或伴有明显的间质性肺病。它可能导致多达五分之一吸烟者的亚临床放射学改变(见下文)。
而呼吸性细支气管炎在几乎所有的吸烟者发生,是在绝大多数情况下的临床意义不大,在吸烟者中的一小部分,可以与这种病变的关联而发生症状的间质性肺病。1987年,迈尔斯等。34描述的内容随后被标记的呼吸性细支气管炎相关性间质性肺病(RBILD)。这是一个临床病理实体在当前或以前吸烟者看到几乎完全并且可以与其他间质性肺疾病混淆,特别是,IPF11,34-36。
RBILD is characterized by the presence of pigmented macrophages and mild interstitial inflammatory changes centring on respiratory bronchioles and neighbouring alveoli (fig. 1⇑)11,32,34。细支气管周围的肺泡隔可轻度增厚,但无纤维化。类似的病理发现也见于其他吸入性损伤,特别是石棉和非石棉矿物粉尘暴露,以及其他情况36,但是数字是这样的情况是罕见的,呼吸性细支气管炎的几乎所有的病例是由于吸烟。
RBILD和DIP之间的组织学区别主要基于炎症过程的程度。相比RBILD组织病理学变化更广泛和DIP弥漫9,11,32,34。在RBILD中,巨噬细胞聚集局限于细支气管周围的空气空间,远端空气空间相对较少。RBILD的间质增厚伴随着空气空间的改变,并趋向于局限于支气管周围的实质。
对于多数患者RBILD,发病症状通常是在第四或第五十年的生活11,34,36and is considerably earlier (table 1⇑)患者的普通型间质性肺炎(UIP)9。有一个轻微的男性居多11,34,36。患者RBILD普遍出现咳嗽和呼吸困难11,34,36。这些症状一般较轻微,但有时可能很严重38。肺部听诊揭示患者约半数吸气性爆裂音11,36,39。数字俱乐部偶尔可见36,38。
肺功能结果可能是正常的,但更常见的是一种混合的阻塞-限制性模式,从轻度到中度11,34,36。减小扩散能力也是共同11,34,36。总肺活量可正常、轻度增加或轻度减少11,34,36。
胸片通常异常11,34,36. 超过三分之二的RBILD患者存在弥漫性、细网状或网状结节样混浊11,34,36。普通胸片5例(28%)被指出的18例报告Yousem等。11。毛玻璃模式可能在某些患者出现的主要异常36。RBILD通常可以从IPF上由不存在蜂窝状的胸片区分。
在RBILD的HRCT发现在一些病例中有报道。毛玻璃衰减的区域是最常见的发现(图2⇑),但也可见细小结节26,36,40,41。相关肺气肿改变可能存在,但IPF的迹象,如胸膜下蜂窝状和牵拉性支气管扩张,是不存在的。据推测,地面玻璃衰减的领域体现“吸烟者的肺泡炎”,而micronodules代表呼吸性细支气管炎26,40。RBILD的箱子中越来越多的被由于广泛使用的HRCT识别。
患者RBILD具有一般预后良好,特别是与戒烟11,34,36。大多数患者要么病情好转,要么病情稳定,没有人死于RBILD11,34,36。渐进纤维化的肺部疾病不治疗RBILD发生。皮质类固醇治疗已在少数情况下,传闻已采用,并与有利的结果相关34。有些治疗的患者最初被认为有DIP11. 然而,皮质类固醇治疗在大多数RBILD患者的治疗中几乎没有作用。戒烟是治疗RBILD最重要的治疗策略11,34,36。
There are similarities between RBILD and DIP with respect to demographics, clinical features, and radiological features (table 1⇑)。此外,重叠RBILD和DIP的组织病理学模式可以在一些患者和术语可以看到“吸烟相关的间质性肺疾病”已建议对于这些情况36。这两种病变在组织学上没有明显的区别,这表明RBILD和DIP可能代表由同一种物质(即香烟烟雾)引起的同一种疾病光谱的不同末端9,26,36。
肺郎格罕组织细胞增生症
组织细胞性病症包括临床综合征的一种罕见的和混乱的组为特征的任一巨噬细胞或树突状细胞的细胞的增殖(包括朗格汉斯细胞)谱系42,43。1997年,该组织细胞协会的重新分类工作组分类组织细胞障碍分为两个主要的亚型:的变化生物学行为和恶性疾病障碍42。根据异常细胞是来自树突状细胞还是巨噬细胞,进一步细分每一类。朗格汉斯细胞组织细胞增多症(LCH)被归类为多种生物行为(非恶性)的树突状细胞相关疾病,其严重程度从自限性疾病到致命性疾病不等。LCH包括几种以朗格汉斯细胞过度增殖为特征的疾病,病理上以含有朗格汉斯细胞的破坏性浸润为特征。弥漫性累及多种脏器,伴有严重的体质症状和不良预后,最常见于婴儿(莱特-西韦病)。儿童常出现两种或两种以上组织的多灶性受累,常伴有骨骼、皮肤、肝脏、脾脏、肺、下丘脑和/或淋巴结的病变(手-舒乐-克里斯蒂安综合征)。局限于单一组织的病变,特别是骨、皮肤和/或肺,可在任何年龄发生(嗜酸性肉芽肿)。
朗格汉斯细胞根据其特性五层状板状通过电子显微镜看到细胞器(伯贝克颗粒或X体)和抗原的CD1a的细胞表面上其强表达从树突状细胞区分开44,45. 他们还用S-100抗体染色45。朗格汉斯细胞存在于正常肺和具有有效的抗原呈递能力44,45。吸烟与呼吸道上皮表面朗格汉斯细胞的积聚有关46。
LCH的肺部受累通常是孤立发生的,很少作为全身性疾病的一部分(通常发生在儿童身上,与吸烟无关)47-49。成人LCH的孤立性肺形式几乎都发生在吸烟者44,47,48。PLCH也被称为原发性肺组织细胞增多症X、肺嗜酸性肉芽肿和肺兰格罕细胞肉芽肿病,通常被归类为来源不明的肺间质性疾病。虽然LCH的某些形式可能代表朗格汉斯细胞的单克隆增殖50,它是目前未知这是否是在成人中发生的LCH的隔离肺形式也是如此。它似乎更可能是成人PLCH代表由吸烟引发的多克隆抗体,反应性疾病51。
The characteristic histopathological finding in PLCH (fig. 1⇑)结节性硬化性病变是否含有朗格汉斯细胞并伴有混合细胞浸润45。结节病变定义不清和被分布在bronchiolocentric方式与居间正常肺实质中。朗格汉斯细胞的存在需要明确的诊断。作为病变的发展,有纤维化和相邻的肺组织相关联pericicatricial腔扩大占伴随囊性改变的渐进参与。
病理结果与阶段有所不同:在早期阶段,大量的朗格汉斯细胞中积聚的区域邻近于终端或呼吸性细支气管45。这些细胞似乎侵入细支气管,以一种古怪的方式破坏细支气管壁。结节的中央囊性改变(也称为空化)有时可追溯到扩张的、被破坏的小气道。淋巴细胞、肺泡巨噬细胞和嗜酸性粒细胞也存在,通常在病变周围。炎性细胞浸润可使靠近支气管病变区域的肺泡壁增厚,朗格汉斯细胞数量减少。随着病变愈合,细胞浸润变得不明显,并出现纤维化,形成典型的星状瘢痕。此阶段的活检未见朗格汉斯细胞。此外,经常观察到邻近星状疤痕的肺泡牵拉性肺气肿和支气管周纤维化。结节中央囊性改变和邻近的牵拉性肺气肿可能都是HRCT所见囊性改变的原因52。肺气肿和呼吸性细支气管炎通常也都是从PLCH的结节性损害存在了。
大多数患者在他们的第三个和第四个十年的生活青壮年45,53-57。总体而言,性别分布大致相等45,53-57。一些研究一致表明> 90%的病人有PLCH是当前或以前吸烟者45,53-57。此外,在一项病例对照研究中,吸烟已被证明是PLCH发生的一个重要危险因素58. 病理性病变的细支气管分布与吸入抗原参与本病发病的可能性一致。
Patients with PLCH commonly present (table 1⇑)有呼吸困难(35-87%)及咳嗽(50-70%)45,52-55。患者〜10%获得气胸史45,53-56。其他症状可包括气喘,发烧,疲劳,体重减轻,胸痛和咯血。在疾病的早期阶段,到受影响的患者的四分之一可无症状或有轻度,非特异性症状51,56. 在体格检查中,很少出现裂纹和数字棒,但偶尔会听到喘息声45,51,57。囊性骨病变可在约10%患者来识别与PLCH和最经常出现在颅骨,肋骨,骨盆和45,53,54,57,有的这些骨病变可无症状与没有疼痛。骨病可能先于肺部疾病的发展。尿崩症报道多达10%的患者45,53,56,57但这个相对较高的数字可能是选择偏差的结果。
体格检查常为正常,肺部听诊偶尔可见散在的爆裂声或喘息声44,53,57。在该疾病的晚期阶段,仅降低呼吸音可以理解53。
在患者PLCH,胸片上典型的表现包括结节状或网状结节阴影在中上肺野最为突出44,45,47,49,53,55。通常有节约肋膈角和肺容积显示正常或增加。随着疾病的进一步发展,囊性变化和大疱出现和肺容积增加。胸部HRCT确认与肺底的相对备用的主要上部肺部受累47,48,59,60。Thin-walled cysts, nodules (with or without cavitation) or a combination of nodules and cysts may be seen (fig. 2⇑)。网状密度和毛玻璃衰减的区域并不常见60,61。孢囊的形状可以是不规则的,并与那些在肺淋巴管肌瘤病看到更加复杂。肺底的节约也是从肺淋巴管肌瘤病鉴别PLCH一个重要发现59。
无论阻塞性和限制性的变化可能在患者PLCH可以看出。从吸烟的影响可以被叠加并从难以PLCH本身的效果来区分。扩散能力通常是异常44,45,53,54。运动性能通常受损,可能反映了肺血管功能障碍54,62,63。
PLCH的诊断可以强烈怀疑根据流行病学,临床,放射照相,和生理特征。弥漫性间质混浊,主要在中期和上肺与一个年轻的成年烟民胸片可见正常或增加肺容量,强烈建议PLCH在没有职业或环境暴露的诊断。看到在HRCT,典型情况下,该功能用于诊断这种疾病59。香烟吸烟史的缺失使得PLCH的诊断不太可能。用于诊断的组织病理学确认,通常需要外科肺活检虽然支气管肺活检可以是诊断,如果得到足够的组织45,47,48,53,64。在支气管肺泡灌洗液≥5%的CD1a阳性细胞(朗格汉斯细胞)的结果也支持PLCH的诊断55。
由于PLCH的自然史的巨大差异,也有关于治疗和预后几个可靠的指导方针。一般来说,程度和所评估的胸片和肺功能测试初始肺部受累的严重性似乎具有预后价值45,53,55。本病以先进的肺纤维化和死亡的进展是罕见45,53。虽然糖皮质激素治疗已在患者PLCH治疗中使用,它的好处还不清楚45,47,48,53,55,65. 其他疗法包括细胞毒性药物,包括环磷酰胺、长春碱和氯霉素。不幸的是,没有人能明显改善病情45,47,48,53,55。胸膜融合术可能是必要的病人复发性气胸。
尚未执行的对患者的PLCH戒烟治疗作用明确的研究。类似地,该疾病遗体吸烟状态和进展之间的关系加以澄清。放射改善和戒烟后PLCH的甚至完全分辨率的情况下,报告中描述66,67。移植肺中PLCH的复发见于肺移植术后恢复吸烟的患者68。戒烟可以阻止疾病的进展,应大力鼓励患者PLCH谁继续吸烟。
特发性肺纤维化
IPF,又称欧洲隐原性纤维化肺泡,是间质性肺疾病的最常见形式4,69。IPF的患病率尚不确知,但估计是每10万人中约3-29例69。宽范围在该估计可能是由缺乏识别IPF的情况下,以及在研究设计和人群不同使用统一的定义的说明。的男女比例已范围:〜1:1-2:169,70病人通常在60到80岁之间4,35,71。IPF的大多数病例是零星的,但确实发生家族形式72,73。
在早期病例系列,IPF的诊断是基于临床/放射学发现没有在许多情况下,组织学证实74。近日,组织模式已经被更仔细地定义,并建议患者以前诊断为IPF显示品种,与不同的反应,治疗和预后相关的组织模式9,35,75。The most common histological pattern in cases previously diagnosed as IPF is UIP (fig. 1⇑)。IPF / UIP与预后更差(〜3年的平均存活)和相对耐火度皮质类固醇治疗相比于其他形式的慢性间质性肺炎,包括DIP,非特异性间质性肺炎和闭塞性细支气管炎机化性肺炎相关联35,77-78。术语“特发性肺纤维化”,现在应该留给那些患者不明原因的UIP35,78。
IPF的典型临床特征包括渐进的劳力性呼吸困难,慢性咳嗽(通常是干重)和bibasilar吸气(“维可牢”)裂纹35,78。杵状指见于患者约三分之二的IPF35。临床病史、检查和筛选实验室检查对进展性肺纤维化的病因没有提示。特别是,需要排除环境和职业接触以及药物的可能原因。
胸部X线检查表明双边网状或网状结节阴影小肺容量35,78。通常,存在于这些浸润的分布下肺区和外围优势。HRCT of the chest (fig. 2⇑)典型表现为不规则线状混浊和蜂窝状,主要分布于肺基底部和胸膜下79,80。磨玻璃衰减的领域可以看到,但通常不广泛。当这些HRCT特征存在于一个适当的临床背景下,IPF的诊断是正确的患者85-90%81,82. 然而,小部分经活检证实的IPF患者的胸部HRCT可能是正常的83。此外,HRCT可能无法从IPF在某些情况下,区分慢性过敏性肺炎84。
肺功能测试通常证明限制性缺陷具有减少的肺容积和容量扩散35,78。用力呼气量的在一秒用力肺活量(比率FEV1/FVC)正常或升高,与限制性功能障碍一致。肺泡动脉氧分压升高通常会影响气体交换(PA-A,O2)梯度。即使当在动脉血液静息氧张力(Pa、 O型2)是正常的,运动诱发的饱和几乎总是看到。
应当指出的是,在患者与预先存在的肺气肿,肺体积和流速可能是正常的,由于肺气肿和纤维化的抵消生理效应85。在这样的患者的共存肺气肿和IPF,肺功能测试可以只露出一个严重降低弥散能力。HRCT将验证在肺这两个进程并存。
UIP的组织学确诊需要手术活检通过开胸(开放肺活检)或胸腔镜。近年来,电视胸腔镜(VATS)活检实际上已经取代开胸肺活检的患者评价与间质性肺病4,86。以这种方式获得足够的和有代表性的肺组织将提供有关潜在病理病变的性质和疾病的活动信息。然而,这是有争议的,因为与疑似IPF每一位患者是否应进行外科肺活检。在由英国胸科协会的报告显示,只有12%的患者诊断为IPF过外科肺活检,而IPF患者伯纳利欧县的一项调查显示,美国新墨西哥州,结果表明11%的外科肺活检在初步诊断的时间69,70。因此,很明显,IPF的诊断在临床上是不需要手术肺活检的。活检确诊率低,部分反映了对现有治疗方法的失望。
在患者怀疑IPF可以以不含肉芽肿过程,如结节病和过敏性肺炎,淋巴管炎癌病或淋巴瘤,感染,并具有可在一个小的被识别诊断或特性的组织病理学特征的其他的ILD帮助肺的支气管镜(支气管)活检活检标本35. 然而,在支气管镜活检标本上发现间质炎症和纤维化是非特异性的,在诊断或排除UIP方面是不可靠的87。
IPF患者的主要治疗方法是皮质类固醇治疗,但疗效尚未得到证实35,88。大多数对IPF治疗的研究已经追溯,非对照试验35,88。此外,只有少数研究确定适当的底层组织学病变患者的IPF9,35。卡林顿等。10在没有他们的53例UIP的注意自发改善,只有11.5%的患者对激素治疗反应良好。大多数患者诊断为IPF,有或没有治疗疾病的经验进展,导致肺心病和呼吸衰竭10,35,89。近年来,出现了在抗纤维化治疗越来越多的关注与代理商,如秋水仙碱和吡非尼酮35,90,91。肺移植,则应及早考虑,因为对于肺移植的等待时间可能是1-2岁92。
吸烟与肺纤维化之间的关系一直怀疑多年93。当前或先前吸烟者串联IPF的患病率的变化取决于在识别IPF情况下使用的情况下定义及已经从41-83%不等10,69,74-77,94,95。在一些研究中,并没有要求IPF由外科肺活检诊断的确认70,74,94。鲍姆加特纳等。94发现吸烟史与IPF发病风险增加相关,比值比为1.6。在他们的报告中,手术肺活检标本的切片可用于不到一半的研究对象的复查94。
肺纤维化和肺癌风险之间的关系一直争论不休96。哈伯德等。97最近描述了一个基于人群的队列研究中,肺癌的发病率在患者增加与IPF,独立的吸烟效果。总的来说,然而,证据是相互矛盾的关于这点和需要进一步研究96。
结论
吸烟对肺间质性疾病的影响尚不清楚。由于这些肺间质疾病的罕见性,很难确定吸烟在这些疾病的发病机制中的直接致病作用。尽管如此,现有的流行病学数据表明,吸烟与某些间质性肺部疾病的发展有因果关系,包括RBILD、DIP和PLCH(表2)。吸烟者的优势一直被观察到在报告的病例系列患者这些疾病。在这些患者中,戒烟可能是最重要和有效的治疗选择,应大力鼓励。这些病变也被视为偶然发现吸烟者尸检33,98。吸烟在RBILD、DIP和PLCH发病机制中的直接作用进一步被放射学和临床改善所证实,这些改善有时发生在戒烟之后。常见的因果关系也表明,存在这些联合病变的一些受影响的吸烟者。作者观察了三种病变同时存在的病例(图1)⇑)。
吸烟在IPF发病机制中的作用存在争议。吸烟似乎会增加IPF发展的风险,但没有令人信服的证据表明吸烟本身直接导致IPF的发展。
呼吸性细支气管炎相关性间质性肺病、脱屑性间质性肺炎和肺兰格罕氏细胞组织细胞增生症与其他形式的特发性间质性肺炎,特别是特发性肺纤维化之间的区别具有重要的临床意义。一般来说,呼吸性细支气管炎相关性肺间质性疾病、脱屑性肺间质性肺炎和肺兰格罕氏细胞组织细胞增生症的预后明显好于特发性肺纤维化。特发性肺纤维化患者的中位生存期约为3年,而呼吸性细支气管炎相关肺间质性疾病、脱屑性肺间质性肺炎和肺兰格罕氏细胞组织细胞增生症患者大多在诊断后10年仍存活9,74。
- 收到2000年4月10日。
- 公认2000年8月18日。
- ©ERS期刊有限公司