文摘
哮喘是一种异构炎症气道疾病,白介素(IL) 1β被认为是一个关键的中介,特别是中性亚型哮喘。代活跃IL-1β需要蛋白水解乳沟通常通过形成介导caspase-1-containing inflammasome。本研究提出一个IL-1βendotype nucleotide-binding相关领域,富亮氨酸repeat-containing家族蛋白(NLRP) 3 /凋亡speck-like蛋白质包含caspase-recruitment域(ASC) / caspase-1 inflammasome是中性亚型患者哮喘的特征。
参与者与哮喘(n = 85)和健康对照组(n = 27)进行临床评估,肺量测定法和痰诱导。痰是微分处理细胞计数、基因表达和蛋白质介质。NLRP3和caspase-1表达也由免疫细胞化学。痰巨噬细胞分离(n = 8)和基因表达NLRP3 IL-1β确定。
NLRP3基因表达显著升高,caspase-1 caspase-4, caspase-5和IL-1β参与者,中性粒细胞哮喘。IL-1β蛋白质含量都明显高于那些与中性与痰引发哮喘和相关的水平。痰巨噬细胞、中性粒细胞哮喘痰中性粒细胞,表示NLRP3和caspase-1蛋白质。
NLRP3 inflammasome调节中性粒细胞哮喘和可能调节炎症过程中观察到通过生产IL-1β哮喘表型。
文摘
的NLRP3 inflammasome可能是一个中性的关键调节器通过生产IL-1β在哮喘气道炎症http://ow.ly/t8HCe
介绍
哮喘是一种复杂的疾病与异构的炎症反应,可子类型基于痰粒细胞和辅助细胞因子反应(1,2]。这个炎症亚型已经有效地管理吸入激素治疗和减少嗜酸性哮喘急性加重。而导致哮喘的嗜酸性粒细胞的炎症反应的机制都进行了广泛的研究,对noneosinophilic哮喘,尤其是积累和响应性中性粒细胞的航空公司。哮喘的中性亚型已被确定在稳定的哮喘1),急性哮喘急性加重(3)和严重corticosteroid-dependent哮喘(4]。先天免疫系统的功能障碍的作用在中性粒细胞哮喘是提出,toll样受体(TLR) 2激活在哪里报道(5];然而,精确的和触发器机制尚不清楚。在转录组分析,我们确定了白介素(IL) 1受体和相关信号中间体是调节中性粒细胞哮喘(6]。然而,是否表达和成熟的通路,促进IL-1β改变在哮喘定义仍然不佳。
不成熟的合成pro-IL-1β被激活先天免疫受体诱导,如TLR和nucleotide-binding oligomerisation域(点头)同受体家族,这感觉守恒的微生物图案称为其分子模式。第二个信号诱导蛋白水解分裂所需的pro-IL-1β活跃,强有力的炎症。第二个信号可以通过形成multisubunit发生复杂的称为“inflammasome”,这是由炎性半胱天冬酶(s), nucleotide-binding域中,富亮氨酸repeat-containing家庭(NLR)蛋白质分子(NLRP)和适配器,ASC(凋亡speck-like蛋白质包含caspase-recruitment域)(7- - - - - -9]。成熟IL-1β然后激活促炎细胞因子il - 1受体诱导产生包括引发,在中性粒细胞哮喘(通常是高10]。
NLRP3, NLRP1 NLRC4和AIM2 inflammasomes黑色素瘤(缺席)都含有caspase-1,自身合成的一种活动形式。在小鼠,caspase-11 caspase-1激活至关重要11),这表明人类的小鼠caspase-11 orthologues, caspase-4和5,可能把inflammasome复杂调节caspase-1激活(9]。的NLRP3 inflammasome是最广泛的特征,人类和老鼠和新兴数据表明caspase-4/5 caspase-11,分别为NLRP3 inflammasome激活(12- - - - - -14]。在人类的航空公司,功能性NLRP3 inflammasome已被确定在气道上皮细胞15),外周血中性粒细胞表达所有组件的NLRP3 inflammasome,以及IL-1β[16];然而,没有数据报告的表达NLRP3 inflammasome组件在其他细胞在哮喘患者气道。大量的细菌病原体已被证明需要TLR2和inflammasome信号引起宿主的免疫反应(17- - - - - -19),虽然我们以前调查的表达TLR2在哮喘亚型,inflammasome-associated蛋白质的表达和IL-1β哮喘亚型是未知的。本研究提出一个IL-1βendotype与NLRP3 ASC / caspase-1 inflammasome或许构成了中性粒细胞炎症的表型观察患者的中性粒细胞哮喘。
方法
研究参与者
我们研究不吸烟的成年人患有哮喘(n = 85)从呼吸和睡眠医学约翰亨特医院门诊服务(新蓝白屯、澳大利亚)和健康对照组(n = 27)招收来自社区的广告。哮喘被定义为被诊断出的哮喘和历史证明气道代高渗盐水(挑衅剂量导致用力呼气量下降了15%在1 s (FEV1)< 15 L)和/或支气管扩张剂反应> 12%或> 200毫升。参与者给书面知情同意。猎人区卫生服务和纽卡斯尔大学的研究人类伦理委员会批准了这项研究。
研究设计
参与者参加了一次,症状,特异反应性,药物的使用和吸烟状况进行了评估,并进行了肺量测定法和痰诱导。痰液处理对炎症细胞计数,炎性蛋白的基因表达和评估上层清液和使用免疫细胞化学。吸烟的进一步细节评估、肺功能和痰处理在线提供的补充材料。
痰炎症亚型
参与者被归类为嗜酸性(痰痰中性粒细胞和嗜酸性粒细胞≥3% < 61%),中性粒细胞(痰中性粒细胞≥61%,痰液嗜酸性粒细胞< 3%)或paucigranulocytic哮喘痰(痰中性粒细胞< 61%,嗜酸性粒细胞(< 3%)20.]。只有三个参与者与混合粒细胞性炎症的哮喘(痰中性粒细胞≥61%,痰液嗜酸性粒细胞≥3%),这些都是不包括在分析由于小数字。
痰基因表达
提取RNA,反转录的互补和实时PCR进行如前所述[6]。结果计算使用2-ΔΔCt阈值周期(Ct)相对于内部两个管家基因(18 s核糖体RNA)和平均ΔCt健康对照组。
痰液浮在表面的中介评估
IL-1β,引发和嗜中性粒细胞弹性蛋白酶(NE)评估使用商业化验(研发系统,明尼阿波利斯,美国)。引发的优化痰报道之前(21]。没有观察到任何二硫苏糖醇的影响分析和恢复的IL-1β痰样品> 80%。
痰液免疫细胞化学
Cytospins被固定在PLP固定剂(3%多聚甲醛,l赖氨酸一水,钠m-periodate) [22),干和涂层在15%蔗糖之前存储在-20°C。解冻cytospins洗,permeabilised (0.1% Triton x - 100;Sigma-Aldrich,圣路易斯,密苏里州,美国)和阻塞(1.5%的牛血清白蛋白,1.5%的驴血清(Sigma-Aldrich), 0.1% Triton x - 100 / PBS)。主要抗体caspase-1 p10 (C-20)兔反多克隆(sc - 515;圣克鲁斯生物技术有限公司、圣克鲁斯、钙、美国),NE(克隆NP57)鼠标反单克隆(M0752;DakoCytomation、斯特鲁普、丹麦)和CIAS1 / NALP3山羊反多克隆(ab4207;Abcam plc。,Cambridge, UK) were added followed by secondary donkey Alexa Fluor® antibodies matched for species (Life Technologies, Carlsbad, CA, USA). Primary antibody incubation was performed at 4°C whilst secondary antibody incubations were performed at room temperature. Cells were mounted using ProLong Gold antifade reagent with 4,6-diamnio-2-phenylindole (DAPI) (Life Technologies) for nuclear detection and stored at 4°C protected from light. Slides were analysed on a Nikon Eclipse 90i Fluorescent Microscope and images were collected with NIS Elements software (Nikon Instruments Inc., Melville, NY, USA). Images were then merged using Image J (National Institutes of Health, Bethesda, MD, USA).
痰IL-1β免疫印迹
蛋白质评估进行解冻痰上层清液使用ProStain蛋白量化工具(活动主题Inc .,卡尔斯巴德、钙、美国)。唾液蛋白(5μg)与Laemmli混合样品缓冲(Bio-Rad实验室、大力神、钙、美国),煮10分钟前SDS PAGE分离在预制的聚丙烯酰胺凝胶(Mini-PROTEAN TGX kD没有污点凝胶;Bio-Rad实验室)。分离蛋白质被转移到聚乙二烯二氟化物(PVDF)膜(Immobilon-P膜、PVDF、0.45μm;美国马EMD密理博公司Billerica),阻塞(Tris-buffered脱脂奶粉5%生理盐水和渐变20 (TBS-T)缓冲区)和孵化隔夜anti-IL-1β抗体(ab2105;Abcam plc)。洗后,膜在anti-rabbit孵化免疫球蛋白结合辣根过氧化物酶(ab6721;Abcam plc)在室温下1 h。蛋白质乐队被发现使用西方SuperSignal毫微微最大灵敏度衬底试剂(热费希尔科学Inc .)、沃尔瑟姆,妈,美国)在ChemiDoc议员成像系统(Bio-Rad实验室)。
巨噬细胞与痰
痰巨噬细胞分离通过负选择使用磁性细胞分离与CD15微(Miltenyi研究,悉尼,澳大利亚),LS细胞分离列和VarioMACS系统根据制造商的指示(Miltenyi研究)。
分析
数据分析使用占据软件版本11(美国StataCorp,大学城,TX)。结果报告为±sd或中位数(四分位范围),除非另有指示。分析使用两个示例Wilcoxon的排名和测试,和克鲁斯卡尔-沃利斯检验被用于超过两组。确切概率法是用于分类数据。使用逐步回归进行了多元线性回归与显著性水平从模型中去除p = 0.100显著性水平的模型,p = 0.050。模型中的变量包括当p < 0.250在单变量回归;年龄和性别被迫到模型中。所有结果报告为显著p < 0.05, p < 0.008事后四组的测试分析。
结果
参与者与哮喘炎症亚型不同的相似的年龄,性别和FEV1%预测。那些noneosinophilic气道炎症(中性和paucigranulocytic)倾向于与吸烟久比老嗜酸性组(表1)。减少FEV1/用力肺活量%随着增加总细胞和巨噬细胞比例减少,观察中性粒细胞哮喘患者较其他三组(表1)。所有的参与者与哮喘痰样本的可行性(> 40%)。
Inflammasome组件
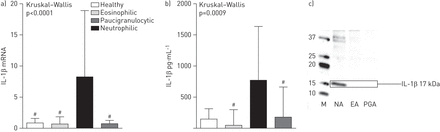
基因水平表达的组件NLRP3 inflammasome在中性粒细胞哮喘更高。具体来说,NLRP3表达明显高于中性粒细胞哮喘与嗜酸性和paucigranulocytic哮喘以及健康对照组(图1一个)。最高在中性粒细胞哮喘,ASC基因表达并不是不同组(图1 b)。为了进一步研究这个,然后我们比较了NLRP3 / ASC比率,发现这也显著升高与中性粒细胞哮喘与嗜酸性哮喘相比,paucigranulocytic哮喘和健康对照组(图1 c)。还存在基因表达的促炎、caspase-1 caspase-4和caspase-5显著升高的参与者与中性粒细胞哮喘(图1 d-f])。
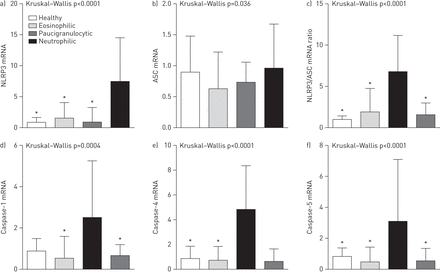
Nucleotide-binding域,富亮氨酸repeat-containing家族蛋白(NLRP) 3 b)凋亡和speck-like蛋白质包含caspase-recruitment域(ASC), c) NLRP3 / ASC比率,d) caspase-1, e) caspase-4和f)为健康对照组caspase-5基因表达,嗜酸性哮喘、中性粒细胞哮喘和paucigranulocytic哮喘。酒吧代表值和误差显示第三个四分位数。*:p < 0.05与中性。
IL-1βmRNA评估85年18名健康对照组和所有参与者患有哮喘,和IL-1β蛋白质含量测定在八个健康的控制,和75名参与者哮喘,由于有限的可用的痰上层清液量。IL-1β的基因表达和蛋白水平升高与中性粒细胞哮喘与嗜酸性哮喘相比,paucigranulocytic哮喘和健康对照组(图2一个和b)。然后,我们证实了成熟的存在形式的IL-1β上层清液的中性粒细胞哮喘患者使用免疫印迹(图2 c)。
)痰白介素(IL) 1β基因表达和b)痰IL-1β蛋白质含量为健康对照组,嗜酸性哮喘、中性粒细胞哮喘和paucigranulocytic哮喘。酒吧代表值和误差显示第三个四分位数。c)代表免疫印迹图像显示17-kDa成熟IL-1β观察中性粒细胞哮喘(NA)。M:分子量标记;EA:嗜酸性哮喘;PGA: paucigranulocytic哮喘。#:p < 0.008与中性。
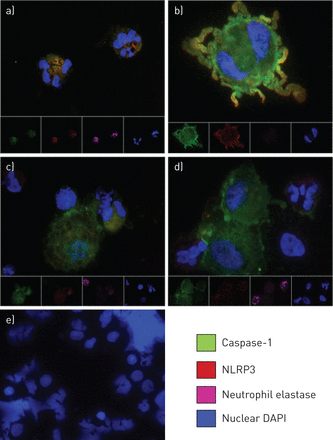
接下来,我们评估的表达NLRP3和caspase-1混合痰细胞利用免疫细胞化学。不被用来清楚地识别痰中性粒细胞嗜酸性粒细胞和巨噬细胞。NLRP3和caspase-1免疫反应性在痰从所有亚型的哮喘患者巨噬细胞(图3罪犯)。在中性粒细胞哮喘痰中性粒细胞NLRP3)阳性(图3),而caspase-1痰中性粒细胞的免疫反应性检测中性粒细胞和嗜酸性哮喘(图3 a和c)。
痰液免疫细胞化学图像。)从中性粒细胞哮喘患者痰中性粒细胞,b)痰中性粒细胞哮喘患者巨噬细胞,c)痰巨噬细胞和中性粒细胞嗜酸性的哮喘患者,和d)痰从paucigranulocytic哮喘患者巨噬细胞和嗜中性粒细胞。e)次级控制图像。NLRP: nucleotide-binding领域,富亮氨酸repeat-containing家庭蛋白质;6-diamino-2-phenylindole DAPI: 4。
Inflammasome基因表达在孤立的气道巨噬细胞
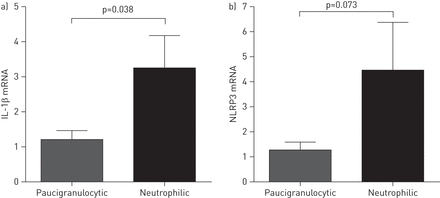
在样品的一个子集(三中性和五paucigranulocytic哮喘),痰巨噬细胞被孤立使用磁性细胞分离纯度> 90%。IL-1β的基因表达显著增加,NLRP3高隔离在中性粒细胞哮喘痰巨噬细胞(图4)。
基因表达的)白介素(IL) 1β和b) nucleotide-binding领域,富亮氨酸repeat-containing家族蛋白(NLRP) 3是孤立的痰里增加巨噬细胞与paucigranulocytic相比,中性粒细胞哮喘哮喘。
TLR和NOD2表达和中性粒细胞炎症介质
NOD2基因表达和TLR2在那些明显高于中性粒细胞哮喘,但是没有观察到病人组之间差异TLR4基因表达(表2)。水平与中性粒细胞炎症相关的介质(引发和NE)也有中性粒细胞哮喘最高(表2)。
哮喘患者协会inflammasome组件
利用逐步多元线性回归,NOD2基因表达,引发的中性粒细胞和蛋白质水平在哮喘痰NLRP3基因表达的重要预测因子校正了年龄和性别(表3)。模型包括69数据点和解释> 50%的变异NLRP3基因表达(p < 0.0001)。
此外,逐步回归模型显示,痰caspase-1 IL-1β和蛋白质的基因表达水平的引发严重的独立预测因子痰上层清液IL-1β水平在哮喘患者(表4)。模型包括69数据点和解释方差的42%痰IL-1β和非常显著(p < 0.0001)。散点图与IL-1βIL-1β基因表达和引发蛋白质蛋白质所示图5。
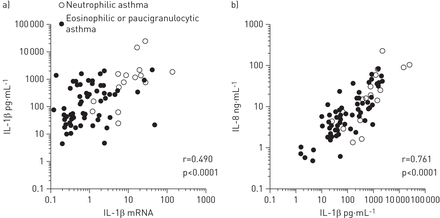
散点图的独立预测因子痰白介素(IL) 1β蛋白水平作为IL-1βmRNA和b)引发的蛋白质。
讨论
在这项研究中,我们已经表明,中性粒细胞哮喘患者增强表达的关键inflammasome组件和增加IL-1β蛋白质的释放。这是第一个研究涉及到inflammasome在中性粒细胞哮喘。NLRP3基因表达显著升高,caspase-1 IL-1β。此外,基因表达caspase-4和5在参与者与中性粒细胞哮喘也显著升高。痰上层清液IL-1β蛋白质含量都明显高于中性粒细胞哮喘哮喘与其他亚型和IL-1β的成熟形式被确定在中性粒细胞哮喘患者的痰上层清液。其他先天模式识别受体的表达,促进pro-IL-1β的合成信号(1),包括NOD2和TLR2,也显著升高患者痰液细胞中性粒细胞哮喘。蛋白质NLRP3和caspase-1表示在所有哮喘痰巨噬细胞亚型,但也有表达中性粒细胞哮喘患者的中性粒细胞。
兴趣NLRP inflammasomes近年来已经增加,但据悉inflammasome激活的角色在哮喘患者的气道,特别是那些有中性粒细胞哮喘没有被报道。我们理解inflammasome激活人类哮喘的作用是有限的少数研究使用临床样本。最近的一项研究显示,NLPR3 inflammasome介导的中性粒子引起的气道炎症50%切断空气动力学直径10µm [15),证明nonmicrobial触发器可以影响气道中性粒细胞的积累。感染等Chlamydophila肺炎也和呼吸道合胞体病毒(导致中性支气管炎)诱导NLRP3 inflammasome-mediated IL-1β释放(23,24]。最近的一项小型研究轻度哮喘患者(n = 7)曾正常肺功能显示从健康志愿者为ASC,降低基因表达caspase-1和IL-1β25]。一个可能的原因可能是少数研究和非常轻微的疾病的存在。我们的病人有中度到重度疾病(意味着FEV1%的预测是71.5%),中性粒细胞和嗜酸性粒细胞数量高出10倍比报告的B利克酒et al。(25),这表明更强烈和活跃的炎症过程正在发生。
除了caspase-1外,我们还观察到基因表达在中性粒细胞哮喘caspase-4和5明显升高而不是其他哮喘亚型。在老鼠身上,caspase-11(同源人类caspase-4和5)已被证明有助于NLRP3 / caspase-1-induced IL-1β分泌(14),而在人类,caspase-4已被证明与NLRP1和NLRP3 inflammasomes激活pro-caspase-1和pro-IL-1β12,26]。这些数据,再加上我们的基因表达增加caspase-4 caspase-5中性粒细胞哮喘,建议这些还在呼吸道疾病的重要作用。
Inflammasome形成可以被各种微生物和host-derived触发因素,包括尿酸晶体、石英和活性氧。触发器(s),导致NLRP3 inflammasome形成哮喘仍然是难以捉摸的。然而,我们之前报道增加了细菌殖民化中性粒细胞哮喘,以及8-isoprostane水平的增加,氧化应激的标记与痰中性粒细胞和细菌殖民化,表明活性氧和居民呼吸道致病菌都可能触发inflammasome的形成和随后的IL-1β生产(5,27]。
IL-1β是一个强有力的炎性细胞因子与许多慢性炎症性疾病,包括哮喘和慢性阻塞性肺疾病,我们最近报道基因的超表达il - 1通路中性亚型的哮喘(6]。扩展这个,我们发现浮在表面的水平和mRNA的表达IL-1β明显升高,中性粒细胞哮喘与其他哮喘亚型和健康对照组相比,表明一个关键的角色在中性IL-1β哮喘。痰IL-1β水平独立与中性粒细胞化学引诱物引发校正年龄后,性和中性粒细胞数量。我们的研究结果支持最新发现,这显示IL-1β增加哮喘,特别是在严重哮喘(28),特别是在中性严重哮喘29日),并提供证据的介入NLRP3 inflammasome。
NOD2基因表达水平和TLR2也显著升高患者痰液细胞中性粒细胞哮喘和免疫反应性的colocalisation NLRP3和caspase-1痰细胞(信号2),痰IL-1β水平升高,支持了NLRP3 inflammasome被激活的中性粒细胞哮喘。TLR2的激活或NOD2和随后NLRP3激活不不同的“多个支安打”假设最初提出的Pavordet al。(30.在严重的难治性哮喘,在多个点可能出现的刺激免疫系统,导致更严重的呼吸道疾病。
我们研究了痰液细胞表达NLRP3 caspase-1用免疫细胞化学和显示,从哮喘患者气道巨噬细胞,无论炎症亚型,对蛋白染色阳性。有趣的是,从中性粒细胞哮喘患者中性粒细胞(但不是其他表型)也为NLRP3和caspase-1彩色强烈。这表明,哮喘表型之间的差异在inflammasome激活可能是由嗜中性粒细胞和巨噬细胞的贡献inflammasome表达式。嗜中性粒细胞的重要性NLRP3 inflammasome最近所示ankan等。(16),显示功能NLRP3 inflammasome在中性粒细胞,而其他人则表明,遗传变异NLRP3导致延迟凋亡中性粒细胞,影响炎症的决议31日]。进一步的工作需要阐明的具体贡献的中性粒细胞inflammasome哮喘。
横断面的研究限制在允许原因和/或结果确定和进一步的研究是必要的建立。大部分的参与者在这个研究哮喘服用大剂量吸入糖皮质激素和,因此,不可能检查的影响,吸入糖皮质激素可能对先天免疫基因的表达在哮喘。然而,尽管频繁使用吸入糖皮质激素在所有亚型的哮喘,我们还观察到显著差异NLRP3受体表达之间哮喘表型。我们调查的表达NLRP3 inflammasome IL-1β使用痰诱导的非侵入性方法;然而,这项研究的结果并不代表那些气道组织,这是一个地区进行进一步的研究。
总之,我们已经表明的存在增加了基因表达的NLRP3 inflammasome在混合患者痰液细胞中性粒细胞哮喘和进一步证明NLRP3和caspase-1蛋白质在中性粒细胞哮喘痰巨噬细胞和中性粒细胞。Upregulation的NLRP3 inflammasome发生在哮喘和,特别是,在中性表型有证据表明两个或两个以上的天生的信号,包括NLRP3、TLR2和NOD2。痰IL-1β蛋白质含量分别与有关痰引发水平暗示与中性粒细胞招募和激活。
确认
作者要感谢m . Tooze的技术援助,c .加赛德n .贝尔h .烛台,n . Fibbens k .假货,b . Ridewood和r·奥尔德姆(部门呼吸和睡眠医学中心哮喘和呼吸道疾病和猎人医学研究所,学院健康、医学和公共卫生学院的纽卡斯尔大学的卡拉汉,澳大利亚)。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明:这项工作是支持的国家卫生和医学研究委员会(NHMRC)(澳大利亚堪培拉)项目资助(批准号631020)。辛普森和s·菲普斯。J.L.辛普森持有澳大利亚呼吸委员会安Woolcock研究奖学金。p·吉布森持有NHMRC从业者奖学金。
利益冲突:披露可以找到与本文的在线版本www.www.qdcxjkg.com
- 收到了2013年6月20日。
- 接受2013年9月9日。
- ©2014人队