文摘
在这个阶段2概念验证研究我们检查的安全性和有效性selexipag,可用一个口头,选择性环前列腺素受体(IP)受体激动剂,用于治疗肺动脉高压(PAH)。
43岁的成年患者症状多环芳烃(接收稳定内皮素受体拮抗剂和/或5型磷酸二酯酶抑制剂疗法)是随机三比一接收selexipag或安慰剂。从200年用量在200 -μg up-titrated增量μg每天两次在第一天35天的最大耐受剂量(每天两次800μg最大允许剂量)。肺血管阻力的变化在17周表示为一个百分比的基线值的主要疗效终点,每个协议,分析了设置,然后在所有治疗组评估结果的鲁棒性。
几何平均数的显著减少30.3% 17周的治疗后观察肺血管阻力与selexipag与安慰剂相比(95%置信区间-44.7 - -12.2;p = 0.0045, Wilcoxon等级和测试)。这是由类似的结果从所有治疗组。Selexipag是良好的耐受性和安全性符合预期的药理效应。
我们鼓励进一步的调查结果selexipag PAH的治疗。
肺动脉高压(PAH)是一种危及生命的疾病的定义的肺血管平均肺动脉压力升高静止≥25 mmHg和正常肺毛细血管楔压(≤15毫米汞柱)1,2)在正常或降低心输出量(1]。环前列腺素是前列腺素家族的一员,环前列腺素通路的失调与多环芳烃的发病机制和提供的理由使用环前列腺素类似物治疗(3- - - - - -6]。这些强有力的血管舒张和血小板聚集抑制剂7,8]也抵消了血管收缩剂,凝血活性的内皮素(9]。他们结合环前列腺素受体受体(IP), g蛋白耦合的血小板表面受体和血管平滑肌细胞(10]。受体的激活导致环腺苷酸的生产,导致血管平滑肌的松弛。
Epoprostenol内皮合成模拟管理持续静脉输注,是第一个目标PAH疗法批准,并改善患者的预后多环芳烃(11- - - - - -13]。然而,复杂的管理和潜在的严重副作用后急性和慢性政府严重限制其使用[3]。替代epoprostenol包括皮下注射treprostinil管理,也可用于静脉注射和吸入使用在美国,和。吸入性伊洛前列素虽然这些与epoprostenol前列腺素类地址的一些限制,他们也有缺点对频繁的剂量(iloprost),注射部位疼痛(皮下treprostinil)和典型prostanoid-associated副作用如头痛、冲洗、腹泻和下巴疼痛(4,5,14]。口服环前列腺素类似物在PAH的治疗将是一个重大的优势。然而,所有的研究到目前为止用口服环前列腺素类似物,如beraprost和口服treprostinil,未能显示持续治疗效果取决于主要疗效终点(14]。
Selexipag是一个口头,选择性IP受体激动剂。在肝微粒体迅速水解是一个活跃的代谢物(15]。Selexipag及其活性代谢物有更高的人类IP受体的亲和力比任何其他前列腺素类受体(16]。的活性代谢物selexipag > 130倍的IP受体的亲和力高于前列腺素受体(16]。尽管selexipag及其代谢物的行为模式类似于内源性内皮(IP受体激动),它们的化学性质不同于环前列腺素与不同的药理学。因此,selexipag可能是一个有吸引力的口服替代现有环前列腺素类似物治疗的多环芳烃。目前的概念验证研究旨在评估疗效,安全性和耐受性selexipag成人患者的症状多环芳烃。
方法
病人
这是一个多中心、跨国概念验证阶段2,随机、双盲、安慰剂对照、平行对照试验中17周的持续时间。
符合条件的患者包括男性或女性成年人(≥18岁)与PAH特发性或遗传起源,症状与结缔组织疾病(PAH-CTD),纠正先天性心脏病(先天性systemic-to-pulmonary分流手术修复≥5岁以前),或anorexigen使用。背景有针对性治疗内皮素受体拮抗剂(时代)和/或5型磷酸二酯酶抑制剂(PDE-5)强制性和病人不得不一直在稳定剂> 12周之前筛选。病人需要一个基线肺血管阻力(PVR) > 400达因·s·厘米−56分钟步行试验的测试,两个150 - 500米的包容性和在±15%。临床上患者被排除在外,如果他们有不稳定的右心衰在过去3个月内(世界卫生组织功能类(FC) IV),收到或原定于3个月内接受长期epoprostenol筛查,ventilation-perfusion肺扫描或肺动脉造影表明血栓栓塞疾病,心脏病证据的奔袭,30天内或收到任何试验药物的筛选。
研究伦理委员会批准的或研究中心和是根据赫尔辛基宣言的原则和良好的临床实践。所有患者参与研究之前给书面知情同意。
程序
随机调度3:1 (selexipag:安慰剂)是计算机生成的潘制药服务有限公司(美国卓德嘉,旗下英国)。符合条件的患者接受selexipag 200μg每天两次(由日本Shinkyaku合成有限公司,京都,日本)或匹配的安慰剂1天。剂量是400年然后up-titratedμg每天两次3天,7天,每天两次600μg 800天每天两次μg 21。慢up-titration时间表被允许到35天允许最大耐受剂量(MTD)。尽管剂量可以暂时减少了35天以后减轻不良事件,最后剂量需要稳定≥4周之前评估在17周。
这项研究是失明,调查人员评估不良事件之间的关系和研究治疗前的代码被打破了。急诊是破解密码的唯一理由。为每一个病人,治疗仍然蒙蔽星期17了,直到最终数据锁定。在17周数据是固定和锁定,病人有资格进入开放的扩展被选取。病人过早停止或者没有进入开放的扩展,研究治疗仍然蒙蔽,直到所有17周数据清洗和和解。
患者接受了右心catheterisation (RHC)在基线和17周(日112 - 126包容)。17周RHC血液动力学的评估进行了4 h post-dose。病人过早退出或不进入开放扩展随访30天内他们最后研究访问,在研究结束时,评估进行超声心动图,如果可能的话。
PVR 17周的变化表示为一个百分比的基线值被选中作为主要疗效终点和总结使用几何平均,其95%的两面信心(CL)的限制。从RHC获得额外的血液动力学的数据支持,数据从次要疗效端点,包括建立措施PAH患者的临床状态,如[6分钟步行距离11PAH,加重(定义为死亡、移植、住院由于不断恶化的多环芳烃,或多环芳烃症状加重,即。6分钟步行试验的距离≥10%恶化或需要额外的PAH-specific疗法),以及探索性端点,比如Borg呼吸困难评分,FC,氨基端血浆氨基末端前脑利钠肽(中位数水平以上病人)浓度(17,18]。
selexipag是评估的整体安全性和耐受性与治疗诱发的不良事件的频率和过早停止治疗,以及改变从基线到最后测量生命体征治疗期间,心电图和实验室参数。
统计分析
44名患者的样本容量的估计是基于的假设300达因·s·厘米−5差异意味着PVR的变化从基线到17周治疗组之间,300达因·s·厘米−5常见的标准偏差,一个3:1 (selexipag:安慰剂)随机比例。这样的样本容量将提供80%的电力检测区别selexipag基于双边未配对t检验和安慰剂在5%的显著性水平。
主要终点分析是基于每个协议(PP),由所有治疗的患者并没有违反协议的方式可能会影响药物的效果的评价研究主要终点。所有治疗的敏感性分析进行测试,包括所有病人收到至少一个剂量的药物研究。二、探索是基于所有治疗组疗效分析。
对每个分析集,缺失值在17周与最近的价值估算时间在治疗期间,除非病人死亡或有经验的疾病恶化;然后缺失值估算价值最差的17周对所有病人在分析集。Wilcoxon等级测试和渐近近似t分布(主要)和t(二级)用于治疗比较。安全性和耐受性评价进行了描述性的安全设置,包括所有病人收到至少一个剂量的研究药物和至少一个post-baseline安全评估。事后分析包括患病率治疗诱发的不良事件,不良事件的PAH背景治疗。
结果
病人的人口统计和处理
7点45病人筛选,43为中心在7个欧洲国家和随机接受selexipag 200μg每天两次(n = 33)或安慰剂(n = 10), 2008年4月至2009年6月(图S1)。40例完成了研究。数据来自29个病人selexipag组和6个病人安慰剂组页设置进行分析;每组4名患者违反主要入口准则。
治疗组平衡人口和目的(表1)和患者稳定背景PAH疗法(表2)。页设置,selexipag组中11例(37.9%)患者在时代和西地那非治疗的结合与一个(16.7%)病人在安慰剂组。
患者selexipag意味着±接受治疗sd143.3±28.6天(平均149.0天;范围17 - 176天),而135.1±27.4天(平均146.0天;范围61 - 152天)患者服用安慰剂。selexipag-treated患者中,14个(42.4%)在800年最后一次剂量的μg每日两次,七个(21.2%)在600年μg每天两次,6个(18.2%)在400年μg每天两次和4个(12.1%)在200年μg每天两次。MTD不能确定两个患者由于治疗过早停药。9个(90.0%)病人安慰剂达到MTD 800μg。
功效
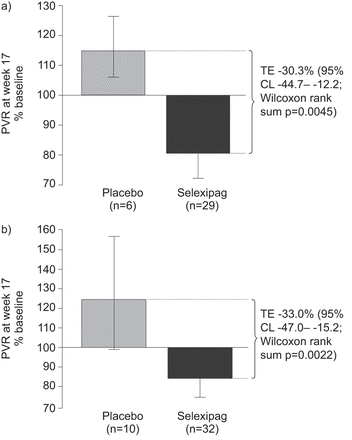
在17周,PVR(几何平均变化量表示为一个百分比的基线值,95%的CL) selexipag和安慰剂组为80.7% (72.8 - -89.6%;n = 29)和115.9% (106.5 - -126.1%;分别为n = 6) (图1一个)。这代表一个统计上显著的治疗效果为-30.3% (-44.7 - -12.2%;Wilcoxon秩和检验p = 0.0045)。所有治疗分析,包括所有43例随机在这项研究中,证实了PP分析(图1 b)。绝对值在基线,17岁,改变从基线到17周表S1 PVR在线提供了补充。与安慰剂相比,似乎selexipag治疗与心脏指数增加意味着伴随着意味着降低全身血管阻力(SVR),在收缩期或舒张期血压(几乎没有变化表3和4)。右心房压力的治疗效果出现被减少的安慰剂在基线值(表3)。在17周,平均(95% CL) 6分钟步行试验的距离基线的改变是+ 24.7(-1.6 - -50.9)米和0.4 +(-19.7 - -20.5)米selexipag和安慰剂组,分别为(图2)。
改变肺血管阻力(PVR)从基线到17周。)/协议组和b)所有治疗组。数据提出了手段和误差代表95%置信区间(CL)。基线PVR值(意味着±sd)为每协议人口selexipag分别为951.9±434.5达因·s·厘米−5和安慰剂分别为826.8±195.8达因·s·厘米−5。基线PVR值(意味着±sd)的所有治疗人口selexipag分别为948.6±428.0达因·s·厘米−5和安慰剂分别为867.2±379.38达因·s·厘米−5。TE:治疗效果。
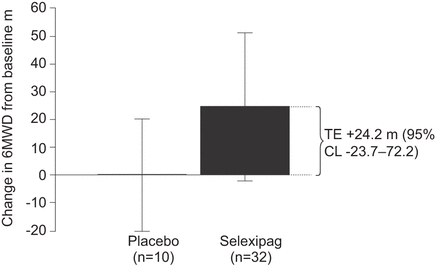
6分钟步行试验的距离变化量(6随钻测量)从基线到17周(所有治疗的人口)。基线值(意味着±sdselexipag是394.7±72.0米)和安慰剂分别为350.3±123.5 m。17周值(意味着±sdselexipag是419.3±106.3米)和安慰剂分别为350.7±139.6 m。TE:治疗效果;CL:置信区间。
一个病人(3.0%)selexipag-treated和两个(20.0%)接受安慰剂的患者多环芳烃的恶化。5 (15.6%)selexipag-treated FC患者改善,相比之下,一个(10.0%)安慰剂收件人。每组两个病人经历了FC的恶化。没有区别治疗对Borg呼吸困难评分(CL平均处理效应-0.1单位,95% -1.4 - -1.1)或等离子体中位数水平以上病人(平均处理效应-212.8 pg·毫升−1,95% CL -1012。1 - 586.5 pg·mL−1)。
安全
几乎所有病人在两个治疗组经历过至少一次不良事件,头痛,下巴疼痛,肢体疼痛,恶心,最频繁的报道和鼻咽炎selexipag组(表5)。大多数selexipag组的不良事件被归类为轻度(n = 5;15.2%)或中度(n = 20;60.6%)。六名(18.2%)患者selexipag组和四个(40.0%),安慰剂组至少经历了一次严重不良事件(在线补充表S2)。严重不良事件被研究者认为是至少可能相关selexipag治疗包括头痛、恶心、呕吐、肌痛,呼吸困难,胸痛。没有安慰剂被认为是事件与研究药物有关。没有人死亡。事后分析表明,在治疗组不良事件没有区别当分层背景治疗,即。时代PDE-5抑制剂单一疗法或时代+ PDE-5抑制剂联合治疗。患病率与环前列腺素类似物治疗相关的不良事件,例如头痛、肢体疼痛,下巴疼痛,恶心和腹泻,减少患者在selexipag(在线补充表S3)。没有临床相关的生命体征的变化从基线到17周,包括血压、脉搏,心电图参数,包括QT间隔变化,和实验室测试,观察。
讨论
这个概念验证阶段2的研究设计提供初步证据的有效性和耐受性selexipag PAH患者。研究显示显著减少30.3% PVR后17周的selexipag治疗,而安慰剂。PVR曾被用作治疗效益的指标(19),可能与多环芳烃的长期结果(12,13]。此外,显著减少PVR和epoprostenol已报告,prostacylin的合成形式(20.]。改善其他血流动力学参数,如增加心脏指数和SVR减少,也可能被解释成常IP受体激动的效果。然而,SVR的减少并不伴有全身性低血压。的有利影响selexipag观察一个时代尽管患者接受背景治疗和/或西地那非,大约三分之一的患者在两者的结合。PAH患者通常需要一个以上的治疗,因为临床恶化或未能达到指定的治疗目标。附加或与药物联合治疗的功效不同的形式,如时代和PDE-5抑制剂,评估和建议在当前治疗指南(1]。
统计上显著的治疗效果并没有观察到6分钟步行试验的距离的二次参数或中位数水平以上病人的探索性参数。鉴于这项研究没有动力来检测这些参数的差异,这不是一个完全意想不到的结果。placebo-corrected意味着治疗效果的大小6分钟步行试验的距离+ 24.2米的类似于第二阶段获得24周的概念验证研究伊马替尼(+ 21.7)21]。为这个参数统计学意义并不在这个试验。在我们的研究中,病人背景PAH治疗伊马替尼的审判,这可能导致缺乏6分钟步行试验的距离有明显改善。关于中位数水平以上病人,安慰剂,selexipag-treated患者基线区别。加之大标准差的意思是基线研究结束,意味着它是不可能治疗的差异在我们的研究中观察到。
17周的治疗selexipag被大多数患者耐受良好。不良事件符合已知的副作用的IP受体激动和本质上类似这些报道的12周试验口服环前列腺素beraprost [22]。有明显减少不良事件的发生率在维护阶段的beraprost研究与滴定阶段。同样的,事后selexipag数据的分析表明,一些不良事件的发生率,如头痛、下巴疼痛,疼痛的肢体和冲洗,随时间减少。很可能他们快速up-titration MTD有关。up-titration协议相对激进的和病人可能仍住院1星期后第一个剂量。因此,63.6%的selexipag-treated患者取得了最后的最佳剂量的600μg每日两次或更高。然而,较长的up-titration阶段可以允许更多的患者达到最高的剂量研究(800每天两次μg),甚至可能更高的剂量。
3:1随机比例,加上小样本量,可能导致失衡之间疾病的治疗组在对一些特征比如FC, 6分钟步行距离和中位数水平以上病人,建议服用安慰剂的病人病情恶化比活跃群体。此外,人民党分析导致一个活跃的药物安慰剂5:1的比例,有四个病人在每个治疗手臂排除由于重大违反协议。这确实限制这项研究的结果的概括。即便如此,PP的治疗效果在PVR是一致的分析和所有治疗敏感性分析,其中包括所有43随机患者。也有积极的趋势的一些次要结果措施,我们考虑足够的概念验证研究一种罕见的和致命的疾病来支持持续调查selexipag大规模研究。我们的研究缺乏超越一个预先确定的潜在最大剂量的selexipag 800μg每天两次。然而,更高的剂量selexipag正在调查目前正在进行第三阶段的研究。
Selexipag是一个口头,选择性IP受体激动剂有可能解决一些相关的药代动力学和安全限制环前列腺素类似物。selexipag的活性代谢物的相对较长的消除半衰期为7.9 h,允许每天定量和对比环前列腺素类似物,需要连续或非常频繁的剂量达到持续反应(16,23]。不良事件相关环前列腺素类似物通常是由于突然改变等离子体水平的药物。作为selexipag迅速水解活性代谢物在肝脏,peak-trough血清水平的活性化合物的波动可能会减少,从而减少不良事件的可能性(16]。此外,连续接触引起的血管舒张selexipag被重复剂量不减,这表明严重的脱敏的IP受体不太可能16]。因此,可能会有少剂量升级需要维持疗效。
总之,这个概念验证研究表明,治疗selexipag导致显著降低30.3% PVR 17周后,这是由心脏指数的增加和减少SVR没有全身性低血压。Selexipag是耐受性良好,安全性符合预期的药理作用。总的来说,这项研究的结果进一步鼓励调查selexipag的多环芳烃。
确认
我们感激地承认所有人员参与本研究。作者感谢l·托马斯(英国元素沟通,Westerham)写作提供医疗援助。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
临床试验
本研究在clinicaltrials.gov注册标识号NCT00993408。
感兴趣的语句
语句对g . Simonneau a . Torbicki M.M. Hoeper, m . Delcroix k . Karlocai n . Galie m . Kurzyna m . Efficace r . Giorgino和贝聿铭朗,研究本身可以找到www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2011年8月11日。
- 接受2012年1月11日。
- ©2012人队