摘要
肺血管床是许多血管活性因子的来源和靶点。在肺血管内稳态最重要的因素是利用环鸟苷单磷酸(cGMP)作为细胞内第二信使。这些包括一氧化氮和利钠肽家族(心房型、脑型和c型利钠肽)。在寻找利用cGMP信号通路治疗肺动脉高压(PAH)的治疗策略中,磷酸二酯酶5 (PDE5)靶向化合物对cGMP代谢的抑制被证明是迄今为止最成功的。PDE5抑制剂西地那非(sildenafil)已被证明可以改善PAH患者的肺血流动力学和运动能力,目前已被批准为一种治疗方法。其他公司正在接受调查。
一个有趣的,但仍是试验性的观察是西地那非在不影响通气-灌注匹配的情况下降低肺血管阻力的潜力。另一个是肥厚的右心室中5型磷酸二酯酶的表达。这些数据表明,5型磷酸二酯酶抑制剂可能具有区别于其他肺动脉高压治疗方法的效果,值得进一步研究。
“肺动脉高压:实际管理的基本概念”系列
由M.M. Hoeper和A.T. Dinh-Xuan编辑
本系列的第4个
环鸟苷单磷酸信号通路
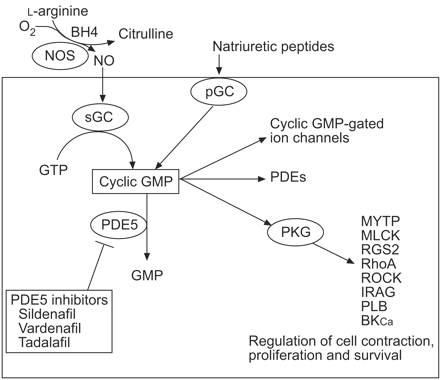
一氧化氮(NO)是一种高活性分子l-精氨酸的NO合成酶(NOS):内皮(eNOS),诱导(iNOS)和神经元。敲除小鼠的研究表明,eNOS衍生的NO是肺循环中内皮依赖性血管舒张的主要中介因子,但eNOS和iNOS都在慢性调节基底调中发挥作用1.NO扩散到血管平滑肌细胞,在那里它刺激可溶性鸟苷环化酶产生环鸟苷单磷酸(cGMP)(图1)⇓).
一氧化氮(NO) -环磷酸鸟苷(GMP)信号通路示意图。NO是由l-精氨酸的NO合成酶(NOS)和辅因子四氢生物terin (BH4)。在血管平滑肌细胞中,NO与可溶性鸟苷酰环化酶(sGC)相互作用,将鸟苷三磷酸(GTP)转化为环GMP,环GMP被磷酸二酯酶5 (PDE5)水解灭活。环GMP的功能包括调节阳离子通道和PDEs以及激活环GMP依赖性蛋白激酶(PKG)。PKG的激活导致了几个下游靶点的调控,包括肌凝蛋白磷酸酶靶向亚基(myypt),肌凝蛋白轻链激酶(MLCK), g蛋白信号(RGS)2, RhoA, Rho激酶(ROCK),肌醇1,4,5-三磷酸受体相关的PKG底物(IRAG),受磷蛋白(PLB)和钙敏感钾通道(BK)Ca).PGC:颗粒状鸟酰基环化酶。
利钠肽与特定的细胞膜受体相互作用2.利钠肽受体(NPR)的两种亚型,np - a和np - b,是跨膜鸟苷基环化酶(颗粒鸟苷基环化酶),其中细胞外结构域结合心房利钠肽(ANP)、脑利钠肽(BNP)或c型利钠肽,细胞内结构域水解鸟苷三磷酸(GTP)到cGMP。
越来越多的证据表明,cGMP在细胞内的分布不是均匀的,而是在细胞内分隔开的,这可能是可溶性和颗粒状鸟酰基环化酶产生的cGMP的不同作用的基础3..刺激心血管组织中cGMP产生的不同效果依赖于它与至少三组蛋白质的结合:cGMP依赖性蛋白激酶(或蛋白激酶- g;PKG)、cgmp调节的磷酸二酯酶(PDEs)和环核苷酸门控离子通道4.PKG是这些细胞内介质中最重要的,而cGMP调节的PDE5型(PDE5)主要负责调节细胞内cGMP水平和由NO和利钠肽产生的PKG依赖性信号5- - - - - -7.除了被PDE5水解外,cGMP及其下游介质PKG也调节该酶的活性。因此,ppg诱导的PDE5磷酸化增加了cGMP结合亲和力和水解能力8.cGMP与所谓的GAF-A (cGMP激活的PDEs,腺环酶和Fh1A)结构域的结合也促进了PDE5的磷酸化,增加了催化活性9,10.除了这些反馈机制,还有基因调控的潜力,因为人类PDE5的启动子区域包含对环核苷酸响应的位点11,12.
cGMP作为一种调节肺血管内稳态的药物
cGMP通路在调节肺血管张力方面的关键作用从该通路的药理学和遗传操作中可见一斑在体外而且在活的有机体内.例如,据报道,缺乏eNOS、GTP环酐酶-1(四氢生物terin合成中的速率限制酶,NO产生的辅助因子)或二甲精氨酸二甲氨基水解酶(负责代谢内源性NOS抑制剂的酶)的小鼠在正常含氧的大气中都表现出肺动脉高压(PH)13- - - - - -15而缺乏NPR-A的小鼠对缺氧表现出夸张的反应16.偶尔也有相互矛盾的报道17.显著地,抑制NO的产生在人类使用NG单甲-l-精氨酸,NOS的竞争性拮抗剂,导致肺血管阻力增加18,19.
除了调节肺血管张力外,cGMP水平也明显通过影响血管平滑肌增殖和存活直接影响肺血管结构。对培养的人肺远端血管平滑肌细胞的研究表明,通过刺激可溶性鸟苷酰环化酶或抑制其分解,提高cGMP可抑制血清刺激的增殖并促进凋亡20..
对人体的研究表明,PH值与内源性NO生成的减少有关。特发性肺动脉高压(IPAH)患者呼出气体中NO的测量值低于健康对照组21.人类肺样本的组织学检查显示,与健康肺相比,IPAH患者肺血管中eNOS的表达减少,尽管eNOS在丛状病变中表现良好22.在高海拔地区的研究表明,增加或维持肺中NO的生成对降低缺氧引起的PH值很重要;那些能力较差的人出现酸碱度的风险最大23.相反,在各种PH值下,循环ANP和BNP水平升高,这是右心室和心房压力过载刺激这些肽的合成和释放的结果24- - - - - -26.这是一种代偿性反应,试图通过减少肺血管阻力来减轻右心的负荷,但这种内源性反应的强度不足以抵消疾病过程。最后,非对称和对称二甲基精氨酸(已知是NOS的有效内源性抑制剂)水平的升高和分解代谢的降低可能导致肺血管紊乱患者的PH值升高27,28.
Pde在肺中的表达
共鉴定出11个PDE家族,它们在底物亲和性、选择性和调控机制上各不相同29.在这些酶中,PDE5、-6和-9对cGMP具有高度选择性,PDE1、-2和-11结合cGMP和环磷酸腺苷(cAMP)具有同等亲和力,PDE3和-10对cGMP敏感,但对cAMP有选择性。在肺循环中,PDE5和-1因其组织分布而备受关注。
PDE5 mRNA广泛表达于人体组织中,但在肺和肺血管平滑肌细胞中最为丰富30..已经鉴定出三种剪接变体(PDE5A1, PDE5A2和PDE5A3),它们编码的蛋白质具有类似的cGMP催化活性和对西地那非的敏感性,但n端序列不同,虽然PDE5A1和A2变体出现在大多数组织中,但最小的剪接变体PDE5A3的表达似乎仅限于平滑肌细胞31.对于PDE5的所有三种分子形式,已在肺匀浆和分离的肺血管平滑肌细胞中证明了免疫反应性6,31.PH患者肺组织中PDE5和α-平滑肌肌动蛋白(SMA)的表达高于对照组20..具体来说,主要98 kDa (PDE5A1)和77 kDa PDE5亚型的表达显著增加,PDE5免疫反应性与α-SMA共定位于内膜病变细胞和新肌肉化的远端血管,以及病变肺血管内侧层的平滑肌细胞。这些发现与高血压肺血管中PDE5表达和肌肉质量的增加一致,并提示PDE5可能是血管重构的标志,以及一个潜在的治疗靶点。
最近的一份报告证实了PH患者右心室中PDE5表达的诱导,从而扩展了这些发现32.PDE5在冠状动脉血管中正常表达,而在肌细胞中不表达。心肌压力过载导致心肌细胞中PDE5的表达。此外,研究在体外表明PDE5抑制增强了表达该酶的心肌的收缩力,提示PDE5抑制可能直接改善PH下的右功能。
正常情况下,PDE1在肺组织中表达量较低33.然而,最近的研究表明,这种酶在增殖的肺血管系统中显著上调,表明在疾病条件下具有致病作用33- - - - - -35.有趣的是,当分析PDE1在全肺组织匀浆中的表达时,PH没有显著增加与正常对照组织。然而,免疫组化和来自显微解剖组织的表达分析显示,PDE1A和PDE1C在毛细血管前肺动脉阻力血管中强烈上调33.在同一项研究中,8-甲氧基甲基3-异丁基-1-甲基黄嘌呤对PH动物模型中PDE1的抑制改善了血流动力学、右心肥厚和血管重构33.最后,pde1选择性抑制剂PI79抑制了增殖的人肺动脉平滑肌细胞的DNA合成。综上所述,这些发现表明PDE1C的上调在严重PH下的结构重构过程中发挥了作用,因此提供了一个新的治疗靶点。有趣的是,西地那非是经批准用于治疗肺动脉高压(PAH)的PDE5抑制剂,除了其PDE5抑制能力外,在临床相关剂量下也对PDE1有显著影响。
PDE5抑制剂
药理学
许多药物,包括双嘧达莫和茶碱,抑制PDE5作为其药理活性谱的一部分。三种选择性PDE5抑制剂西地那非、他达拉非和伐地那非已获准用于人类,并对其对肺循环的影响进行了研究。这些药物在化学结构上有显著差异,但均具有中等抑制浓度(IC)50)低纳米范围内的值:西地那非1-9纳米36- - - - - -39;他达拉菲1-7 nM37,39,40;伐地那非0.09-0.8 nM37,40- - - - - -42.西地那非、他达拉非和伐地那非对其他pde的影响见表1⇓.简而言之,西地那非抑制视网膜PDE6的浓度是PDE6浓度的10倍,对PDE1的选择性是PDE1的80倍。伐地那非也抑制PDE6(选择性相差4 - 25倍),但对其他pde无显著影响。他达拉非对PDE6影响不大,但对PDE11的抑制作用在IC上相差5倍50.与西地那非相比,他达拉非对PDE1c无影响。
选择性PDE5抑制剂的药代动力学
西地那非吸收迅速,单次口服剂量吸收可达95%,尽管由于第一次代谢,绝对生物利用度降低至40%43.达到最大浓度的时间(T马克斯)在血浆中减少约1小时,但如果与高脂肪餐一起服用,则进一步增加约60分钟,血浆浓度峰值下降29%(对曲线下面积没有影响)。这很可能是胃排空延迟的结果。考虑到IC,等离子半衰期为~ 4 h50PDE5的抑制作用在体外由于与母药的高蛋白结合,西地那非的血药浓度维持在IC以上50100mg剂量后持续12-18小时。清除的主要途径是肝脏代谢,正如预期的那样,相对亲脂性药物。主要的代谢物是N-desmethylsildenafil。这种代谢物具有与西地那非相同的PDE特异性,但约为其效力的一半,血浆水平为母体药物的约40-50%43,44.
对人类肝脏微粒体和表达单个人类细胞色素P (CYP)酶的微粒体的研究表明,75%的西地那非代谢是由于CYP3A4,其余CYP2C945- - - - - -47.这些研究预测了通过CYP3A4的显著药物-药物相互作用,这在实践中已经被发现。联合应用强效CYP3A4抑制剂如红霉素、酮康唑和沙奎那韦可显著提高西地那非的血浆峰值浓度和曲线下面积,而对血浆半衰期无影响;这与抑制系统前代谢而不影响消除是一致的。西他森坦是一种弱CYP3A4抑制剂在体外对西地那非水平影响不大。相反,与波生坦(一种CYP3A4诱变剂)联合治疗,波生坦治疗剂量显著降低血浆西地那非水平(降低~ 50%)。西地那非是几种主要药物代谢酶的弱抑制剂,但即使达到最大推荐剂量(100 mg),其血浆浓度也不太可能具有临床意义。尽管如此,通过CYP3A4代谢,与共服波生坦的竞争导致波生坦水平显著增加。由于药物清除率降低,老年患者(年龄为> ~ 65岁)和肝脏或严重肾损伤患者血浆西地那非水平轻度升高。
他达拉菲口服吸收很快马克斯在血浆中约2小时。生物利用度为36%,蛋白结合(主要是α1-酸糖蛋白和白蛋白)为94%,血浆半衰期为17.5 h。在2.5-20毫克的每日剂量范围内,全身暴露量呈线性增加,在稳定状态下(~ 5天),血浆水平比治疗开始时高出1.6倍。
他达拉非通过氧化代谢(主要是由CYP3A4)清除,生成儿茶酚,然后进行甲基化和葡萄糖醛酸化。邻苯二酚葡糖苷甲酯对PDE5的作用比母体分子弱13000倍。血浆tadalafil T马克斯肾功能衰竭的半衰期略有增加。主要代谢物通过肾脏排泄,在进行性肾损害患者的半衰期显著增加(健康时36小时,终末期疾病54-77小时)。CYP3A4抑制剂降低他达拉非清除率;例如,酮康唑治疗剂量使他达拉非曲线下面积增加了4.1倍,最大浓度(C马克斯)翻了1.2倍。研究在体外预测他达拉菲不会可逆地抑制其他药物代谢的主要人类cyp,但有潜力成为一个弱机制的抑制剂和CYP3A4的诱导剂。然而,在临床研究中,他达拉非10和20 mg对其他CYP3A4底物咪达唑仑和洛伐他汀的清除作用几乎没有影响48.
伐地那非被迅速吸收(T马克斯~ 40分钟)和代谢,血浆半衰期为~ 4小时,绝对生物利用度为14.5%(相比之下,西地那非和伐地那非为40%)。全身暴露在5-20毫克剂量范围内呈线性。一份高脂肪(55%脂肪卡路里)的早餐适度减少C马克斯延长了18%的T音马克斯而中等脂肪餐(30%脂肪热量)对伐地那非药代动力学没有显著影响。与其他选择性PDE5抑制剂一样,主要的代谢途径是通过包括CYP3A4在内的肝酶主要代谢物,anN-去乙基衍生物和其他少量代谢物主要通过胆道排泄去除。联合使用CYP3A4抑制剂,如利托那韦,可影响肝脏代谢。的N-去乙基衍生物对PDE5的抑制作用是其母化合物的四倍,对伐地那非的总疗效贡献约7%。
临床前研究
在离体的啮齿动物肺制剂中,PDE5抑制剂抑制对急性缺氧的升压反应和血栓素拮抗剂U4661949- - - - - -52.PDE5作为PH治疗靶点的进一步支持明显来自动物模型的慢性给药研究。最常用的是慢性缺氧诱导和野百合碱诱导的啮齿动物模型。这些研究表明,如果在暴露于缺氧或单野莨菪碱(预防策略)之前给予PDE5抑制,则可减弱肺动脉压升高和血管重构,如果在诱导PH值后2周内给予PDE5抑制,则可部分逆转病理(治疗策略)。53,54.右心室肥厚减轻,生存率提高。对转基因小鼠的研究表明,eNOS和利钠肽都有助于PDE5抑制的治疗效果16,52.
PDE5抑制也与其他治疗结合进行了检查。西地那非已与前列环素类似物贝拉前列素联合使用55.这两种药物分别口服或联合灌胃,每日两次,持续3周,从给药时间开始。两种药物都能减弱PAH的发展,但两种药物联合使用对血浆cAMP和cGMP、肺血流动力学和血管重构有附加作用。在一项关于生存影响的研究中,联合治疗再次显得更优越,6周生存率为100%,相比之下,单百合碱治疗的生存率为30%,单百合碱联合西地那非治疗的生存率为90%,单百合碱联合培拉前列素治疗的生存率为80%。据报道,西地那非和波生坦联合使用在单野百合碱治疗的大鼠模型中优于任何一种治疗56.
选择性pde5抑制剂的临床药理学
与PDE5的血管分布一致,全身给药PDE5抑制剂对心血管系统产生可测量的影响,同时增加血浆和尿cGMP水平。
对健康男性的研究表明,单剂量100-200毫克的西地那非可适度降低收缩压和舒张压;收缩压/舒张压在3小时时的平均最大下降为10/7 mmHg, 6小时时恢复到基线水平,无剂量-反应关系57.没有伴随心率或心脏指数的变化。曲线下血浆cGMP面积较基线增加了约50%。有报道称,男性勃起功能障碍患者使用伐地那非可降低平均收缩压1.4 - 6.6 mmHg和平均舒张压2 - 4.8 mmHg58.在一项针对勃起功能障碍男性的交叉研究中,西地那非50mg和伐地那非10mg均能显著降低全身血压。使用伐地那非的反应有更大的可变性,有3名患者报告在第一次剂量后昏厥59.在服用他达拉非20mg的健康志愿者或年龄为> ~ 45岁、勃起功能障碍的男性患者中,观察到系统血压几乎没有变化,每日治疗26周60.与其他血管扩张剂(特别是硝酸盐,但也包括多沙唑嗪)联合治疗可进一步降低血压60,61.硝酸盐的作用很可能是通过增强NO-cGMP途径介导的60,61.
在稳定缺血性心脏病患者中,静注西地那非(最高40 mg / 60分钟)可使静息时右心房压、肺动脉闭塞压和收缩压、舒张压系统动脉压略有降低,但心率无变化57.与基线相比的百分比变化是:右心房压-28%,肺动脉压-27%,肺动脉闭塞压-20%,收缩期全身动脉压-6%,舒张期全身动脉压-10%。心排血量较基线也有轻微(7%)降低。在男性缺血性心脏病患者中,2 h (即。在T马克斯)在单次口服剂量(5或10毫克)他达拉菲后60.
在西地那非输注后进行的运动测试中(超过60分钟可达40毫克),最大肺动脉闭塞压和平均肺动脉压分别比输注前的运动测量值降低了23和19%。收缩压和舒张压均降低6%,心排血量降低11%,心率不受西地那非治疗影响。在类似的患者群体中,伐地那非10mg和他达拉非10mg没有改变跑步机运动时间或第一次意识到心绞痛的时间,也没有改变达到的血压或心率62,63.
单剂量50mg口服西地那非已被报道可预防健康志愿者缺血和再灌注引起的内皮功能障碍64还有慢性心力衰竭的病人65,66,当使用流量介导的扩张协议测量时。据报道,在心血管风险增加的男性患者(10年心血管风险>20%)中,交替服用20 mg他达拉非,持续4周,可改善内皮功能。67.西地那非的作用被格列苯脲阻断,提示西地那非的作用是打开三磷酸腺苷敏感钾通道的结果64.
单次口服治疗和超治疗剂量西地那非(50和400 mg)和伐地那非(10和80 mg)对校正心率的Q-T间期(QT)的影响c)已经在一项针对健康男性的精心设计的研究中得到了检验68.安慰剂校正后QT平均变化c采用两种方法进行计算。平均(范围)弗里德里克校正QTc剂量后1小时的持续时间为伐地那非10mg为8 (6 - 9)ms,西地那非50mg为6 (5-8)ms。个性化QTc结果显示相似的趋势:伐地那非10 mg为4 (3-6)ms,西地那非50 mg为4 (2-5)ms。在较高的剂量下,QT间期有小的增加,但剂量-反应关系很浅,由此得出结论QT间期有小的增加c与这些PDE5抑制剂的临床意义不显著。
PDE5在血小板中含量丰富,抑制PDE5可减少血小板聚集69,70.西地那非的作用在较高剂量时可检测到。对健康志愿者富含血小板的血浆的研究发现,单次100mg口服剂量后,胶原蛋白对血小板聚集时间的反应在1小时后延长,但在4小时后没有延长71.而50毫克则没有效果。西地那非在两种剂量下都没有抑制二磷酸腺苷诱导的聚集。
对ph
典型的PH药理学研究,大多数研究涉及与结缔组织疾病相关的IPAH或PAH患者和世界卫生组织(WHO) III级。
急性影响
当单次口服剂量时,西地那非以剂量依赖性的方式降低肺血管阻力72.值得注意的是,与体循环相比,血管扩张剂效应在肺循环中最为明显,至少与临床相关剂量吸入NO一样强烈73,74.此外,西地那非增加和延长吸入伊洛前列素的作用72,75.
对西地那非、他达拉非和伐地那非急性反应的比较表明,每种药物都必须单独评估,尽管它们通常被分类为PDE5抑制剂76.总共有60名连续的PAH患者(纽约心脏协会功能分级II-IV)被分配口服西地那非50 mg (n = 19),伐地那非10 mg (n = 7)或20 mg (n = 9),或20 mg (n = 9), 40 mg (n = 8),或60 mg (n = 8)。在随后120分钟的观察期内评估血流动力学和氧合变化。所有三种PDE5抑制剂都引起了显著的肺血管舒张,在40-45分钟(伐地那非)、60分钟(西地那非)和75-90分钟(他达拉非)后效果最大。西地那非和他达拉非,而不是伐地那非,导致肺与全身血管阻力比显著降低。只用西地那非可显著改善动脉氧合(相当于吸入NO)。结论是,三种PDE5抑制剂在肺血管舒张动力学(作用最快的是伐地那非)、它们对肺循环的选择性(西地那非和他达拉非是选择性的,而伐地那非不是)以及它们对动脉氧合的影响(仅用西地那非改善)方面存在显著差异。在起草本综述时,一项评估他达拉非慢性治疗PAH患者效果的大型随机安慰剂对照试验刚刚完成招募(ClinicalTrials.gov IdentifierNCT00125918)77.
慢性治疗
一些小型单中心研究报告了长期使用西地那非治疗多环芳烃患者的有益效果78- - - - - -81(表2⇓3⇓和图4⇓).一项研究比较了西地那非治疗和波生坦治疗,以心脏磁共振为基础的测量右心室质量为终点80.两种处理之间无显著差异(表3⇓).在4个月的研究期间,两者都改善了6分钟的步行距离,但只有西地那非显著降低了右心室质量,该效果伴随着循环BNP水平的降低。这些数据是特别有趣的,鉴于最近的报告,诱导PDE5在PH下的右心室表达32西地那非可改善伴有继发性PH的心力衰竭患者的右心室功能82.
西地那非在PH中的标志性研究是西地那非在肺动脉高压中的使用(SUPER-1)研究81(表4⇑).这项研究检查了278例症状性多环芳烃患者,他们分别接受安慰剂或口服西地那非(20、40或80 mg)治疗t.i.d。),持续12周。主要终点是6分钟步行测试从基线到第12周的变化。与安慰剂治疗的患者相比,所有三个剂量的西地那非提高了运动能力(80 mg组在对安慰剂进行校正后达到50 m)、功能等级和血流动力学,药物耐受性非常好。在安慰剂对照期3个月后,继续接受开放标签治疗(80毫克)的患者保持6分钟步行距离的增加t.i.d。).根据这些数据,西地那非20毫克t.i.d。已于2005年获得美国食品和药物管理局和欧洲药品评估机构的批准,用于治疗多环芳烃患者。批准最低研究剂量是基于20-80 mg之间的剂量-效应关系(不显著)t.i.d。作为研究的主要终点。
只允许20毫克的决定t.i.d。PH的剂量给医生管理这些患者带来了一些困难。首先,与波生坦的相互作用意味着,联合使用西地那非的有效剂量减半,因此低于批准的治疗剂量。监管部门已经要求对使用10毫克低剂量的西地那非进行进一步研究t.i.d。和波生坦的联合研究。其次,许多医生认为,随着时间的推移,随着疾病的进展,西地那非的剂量需要增加,目标剂量为50 mgt.i.d。已经被提议83.为了支持这一点,80毫克t.i.d。剂量确实对肺血管阻力有较大影响81.此外,还有一个悬而未决的问题是是否t.i.d。需要给药。这是基于药物的血浆半衰期,但有证据表明,从一些临床和实验设置,西地那非的作用时间可能不能准确反映血浆水平84.细胞内磷酸化酶后,西地那非对PDE5亲和力的增加,以及西地那非从酶的缓慢解离率,可能有助于平剂量-效应关系40,85.显然,要确定PH患者的最佳剂量方案以及确定对生存率的影响,还有更多的工作要做。
建立西地那非与其他药物联合作用的研究是令人鼓舞的,但不是盲目的。西地那非与波生坦联合使用的频率越来越高,有报告显示有疗效(即。在短期内拯救患者免于恶化),尽管对药代动力学相互作用的担忧86,87.该联合用药可在不增加血浆波生坦水平而增加肝毒性的情况下使用。西地那非与西他森坦或氨布里森坦联合使用具有更可预测的药代动力学(因为没有显著的临床相互作用),但目前还没有这类联合药物的药动力学数据。临床上,西地那非与吸入性伊洛前列素急性联合使用72作为长期治疗88显示出有益的附加效应,而不增加任何一种药剂的副作用。在未来,PDE5抑制剂和增加cGMP生产的制剂的组合可能具有治疗上的优势73,74.
有趣的是,西地那非似乎对治疗伴有PH伴随的其他疾病的患者也有效。在患有hiv相关PH的患者中,西地那非可有效降低肺血管阻力89,90.最近的数据也表明,长期口服西地那非治疗对不能手术的慢性血栓栓塞性PH患者是有益的91,92.
HYPOXIA-ASSOCIATED PH值
有兴趣使用PDE5抑制剂治疗与缺氧相关的PH。一项早期研究表明,单剂量口服西地那非(50 mg)可抑制健康志愿者对缺氧(11%激发氧)的急性升压反应60.为了进一步解决这个问题,在高海拔地区进行了几项研究93- - - - - -95.
在一项这样的研究中,测量了14名健康的登山者和徒步旅行者在休息时和在循环能量测量法评估最大运动能力时的收缩压、心排血量和外周动脉氧饱和度,第一次是在低海拔地区呼吸含10%吸入氧的低氧气体混合物,第二次是在高海拔地区(珠穆朗玛峰大本营)。93.受试者分别服用西地那非50mg或安慰剂。西地那非治疗显著降低了两种情况下休息和运动时的肺动脉收缩压,同时增加了心排血量和最大负荷。
另一项研究比较了40毫克西地那非的效果t.i.d。12名受试者在4350米的地方接受6天的安慰剂治疗94.从海平面到高海拔6-8 h后开始治疗。治疗前,在高海拔地区,肺动脉收缩压(心电图测量)升高(+29%)与但在服用西地那非后恢复正常,而在安慰剂组中仍保持升高。在休息和运动时,服用西地那非的患者动脉氧张力较高,肺泡-动脉氧张力差较服用安慰剂的患者低,服用西地那非的患者最大耗氧量在海拔引起的下降较小。这些数据表明,西地那非可以防止高原诱发的PH值的发展,并改善气体交换,限制高原诱发的低氧血症和运动性能的下降。
一项研究检查了生活在吉尔吉斯共和国海拔2500米以上的PH患者服用西地那非的效果96.3个月时,患者服用西地那非25 mgt.i.d。在给药间隔结束时,两组患者的平均肺动脉压显著低于安慰剂组(低6.9 mmHg)。服用100毫克西地那非也有类似的效果t.i.d.两种剂量都缩短了6分钟步行距离,低剂量增加了45.4米,高剂量增加了40.0米。
从这些研究中推断PH与慢性阻塞性肺疾病(COPD)和间质纤维化相关的治疗是不恰当的。尽管如此,PDE5抑制剂在这些疾病的治疗中仍有应用兴趣。有肺部疾病时使用血管扩张剂的一个问题是通气-灌注的干扰(V' /问”)匹配。非特异性血管扩张剂可引起血管扩张,增加通气不良肺泡的灌注,从而降低动脉氧饱和度。有一些证据表明PDE5抑制剂可以保存V' /问的匹配97.肺泡氧合是局部NO产生(以及cGMP水平)的重要决定因素。肺通气不良区域的NO和cGMP水平较低,因此PDE5抑制的局部作用比通气良好的肺要小。在一项随机、对照、开放标签试验中,在16例继发于肺纤维化PH值的患者中,单剂量口服西地那非50 mg可降低肺血管阻力指数并改善V' /问’匹配,用多重惰性气体消除测量。分流流量和灌注低V' /问的区域在这种药剂下减少,导致部分动脉氧压显著增加97.
这些研究的结果刺激了进一步研究西地那非在慢性低氧性肺动脉高压伴COPD、间质性肺疾病和阻塞性睡眠呼吸暂停患者中的治疗潜力98- - - - - -102.事实上,最近的研究支持了有效治疗晚期COPD患者肺动脉高压的可能性102.基于慢性阻塞性肺病对公共健康的重大影响,有必要在这一领域进行进一步明确的研究。
结论
口服活性PDE5抑制剂的可用性为PH的治疗增加了另一个维度。西地那非的数据表明,在与结结组织疾病和高海拔生活相关的IPAH和PH患者的几个月时间里,临床血流动力学和运动能力有显著改善。证据基础表明,西地那非是世界卫生组织II类和III类IPAH患者的一线或二线治疗选择。它可能在治疗PH的其他表现和作为附加治疗中有作用,但who IV级的患者最好使用前列腺素。
值得注意的是,PDE5抑制可能在两个方面不同于其他可用的PH处理方法。其一是在不产生不良影响的情况下降低肺血管阻力的潜力V' /问’匹配,这一特性将有助于治疗与肺部疾病相关的PH值。第二个是在PH患者肥厚的右心室中发现PDE5。考虑到右心室功能作为PH患者预后的决定因素的重要性,对右心室的直接作用可以增强收缩力和心排血量,这是一个潜在的有价值的属性。
但是,必须注意避免对现有数据的过度解释。为了检验这些可能性,还需要进一步的研究,而且迫切需要更多关于西地那非长期生存的信息。最后需要提醒的是:鉴于5型磷酸二酯酶抑制剂对肺循环的急性作用存在差异,这可能与它们的磷酸二酯酶特异性有关,因此有必要仔细检查每种磷酸二酯酶5型抑制剂对慢性治疗的临床效果。
权益声明书
本研究所有作者的兴趣声明可以在www.www.qdcxjkg.com/misc/statements.shtml
脚注
本系列以前的文章:第一篇:内皮素受体拮抗剂在肺动脉高压中的作用。欧元呼吸2008;31日:407 - 415。2号: Gomberg-Maitland M, Olschewski H.前列环素治疗肺动脉高压的疗效观察。欧元呼吸2008;31日:891 - 901。3号: Behr J, Ryu JH。间质性肺病中的肺动脉高压。欧元呼吸2008;31日:1357 - 1367。
- 收到了2007年9月20日。
- 接受2008年3月10日。
- ©ERS期刊有限公司