文摘
治疗的临床效益和steroid-sparing效应与anti-immunoglobulin-E IgE抗体,omalizumab,评估患者的严重过敏性哮喘。
后试车期间,546年过敏性哮喘患者(年龄在12 - 76岁),症状虽然吸入糖皮质激素(500 - 1200年µg每日二丙酸倍氯米松),被随机分配接受双盲安慰剂或omalizumab每2或4周(根据体重和血清总IgE)皮下注射了7个月。一个常数倍氯米松剂量保持在16周stable-steroid阶段,逐步减少哮喘控制所需的最低剂量以下8周。后者剂量保持在接下来的4周。哮喘发作的主要变量表示。
omalizumab集团相比安慰剂组显示每个病人发作在stable-steroid阶段减少58% (p < 0.001)。在steroid-reduction阶段,加重omalizumab组减少了52%与安慰剂组(p < 0.001),尽管大omalizumab倍氯米松用量的减少(p < 0.001)。治疗omalizumab耐受性良好。不良事件的发生率在两组相似。
这些结果表明,omalizumab疗法安全改善哮喘控制仍在过敏性哮喘患者症状尽管经常使用吸入型皮质类固醇激素,同时减少皮质类固醇的要求。
这项研究是由诺华制药公司在瑞士巴塞尔和Genentech公司南部旧金山,加州,美国。
轻度和中度哮喘患者通常是由吸入型皮质类固醇激素和β控制2肾上腺素能受体受体激动剂1- - - - - -5但有些病人更难以管理,保持症状尽管高剂量吸入糖皮质激素和遭受频繁的发作4,5。这表明持续的气道炎症由于反应不足或可怜的符合规定的皮质类固醇疗法。
中央过敏性炎症的病理生理机制是释放大量炎性介质,如组胺、前列腺素、白细胞三烯,趋化因子和细胞因子,当过敏原结合免疫球蛋白e的(IgE)位于效应细胞的表面6- - - - - -10。所有年龄段的过敏性哮喘患者高于正常血清IgE水平和这些与支气管收缩的加剧对各种刺激的反应和症状的发生11- - - - - -14。ige炎症反应可能因此导致持久性过敏性哮喘患者的气道高反应性和症状。
在这种背景下,ige抗体的最新发展打开了一个有前途的方法来管理过敏哮喘和其他过敏性炎症性疾病15- - - - - -20.。使用这个代理可以显著降低血清浓度的免费IgE第一次注射后立即17和IgE封锁的结果在早期和晚期的衰减哮喘过敏原吸入反应,减少痰中嗜酸性粒细胞计数,降低气道高反应性,并在过敏性哮喘患者改善症状控制15- - - - - -17。支持这种方法的有效性的研究结果季节性过敏性鼻炎患者的临床疗效IgE抗体与无血清IgE浓度的降低有关19,20.。
Omalizumab (XolairTM),也称为rhuMAb-E25文学15- - - - - -20.是一个重组人源化单克隆抗体21承认在同一站点的高亲和性受体IgE IgE (FcεRI)22。它形成复合物与循环自由IgE的绑定,防止IgE高和低亲和力受体在细胞膜上。因此,它阻碍识别过敏原的效应细胞,如肥大细胞、嗜酸性粒细胞、巨噬细胞和树突细胞,抑制allergen-induced激活23- - - - - -25。cell-bound IgE抗体不绑定,因此,不触发细胞激活IgE交联的分子在细胞膜上。
当由静脉注射患者的严重过敏性哮喘17,这个代理是耐受性良好。它改善哮喘控制和生活质量与安慰剂相比,并允许显著减少吸入和口服皮质类固醇的剂量17。
本研究的目的是评估疗效,安全性和corticosteroid-sparing omalizumab皮下接种在过敏性哮喘的效果。
材料和方法
病人
合格的受试者患者年龄在12 - 75年诊断为哮喘的≥1年时间符合标准的标准的美国胸科学会(ATS)26和下面的附加条件:积极的至少一个的变应原皮试Dermatophagoides farinae,d . pteronyssinus猫或狗;血清总IgE水平≥30和⪕700国际单位(IU)·毫升−1和体重⪕150公斤允许omalizumab最佳剂量;一秒钟用力呼气容积(FEV基线1)支气管扩张剂≥40%,⪕≥80%的预测增加12% - 30分钟内吸入舒喘灵;平均每日症状总分≥3.0(最高9)在随机化前14天;吸入糖皮质激素治疗的剂量相当于500 - 1200µg二丙酸倍氯米松(BDP)≥3个月每天随机化前和使用β2肾上腺素能受体受体激动剂在需要或定期。哮喘是稳定的,没有重大变化在常规药物治疗和急性恶化需要额外皮质类固醇治疗≥1个月前检查访问。患者定期服用口服糖皮质激素并不包括在内。
研究机构审查委员会批准的协议是在每个站点,和所有的病人或他们的父母或监护人,在适当的时候,给书面知情同意。
研究设计
这是一个多中心、随机、双盲、安慰剂对照,与这些相应平行的组织学习。试车时间4 - 6周后,病人被随机分配接受安慰剂或omalizumab皮下注射了7个月。表将体重和总IgE筛选被用来确保omalizumab≥0.016毫克·公斤体重−1每总血清IgE·毫升的国际单位−1每4周(表1⇓)。病人需要150 - 300 mg omalizumab,政府每隔四周。450 - 750毫克omalizumab病人要求,每月剂量分为两个相等的部分管理间隔2周注射一次的数量降到最低,仍然保持足够的药物水平。
与舒喘灵救援药物的使用,由一个加压metered-dose吸入器(100µg /膨胀),被允许在整个研究。
在试车期间,所有患者转而使用的剂量吸入BDP是稳定的。这个剂量保持不变在第一次研究16周(stable-steroid阶段)。在接下来的12周(steroid-reduction阶段)所有的病人被认为每2周。和平民主党剂量降低了25%的基准剂量在每个访问8周,直到全部消除,或直到FEV下降1≥20%的最后测量相比前一阶段(上周stable-steroid的试车阶段)或一个事件定义哮喘恶化的发展如下所述。如果有FEV下降1≥20%,或发生哮喘恶化,前一剂量的BDP是恢复。哮喘控制所需的最低BDP剂量为其余4周举行。
无血清IgE水平测定在不同时间点之前和期间发表的方法治疗18。
结果测量
变量的主要功效是哮喘急性加重次数在stable-steroid阶段每个病人和steroid-reduction阶段的研究。
患者提供书面指示联系研究者如果有下列事件,表明哮喘恶化,发生:恶化的症状需要紧急或意外来访;最大呼气流量(PEF) < 50%的病人的个人最好成绩;清晨PEF下降≥20%≥2连续3天,相比前一阶段的最后一个星期(上周stable-steroid的试车阶段);≥50%增加救援药物≥2的连续3天,相比之前的最后一个星期的平均使用阶段,每天超过八泡芙的舒喘灵;≥2 3连续几晚觉醒由于哮喘症状需要救援药物。在恶化哮喘患者的评估和管理的急性发作,调查人员要坚持当前的指导方针1。
功效分析,哮喘恶化被定义为一个恶化的症状需要治疗系统性皮质类固醇或翻倍基线剂量的BDP试车期间决定的。
辅助变量的经历至少一个哮喘恶化的患者数量在stable-steroid和steroid-reduction阶段,减少百分之BDP剂量steroid-reduction阶段结束时作为一个连续变量和类别,舒喘灵救援使用哮喘症状评分、清晨PEF和FEV1%的预测。
哮喘的症状,清晨PEF和白天救援药物的病人,每天晚上记录在病人的日记。分制评分对患者使用他们的症状在白天,晚上,0表示没有症状,4表示静止呼吸问题与主要不适,白天有限的常规活动,激起了夜间症状尽管救援药物的使用。总分也计算日间和夜间分数之和+早上得分= 1或否= 0的症状在觉醒,最高得分为9。
生活质量评估作为额外的疗效变量,但由于空间限制,结果将另行公布。
统计分析
统计分析使用所有随机患者(intent-to-treat人口)。哮喘发作的数量每个病人和病人的数量至少经历一个哮喘恶化分析在每个阶段使用广义Cochran-Mantel-Haenszel测试(van Elteren测试)分层定量计划(2或4周剂量)。一个先天的调整是为病人过早停止阶段添加1恶化每2周内(错过治疗阶段)任何观察哮喘恶化计数的阶段。患者中断stable-steroid阶段包含在steroid-reduction阶段,哮喘恶化数量作为steroid-reduction阶段内的最大观测+ 1。为了避免重复,哮喘发作不算作不良事件,除非他们住院(默认严重不良事件)引起的。
减少百分之BDP剂量和患者的比例减少了使用广义Cochran-Mantel-Haenszel BDP使用进行分析测试分层定量时间表。那些没有进入steroid-reduction阶段包括在分析BDP减少0%。
所有其他的疗效变量进行分析的广义Cochran-Mantel-Haenszel测试,Cochran-Mantel-Haenszel测试或协方差分析与基线值作为协变量,是适当的。在steroid-reduction阶段,这些变量进行分析事后。
这项研究是驱动显示不同数量的哮喘发作在这两个阶段,利用二项式近似正态分布。基于之前的研究结果17,是预期的68%,69%的病人安慰剂,80%和82%的患者omalizumab不会经历的哮喘恶化stable-steroid和steroid-reduction阶段,分别。为实现这一目标,550名患者被随机。这些计算是基于≥85%的力量和5%的显著性水平。
结果
病人
共有546名患者被随机分配:274 omalizumab和272年安慰剂。四百和八十七名患者完成了研究:255 232 omalizumab和安慰剂。
患者在安慰剂组的两倍(40 14.7%)omalizumab组(19 6.9%)过早地停止。19岁的病人停止omalizumab 13(4.7%)停止在stable-steroid阶段和6(2.2%)在steroid-reduction阶段,相对于27(9.9%)和13例(4.8%),由于安慰剂。14例(5.1%),安慰剂与三个病人(1.1%)omalizumab撤回了他们的同意。11个病人(三omalizumab和八安慰剂)停止,因为不满意治疗效果。没有病人omalizumab组由于不良事件退出与五个病人(1.8%),安慰剂组。
人口和基线特征的总结报告在表2⇓。治疗组平衡对人口统计数据。
无血清免疫球蛋白e的变化量
在omalizumab病人,在剂量方案,中间无血清IgE范围从145 - 1246 ng·毫升−1(60 - 515 IU·毫升−1在基线),17岁ng·毫升−1(5 - 7 IU·毫升−1)初始剂量stable-steroid阶段,年底和第12 - ng·毫升−1(5 - 8 IU·毫升−1)初始剂量在24周的治疗期。减少无血清IgE从基线治疗期间89 - 99%不等。
哮喘急性加重
分析每个病人的哮喘发作omalizumab intent-to-treat人群表现出显著差异和安慰剂的omalizumab stable-steroid和steroid-reduction阶段(p < 0.001)(表3所示⇓)。同样的分析进行了切除后患者主要的协议违反了相似的结果(数据没有显示)。
患者的比例至少经历一个恶化omalizumab组也显著低于安慰剂组为两阶段(p < 0.001)(表3所示⇑)。
大约80%的哮喘发作在两个治疗组与系统性皮质类固醇治疗。
二丙酸倍氯米松减少剂量和二丙酸倍氯米松撤军
在治疗期的结束,每分减少每日BDP剂量从起始剂量明显omalizumab组比安慰剂组(图1所示⇓)。规定的每日剂量steroid-reduction阶段结束时(对于那些患者达到治疗28周)omalizumab显著较低(中位数:100µg,四分位范围:0 - 400µg)比安慰剂(中位数:300µg,四分位范围:100 - 600µg) (p < 0.001)。
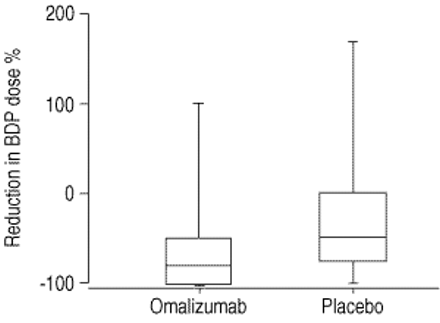
Box-and-whisker情节展示中位数和四分位范围和减少百分之最大和最小值的规定剂量吸入二丙酸倍氯米松(BDP) steroid-reduction阶段的末尾(星期28)相比stable-steroid阶段。Intent-to-treat人口。p < 0.001。
患者的比例能够降低BDP剂量steroid-reduction时期结束时相比stable-steroid阶段omalizumab组明显高于安慰剂组(p < 0.001)。患者的比例能够降低BDP omalizumab≥50% 79%和55%剂量安慰剂。此外,43%的病人在omalizumab撤回BDP完全19%相比安慰剂。
症状评分和救援药物的使用
总哮喘症状评分中位数的两个阶段研究报告的处理如图2所示⇓。在统计上有显著差异的omalizumab被认为在整个stable-steroid阶段。症状的改善omalizumab组保存在steroid-reduction阶段尽管omalizumab BDP减少剂量越大。的有益作用omalizumab症状发生在夜间尤为明显(图3所示⇓)。
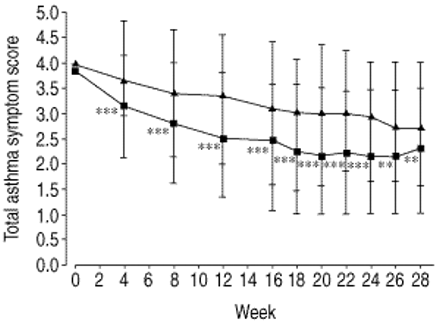
总在stable-steroid症状评分(周0-15)和steroid-reduction阶段15-28(周)。Intent-to-treat人口。数据值的白天分数,夜间早上分数和分数和四分位范围。▴:安慰剂;▪:omalizumab。* *:p⪕0.01与安慰剂;* * *:p⪕0.001与安慰剂。
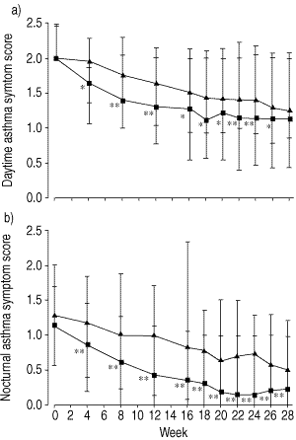
一)白天症状评分在stable-steroid(周0-15)和steroid-reduction阶段;在sable-steroid b)夜间症状评分和steroid-reduction阶段15-28(周)。Intent-to-treat人口。数据中位数和四分位范围。▴:安慰剂;▪:omalizumab。*:p < 0.05;* *:p < 0.01与安慰剂。
救援药物的平均数量的泡芙也omalizumab组低于安慰剂组在整个疗程(图4所示⇓)。支持omalizumab是显著的差异在stable-steroid阶段和在steroid-reduction阶段仍然重要,尽管omalizumab BDP用量显著减少。
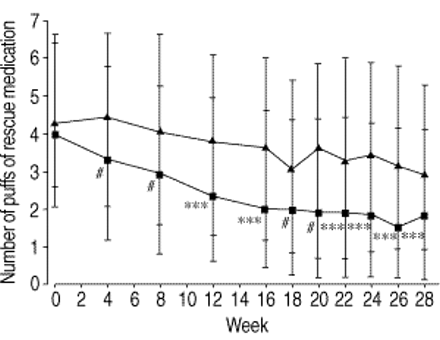
舒喘灵救援药物的泡芙stable-steroid期间每日(周0-15)和steroid-reduction阶段15-28(周)。Intent-to-treat人口。数据中位数和四分位范围。▴:安慰剂;▪:omalizumab。#:p < 0.005;* * *:p < 0.001与安慰剂。
早上呼气流量峰值,在一秒钟用力呼气量
分析意味着清晨PEF显示显著差异治疗支持omalizumab stable-steroid阶段的时间点。这种改善持续在steroid-reduction阶段(图5所示⇓)。
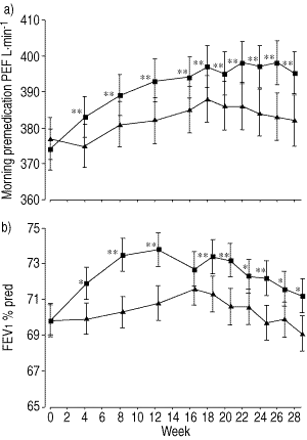
早上)最大呼气流量(PEF)值和b)在一秒用力呼气量(FEV1期间)值% pred stable-steroid 0-15(周)和steroid-reduction阶段15-28(周)。Intent-to-treat人口。数据意味着±se。▴:安慰剂;▪:omalizumab。*:p < 0.05;* *:p < 0.01与安慰剂。
FEV1omalizumab组显著优于安慰剂组的周4和12之间stable-steroid阶段(图5 b吗⇑)。在steroid-reduction阶段,意味着FEV1在omalizumab值显著高于安慰剂周18至28岁之间(图5 b⇑)。
安全性和耐受性
在这项研究中没有人死亡。9个(3.3%)病人omalizumab和三个(1.1%)病人安慰剂有严重不良事件,排除哮喘急性加重。这些在omalizumab外伤性手指截肢、抑郁、阑尾炎、流感样综合征,疑似颅骨嗜酸性肉芽肿,肠道绒毛状腺瘤发育不良,传染性单核细胞增多症,鳞状细胞癌的脸,左胳膊骨折。服用安慰剂的那一组心绞痛,心律加快,I型畸形。都不怀疑与毒品有关。6个病人(2.2%),安慰剂组omalizumab组中,没有经历过哮喘急性加重导致住院治疗。
5个(1.8%)患者安慰剂相比没有omalizumab过早撤回,因为不良事件。
1例轻度蛋白尿的患者接受omalizumab评估肾脏。肾活检分析显示只有次要的非特异性免疫复合物疾病的变化没有证据。蛋白尿的被认为是与高血压有关。
的总体发病率不良事件发生率在治疗组(p = 0.504)是整个涉嫌与毒品有关的不良事件的发生率(p = 0.183)。疲劳和感觉异常是最常见的怀疑与毒品有关的不良事件发生在1.1%的病人接受omalizumab和没有接受安慰剂。每组3例(1.1%)有疑似毒品头痛。注射部位局部症状与11.8%的omalizumab注射相比,7.7%的安慰剂注射。最常见的注射部位事件两组是艰难的。更频繁的在omalizumab发红的症状,温暖和瘙痒。大多数的这些事件是温和的严重程度。的七个经验丰富的荨麻疹患者在研究过程中,五个是接受安慰剂。这些事件严重。
没有病人omalizumab发达anti-omalizumab抗体。
讨论
变应性疾病的症状是由于炎症过程ige事件起到至关重要的作用6- - - - - -10。通过减少无血清IgE水平,omalizumab (rhuMAb-E25 XolairTM)提供了一个特定的方法来治疗这些疾病,无论涉及的过敏原。之前的研究在过敏性哮喘患者15,16表明omalizumab减少allergen-induced哮喘反应后期,嗜酸性粒细胞和痰气道高反应,表明该代理可能会有长期的抗炎效果。
在哮喘急性发作的临床表现疾病控制与一个强大的不足影响疾病发病率、死亡率、生活质量和总成本的疾病1,2,27。这个识别日益引起研究者选择恶化率作为主要结果测量指标在临床试验中评估新的抗哮喘药物的有效性28,29日。
结果随机、双盲、安慰剂对照研究表明,添加omalizumab在过敏性哮喘患者仍然不受控制,尽管常规吸入糖皮质激素治疗,同时减少哮喘急性加重和皮质类固醇需求同时提高疾病控制的其他参数。
每个病人减少了58%哮喘发作在stable-steroid阶段omalizumab组比安慰剂组。显著降低恶化率也观察到omalizumab组与安慰剂组相比在steroid-reduction阶段,与事件减少了52%,尽管大减少的BDP剂量和使用舒喘灵omalizumab救援药物的患者。
的steroid-reduction阶段3个月可能是太短充分观察哮喘恶化。然而,在研究皮质类固醇引起的哮喘发作,BDP的每日剂量降低了200µg每周间隔30.7之间,每个主题出现了恶化的症状和减少发生后26天的类固醇。此外,根据数据> 12000哮喘病人的回顾性研究31日每年,估计平均数量的哮喘发作严重哮喘患者(BTS治疗步骤3 - 5)是2 - 2.5每个病人31日。因此,经历了哮喘急性加重患者的平均数量在3个月的安慰剂steroid-reduction阶段(0.75)将高于预期类似的人口类似一段观察,虽然经历了哮喘急性加重患者的平均数量在同期omalizumab >低50%。
omalizumab治疗的好处是支持的证据,没有住院病人omalizumab组由于哮喘发作与6个病人安慰剂组。此外,取款的数目是双重的低omalizumab比安慰剂(19与40)。
有非凡能力的安慰剂治疗患者减少皮质类固醇剂量(50%)。这可能是由于过度BDP剂量在条目,但患者仍在这个剂量症状。或者,它可能是一种改进的表达符合BDP治疗造成频繁的评估由一个医生和鼓励遵守治疗方案在研究过程中。尽管这标志着安慰剂效应,减少BDP也显著大于omalizumab-treated患者(83%),和两倍多病人omalizumab组(43%),安慰剂组(19%)完全退出和平民主党。
其他次要疗效变量的结果反映哮喘控制的程度是一致的与主变量,包括症状评分、清晨PEF和FEV1期间,治疗差异总是赞成omalizumab stable-steroid和steroid-reduction阶段。
在清晨PEF和FEV绝对改进1观察omalizumab组相对较小。然而,患者加入这项研究已经接受抗炎治疗推荐当前慢性持续哮喘治疗的指导类似的严重性1,2。与抗炎作用的另一个代理,并不拥有支气管扩张剂属性,预计不会外提供大型气流阻塞的改善哮喘发作在这些情况下。
omalizumab的安全性是优秀的和治疗耐受性良好。没有与毒品有关的严重不良事件。
这项研究的结果证实和扩展这些报道在最初的试验调查omalizumab由静脉注射的功效17。皮下给药途径和给药时间提出本研究采用的是那些用于治疗,因此,结果更有实用意义。这项工作的其他原始方面包括的选择数量的减少主要终点(哮喘急性加重与改善哮喘症状评分),一个更大的和更均匀的哮喘病人与更广泛的年龄范围和较长时间的治疗阶段。
总之,这项研究表明,与omalizumab是有效和安全的治疗过敏性哮喘和提供了一个创新的解决方案来控制疾病,同时减少类固醇消费。其最佳的应用可能是在一种难治性疾病,患者的长期管理那些遭受持续症状尽管常规激素治疗,和那些需要高剂量吸入糖皮质激素或与使用相关的副作用。罕见的剂量的时间表可能大大提高遵守治疗过敏性哮喘病人需要复杂的治疗方案。此外,由于omalizumab是有效和安全的过敏性鼻炎的管理18,20.,病人患有两种情况下与此同时也可能从治疗中获益。
确认
以下调查,列出了国家,也造成病人数据:澳大利亚,r .鲁芬,r·西奇塔诺;奥地利、g . Kaik;德国,g . Kunkel c . Kroegel c。伯格曼,h . lein;意大利,G.W. Canonica、g D’amato g . Moscato e·马奇;荷兰,r . Aalbers J.P.H.M. Creemers, E.F. Dubois, a . Greefhorst P.B. Luursema, a口;南非,美联社Foden, j . Terblanche;英国,a·米勒,m . Spiteri a . Tattersfield f·钟;美国、g . Bensch t·萨莱·l·福特,a . Nayak h . Beede j . Yarbrough s费恩曼n .拉胡德G.G.夏皮罗,j·沃尔夫,e . Lisberg t·李,a·马丁h . Windom B.Q.拉尼尔,w·伯杰。诺华临床p . Rohane项目负责人。
- 收到了2000年10月26日。
- 接受2001年4月5日。
- ©人期刊有限公司














