文摘
检查是否丙酸(FP)剂量依赖性抑制炎症以及结构性变化,布朗挪威老鼠敏感卵白蛋白(OA)在0到7天。从天14-28,老鼠被暴露于aerosolised OA(1%)或磷酸缓冲盐每2天。三十分钟每个过敏原接触之前,动物被预处理与aerosolised安慰剂或FP(0.1, 1或10毫克)或强的松3毫克公斤−1i.p。
在29天,0.1毫克FP没有可衡量的影响,在炎症或结构变化,如杯状细胞增生和气道壁增厚。allergen-induced增加嗜酸性粒细胞的炎症反应在支气管肺泡灌洗液和呼吸道黏膜,以及增加纤连蛋白沉积,抑制了FP从1毫克的剂量开始治疗。杯状细胞增生和抑制气道壁增厚10毫克吸入FP要求。在这个剂量,观察系统性影响。然而,对于同等程度的系统性活动,强的松是更有效地防止气道变化。
所需的剂量吸入丙酸抑制allergen-induced结构性改变高于预防嗜酸性粒细胞涌入,并造成系统性副作用。然而,对于类似的系统性活动,强的松在预防气道重塑是无效的。
新泽西州Vanacker由FWO-Flanders资助(基金科研、弗兰德斯)。这项工作的部分支持由根特大学的共同研究项目(项目号果98 - 6)和由FWO-Flanders(项目没有。3 g006298)。
吸入激素(ICS)广泛用于治疗哮喘。近年来,它已成为越来越明显,他们是临床上非常有效的向上从最低有效剂量。关于他们对航空公司的影响,这些商业化剂量的剂量反应曲线是平的1。气道结构变化的影响,所谓的气道重塑,尚不明朗。这些变化包括杯状细胞增生(我们),平滑肌肥大增生、气道壁增厚和增加细胞外基质的沉积蛋白质存在即使在轻度哮喘患者2和在疾病过程的早期3,4。大多数5- - - - - -9,但不是全部10,11,活检研究显示效果有限的ICS在哮喘气道重塑,可能由于对生长因子表达的影响8或平衡矩阵metalloproteinase-9 metalloproteinase-1和组织抑制剂9。比较这些研究是受不同的类固醇使用,药物剂量或治疗持续时间。此外,这些研究不允许建立的影响类固醇的剂量反应关系结构与急性炎症变化。从有限的数据目前看来影响气道重构需要更高的剂量ICS比影响支气管嗜酸性粒细胞数。是et al。12表明减少(AHR)气道高反应,需要更高的剂量ICS比控制症状和肺功能基线。只有高剂量导致减少牙龈纤维化,而低剂量明显减少嗜酸性粒细胞数。在这个高剂量范围内,ICS已知一些系统性的活动。
直接比较试验,评估口腔的作用与吸入类固醇气道重塑指标,迄今为止尚未执行。因此,它是未知的系统性活动在多大程度上需要类固醇来影响这一现象。
作者以前所示的老鼠模型气道重构,10毫克的气溶胶丙酸(FP)完全阻止支气管旁的嗜酸性粒细胞的炎症反应,我们为了,上皮细胞增殖,增加纤连蛋白(FN)沉积在气道壁,部分抑制气道壁增厚的发展13。这个模型提供了机会比较FP的剂量反应曲线在不同的组织学方面allergen-induced气道变化。为了区分局部和全身吸入类固醇诱导的影响,作者还包括一组与强的松治疗,给系统。
方法
动物和研究设计
特定的无菌,男性布朗挪威大鼠(哈伦CPB泽斯特,荷兰)每组(n = 10)是敏感的i.p。注射在0和7天1毫克卵白蛋白(OA)(三级;西格玛化工有限公司,普尔,英国多塞特郡)和200µg Al (OH)3在0.5毫升生理盐水。
从天14-28,老鼠被暴露于aerosolised 1%重量/体积OA(三级;西格玛化工有限公司)为30分钟,每2天,如前所述13。三十分钟前每个OA曝光,不同群体接受0.1,1或10毫克aerosolised FP(英国葛兰素史克、中的)(nebuliser浓度在30毫升0.1%乙醇/磷酸缓冲盐(PBS))或安慰剂。另一组是腹腔内注射3毫克公斤−1prednisolone-21-hemisuccinate(西格玛化工有限公司)。对照组由敏感动物暴露在PBS和安慰剂治疗。
结果测量
24小时过去气溶胶暴露后,老鼠犀牛(60 mg·公斤−1戊巴比妥(赛诺菲、Libourne、法国),i.p。)和支气管肺泡灌洗(BAL)。肺灌洗通过气管插管2×4毫升和2×6毫升汉克斯平衡盐溶液,自由离子钙和镁,并配以0.05毫米钠乙二胺tetra-acetic酸。BAL液白细胞的总数(BALF)测定伯克室。微分细胞计数进行cytocentrifuged准备(Cytospin 2;Shandon有限公司、道与May-Grunwald-Giemsa英国)染色,是基于标准≥400个细胞的形态学标准。
血液收集的测量OA-specific免疫球蛋白E (IgE)14和皮质甾酮水平。皮质甾酮测定作为抑制hypothalamo-pituitary-adrenal轴使用的标记与兔子CpdB抗体放射免疫检定法T54(抗原:皮质甾酮3-carboxymethyloxime-bovine血清白蛋白;在兔子)(实验室生产)和二氯甲烷萃取后。不利的系统性影响的另一个标志,是动物可能被监控,胸腺萎缩15,16。因此,胸腺摘除重。
组织学
组织学分析进行4%多聚甲醛固定的组织。组织的形态学分析部分,与刚果红染色,是由光学显微镜和度量进行使用蔡司Axiophot显微镜(卡尔蔡司、从、德国)×400的放大。平均22大航空公司(范围)21 - 24日(基底膜的长度(Pbm)> 2毫米14每个治疗组)进行了分析。除了Pbm外周皮周长(Po),这些参数定义的领域(一个bm和一个o)测量。总气道壁面积计算(佤邦合计=一个o−一个bm)和正常化Pbm2。嗜酸性粒细胞的数量在总气道壁量化并表示每毫米2佤邦合计。杯状细胞数量每毫米Pbm是衡量Periodic-Acid-Schiff染色组织。
免疫组织化学染色的FN进行了山羊antirat FN (Calbiochem-Novabiochem GmbH, BadSoden,德国)使用streptavidin-biotin过氧化物酶的方法14。消极的控制,主要与正常山羊血清抗体被替换下场。采用计算机图像分析系统定量测量进行(KS400蔡司,卡尔蔡司)平均18大航空公司(每组范围24里面)。染色的面积总气道壁(FN的WF合计每μm基底膜)表示。
为了避免观察者偏见,所有微观幻灯片被一位观察家之前编码分析,盲目的阅读。
数据分析
报道值表示为±sem。BALF细胞组成,OA-specific IgE血清皮质甾酮,杯状细胞和支气管旁嗜酸性粒细胞不同的实验组,每组比较通过克鲁斯卡尔-沃利斯检验的多重比较。显著差异观察时,两两比较了使用Mann-Whitney紫外线测试Bonferroni调整。形态测量学的分析和测量FN在气道壁沉积,不同的老鼠在一个组的数据集中在一起。的平均值佤邦合计正常化,Pbm2和WF正常化,Pbm比较实验组之间用单向方差分析吗事后测试(至少显著差异和矫正)。一个假定值< 0.05被认为是显著的。
结果
炎性细胞浸润支气管肺泡灌洗液
OA暴露显著增加总细胞数以及嗜酸性粒细胞的数量,淋巴细胞、中性粒细胞和巨噬细胞在BALF与PBS曝光(表1⇓)。FP 0.1毫克剂量没有任何影响和微分细胞计数。1毫克FP剂量明显减少OA-induced总细胞数的增加,和嗜酸性粒细胞,中性粒细胞和巨噬细胞;然而,数字仍明显高于PBS-exposed动物。10毫克FP剂量总细胞数减少,嗜酸性粒细胞的数量,淋巴细胞、中性粒细胞和巨噬细胞。除了细胞总数和淋巴细胞和中性粒细胞的数量,在微分细胞计数无显著差异仍然PBS-exposed老鼠相比。嗜酸性粒细胞和淋巴细胞的数量在大鼠明显低于1毫克FP对待。强的松,虽然大大减少总细胞数和嗜酸性粒细胞的数量,淋巴细胞和中性粒细胞,没有细胞数量恢复到基线水平。10毫克FP剂量减少嗜酸性粒细胞数量比强的松在更大的程度上。其他细胞数量这两个治疗策略没有显著不同。
肺组织学
敏感大鼠与OA挑战更高数量的浸润在气道嗜酸性粒细胞比PBS-exposed动物(p < 0.0001)。
FP 0.1毫克剂量没有效果,而1毫克和10毫克FP和强的松显著抑制增加(p < 0.0001 1毫克和10毫克FP和强的松p < 0.05与placebo-OA)。只有嗜酸性粒细胞的动物数量与0.1毫克FP和强的松治疗仍显著高于PBS-exposed动物(分别为p < 0.05和p < 0.0001与placebo-PBS)(图。1⇓)。
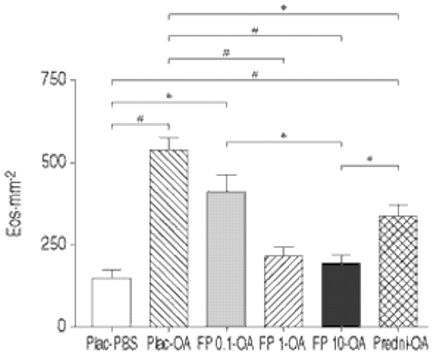
效果与磷酸缓冲盐(PBS)(□)暴露在卵白蛋白(OA)和伴随的治疗与安慰剂(温馨的)(┘),0.1毫克丙酸(FP)(▓), 1毫克FP(└), 10毫克FP(▪)和强的松(predni) ( )在支气管旁嗜酸性粒细胞(Eos)的数量。*:p < 0.05;#:p < 0.0001。
)在支气管旁嗜酸性粒细胞(Eos)的数量。*:p < 0.05;#:p < 0.0001。
FN沉积在OA-exposed动物相比显著增加在placebo-OA PBS (11.74±1.07与3.90±0.51µm2·µm−1在placebo-PBS;p < 0.0001)。增加显著抑制≥0.1毫克的剂量在FP 0.1 mg-OA FP (6.69±0.89与在placebo-OA 11.74±1.07;p < 0.0001)。FP 1和10毫克进一步减少FN沉积在气道壁(6.06±1.67 FP 1 mg-OA和4.97±0.57在FP 10 mg-OA;p < 0.0001与placebo-OA)。0.1 mg-FP组才PBS-exposed控制动物的区别仍然显著(p < 0.05与placebo-PBS)。强的松也显著降低了FN的数量,而不是基线水平(6.70±1.11 prednisolone-OA;p < 0.0001与placebo-OA, p < 0.05与placebo-PBS)(图。2⇓)。
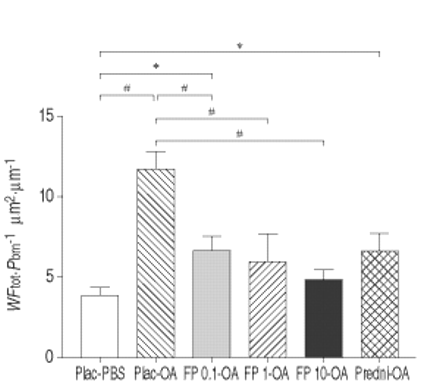
效果与磷酸缓冲盐(PBS)(□)暴露在卵白蛋白(OA)和伴随的治疗与安慰剂(温馨的)(┘),0.1毫克丙酸(FP)(▓), 1毫克FP(└), 10毫克FP(▪)和强的松(predni) ( )在总气道壁纤连蛋白沉积(WF合计)。Pbm:基底膜的长度。*:p < 0.05;#:p < 0.0001。
)在总气道壁纤连蛋白沉积(WF合计)。Pbm:基底膜的长度。*:p < 0.05;#:p < 0.0001。
OA也暴露诱导我们(p < 0.0001与placebo-PBS)。FP的0.1和1毫克和强的松没有显著减少GCH,杯状细胞的数量也不是团体之间的明显不同。与10毫克FP预处理,然而,阻止GCH (p = ns与placebo-PBS)(图3所示⇓)。
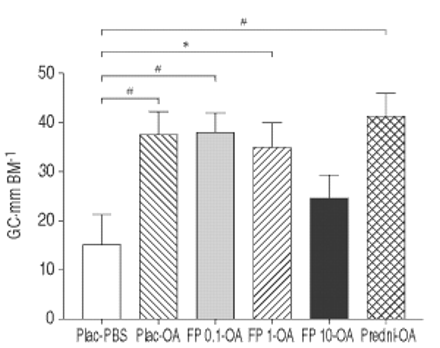
效果与磷酸缓冲盐(PBS)(□)暴露在卵白蛋白(OA)和伴随的治疗与安慰剂(温馨的)(┘),0.1毫克丙酸(FP)(▓), 1毫克FP(└), 10毫克FP(▪)和强的松(predni) ( 杯状细胞的数量(GC)上皮细胞。BM:基底膜。*:p < 0.05;#:p < 0.0001。
杯状细胞的数量(GC)上皮细胞。BM:基底膜。*:p < 0.05;#:p < 0.0001。
总气道壁,正常化Pbm2显著增厚,OA比PBS(0.0258±0.0019µm曝光2·µm−2在placebo-OA与0.0187±0.0011µm2·µm−2在placebo-PBS;p < 0.005)。只有10毫克FP治疗抑制这种增厚(0.0189±0.0014µm2·µm−2在《外交政策》10 mg-OA;p < 0.005与placebo-OA)。佤邦合计µm prednisolone-treated集团(0.0227±0.00122·µm−2prednisolone-OA)没有明显的下降与安慰剂组相比,虽然增加的厚度没有达到统计学意义PBS-exposed控制动物相比(图4所示⇓)。
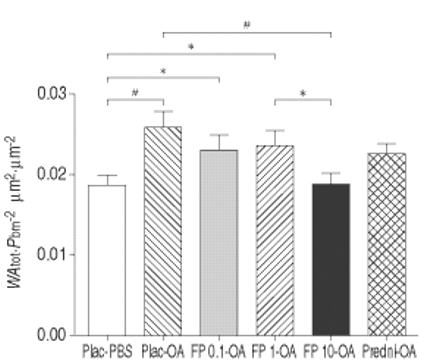
效果与磷酸缓冲盐(PBS)(□)暴露在卵白蛋白(OA)和伴随的治疗与安慰剂(温馨的)(┘),0.1毫克丙酸(FP)(▓), 1毫克FP(└), 10毫克FP(▪)和强的松(predni) ( )在总气道壁面积(佤邦合计)。Pbm:基底膜的长度。*:p < 0.05;#:p < 0.005。
)在总气道壁面积(佤邦合计)。Pbm:基底膜的长度。*:p < 0.05;#:p < 0.005。
Ovalbumin-specific血清免疫球蛋白E
OA-specific IgE水平血清在敏感大鼠升高的挑战与OA PBS-exposed相比大鼠(p < 0.001;表2⇓)。FP 0.1毫克和1毫克并不影响增加。另一方面,10毫克FP略,但值得注意的是,降低血清OA-specific IgE水平(p < 0.05)与placebo-OA),而强的松显示趋势降低IgE水平(p < 0.076)与placebo-OA)。没有统计学差异的不同剂量吸入FP或强的松i.p。
讨论
目前的研究表明防止allergen-induced结构性变化,比如我们和气道壁增厚,需要更高的剂量ICS比抑制嗜酸性粒细胞招募。
在作者的老鼠模型的气道重塑14,分别对OA的敞口引起嗜酸性粒细胞增多,在BALF以及支气管壁。治疗FP引起嗜酸性粒细胞的数量减少,存在剂量依赖的相关性显著抑制从1毫克。抑制作用在组织嗜酸性粒细胞似乎从这个剂量达到高原开始,而10毫克FP需要正常化BAL嗜酸性粒细胞。到目前为止,ICS的存在剂量依赖的相关性影响上气道嗜酸性粒细胞主要评估诱导痰液样本。这些研究还表明,ICS是有效的,从低剂量开始,减少嗜酸性粒细胞数量,剂量反应曲线相对平坦17- - - - - -20.。这是平行的变化在多大程度上粘膜嗜酸性粒细胞数量尚未完全建立在人类身上。
allergen-induced气道嗜伊红血球过多的机制仍然是一个争议的问题。增加骨髓eosinophilopoietic活动由于当地白介素(IL) 5生产发生21,22。航空公司之间的确切信号事件和骨髓,然而,仍不清楚。目前的研究表明同样的影响胸腺重量,10毫克FP抑制嗜酸性粒细胞浸润在支气管壁在更大程度上比3毫克公斤−1systemically-administered强的松。这进一步说明这些因素诱导eosinophilopoesis负责在当地生产的气道组织和类固醇必须达到足够的粘膜浓度来发挥其疗效。
OA-induced增加FN在气道壁可能既反映了血管通透性的增加,加上当地的合成。事实上,Erjefalt等。23表明等离子体是一个主要来源FN在迁徙的早期阶段上皮损伤后的修复过程。然而,它是最有可能的增加数量的FN还取决于当地的合成,Meerschaert等。24证明FN在哮喘患者BALF的浓度大于预期的FN扩散循环由于血管通透性增加。此外,Hernnas等。25显示在bleomycin-induced肺纤维化模型大鼠血浆泄漏可能不是唯一的来源观察灌洗FN的增加。符合这一点,FN的数量的减少气道壁的FP目前的研究都可以归结到一个影响等离子体泄漏和纤维母细胞的功能。吸入治疗FP显著降低血浆蛋白漏在人类的航空公司26。它也被证明在体外,地塞米松剂量依赖性抑制FN鼠肺成纤维细胞合成27。
虽然FN沉积可以是结构组件以及等离子体组件,我们是更成熟的参数结构改变。目前的结果表明,我们对外交政策的影响。符合作者的观察,治疗600µg布地奈德b.i.d。据报道大幅增加上皮细胞纤毛/杯状细胞指数的人类的航空公司28。在老鼠身上,用糖皮质激素治疗在过敏原暴露导致我们的抑制29日,30.。这些steroid-mediated效应机制需要完全阐明。一种可能性包括辅助2细胞因子的合成的抑制作用,这为我们做出贡献。在老鼠身上,anti-IL-5 allergen-induced没有影响我们,虽然这几乎抑制牙龈纤维化的感应和消除气道嗜酸性粒细胞浸润。在最近的一项研究中,Trifilieffet al。31日表明OA-sensitised和暴露IL-5嗜酸性粒细胞缺乏的老鼠没有开发改造的我们和其他特征。但是,治疗重组IL-5未能诱导改造的特点,表明IL-5本身不负责这些结构性变化,包括我们。这进一步说明了其他细胞因子诱导我们的重要性,如il - 4和IL-1332。从目前的结果,它可以提出这些细胞因子可能不那么容易抑制比IL-5 ICS,构成气道嗜伊红血球过多的发展。在体外,类固醇似乎对il - 4和IL-5起到类似的抑制作用,但相对较少的数据情况在活的有机体内。在最近的一份报告中,局部应用布地奈德鼻灌洗液IL-5水平下降,而il - 4的水平都不受影响33。
在目前的研究中,气道壁增厚只是被FP的最高剂量,而不受到强的松。没有提供的形态学研究人类因为技术原因,对这方面的人体steroid-mediated活动。数学模型强调气道壁厚的重要性AHR的发病机理34。在这项研究的et al。12,这是显示的剂量ICS不仅适应控制症状和肺功能基线,但除了气道高反应性降低,导致减少牙龈纤维化的程度。采用后一种策略意味着受试者接受意味着额外剂量的400µg ICS治疗时颁发新加坡莱佛士学院集团与段。此外,Jatakanonet al。17证明只有一剂1600µg布地奈德足以减少乙酰甲胆碱气道反应,而400µg足以减少呼出一氧化氮水平和痰液嗜酸性粒细胞数。这些观察表明,气道高反应性的机制相对耐类固醇治疗。间接的,这也表明,只有更高的剂量ICS能够降低哮喘患者气道壁厚。目前的结果支持这一假设。
评估的一个重要方面ICS的影响与潜在副作用的有利影响。在低剂量ICS展览没有明显的系统性活动,但在高剂量范围内,有一个系统性不良反应的剂量反应曲线35。更高的ICS沉积在肺内的航空公司提高了疗效,但导致更高的系统性影响。这是目前的研究证实,说明10毫克FP和3毫克公斤−1强的松等价的系统性活动,反映在胸腺体重的减少,这是一个适当的参数来评估系统性毒性16。重要的是,减少类似胸腺重量、强的松是更有效地防止allergen-induced结构性变化。
它可以得出的结论是,丙酸存在剂量依赖的相关性影响的各个方面allergen-induced气道变化,但是这些剂量反应关系根据测量结果不同。预防杯状细胞增生和气道壁增厚要求更高的剂量丙酸比的嗜酸性粒细胞的炎症反应的抑制支气管肺泡灌洗液和气道组织,以及纤连蛋白沉积。剂量水平防止结构改变、系统性影响被观察到;然而,对于类似程度的胸腺athrophy,吸入丙酸比系统性强的松更有效。
确认
作者要感谢e . Castrique c . Snauwaert a . Neesen i . De Borle k . De Saedeleer m .羊皮和l . Verdonck技术援助。他们也想承认m·约翰逊,葛兰素史克,中的,英国,请提供丙酸。
- 收到了2001年12月12日。
- 接受2002年5月28日。
- ©人期刊有限公司














