摘要
间充质基质细胞输注可能为COPD患者提供另一种基于免疫的治疗选择http://ow.ly/5DpA30hQS6y
编辑器:
慢性阻塞性肺疾病(COPD)是全球发病率和死亡率的主要原因,原因是该疾病的特征是持续性肺部和全身炎症,但治疗选择有限[1].最近,间充质基质细胞(MSCs)在COPD中的临床前研究表明,无论是全身或气管内给药,均能有效缓解炎症和减少肺气肿[2,3.].人类试验已经证明,在给COPD患者使用MSCs后,MSCs并没有改善肺活量;然而,据报道,c反应蛋白(CRP),全身炎症的标志,在输注后1-3个月下降。在这些试验中没有详细评估早期的时间点,这限制了对这些变化的进一步调查[4,5].确定静脉输注间充质干细胞的命运及其生物分布的潜在影响,以及在以前的试验中未探索的短期间充质干细胞诱导的全身变化,将更好地描述间充质干细胞治疗慢性阻塞性肺病的效用。
该研究由珀斯皇家医院伦理委员会批准(批准号EC2012/103),所有患者均提供书面知情同意书。一个地点,第一阶段研究(澳大利亚临床试验注册编号12614000731695)进行确定MSC biodistribution,遵循系统性炎症和临床端点MSC灌注组(n = 9)的轻微到严重稳定的慢性阻塞性肺病患者(n = 1全球倡议对慢性阻塞性肺疾病(黄金)阶段,我所有被招募的患者在试验开始前至少3个月没有经历病情加重,常规药物治疗也没有变化。患者接受两次低通道输注(p4- - - - - -5)约2×10的异基因骨髓来源的MSC6每公斤间充质干细胞,间隔1周,第一次输注含有放射性标记细胞,第二次输注未标记细胞。首次输注使用的间充质干细胞用铟-111进行标记,铟-111是一种半衰期为68小时的低能量放射性同位素,可以在数天内进行追踪。标记的MSCs能够充分抑制外周血单个核细胞(PBMC)的增殖在体外与未标记MSC相比(p>0.05),并保持正常的形态特征。可在一年后监测归因于慢性阻塞性肺病急性加重的安全性和住院情况。采用Wilcoxon配对试验比较输注前后细胞亚群水平和循环血浆生物标志物。
MSC输注显示出可归因的不利副作用,并且耐受良好。输注后,通过计算断层摄影(CT)扫描在肺部内在肺部检测铟-111,24小时后保持可检测,然后在肝脏,脾脏和骨髓中检测到液体后7天,液体骨髓(图1一个b)与评估MSC定位的小鼠研究一致[6,这种模式可能部分是由于间充质干细胞中铟的渗漏,然后与转铁蛋白结合,被网状内皮系统吸收,在肝脏和脾脏中积累。患者在首次输注后4小时通过单光子发射计算机断层扫描(SPECT)进行评估,并与低剂量CT叠加,以确定铟-111活性和MSC在肺部的定位。肺气肿肺中铟-111减少(红色箭头;图1 c)与正常肺(蓝色箭头;图1 c).铟-111在肺中的滞留量也与基线1秒用力呼气量(FEV)呈正相关1) (R2=0.68, p=0.02)和肺对一氧化碳的扩散能力(R2=0.81, p=0.01),提示轻度疾病患者的MSCs在肺血管中的保留时间较严重疾病患者长,严重疾病患者重塑肺气肿时血流灌注较差。这种分布可以保护健康的肺组织。
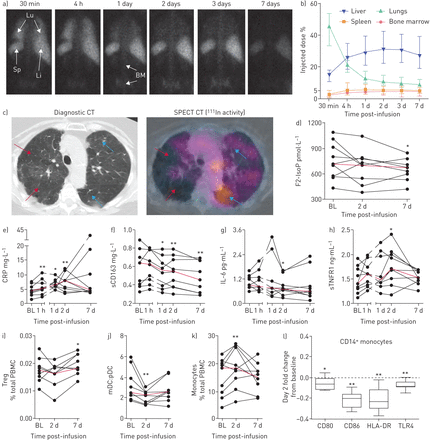
静脉输注间充质基质细胞(MSCs)不能迁移到肺气肿重塑区域,同时诱导许多全身免疫反应。铟-111存在于肺部(Lu),其次是肝脏(Li)、脾脏(Sp)和骨髓(BM),共有7种 输注后天数(a),通过感兴趣区域(ROI)分析(平均值和标准偏差)进行定量测量,校正背景和衰减(b)。可见肺气肿改变的区域显示极少的放射性标记(红色箭头),而受影响较小的区域显示较高水平的放射性标记积聚(蓝色箭头)(c)。氧化应激标记物F2异烷(F2 IsoP)水平下降7 输注后天数(d)。促炎标志物,如C反应蛋白(CRP)在1-6之间显著增加 h和2 输注后第天(e),而可溶性CD163水平从1 输注后第2天(g)和第2天(f)和白细胞介素(IL)-6。循环中的sTNFR1也增加了2 输注后天数(h)。包括调节性T细胞(Treg)在内的循环免疫细胞比例增加7 而髓样(mDC)与浆细胞样(pDC)树突状细胞(j)的比率降低。CD14水平+灌注后2天单核细胞增加(k),第2天这些单核细胞的CD80, CD86,人类白细胞抗原- dr (HLA-DR)和TLR4与基线相比显著减少(l)。每个患者的影像学图像中都显示了代表性图像。黑线代表每个患者的时间过程,红线代表中位数水平,显示总体趋势。使用Wilcoxon标记等级试验进行统计分析,比较基线和输注后的水平。CT:计算机断层扫描;单光子发射计算机断层扫描;PBMC:外周血单核细胞。*:p < 0.05;* *: p < 0.01。
我们首先通过将健康对照组(n=3)和稳定COPD组(n=3)的PBMC与含有0.001–0.1的血浆共培养,确定铟-111是否诱导独立于MSCs的炎症反应 铟的MBq,因为这些浓度反映了我们队列中铟暴露的范围。在单独培养基中以及用炎症刺激物αCD3和脂多糖(LPS)刺激后,暴露于铟的PBMC中细胞因子的产生(白细胞介素(IL)-1β、白细胞介素-6、白细胞介素-8、白细胞介素-10和肿瘤坏死因子(TNF)-α)没有差异与非铟暴露对照组,表明铟不会引起炎症反应。从相同的培养物中,还通过流式细胞术评估淋巴细胞亚群和基于磷脂酰丝氨酸表达的细胞活力,并且我们观察到铟-111对细胞比例或活力没有影响在体外(数据未显示).
采用气相色谱-质谱法定量f2 -异前列腺素[7]作为中性粒细胞和巨噬细胞氧化负荷的标记。MSC输注后7天f2 -异前列腺素减少(图1 d)这与在LPS诱导的急性肺损伤大鼠模型中输注异基因人脐带来源的MSC后氧化应激的降低一致[8].我们通过ELISA和multiplex评估了几种在COPD中很重要的炎症介质;然而,一些介质,包括IL-1β, IL-10, IL-12p70和IL-17A在我们的队列中检测不到。CRP水平在MSC输注后1小时至2天升高(图1 e),对比了其他试验的数据,其中COPD患者全身应用同种异体骨髓源性间充质干细胞在输注后1-3个月降低了CRP水平[4,5].值得注意的是,某些炎症介质发生了变化,包括可溶性CD163,这是一种与COPD疾病严重程度相关的巨噬细胞激活的生物标志物[9]在输注后1 ~ 7天显著降低(图1 f).此外,IL-6(9例患者中有7例)下降,IL-6是COPD的主要介质,它刺激基质金属蛋白酶的分泌和t细胞反应,有助于气道重塑(图1 g) [10].此外,抗炎循环sTNFR1 (图1 h),一种诱骗非细胞相关受体,结合并隔离过量的循环TNF-α,从而减少全身炎症[11].内毒素血症小鼠MSCs上调sTNFR1支持了这一数据[12].
通过流式细胞术评估,MSC给药也将平衡转移到更抗炎的循环细胞谱。循环treg在炎症解决中起核心作用,通常在COPD中减少,MSC输注后7天增加(图1我) [13].在第2天,MSC输注也改变了树突状细胞(DC)亚群的比例,更倾向于浆细胞(p)DC而不是髓细胞(m)DC (图1 j).pDCs是干扰素-α的最大生产者,干扰素-α可以增强COPD中的抗病毒反应,而mDC提供了t细胞刺激和炎症细胞因子的主要来源。MSC输注降低mDC:pDC比例可能对COPD有直接益处,因为mDC:pDC亚群比例的增加与COPD患者更高级别的肺气肿损害相关[14].此外,CD14+单核细胞在第2天显著增加(图1 k). 这些单核细胞还表现出共刺激分子(CD80、CD86、HLA-DR)和促炎症受体(TLR4)的表达减少,采用免疫调节表型(图1 l).确实,脐带和脂肪来源的MSCs与纯化的单核细胞共培养降低了它们的共刺激受体,并能够抑制t细胞的反应在体外[15].
慢性阻塞性肺病急性加重期住院人数从MSC输注前一年内发生的11起事件减少到输注后一年内发生的6起事件。在输注后的一年中没有使用额外的干预措施,除非在此期间病情恶化后需要治疗。第二次输注后3周测得的肺功能与输注前水平相比没有变化:FEV中位数(范围)137% (23-87%)与41%pred(41-98%pred),p=0.48;强制肺活量为80%pred(59-106%pred)与82% pred (56-101% pred), p=0.84。这些发现也与COPD的其他MSC试验相一致,后者在肺活量测定方面也没有显示出统计学上显著的改善。
我们的研究描述了快速的全身免疫变化,这在以前的MSC治疗慢性阻塞性肺病的试验中没有发现,我们将其与静脉输注后MSC的生物分布联系起来。我们假设系统管理的MSCs在30分钟内到达肺,并可能释放营养因子,包括细胞外囊泡,这导致免疫调节和重要炎症介质的减少。尽管肺测量缺乏改善,全身MSC输注可能有助于COPD患者的炎症减轻。
确认
作者感谢在皇家珀斯医院的Cell和Coass疗法WA的学习参与者和员工进行研究中使用的MSCs。该作者还承认使用设施,以及澳大利亚显微镜和微观分析研究设施的科学和技术援助,西澳大利亚大学,由大学,国家和英联邦各国政府提供的设施。我们还感谢皇家珀斯医院的医学研究基金会在整个研究中使用实验室设施。该研究得到了治疗学创新澳大利亚(TIA)和国家卫生和医学研究委员会的资助。
脚注
该研究在澳大利亚临床试验注册处注册,注册号为12614000731695。
支持声明:这项研究由国家健康和医学研究委员会资助。
利益冲突:M. Sturm是Isopogen Pty Ltd的董事;此外,M. Sturm拥有CTTWA的PCT/AU2014/001031专利(免版税)。Y. Moodley因在勃林格殷格翰(Boehringer Ingelheim)和罗氏(Roche)提交的工作之外担任科学顾问委员会成员而获得酬金。
- 收到了2017年8月1日。
- 接受2017年12月28日。
- 版权©2018人队