文摘
儿童间质性肺疾病包括一系列的罕见ILDs影响婴儿、儿童和青少年。Nintedanib许可成人治疗肺纤维化。InPedILD试验的主要目标是确定剂量的和安全的儿童和青少年nintedanib fibrosing ILD。6岁到17岁的病人fibrosing ILD HRCT和临床重大疾病随机2:1获得nintedanib或安慰剂24周然后非盲nintedanib。剂量是根据weight-dependent异速生长的伸缩。Co-primary端点是在稳态血浆浓度时间曲线下的面积(AUC)τ,党卫军在2周和26和患者的比例在24周的治疗诱发的不良事件。26患者接受nintedanib和13安慰剂。几何(gCV %) AUC的意思τ,党卫军对于nintedanib 175µg×h·L−1(85.1)患者6尺11寸岁和160年µg×h·L−1(82.7)12 - 17岁的病人。在双盲阶段,不良事件被报道在每个治疗组84.6%的患者。两个病人停止nintedanib由于不良事件。据报道在38.5%和15.4%的腹泻nintedanib和安慰剂组,分别。调整的意思(se)改变FVC %预计在24周是0.3 (1.3)nintedanib组和安慰剂组−0.9 (1.8)。总之,在儿童和青少年fibrosing ILD,体重依赖型剂量给药方案导致接触nintedanib类似于成人和可接受的安全性。这些数据提供了一个科学依据nintedanib在这个患者人群的使用。
介绍
儿童间质性肺疾病(孩子)由一系列的罕见和异构肺疾病影响婴儿,儿童和青少年可能带来重大的发病率(1,2]。病理生理学的孩子通常包括遗传因素,有时结合相关敞口受伤或自身免疫失调,虽然在某些情况下,病因学是未知的(1,3- - - - - -6]。一些孩子与ILD发展肺纤维化。在成人、儿童、肺纤维化涉及组织损伤,细胞外基质过度沉积,和异常的肺的改造,虽然成纤维细胞的焦点与纤维化(儿童组织学检查未见1,7]。没有许可的药物治疗的儿童,治疗通常涉及免疫调节(8),但缺乏证据支持这种方法。
Nintedanib是一种细胞内酪氨酸激酶抑制剂,抑制过程基础肺纤维化的进展(9,10]。随机对照试验表明,在成人特发性肺纤维化(IPF),其他形式的进步肺纤维化和fibrosing ILD与系统性硬化症,nintedanib持续减少的速度下降用力肺活量(FVC)、代孕ILD的进展在成人(11),与安慰剂相比,不良事件概要特征主要由胃肠道事件(12- - - - - -15]。基于nintedanib在成人的临床疗效,并假定相似性肺纤维化的病理生理学的改造在成人和儿童,这是假定nintedanib可能提供类似的好处在儿科人口和临床重要的或进步的肺纤维化。的验证性试验的功效nintedanib儿科患者被认为是不可行的,InPedILD试验(ClinicalTrials.govNCT04093024;Eudra-CT 2018-004530-14)设计的主要目标,评估剂量的和安全的儿童和青少年nintedanib fibrosing ILD。此外,疗效端点收集数据来支持其评价nintedanib在儿科人口。
材料和方法
病人
InPedILD试验了6岁到17岁与儿童或青少年fibrosing ILD在高分辨率ct (HRCT)扫描执行≤12个月在筛选之前,经中心审核(见补充材料),FVC≥25%预测和临床意义上的疾病16]。临床重大疾病定义为一个球迷评分≥3 (17]或临床进展的证据记录在任何时间框架。风扇分数评估疾病严重程度与ILD基于症状的儿童和青少年,血氧饱和度和肺动脉高压;分数范围从1到5,得分越高表明更大的疾病严重程度(17]。临床进展的证据是基于FVC≥10%预测的相对衰落,FVC相对下降5 - 10%的预期恶化的症状,在HRCT上纤维化恶化或其他措施的临床恶化归咎于进行性肺纤维化(如。增加氧气的需求,减少扩散能力)。列出关键的排除标准的补充材料。
试验设计
InPedILD审判是3期临床试验在21个国家的43个网站进行的(16]。四周后筛选期,患者随机接受nintedanib 2:1或安慰剂使用交互式响应技术,分层的年龄组(6尺11寸12 - 17年)(图1)。剂量是根据weight-dependent异速生长的伸缩。起始剂量50毫克,75毫克,100毫克,或每天两次150毫克和剂量调整治疗期间是基于病人的体重(表1)。下面的剂量和治疗剂量减少中断被允许管理不良事件。最低剂量25毫克每日两次。双方持续激烈被允许外交对峙剂量两国在4周的剂量与试验药物相关的不良事件被认为是减少,或在8周内不被认为是不良事件与试验药物有关。
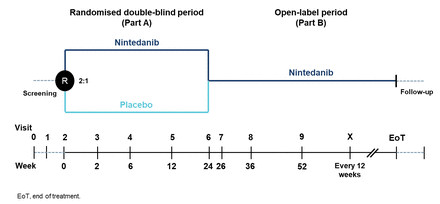
试验设计。
审判由一个安慰剂对照双盲段24周后跟一个变量期间所有患者接受非盲nintedanib (图1)。过早停用研究药物的患者被要求按原计划参加所有访问。一旦≥30个病人(包括≥20例12 - 17岁)已完成药代动力学抽样在26周或过早地停止了试验中,招聘是关闭的。确认足够的药代动力学数据被收集后,所有患者计划进行治疗结束访问,之后,他们进入了一个4周随访期间或滚到一个开放的扩展试验,所有患者接受nintedanib (InPedILD-ON;ClinicalTrials.govNCT05285982;Eudra-CT 2020-005554-23)。
提供科学指导委员会建议的设计试验。安全监测委员会回顾了药代动力学和安全数据来确定的安全性和其nintedanib和建议修改,额外的评估,进一步招生的适当性和审判的延续。一个裁决委员会成立宣判死亡由于心脏,呼吸系统或其他原因和评估不良事件归类为主要不良心血管事件。这次审判是按照协议执行,赫尔辛基宣言的原则和协调三方良好的临床实践的指导协调国际会议上,欧盟指令2001/20 / EC /欧盟法规536/2014和其他相关的指导方针。试验开始在每个站点(补充材料)中列出相应的机构审查委员会批准后/独立伦理委员会和主管机关根据国家和国际法规。书面知情同意和批准(如适用)之前得到试验条目。
端点
co-primary端点是在稳态血浆浓度时间曲线下的面积(AUC)τ,党卫军)在星期2 nintedanib治疗(即。在患者随机接受nintedanib第2周和26周的患者随机接受安慰剂24周的比例其次是nintedanib)和24周后患者治疗诱发的不良事件,这被定义为事件的爆发第一次摄入试验药物直到第一次摄入之前开放nintedanib或随机的最后摄入治疗+ 28天(无论发生第一次)。不良事件编码根据医学词典管理活动(MedDRA)版本25。
病理发现骨骼成像和发育不良的牙科根在牙科成像被定义为特殊利益的不良事件。二级安全端点包括患者病理结果的比例骨骺生长板在牙科成像和病理结果检查或成像在24周。后续成像骨骺生长板只有在患者进行物理开放。从基线在24周的时候身高z分数是一个进一步的端点。
次要疗效端点包括FVC %的变化预测、氧饱和度(热点2)在休息,6分钟步行试验(6 mwt)距离和儿童的生活质量™(PedQL™)问卷分数在24周。肺量测定法是使用标准化执行肺活量计提供给每个站点和根据at /人指南(18]。FVC %预测值计算方程发表的《欧洲呼吸协会全球肺功能行动(188bet官网地址19]。PedsQL问卷由孩子的报告(5 - 7年),报告(8 - 12岁)儿童和青少年报告(> 12年),以及父母报告为每个年龄段;这些分数范围从0到100,得分越高表明更好的与健康有关的生活质量(20.]。
分析
的主药代动力学分析,AUCτ,党卫军计算使用non-compartmental和区划的分析和描述性统计。在病人随机nintedanib, AUCτ,党卫军在星期2使用;如果这个值是失踪,在26周使用价值。在病人随机安慰剂,AUCτ,党卫军在26周(对应nintedanib治疗第2周)使用。药代动力学分析是在病人进行≥1提供的试验药物和剂量可评价的数据≥1药代动力学端点没有违反协议相关药物动力学的评价。安全分析进行病人≥1剂量的试验药物。调整意味着改变从FVC %的基线预测,热点26 mwt距离,PedsQL问卷分数和身高z分数在24周反复的措施,分析了使用混合模型与固定治疗分类的影响在每个访问和年龄组和固定基线每一次访问太阳系时,持续的影响,并为病人随机效应。不良事件叙述地。
样本大小计算根据评估的主要药代动力学端点和间隙参数需要估计有足够的精度。假设变异系数(CV)的70.8%(基于明显的间隙的几何简历nintedanib在等离子体稳定状态(CL / F党卫军)血管外的多个剂量管理),≥20药代动力学测量每年龄组患者(6尺11寸和12 - 17年)才能达到≥80%概率(松散称为功率(21])的95%置信区间的CL / F党卫军和AUCτ,党卫军在几何平均估计的60%和140%。根据入选标准和初步可行性评估,预期,这项研究只会招收足够的病人年龄≥12年实现这个概率;然而,从11岁儿童药代动力学数据收集和分析。样本数量≥30例(≥10胜11岁,≥20 12 - 17岁)是有针对性的。
结果
病人
39岁的87名患者的筛查患者(12胜11岁,27 12 - 17岁)是随机和治疗与安慰剂(26 nintedanib, 13) (图2,表S1)。治疗组之间的基线特征通常是平衡(表2)。大多数患者是女性(61.5%)和白人(79.5%)。意思是(sd)为12.6(3.3)岁,体重为42.2(17.8)59.4公斤和FVC(21.9) %预测。最常见的诊断类别是表面活性剂蛋白质不足(30.8%)。最常见的标准满足临床重大疾病是一个风扇分数≥3 (59.0%)(表S2)。
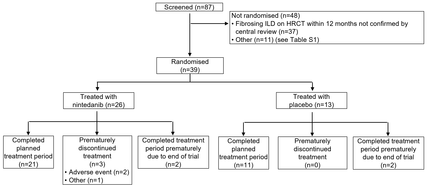
在双盲期间性格的病人。
曝光
意思是(sd)接触试验药物双盲期间是22.3(4.8)周nintedanib group)和22.6(4.2)周的安慰剂组(表3)。在此期间,4名患者(15.4%)在nintedanib组和一个病人(7.7%),安慰剂组有≥1减少剂量和nintedanib 3名患者(11.5%),安慰剂组没有≥1治疗中断;nintedanib组3例(11.5%),安慰剂组停止治疗(图2)。意思是(sd)接触试验药物在整个试验是46.4(22.3)周病人随机nintedanib和49.6(23.6)周病人安慰剂其次是开放性nintedanib (表S3)。
药物动力学
几何平均数(gMean) AUC (gCV %)τ,党卫军对于nintedanib 175µg×h·L−1(85.1)在6到11岁的病人和160年µg×h·L−1(82.7)的患者年龄在12到17年。额外的药代动力学数据所示表S4。
不良事件
双盲期间,不良事件报道nintedanib组22例(84.6%),11例(84.6%),安慰剂组(表4)。腹泻是最常见的不良事件与nintedanib有关,在10位病人(38.5%)nintedanib组和两个病人(15.4%),安慰剂组。两个病人(7.7%)有不良事件导致中断nintedanib(报告为骺过早融合(不是证实了中央对成像)和肝损伤)。nintedanib组的两名患者(7.7%)和一个病人(7.7%),安慰剂组有严重不良事件(见表4详情)。
在整个试验中,不良事件被报道在所有患者随机nintedanib和12名患者(92.3%)接受安慰剂作为随机治疗和非盲nintedanib;严重不良事件报告了5例(19.2%)随机nintedanib和三个病人(23.1%)接受安慰剂的非盲nintedanib(见紧随其后表S5详情)。没有不良事件导致患者治疗期间停止开放。两个病人(7.7%)随机nintedanib有天冬氨酸氨基转移酶和/或丙氨酸转氨酶≥3倍正常范围的上限;没有满足标准Hy定律。
骨骺生长板和牙科检查
在24周,20名患者(76.9%)和nintedanib 9个病人(69.2%),安慰剂组,分别有骨骺生长板成像。病理结果中观察到的两个病人(7.7%),nintedanib组和一个病人(7.7%),安慰剂组(表S6)。
在24周、牙科检查了在23个患者(88.5%)和10个病人(76.9%),和牙科成像在22个(84.6%)和10例(76.9%)患者,分别nintedanib和安慰剂组。牙科检查,新的病理研究结果发表在5名患者(19.2%)接受nintedanib和一个病人(7.7%)接受安慰剂。在牙科成像,发育不良的牙科根据报道在六个病人(23.1%)接受nintedanib和没有接受安慰剂(表S7)。安全监测委员会审查和牙科专家确定在三个病人,根开发完成(即。发育迟缓是难以置信的)和三个病人,不同的测角之间的评估导致了一个通读。治疗三周在所有情况下。在五个六个病人,没有迹象表明牙科根发育不良的中部被审查的牙科成像在52周。提供了这些案件的细节表S8。
身高z分数
调整的意思(se)从基线的变化在24周的时候身高z分数−0.05 (0.03)nintedanib组和安慰剂组−0.03(0.04)(区别−0.02(95%置信区间CI:−0.12, 0.09);名义p = 0.75) (图S1)。
热点;26 mwt距离和PedsQL
调整的意思(se从基线热点)的变化2静止在24周nintedanib组的0.07%(0.77)和(1.08)−2.25%安慰剂组(差异2.31%(95%置信区间CI:−0.39, 5.02);名义p = 0.09) (图4)。调整的意思(se)从基线变化6 mwt距离在24周是17.6(16.5)米nintedanib组和安慰剂组10.5(22.9)米(差异7.2(95%置信区间CI:−50.7, 65.0);名义p = 0.80) (表S9)。
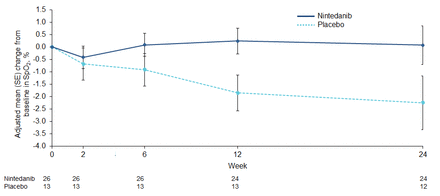
改变热点;2静止在24周。
调整的意思(se)变化的基线PedsQL病人报告的分数在24周是6.5(1.9)和5.5 (2.7)nintedanib和安慰剂组,分别(差异1.0(95%置信区间CI:−5.8, 7.9);名义p = 0.76) (表S8)。调整的意思(se)变化的基线PedsQL家长报告分数在24周是5.5(2.5)和5.6 (3.5)nintedanib和安慰剂组,分别(区别−0.1(95%置信区间CI:−9.0, 8.7);名义p = 0.98) (表S10)。
讨论
InPedILD试验的主要目标是确定nintedanib的剂量会导致儿童和青少年与成年人的敞口,并评估nintedanib在儿童和青少年的安全与临床重大fibrosing ILD。结果表明,nintedanib在这个病人的人口可以接受的安全性。在成人(12- - - - - -14,22),最常见的不良事件与nintedanib InPedILD审判是腹泻,但孩子有经验的腹泻的比例低于观察成人,并没有因腹泻双盲期间停药。
抑制血管内皮生长因子受体(VEGFR)导致血管生成减少,这对骨骼生长和发育是至关重要的(23]。来自动物模型的数据表明,nintedanib, VEGFR抑制剂(24),可能有可逆影响骨骺生长板的大骨头和一个对牙齿发育的影响(25]。因此,密切监测生长,骨骼和牙齿发育InPedILD试验实施。病理结果在骨骺生长板成像显示,没有证据表明过早关闭物理。改变身高z分数显示正常线性增长。虽然阻碍牙科根增长6例报道,这些不能证实了儿科牙医专家考虑额外的临床和人口统计数据。尽管放心,nintedanib的潜在影响骨骺生长板和牙齿将继续监控开放的扩展研究。
InPedILD审判的双盲期间,五个病人在nintedanib组COVID-19相比安慰剂组病人。nintedanib组3例(11.5%)和四个病人(30.8%),安慰剂组在双盲期间收到了COVID-19疫苗;进一步的病人(7.7%),安慰剂组前COVID-19审判。基于的作用机制,临床和临床数据,没有迹象表明nintedanib会增加感染的风险或恶化疾病COVID-19。
150毫克的剂量投标的关键试验研究nintedanib与肺纤维化(成人12- - - - - -14和成人患者的推荐剂量26]。研究调查的影响曝光的疗效和安全性nintedanib成人支持这个剂量(27,28]。在InPedILD试验中,剂量是根据weight-dependent异速生长的伸缩。在成人对待nintedanib 150毫克,派生gMean AUC (gCV %)τ,党卫军nintedanib 203µg×h·L−1(67.5)和中位数AUC(5日,第95个百分位)τ,党卫军181µg * h·L吗−1(81.5,398)(勃林格殷格翰集团数据文件)。InPedILD因此,药代动力学数据试验表明,体重依赖型剂量给药方案取得了相当的暴露在儿科病人观察成年人接受150毫克,支持使用这个药物剂量在儿科人口。
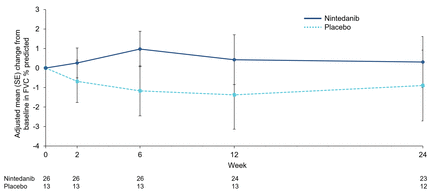
FVC InPedILD审判是一个探索性的端点。均值变化(se)在FVC %预计在24周(1.3)nintedanib组的0.3%与−0.9%安慰剂组(1.8)。我们还观察到一个稳定的热点2静止在24周nintedanib组与安慰剂组下降(意思是[se]0.07%[0.77]的变化与−2.25% [1.08])。这些观察结果进行解释时需要特别谨慎考虑到自然历史数据的缺乏与ILD儿童肺功能的7,29日,30.)的短期试验。然而,观察到的减少与nintedanib FVC %下降预测与安慰剂在儿科人口范围内观察到成人fibrosing ILDs治疗24周。
在患儿进行临床试验fibrosing ILD挑战性是因为因素包括其稀有和缺乏共识如何衡量儿童肺纤维化的进展(1]。InPedILD试验以外,唯一的随机安慰剂对照试验干预儿童fibrosing ILD已经发表在德国进行羟氯喹的审判结果,实质上不同于InPedILD试验的设计(31日]。InPedILD试验是第一个国际安慰剂对照试验进行儿童ILD和代表了该领域的一个里程碑。然而,它也有局限性,包括小样本大小和时间短,限制数据的解释。值得注意的是,随机的39例InPedILD试验所需的参与数十个网站,与未能满足辐射条件基于中央审查屏幕失败的主要原因。
总之,InPedILD试验数据证明nintedanib有一个可接受的安全性和耐受性方面更好的儿童和青少年fibrosing ILD,没有新的安全信号观察与成人患者相比。暴露水平达到与体重依赖型剂量异速生长的剂量范围内观察到成人。这些数据提供了一个科学依据的儿童和青少年中使用nintedanib fibrosing ILD。
平实的语言总结
纯语言的总结这些数据是可用的:https://www.globalmedcomms.com/respiratory/ERS2022/Deterding/plain-language-summary
确认
我们感谢患者参与了InPedILD审判和他们的父母和照顾者。勃林格殷格翰集团支持的InPedILD试验是国际GmbH (BI)。作者作者满足标准所推荐的国际医学期刊编辑委员会(IC188bet手机版188bet手机版MJE)。作者没有收到支付发展的手稿。写作提供的援助是朱莉·弗莱明和温迪FleishmanHillard莫里斯,伦敦,英国,简约而由BI。BI是有机会回顾手稿为医学和科学的准确性以及知识产权方面的考虑。
脚注
ClinicalTrials.govNCT04093024;Eudra-CT 2018-004530-14”cd_value_code = "文本
数据可用性:数据共享声明& # 13;& # 10;确保独立的临床研究结果的解释和使作者能够履行自己的角色和义务国际标准,BI授予所有外部作者对相关临床研究数据的访问。与BI坚持政策透明度和出版的临床研究数据,科学和医学研究人员可以对临床研究数据的访问请求主手稿的杂志上发表后,监管活动是完整和其他标准。研究人员应该使用https://vivli.org/请求访问和更多信息,请访问https://www.mystudywindow.com/msw/datasharing强生# 13;& # 10;" cd_value_code = "文本
数据共享声明确保独立的临床研究结果的解释,使作者履行其角色和义务国际标准,BI授予所有外部作者对相关临床研究数据的访问。与BI坚持政策透明度和出版的临床研究数据,科学和医学研究人员可以对临床研究数据的访问请求主手稿的杂志上发表后,监管活动是完整和其他标准。研究人员应该使用https://vivli.org/请求访问和访问https://www.mystudywindow.com/msw/datasharing为进一步的信息。
资助者:勃林格殷格翰的发言;DOI: http://dx.doi.org/10.13039/100001003。
利益冲突:罗宾Deterding报告咨询费用,费用参与InPedILD试验的指导委员会和支持从勃林格殷格翰集团从罗氏(BI)和咨询费用。
利益冲突:丽莎R年轻报告拨款支付给她的机构从国家卫生研究院(NIH)和孤儿疾病中心宾夕法尼亚大学;从现时的特许权使用费;咨询费用和费用参与指导委员会的InPedILD从勃林格殷格翰集团(BI)试验;咨询费用从罗氏公司和赛诺菲;并从纽约大学Langone健康谢礼。
利益冲突:艾米丽M DeBoer报告费用从BI InPedILD审判指导委员会的参与。史蒂文·坎宁安报告费用由BI为他支付给他的机构参与的指导委员会InPedILD审判。
利益冲突:大卫·沃伯顿报道格兰特re:恢复(COVID-19)倡议国家心脏,肺和血液研究所(NHLBI)和费用从BI InPedILD审判指导委员会的参与。
利益冲突:Nicolaus Schwerk报告从诺华咨询费用;支付从AbbVie讲座,Allergopharma,基耶西,Infectopharm,诺华,辉瑞、赛诺菲;费用参与数据安全监测委员会或BI和诺华顾问委员会;费用从BI参与InPedILD审判指导委员会;他是一个德国儿童肺病学学会的成员,欧洲呼吸协会儿童间质性肺病的临床研究合作(chILD-EU),欧洲科学和技术合作(成本)网络188bet官网地址转化研究儿童和成人ILD (ENTeR-chILD)和Kinderlungenregister部长。
利益冲突:凯文·R Flaherty拨款支付给他的机构从BI报告;从现时的特许权使用费;柏勒罗丰咨询费用从箭头,阿斯利康,BI, CSL贝林,Daewoong, DevPro, Dispersol, FibroGen,地平线,Immunet,卢平,NeRRe疗法,顺从,Polarean,纯健康,PureTech, Respivant,罗氏/基因泰克,赢家,太阳制药、许愿,联合治疗;他是一个指导委员会主席为肺纤维化基金会和报告费用从BI InPedILD审判指导委员会的参与。
利益冲突:凯文·K布朗赠款NHLBI报告;咨询费用,议长费,支持旅游和/或担任顾问或数据监测委员会AbbVie,生原体、叶片疗法,BI,百时美施贵宝公司,CSL贝林,DevPro生物制药,Dispersol,十一P15,加拉帕戈斯群岛,Galecto, Huitai生物医药、Humanetics,开源成像财团(OSIC),顺从,Redx制药公司,赛诺菲,第三极,生物转化;他从BI报告费用参与InPedILD审判指导委员会;他拥有领导与社会和OSIC Fleischner或受托人角色。
利益冲突:米卡尔Dumistracel,埃尔韦拉Erhardt,朱莉娅•Bertulis玛蒂娜Gahlemann和Susanne Stowasser BI的员工。
利益冲突:马提亚Griese chILD-EU寄存器的拨款从BI报告分析;已收到费用从BI InPedILD指导委员会的成员,一个顾问委员会和一个评审委员会和一个基于web的系列。
- 收到了2022年7月29日。
- 接受2022年8月25日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org