文摘
严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)出现在2019年底已经蔓延全球,造成呼吸道疾病指定的冠状病毒疾病的大流行2019 (COVID-19)。一个更好的定义所需的肺SARS-CoV-2感染宿主反应是了解病毒的发病机理,验证假定的COVID-19生物标志物在临床研究已经提出。在这里,我们使用目标转录组FFPE组织使用Nanostring GeoMX™平台生成深入COVID-19肺转录风景的图片,大流行性H1N1流感病人和未感染的控制。主机转录组显示的一个重要upregulation与炎症相关的基因,I型干扰素生产、凝血和肺血管生成的COVID-19患者比未受感染的控制。SARS-CoV-2非均匀分布在肺(强调空间转录组)的优势领域的高病毒载量增加I型干扰素反应。一旦主要细胞类型出现在示例中,在病人的相关性和patient-patient变化已经被控制了,只有非常有限的基因差异表达之间致命的流感和COVID-19患者的肺。引人注目的是,interferon-associated基因IFI27之前确认为一个有用的血液生物标志物来区分细菌和病毒的肺部感染,肺部明显调节COVID-19患者相比,流感患者。总的来说,这些数据表明,空间转录组是一个强大的工具来识别小说在组织基因签名,提供新的见解的发病机制SARS-COV-2帮助病人诊断和治疗。
介绍
自2019年出现以来,严重急性呼吸道syndrome-associated coronavirus-2 (SARS-CoV-2)已经引起了广泛的疾病,从无症状感染到急性呼吸窘迫综合征(ARDS)。尽管死亡率低于其他相关冠状病毒,SARS-CoV-1和中东等呼吸系统综合症冠状病毒(MERS-CoV) SARS-CoV-2是高度传染性,迄今已导致全世界> 175感染和> 3.5死亡和上升1]。COVID-19 SARS-CoV-2感染的临床表现。
ARDS开发42%的肺炎患者COVID-19和大量死亡占COVID-19 [2,3]。ARDS是血氧过低的呼吸衰竭的一种形式定义为弥漫性肺泡损伤的存在(爸爸)通常与细菌性肺炎、败血症、胰腺炎或创伤。ARDS的发病机制通常是由于炎症损伤alveolar-capillary膜导致肺部水肿和呼吸衰竭。为了应对损伤,肺的肺泡巨噬细胞炎症编排招募中性粒细胞和巨噬细胞循环的损伤导致肺泡上皮细胞的死亡和进一步损害肺功能(4]。严重COVID-19也经常以并发血管疾病、凝血障碍。这包括破裂的血管障碍,水肿,endothelialitis和血栓形成。血栓性和微血管并发症通常记录在死去的病人,表明血管病理是严重疾病的主要因素5]。而这些机制导致疾病进展,目前还不清楚哪些机制导致死亡的主要因素。
病人组织的转录组分析提供了一个独特的机会不仅理解SARS-CoV-2的发病机理也协助生物标记验证。迄今为止,主要的搜索临床生物标志物,包括转录组分析COVID-19患者样本,进行全血。受感染的患者的血液样本非常容易,但是尚不清楚血液参数准确反映病毒载量或组织损伤的程度,临床治疗的目标控制(6]。肺是病毒复制的主要网站,但只有有限数量的转录组研究已经进行COVID-19患者的肺。这样的研究利用转录组分析病人只有一小群(1 - 2)7,8]或依靠“散装”测序整个肺组织,任何洞察组织异质性在这个复杂的器官是失去了5,9,10]。相比之下,Nanostring GeoMX™数字空间分析(DSP)基因表达板直接应用于组织部分考虑转录组特征的空间位置,并能直接样本intra-organ异质性(11,12]。这提供了一种更深的细胞变化受病毒感染,是一种强大的方法来定义宿主应对病毒的特点和它们之间的空间关系。事实上,这种初步的转录组分析COVID-19病人肺部出现承诺(13]。然而,这样的分析需要应用先进的生物信息学技术控制的众多潜在混杂因素出现在基因表达数据采样在这样一个复杂的实验设计。此外,有一个明确的需要区分主机SARS-CoV-2转录组响应(和相关的空间异质性)从其他感染性ARDS的诱因,如流感病毒,这可能是与SARS-CoV-2并行循环。
为了解决这些问题,我们研究了在肺组织SARS-CoV-2使用空间转录组的发病机制的方法从快速尸检样本10 COVID-19患者,5 2009流感病毒H1N1大流行性流感(pH1N1)患者和4个控制患者样本收集在一个单一的机构。的Nanostring GeoMX™DSP平台结合生物信息学建模允许反褶积的个人变异病毒和宿主因素。这些数据表明,病毒载量异构影响病人的肺内转录组反应,有明显的重叠在流感病毒之间的基因表达谱和SARS-CoV-2感染样本。然而,一些独特的转录组签名COVID-19患者的肺中被检测到。此研究表明,空间转录组的优势再加上强大的直线造型生物信息学技术广泛识别关键路径参与病毒感染和明确区分不同的细胞和分子的参与途径在不同的感染。
材料和方法
研究设计
组织微阵列(TMA)核心是准备从解剖肺组织从10 SARS-CoV-2和5 ph1n1病人死于呼吸衰竭(ARDS) (补充表1 - 3)。控制材料获得4未受感染的病人(补充表3)。所有SARS-CoV-2和pH1N1患者确诊为感染通过RTqPCR鼻咽拭子标本,并与计算机断层成像(CT)显示弥漫性和毛玻璃衰减和双边的透明,暗示了肺部感染病毒。解剖和活检材料来自天主教大学做巴拉那河PUCPR国家研究伦理委员会(CONEP)伦理批准数字:协议数量3.944.734/2020 (COVID-19组)和2.550.445/2018 (H1N1和对照组)。所有方法进行了以下指导方针和有关规定。家庭允许COVID-19事后活检和H1N1pdm09样品和常规尸检病例的对照组。这项研究还批准了在昆士兰大学和昆士兰科技大学的人类研究伦理委员会(HREC)批准。
最初,两组x射线和CTs等成像考试分析来识别和更严重的肺损伤肺段。一旦我们确认和放射学明显代表病变(尤其是左叶肺段,因为他们可以删除更加敏捷和实际mini-thoracotomy技术),我们收集了样本通过一个前mini-thoracotomy第四或第五肋间隙。病人的死亡之间的时间,获得同意书的亲戚,和删除片段通过mini-thoracotomy没有超过4 h (COVID-19和H1N1组)。在所有这些情况下(COVID-19和H1N1集团),样本同样大小的(3×3厘米),微妙地处理和使用外科手术切除剪刀。样品被固定到一个10%福尔马林溶液浓度和保存至少24小时,直到阻塞和切片进行微观分析。肺formalin-fixed石蜡包埋(FFPE)样本与苏木精和伊红染色())来观察组织病理学方面,找到合适的和代表潘趣和构建TMA的领域。临床数据得到从ICU的住院期间医疗记录(在医院Marcelino Champagnat库里提巴,巴西,COVID-19集团在医院丹尼库里提巴,巴西为H1N1组)。
对照组样本
也包括在本研究的对照组肺患者死于肿瘤样本或心血管疾病(不包括肺部病变)。对照组的样本是通过传统的解剖技术。
病人的死亡之间的时间,获得同意书的亲戚,和删除片段通过常规解剖不超过6小时。
对照组样品被固定到一个10%福尔马林溶液浓度和保存至少24小时,直到阻塞和切片进行微观分析。
肺formalin-fixed石蜡包埋(FFPE)样本与苏木精和伊红染色())来观察组织病理学方面,找到合适的冲压区域构造TMA。
临床数据来自医疗记录在医院住院期间丹尼在库里提巴,巴西。
组织准备和组织病理学
30 5µm厚串行部分被剪切了TMA块上带正电的幻灯片(债券顶点)和部分与苏木精和伊红染色())和马森的三色的污渍。Brightfield图像获得使用Aperio(徕卡生物系统公司、美国)滑动扫描评估组织病理学的病理学家。TMA核心评估整体组织模式。感兴趣区域(roi)方法分析肺泡出血和水肿,透明膜形成、急性炎症、2型pneumocyte增生、鳞状上皮化生,毛细管堵塞,成纤维细胞的疫源地,间质炎症。
免疫组织化学和RNAscope®
免疫组织化学进行莱卡Bond-RX autostainer(徕卡生物系统公司、美国)抗体针对SARS-CoV-2突起蛋白(Abcam ab272504) 2μg·毫升−1。在缓冲ER1热诱导抗原决定基检索进行20分钟100°C,和信号呈现3 3′-Diaminobenzidine(涂)衬底。幻灯片是成像使用蔡司Axioscanner(德国卡尔蔡司)和包含IHC被细支气管上皮细胞的病理学家,得分2型pneumocytes,间质淋巴细胞和肺泡巨噬细胞隔间。
RNAscope®探针(美国ACDbio)针对SARS-CoV-2飙升mRNA (nCoV2019, # 848561 - c3)、ACE2宿主受体信使rna (# 848151 - c2),和主机丝氨酸蛋白酶TMPRSS2 mRNA (# 470341 - c1)按生产指令用于自动化在徕卡债券RX。DNA的视觉与Syto13 (Thermofisher科学),通道1与蛋白石570(1:50 0),通道2蛋白石620(1:1500),通道3蛋白石690 (1:1500)(PerkinElmer)。荧光图像获取与Nanostring火星原型DSP在20 x。
Nanostring GeoMX DSP Covid-19免疫atlas面板
刚割下的每个TMA处理根据Nanostring GeoMX数字空间剖析器(DSP)幻灯片准备手工技术访问计划。简单地说,幻灯片被烤1 h 60°C,然后处理债券RX autostainer徕卡。幻灯片和蛋白酶K预处理,然后用信使rna探针杂交Covid-19免疫Atlas面板中包含额外的SARS-CoV-2激增面板。孵化后,幻灯片被洗,然后沾CD68、CD3, PanCK, Syto83 1 h然后装入GeoMX DSP仪器扫描和ROI的选择。选定的roi是遵循RNAscope®和包含IHC积极性SARS-CoV-2组织类似的组织结构捕获H1N1和未受感染的组织核心。寡核苷酸杂交mRNA目标有关的裂解和收集计数使用Illumina公司i5和i7双重索引。PCR反应进行4μl GeoMx DSP的样本。AMPure XP珠子(贝克曼库尔特)是用于1.2×bead-to-sample率PCR产物纯化。Paired-end测序(2×75)是使用NextSeq550执行总对齐读取多达400。DND Fastq文件处理系统和上传到GeoMX DSP系统,原始和Q3正常数量的目标是与感兴趣的区域(roi)。
转录组数据
数据用于本研究结果从一个信使rna进行分析与NanoString GeoMx Covid-19免疫atlas面板使用GeoMx数字空间剖析器(DSP)。RNA的数据测量大量的超过1800个基因,包括22个插件COVID-19相关基因,4 SARS-CoV-2特定基因和2负控制(SARS-CoV-2底片,NegProbe)基因和基因32内部参考。从3 TMA幻灯片每个包含10获得的样本组织核心来自10个病人。三个幻灯片对应COVID-19, H1N1或控制组织切片。转录组的测量是在每个核心地区的利益。控制样品COVID-19-free H1N1-free,但是他们不一定是无病样本;他们来自其他病毒性疾病患者。总共60 roi分析(47 COVID-19 8 H1N1和5“控制”)。因素被认为是在这个数据集包括疾病类型(COVID-19, H1N1和控制),病人的起源、主要组织类型(类型2 pneumocytes,细支气管上皮细胞,透明膜,巨噬细胞)和病毒载量(基于RNAscope分数)。
生物信息学分析
在第三季度数据进行了探索和质量检查正常计数数据产生的CTA DSP mRNA分析。相对对数表达式(RLE)土地被用来评估存在的变异形式的批处理效果(14]。数据是正常使用的削减意味着M-values (TMM)方法(15使用面板中的所有基因。具体来说,日志2改变转录丰度数据median-centred对于每一个基因,然后在每个样本之间的差异观察和人口平均每个基因的计算。主成分分析(PCA)的样本进行识别变化相关数据中的特定因素和实验设计。
微分表达式(DE)分析、基因本体和KEGG通路富集分析进行了使用R / Bioconductor包磨边机(v3.30.3) [16,17)和limma (v3.44.3) [18]。短暂,微分表达式是使用线性模型模拟各种实验因素预测。基因表达的变化建模是一种常见的分散的组合,适用于所有基因和gene-specific色散。Limma用于模型和估计每个基因的变异由所有其他基因使用借贷信息经验贝叶斯方法,从而使估计的常见和gene-wise变异只有2复制/条件。一次线性模型是适合一个给定的实验设计,用于查询感兴趣的各种对比的数据微分表达式。由此产生的统计是一个经验贝叶斯主持t统计量,比一个更健壮的t统计量从一个典型的学习任务。基于观察到的核心和组织结构之间的差异的PCA分析,考虑了允许存在相似性,来自相同的核心使用的区域duplicationCorrelations在limma [19]。线性模型提供的灵活的建模框架被用来考虑异构组织结构之间的差异(即。细支气管上皮样与其余的样品),包括它们作为协变量的模型。
两个主要因素进行了分析,即疾病类型(COVID-19, H1N1和控制)和病毒载量。疾病类型,两个比较研究:COVID-19反对控制与核和占主导地位的组织类型不,COVID-19对抗H1N1病毒样本,核和占主导地位的组织类型不。对于这两个对比,voom-limmaduplicationCorrelations管道(20.)是用于符合线性模型。然后应用的治疗标准(21](p值< 0.05)进行统计检验,随后计算t统计量,log-fold变化(logFC),并调整所有基因的假定值。病毒载量,voom-limmaduplicationCorrelations管道(20.](p值< 0.05)之间符合线性模型用于比较高、低病毒载量地区来自COVID-19病人核心(疾病类型作为协变量)。对比应用在两个决议,首先通过分组roi从相同的核心也有同样程度的病毒载量(核心/病人的方法);其次,把每个地区/ roi样本作为一个独立的观察(ROI-based方法)。基因集富集分析(GSEA)进行使用弗莱方法从limma包。从分子特征数据库基因集(MsigDB)特点22,23),C2(策划基因集)和C7(免疫特征基因集)类别进行测试使用弗莱。从KEGG通路数据库路径进行测试使用kegga功能limma包和基因本体浓缩是评估使用goana从limma包19]。
结果
病人的特点
解剖肺组织得到迅速从10 SARS-CoV-2感染患者,5 pH1N1流感患者和4病毒性感染控制的病人。SARS-CoV-2队列是由四个女性和六个男性平均年龄76岁(从46 - 93年)。这些患者表现出多种并发症包括肥胖、糖尿病和心脏疾病和住院后收到了不同的治疗。在入院病人生存范围从8 - 38天,机械通气时间从3 - 21天(补充表1)。血液分析进行入学前又立即死亡显示肺动脉栓塞水平升高7 10个病人符合血管凝血病(补充表2)。
pH1N1流感病毒患者队列由五个男性平均年龄为45.8岁(31-53年不等)。所有患者接受机械通气的时间承认,直到死亡。感染控制队列由四个男性平均年龄为36.25(1 60年不等)的组织捐赠后死于病毒性和non-respiratory疾病(扩展数据表3)。
组织病理学描述
组织微阵列(tma)准备从肺formalin-fixed石蜡包埋的核心的三个军团(每个病人一个核心)和盲组织学检查是由一个病理学家(补充表4)。急性弥漫性肺泡损伤阶段(爸爸)的特点是透明膜,2型pneumocyte增生,肺泡间隔增厚是SARS-CoV-2核心的突出特征。爸爸pH1N1组织还显示功能,在两个核心肺泡出血明显。这些发现并没有控制核心。纤维化不是突出特征,除了一个SARS-CoV-2核心,表现出温和的间质和肺泡纤维化与整合组织组织肺炎。两个pH1N1核心显示轻微的间质纤维化的特点是急性期或晚爸爸组织阶段。
RNAscope®和ROI选择数字空间转录剖析
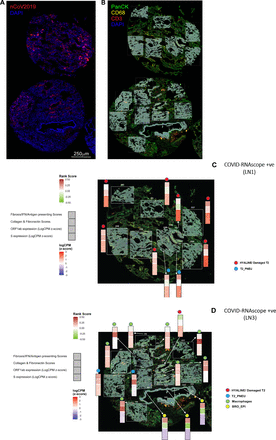
转录分析目标的核心是引导SARS-CoV-2飙升信使rna的检测。两个核心(图2;LN1病毒mRNA和LN3)表现出强烈的信号(图2一个),这些核心是全面评估使用GeoMx DSP平台(阴影区域,图2 b)。25选择感兴趣的区域(ROI)从这两个RNAscope®积极核和21 ROI选择从剩下的八个核心SARS-CoV-2感染患者(至少一个ROI每个病人)的病毒mRNA低于RNAscope的检测。八ROI从肺中选择五个pH1N1病人(至少每个病人一个ROI),和五个ROI选择从控制患者的肺(至少一个ROI /病人)。
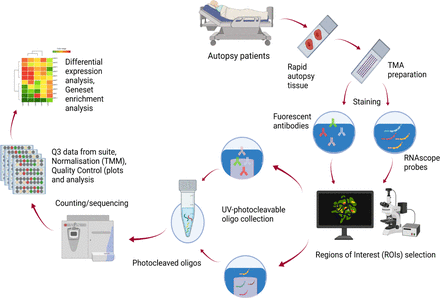
这项研究的示意图。
RNA-FISH空间分析和数字形态学标记可视化nCoV2019 mRNA积极的核心。ROI的选择是遵循RNAscope-FISH染色nCoV2019飙升信使rna。(a)在COVID TMA RNA-FISH染色显示核心LN1和LN3高度积极nCoV2019飙升mRNA(红色)。原子核所示蓝色(DAPI染色)。µm酒吧,规模1000人。(b)代表roi选择跨LN1和LN3 SARS-CoV-2病毒积极核immunohistological石蜡包埋部分为单核细胞染色(CD68、黄色),T细胞(CD3ε、红)、肺上皮细胞(PanCK、绿色)和原子核(DAPI,蓝色)。µm酒吧,规模500人。c。高分辨率图像的高病毒核心LN1每个地区的利益决定了绝大多数细胞类型(透明膜/ T2 pneumocyte)。d。高分辨率图像的高病毒核心LN3感兴趣的每个地区都已经决定了绝大多数细胞类型(透明膜,T2 pneumocyte,巨噬细胞,细支气管上皮细胞)。
SARS-CoV-2 RNAscope®丰度是每个ROI方法评估。代表评分标准,从0到3所示补充图2积极的分数只分配给区域内LN1和LN3 (补充表5)。此外,整合突起蛋白免疫组织化学(包含IHC)似乎是专门针对2型pneumocytes和细支气管上皮地区,然而,一些染色中也观察到间质淋巴细胞和肺泡巨噬细胞(补充图1)。有趣的是,蛋白质包含IHC飙升表明病毒核心除了LN1和LN3 (补充表5),没有产生可检测的信号使用RNAscope®。一些地区低水平非特异性染色观察pH1N1和控制的组织补充表5。我们因此集中ROI选择核心表明高mRNA完整性和病毒的检测RNAscope®。
组织病理学和roi的主导特征
评估组织学的病理学家通过组织架构允许roi分组前进一步分析。主要细胞类型中找到每个ROI注释除了得分的组织病理学和峰值蛋白质包含IHC (补充表5)。roi可以大致分为区域由细支气管上皮结构,2型pneumocytes、透明膜和巨噬细胞(补充图2)。肺泡水肿、急性炎症和鳞状上皮化生中,并未观察到病变或控制核心,然而,2型pneumocyte增生和毛细管堵塞中SARS-CoV-2肺组织。
数据正常化策略和空间转录组数据的探索性分析
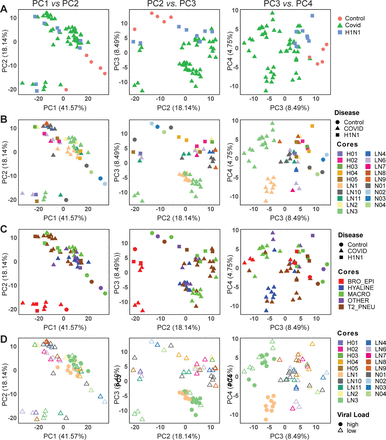
第三季管家正常化TMM是系统性偏差纠正的数据,以便对比SARS-CoV-2, pH1N1流感病毒和控制样品(补充图3)。主成分分析(PCA)的土地被用于探索SARS-CoV-2的可变性,pH1N1流感病毒和控制肺样本,以确定他们是否可以清楚地分开仅仅基于感染病原体的类型和确定因素可能混淆的微分表达式分析。主要组件(pc)捕获正交变化元数据降序的贡献。未受明显在pc上独立于其他样品1和样品3,而SARS-CoV-2和pH1N1流感相关样品仍然在这些轴(图3一)。事实上,在pc 1 - 4, SARS-CoV-2大幅重叠和pH1N1流感样本。这表明SARS-CoV-2和pH1N1流感病毒的转录组剖面组织变量在低病毒载量并不高,而常见的转录组是由这两个病毒死亡病例。
主成分识别转录组数据的可变性和因素。主要组件(pc)捕获正交变异维度在转录组数据降序排列的贡献(即。PC1-PC2, PC3-PC2 PC3-PC4)绘制实验数据分层基于以下因素:(a)疾病类型,(b)核心/患者疾病类型,(c)占主导地位的组织类型与疾病类型和(d)核心/患者的病毒载量。疾病类型板a, b和c贴上形状与控制圈,COVID-19像正方形三角形和甲型H1N1流感。病毒载量标签面板b高病毒载量的形状如固体循环和低病毒低空缺三角形。核和病人标签面板b和c使用不同的颜色。主要组织类型面板c贴上不同的填充颜色(BRO_EPI,细支气管上皮细胞;透明,透明膜;宏巨噬细胞;T2_PNEU Type2 pneumocytes;其他人,其他分类)。
进一步检查的主要变异来源数据集,我们贴上PCA情节由多个不同的参数包括示例的核心(图3 b),占主导地位的细胞类型(图3 c)和病毒载量(图3 d)。样品标签的核心时,PC 3和PC 4,能够区分患者特定的效果,如图所示,一个清晰的分离的核心LN1 LN3,与其他集群的核心与多个roi (LN10) (图3 b)。这表明,在病人的相关性和patient-patient观察转录组变化有一个重要的潜在影响,这需要考虑在任何后续分析此外,PC2样品分离,并明确集群PC1 2绘图时从其他样品,是基于分组的主要细胞类型中找到示例的核心(图3 c)。具体来说,roi,细支气管上皮细胞的主要细胞类型聚在一起独立病人是否pH1N1流感病毒或SARS-CoV-2 (图3 c),或者属于未受感染的控制。这意味着组织异质性被主要细胞类型是一个实质性的因素的变化在我们的实验。在上皮细胞的主要细胞目标SARS-CoV-2和流感病毒(24),我们的数据没有确定病毒上皮取向信号作为核心的关键调节器由支气管上皮细胞没有表现出最高的病毒载量(SARS-CoV-2 RNA所定义的范围)(图3 d)。然而,SARS-CoV-2高病毒载量核独立于其他此外样本和控制生物样品(图3 d)。在一起,这些分析表明无偏和未感染之间的精确比较转录组分析,SARS-CoV-2和pH1N1流感肺样本必须考虑的主要细胞类型出现在样本,inter-patient变化和within-patient相关性。协变量的能力包括结构和空间展示了使用空间转录组的关键优势与散装RNA序列相比,但也需要小心的建设模型用于比较表达式在roi采样。
严重的COVID-19感染的差别导致了全球促炎症反应和对这些免疫细胞效应和再生途径
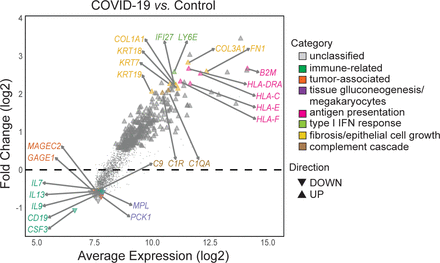
差异基因表达分析随后执行在所有样本核心,考虑的影响占主导地位的细胞类型和适当的内部和inter-patient变化。286个基因被确定为显著调节和20个基因显著下调SARS-CoV-2患者的肺与病毒性感染控制(图4,补充表6、7所示)。
COVID-19感染驱动器促炎症反应和抑制免疫细胞效应和再生。分布差异表达基因的平均记录的函数表达式和褶皱变化(log2)中确定COVID-19样本与未感染(控制)样本。下调基因包括免疫相关细胞因子、肿瘤细胞存活相关的基因和细胞再生的基因,推断和再生抑制免疫细胞的影响。差异基因是富含炎性基因包括I型干扰素(IFN)响应和纤维化的基因。从这些过程是突出代表基因。差异表达基因生成使用voom-limma管道limma: duplicationCorrelations和应用治疗标准与绝对日志褶皱变化与p值< 0.05 > 1.2。
调节基因包括免疫相关基因如B淋巴细胞抗原CD19细胞因子基因等IL7, IL9和使用IL13和组件的补体级联(如。制备过程)一起CSF3,细胞集落刺激因子,通常与动员骨髓(补充表6)。许多肿瘤相关基因包括GAGE1和MAGEC2这些基因表达下调,与细胞的生存。有趣的是,PCK1,需要组织糖质新生MPL,调节巨核细胞和血小板的生成也形成高度降低(25]。
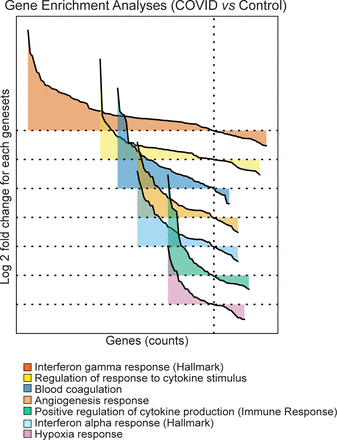
更多样的调节基因被发现差异表达相比,SARS-CoV-2患者的肺与病人死于病毒性原因(补充表7)。这些包括与抗原呈现相关的基因(例如B2M, HLA-DRA HLA-C和HLA-E),I型干扰素(IFN)响应(例如LY6E和IFI27)、纤维化和上皮细胞生长(例如COL3A1、FN1 KRT7、COL1A1 KRT18和KRT19)和补体级联(C1QA和C1R)。与这些观察结果一致,基因集富集分析表明,标志基因的生物过程如活性氧、补充、白细胞介素6 / JAK / STAT3信号、细胞凋亡、p53信号IFN-γ响应,缺氧,IFN-α反应,凝结,TGF-β信号、2 / STAT5信号,血管生成,TNF-α信号通过NFκ-B,炎症反应均显著地调节SARS-CoV-2肺部感染(表1)。使用凝血基因集富集,缺氧反应和血管生成相关基因从nanoString nCounter®PanCancer发展小组进一步证实upregulation与凝血有关的通路和血管生成反应(表2)。这些分析表明,SARS-CoV-2样本显著上调基因与凝血有关,血管生成,IFN-αIFN-γ积极响应和调节细胞因子的生产和细胞因子刺激免疫反应(图5)。这些数据与先前的描述是一致的“细胞因子风暴”反应的患者严重SARS-CoV-2,往往伴随着各种凝血病(26]。他们也同意,后期或延迟I型干扰素反应可能与炎性反应[在音乐会27]。
基因集富集分析(GSEA)显示调节细胞因子反应的凝血障碍COVID-19感染。GSEA差异表达基因比较COVID-19和未感染的样本进行了使用估计log2褶皱变化和分布的假定值显著分化呈现genesets log2褶皱变化的函数(logFC)和基因排序的logFC(瀑布图)。genesets想起是定制genesets“血管生成反应”,“凝血”,“缺氧”反应基于nanoString nCounter®PanCancer进展面板被确定GSEA COVID-19样品中不同调节。(见表2),MSigDB标志基因集IFN-α和IFN-γMSigDB基因本体论(去)基因集》的规定对细胞因子的刺激做出反应”和“积极参与免疫反应的细胞因子的生产监管”。Genesets下令基因数量。指全面的列表中表1。GSEA用limma-fry罗斯福< 0.05进行。的方向和相对变化表达式所示。每个geneset提供的细节补充图4和补充图5。
有限差分与SARS-CoV-2病毒载量相关基因表达
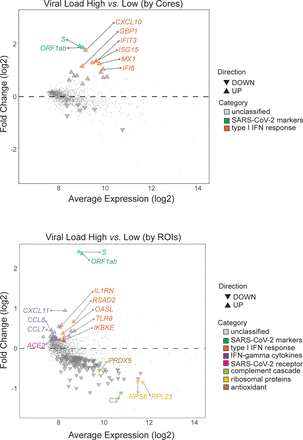
SARS-CoV-2的发病机制是一个复杂的相互作用的宿主免疫病理和病毒载量。来确定病毒载量影响宿主的转录组信号,我们执行SARS-CoV-2样本的微分表达式分析分层基于病毒载量。患者样本核被分为“高”或“低”基于病毒信使rna的存在RNAscope®。因此,两个核心由RNAscope得分积极®,LN1 LN3,被指定为“高”,而剩下的8核SARS-CoV-2患者得分为“低”。这个分析显示,只有17上调和7下调基因差异表达之间的高病毒载量SARS-CoV-2感染核心和其他SARS-CoV-2核心(图6,表3)。符合我们RNAScope分析,SAR-CoV-2特定基因年代和ORF1ab是最强烈的调节基因高病毒载量组(分别为1.916和1.861 log2褶皱变化)。这也符合先前的观察,至少在某些COVID-19病人,这些是最高度表达病毒基因在肺28]。所有其他与> 1 log2褶皱变化调节基因表达相关的I型干扰素反应(CXCL10、IFIT3 ISG15 mx₁, 1英镑和IFI6)(图6,表3)。
决议提供了空间数据揭示了I型干扰素基因签名associates COVID-19病毒载量。分布差异表达基因的平均记录的函数表达式和褶皱变化(log2)中确定高病毒载量与低病毒载量COVID-19样本。分析在两项决议,首先由(前)分组roi从相同的核心也有同样程度的病毒载量(核心病人方法);其次,(底)把每个地区/ roi样本作为一个独立的观察(ROI-based方法)。在这两种方法,SAR-CoV-2特定基因年代和ORF1ab强烈调节高病毒载量组,与RNAscope结果一致。与先前的报道一致,I型干扰素反应基因与SAR-CoV-2 RNA表达。特别是为核心的方法揭示了细分辨率有限微分基因表达ROI-based方法揭示额外微分补体级联变化,核糖体蛋白基因和抗氧化剂。基因是突出代表。差异表达基因使用派生而来voom-limma管道与limma: duplicationCorrelations和应用绝对log2褶皱变化与p值< 0.05 > 1.0。
以上分析认为每个ROI源自相同的核心会有相同程度的病毒感染(即。高或低)。然而,病毒感染可能是统一的组织。的确,没有细支气管上皮roi的两个病毒高核被归类为高(图3 d,补充表5)。检查的影响,我们认为每个ROI看作一个独立的样品是分为“高”(评分> 0)或“低”(得分= 0)RNAscope积极性。通过分层核心这一标准和占主导的细胞类型以及roi来自同一个核心之间的相关性,我们确定了33个不同调节基因和132个表达下调基因在高病毒载量roi相比低病毒载量roi (补充表8)。再一次,年代和ORF1ab是最强烈的调节基因高病毒载量组(分别为2.415和2.365 log2褶皱变化)。其他值得注意的调节基因是那些与I型干扰素反应(例如RSAD2,TLR8 OASL, IL1RN和IKBKE),趋化因子与干扰素−γ(例如CXCL11, CCL8和CCL7)和SARS-CoV-2受体ACE2。更多样的基因表达下调高病毒载量与补体级联相关样本包括(如C3。),核糖体蛋白(例如RPS6和RPL23和抗氧化剂例如PRDX5)(图6 b)。综上所述,这些数据表明,明显的I型干扰素基因签名与SARS-CoV-2 RNA表达和空间上下文所提供的这种技术使病毒载量协会细节有待确定。
严重COVID-19与有限有关,微分转录组相比,严重的流感
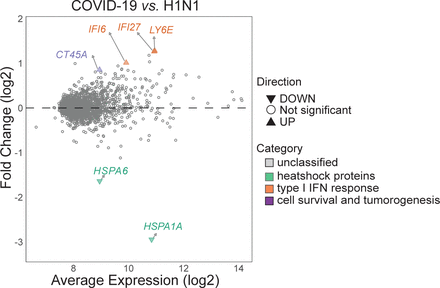
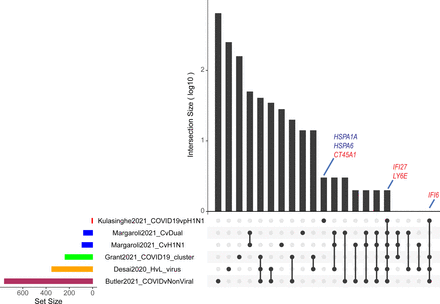
只有数量有限的基因被确定为COVID-19和pH1N1流感样本之间的差异表达(2表达下调和4调节基因,图7)。六个基因显著不同的监管COVID-19样本,三人与I型干扰素反应(LY6E, IFI27&IFI6),两人热休克蛋白家族成员(HSPA6&HSPA1A)和一个CT45A1结合各种生长因子,细胞生存和肿瘤发生。有趣的是,三个interferon-inducible基因也显著调节COVID-19样品相比没有病毒感染(补充表7)。两个热休克蛋白家族成员(HSPA1A和HSPA)也被确定为显著抑制在COVID-19组织。这两个基因同时也显著调节pH1N1组织相比,未受感染的组织(数据未显示),这表明一个潜在的流感特定的签名。理解这些基因的相关性COVID-19 pH1N1,相比我们有这些公布的其他空间的差异表达基因转录组方法实验和分析所显示的不同大小的基因集(图8)。很明显,我们的方法能够识别一套集中特定基因签名COVID-19感染相比其他研究(IFI27和LY6E常见的所有研究,IFI6常见的4 5研究)。在一起,这些数据表明,致命的流感病毒pH1N1和SARS-CoV-2肺样本只有巧妙地不同的主机转录组,但是这可能是潜在的特定的基因签名。这是pH1N1的进一步澄清与控制(补充图6)和GSEA分析(补充图7),显示了许多常见的激活途径COVID-19和pH1N1感染组织相比,控制。这些数据表明,许多DE通路识别COVID-19示例可能表明一个更通用的viral-induced ARDS,虽然只有数量有限的基因可能是COVID-19本身所特有的。
有限的转录组差异相比pH1N1 COVID-19感染。分布差异表达基因的平均记录的函数表达式和褶皱变化(log2)中确定COVID-19样本与pH1N1样本得到的6个差异表达基因标签和分类基于相关的生物过程。与I型干扰素应答相关的基因、热休克蛋白家族成员(相关的)和细胞生存和肿瘤发生。这个独家的基因列表显示COVID-19之间的细微差别和pH1N1感染的转录组,提供了一个潜在的疾病特定转录组为区分这两种疾病类型签名。差异表达基因使用派生而来voom-limma管道与limma: duplicationCorrelations和应用治疗标准与绝对日志褶皱变化与p值< 0.05 > 1.2。
讨论
理解生物功能、网络检测和宿主与病原体相互作用影响器官疾病发展需要两个细胞的信息和空间上下文。分析批量RNA序列或scRNA测序提供了一个全球的概述一个器官对病原体的反应,通常识别广泛的炎症通路。然而,这种方法无法识别微妙的空间不同的个体细胞的变化。这个特定的影响当考虑先天和适应性免疫细胞可能是至关重要的对于理解pathogen-specific响应,并区分这些病原体的形象。相比之下,此外组织的转录组提供了可能性空间解决理清个人感染细胞,病毒载量的贡献,细胞反应,因此患者身上的变化。
COVID-19的临床表现是高度可变的。协会的病毒载量与疾病严重程度提供一种机制为分层的患者早期治疗方案。事实上,鼻咽拭子的分析表明,鼻咽SARS-CoV-2 RNA是独立与疾病严重程度(29日与SARS-CoV-1[],类似于先前的30.]。然而,在肺病毒复制和严重疾病之间的联系仍是更复杂的。这里,我们观察到的病人死了因为COVID-19没有检测到病毒RNA在由RNAscope肺活检。虽然这种病毒RNA检测率可能低于预期,重要的是要认识到病毒抗原沉积在肺是异构的,因此这些数据可能只是反映了随机样本的选择。没有显著的差异在时间从入学到死亡患者积极的与那些被病毒RNA-Scope负面。然而,我们没有信息对这些病人在症状出现和住院这可能影响病毒清除。然而,重要的是要注意,所有患者在这项研究是SARS-CoV-2 RNA PCR阳性通过鼻咽拭子。因此,如果没有病毒RNA在肺部的病人反映病毒清除这是局限于下呼吸道。
转录组的分析表明,区域高病毒载量与明显的I型干扰素反应,符合其他COVID-19患者的肺部的初步空间分析(13其为病原体]和多半由于增加了病毒的分子模式(pamp)用于I型干扰素刺激。然而,即使在没有检测到病毒RNA的样本,明显的I型干扰素基因签名仍然可以观察到肺组织。这些观察体重添加到日益增长的对角色的理解I型干扰素SARS-CoV-2感染(31日]。最近发现COVID-19组织阿特拉斯的一项研究发现upregulation IFN-αIFN-γ响应基因和氧化磷酸化途径COVID-19患者的肺与控制(32]。目前的证据表明,早期和健壮的诱导的I型干扰素可以帮助控制病毒复制和帮助确保轻微感染。相比之下,延迟的I型干扰素诱导(即。峰值后的病毒复制)在很大程度上是无关紧要的病毒控制病毒滴定度已经拒绝在感染但可能有助于使有害的炎性反应和肺损伤(31日,33]。这里介绍的转录组数据从而向潜在的双重角色的I型干扰素SARS-CoV-2感染。
肺转录组分析是一种强大的工具来描绘SARS-CoV-2并确定它如何不同的发病机制与其他呼吸道流感病毒等病原体。先前的研究已经表明,COVID-19患者的肺显示肺泡毛细血管microthrombi发病率的增加和血栓形成微血管病的流感患者相比(5]。符合这些观察,早期报告使用散装肺RNA分析识别69个差异表达基因angiogenesis-related COVID-19病人,而不是流感患者(13]。在目前的研究中,我们观察到COVID-19和流感患者upregulation与凝血和血管生成相关的基因,这些基因没有感染病毒的患者两组之间的差异表达。这些对比数据最有可能反映了这样一个事实:所有样品在本研究收集疾病的最后阶段,因此,早期流感和COVID-19疾病发病和严重程度的差异无法检查。然而,这些数据做突出的困难和发现特定的生物标志物,敏感的重要性足以COVID-19有别于其他呼吸道病毒感染甚至在终末期疾病。
几个潜在的临床和转录生物标志物筛选患者COVID-19已经探索。临床生物标志物包括c反应蛋白、血清淀粉样蛋白A、白细胞介素- 6、乳酸脱氢酶、neutrophil-to-lymphocyte比率,肺动脉栓塞,淋巴细胞和血小板计数(34,35]。然而,大多数这些研究集中在病人的血液生物标志物。虽然外围血液样本是方便临床抽样和高度访问的站点,呼吸的生物标志物,可以快速确定组织(例如,通过鼻拭子)可能更容易在低资源设置。IFI27血液中水平被发现有88%的诊断准确性(AUC)和90%在区别流感和特异性细菌感染患者(36]。有趣的是,之前的分析IFI27COVID-19患者的血液中发现IFI27是调节SARS-CoV-2感染(37- - - - - -39]。在这里,我们发现IFI27中分化调节COVID-19病人的肺与控制病人和高度受限的一组基因差异表达COVID-19与流感病人。这些数据引发了令人兴奋的可能性IFI27不仅可以代表一个严重COVID-19生物标志物,但它也可以帮助区分从其他临床类似的病毒感染这种疾病。,这一点变得尤为重要的“第二波”COVID-19在美国和欧洲将重叠的冬季流感季节。在鼻标本,验证该基因对疾病严重程度需要确认IFI27作为一个有用的基因签名作为分层COVID-19病人。
本研究几个重要的局限性。首先,所有的数据都是来源于一个小样本来自一个研究地点,包括不平衡的病人与对照组,这仍有待决定多少这些数据可以外推到其他的患者群体。与更多的患者重要的是,未来的研究应该包括同等数量的男性和女性是男性独立增加COVID-19严重程度(40]。此外,进一步的研究需要在一个广泛的患者(即。那些有轻度和中度疾病)来确定测量的治疗价值IFI27在感染水平。此外,使用抗体导向ROI捕捉飞速发展,整个转录组分析,推断出细胞类型和细胞反褶积。然而,尽管这些限制这些数据揭示了前所未有的权力空间分析结合详细的多参数生物信息学分析解剖基因差异表达的关键变量,导致在高度可变的病人组和病毒和免疫反应的异构分布在组织内。
确认
我们感谢美国韦弗,m . Haraguchi(弗雷德厨组织病理学实验部门,美国),l .锅a南(美国西雅图Nanostring技术),即蒂芬妮(昆士兰大学Diamantina研究所平移先天免疫组)和g·史密斯(WEHI)。我们感谢病人和他们的家属,让这项研究成为可能。
脚注
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:GTB FSFG,正义与发展党kr,水研究的构想。JM,正义与发展党,AFRDSM JDSMJ CBVDP, SN,缅共,PSFG, LDN, CC, TM,嗯……进行了实验。DB,正义与发展党,CWT JM, CC, BT,基米-雷克南,MJD FSFG, GTB进行数据分析和解释。所有作者批判进行审核和批准之前提交的手稿。
支持声明:这项工作是支持的助学金和奖学金从国家卫生和医学研究委员会(NHMRC),澳大利亚(1157741 AK党;1135898 GTB, 1140406 FSFG)、优先级驱动协作癌症研究计划,由治愈癌症癌症的协助下澳大利亚和澳大利亚也可以基金会(1182179 AK党;1158085 FSFG),亚历山德拉公主研究基金会(水),昆士兰大学(GTB FSFG),昆士兰科技大学(AK),加内特过时和罗德尼·威廉姆斯纪念基金会(AK),沃尔特和伊莱扎霍尔医学研究所(CT, DB, MJD)。支持MJD贝蒂史密斯纪念奖学金在生物信息学。数据库支持陈扎克伯格计划程序授予g·史密斯。陈扎克伯格倡议;DOI: http://dx.doi.org/10.13039/100014989;格兰特:DB / Gsmyth;加内特过时和罗德尼·威廉姆斯纪念基金会;DOI: http://dx.doi.org/10.13039/501100003354; Grant: AKBH2020; Cure Cancer Australia Foundation; DOI: http://dx.doi.org/10.13039/501100001184; Grant: 1182179 AK; 1158085 FSFG; PA Research Foundation; DOI: http://dx.doi.org/10.13039/100009844; Grant: KOB2020; National Health and Medical Research Council; DOI: http://dx.doi.org/10.13039/501100000925; Grant: 1157741 AK; 1135898 GTB, 1140406 FSFG.
利益冲突:Arutha Kulasinghe
利益冲突:下巴小棕褐色
利益冲突:弗里贝罗多斯桑托斯Miggiolaro
利益冲突:詹姆斯Monkman
利益冲突:Sadeghirad博士没有披露。
利益冲突:d . Bhuva
利益冲突:Jarbas da Silva莫塔
利益冲突:卡罗琳Busatta Vaz de宝拉
利益冲突:Seigo长岛
利益冲突:克里斯蒂娜Pellegrino Baena
利益冲突:保罗Souza-Fonseca-Guimaraes
利益冲突:露西娅-迪诺罗尼亚
利益冲突:蒂莫西·麦克洛克
利益冲突:Gustavo罗德里格斯罗西
利益冲突:卡罗琳·库珀
利益冲突:本杰明唐
利益冲突:r .短
利益冲突:梅丽莎·J·戴维斯
利益冲突:费尔南多Souza-Fonseca-Guimaraes Biotheus的顾问公司。
利益冲突:t·茨
利益冲突:肯奥
- 收到了2021年1月7日。
- 接受2021年10月7日。
- 版权©2021年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org