摘要
长冠病毒在成人和儿童中均有发现,其特征是免疫调节障碍。成人患者的自身免疫反应和儿童的过敏反应是关键因素。
大约四分之一的COVID-19患者会出现持续至少一个月的症状,但十分之一的人在12周后仍然不舒服。这种非常虚弱的情况被患者群体定义为“长COVID”,在其他地方被称为后COVID,而患者通常被称为COVID-19长搬运工[1].长时间的COVID严重影响患者重返工作或学校、进行社交生活的能力,并可能对患者、其家人和社会产生重大经济后果。这种疾病的特点是长期后遗症,可能涉及约200种不同和重叠的症状,如持续疲劳、胸部和肌肉疼痛、头痛、呼吸短促、嗅觉丧失、肌肉无力、发烧、认知功能障碍(脑雾)、心动过速、肠道紊乱和皮肤症状。它可以影响任何人,但女性患长时间COVID的可能性似乎是男性的两倍,但只会持续到60岁左右,这时风险水平变得相似[2- - - - - -4].长时间COVID也被描述在儿科年龄[5].意大利的一项研究报告称,在COVID-19感染4个月后,至少有一种症状持续存在[6]而澳大利亚的一项分析表明,只有8%的儿童在轻度SARS-Cov-2感染3-6个月后仍有持续症状[7].在这一人群中,未观察到长冠肺炎患病率的性别差异[5].
长COVID病因
长COVID综合征与基孔肯雅热暴发后的感染后综合征有相似之处[8]和埃博拉[9].导致这种综合症的因素是什么?它们可以是多种多样的。病毒激活的过度炎症反应导致的器官损伤、某些组织中可能引发感染后发病率的SARS-CoV-2持续宿主、免疫失调导致的病原体重新激活、宿主微生物组改变、凝血/凝血问题以及由于SARS-CoV-2和自我蛋白之间的分子拟态而导致的自身免疫,这些都被假设发挥了作用[10].此外,也有人认为,长时间COVID症状可能不是SARS-CoV-2感染的直接结果,而可能是COVID-19炎症诱导的爱泼斯坦Bar病毒重新激活的结果[11].寻找长冠病毒的精细分子机制也在进行中。一些见解来自代谢研究,如。可能导致感染后疾病的色氨酸吸收和代谢改变[12],而来自细胞病理学研究的进一步假设表明,SARS-CoV-2可能能够阻碍宿主细胞的自噬过程,从而有利于病毒颗粒在细胞胞质内的“旅行”和它们的生存。因此,有人认为,细胞代谢调节剂或支持自噬的制剂可能是一种对抗covid后后遗症的治疗策略,有助于消除可能具有免疫原性和活性的病毒颗粒或片段。13].然而,迄今为止,大量不同的长冠肺炎症状和紊乱似乎表明可能涉及不同的并发机制(图1),为了治愈这些患者,应该确定不同的治疗方法。
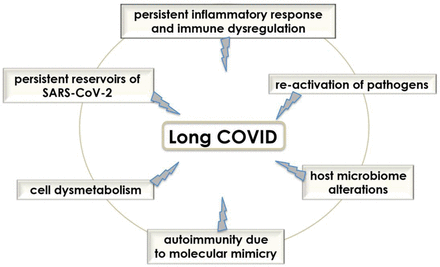
可能导致长Covid的并发机制。
儿童长时间COVID
就儿科人群而言,关于长期COVID-19的临床数据有限。最常见的并发症是肌肉和/或关节疼痛、头痛、胸痛或胸闷感、心悸、呼吸问题和睡眠障碍[5,6].在他们的研究中,Osmanov和同事[5],这得益于国际严重急性呼吸道和新发感染联盟(ISARIC)制定的标准化后续数据收集协议[https://isaric.org/research/covid-19-clinical-research- 498资源/儿科-随访/],观察到老年人和过敏性疾病与随访时出现持续症状的风险较高相关。Osmanov和他的同事认为,至少在儿童中,免疫机制可能是导致感染长期后果风险增加的原因。特别是,COVID-19的后续可能与过敏性疾病儿童的肥大细胞激活综合征和Th-2偏态免疫反应有关[5].重要的是,这些发现与最近的一份病例报告一致,该报告描述了一名青少年在轻度COVID-19后出现持续症状,首次记录持续免疫功能障碍和肺灌注缺陷[14].
性别差异:长时间COVID的“黑洞”
如上所述,女性报告长时间COVID及其症状的频率高于男性[2].这既是一种性别差异,也是公共卫生政策制定者正在以不同的方式讨论和强调的一种性别差异。一种是女性经常更加关注自己的身体和身体的变化。这往往导致更快速的诊断和治疗干预。不幸的是,也有“一派思潮”坚持认为,长时间COVID性别失衡可能只是一种人工制品:它可能只是由“歇斯底里的中年女性”构思出来的。从伦理和临床角度来看,这种性别歧视的做法肯定是一种强烈的偏见,它还可能影响长COVID女性患者的医疗保健和工作权利。
事实上,女性的先天和后天免疫反应都比男性强,基因和激素都与这种性别差异有关。15,16].这些基于性别的免疫差异导致了自身免疫疾病发病率的变化,女性比男性高,对恶性肿瘤和传染病的易感性也不同,男性比女性更常见,这可能是女性在成人中流行长冠病毒的主要原因。最后,正如莱姆病所发生的那样,女性体内的病原体隐藏起来,并产生比男性更高水平的炎症细胞因子[17],可以假设SARS-Cov-2碎片可能仍然隐藏在肾脏或大脑等储层中,引发一些与慢性炎症相关的级联反应,导致长COVID患者经历的疼痛或脑雾等症状。重要的是,如上所述,到目前为止,最年轻的男性和女性患者之间没有显著差异[5].这可能会加强性激素及其免疫调节活性可能在成年长时间COVID患者中发挥作用的假设[18,19].
自身免疫与长冠病毒
据观察,与未感染的对照组相比,至于eb病毒、巨细胞病毒和人类免疫缺陷病毒,SARS-Cov-2感染与产生广泛的自身抗体有关,这些抗体可攻击感染受试者的组织[20.].一些受感染的个体有针对干扰素反应、白细胞转运和淋巴细胞功能/激活等多种免疫活动的蛋白质的自身抗体[21].其他自身抗体是组织特异性的,包括血管、心脏和大脑特异性的自身抗体。已观察到患者产生超过15种不同类型的自身抗体和超过10种不同的自身免疫疾病的倾向[22].可能导致COVID-19自身免疫发展的主要机制有:1)免疫系统的过度激活,2)诱导过度的中性粒细胞胞外陷阱的形成,3)SARS-CoV-2与宿主自身组分的交叉反应。事实上,SARS-CoV-2已被证明与肠道、肾脏、肺、心脏和大脑抗原发生交叉反应,而且SARS-CoV-2蛋白可以与一些自我蛋白表位共享同源性,导致分子拟态路径[22].此外,在炎症条件下,微生物组/病毒体群落的其他有机体,可能在不同的患者之间有很大的差异,也可能有助于自身抗体的产生,并导致自身抗体反应性的巨大变化。这种复杂的情况可以解释在长COVID患者中检测到的临床变异的显著比例
结论
长COVID的特征是特定的持久炎症/免疫失调,不能被视为一种独特的病理,而是一系列不同的发病率状态。因此,更好地了解这种病理的异质性,评估成人患者(特别是女性)血清中自身抗体的出现,以及评估儿童的Th2免疫反应和血浆IgE水平,可能是开始确定针对长COVID患者的个性化和特异性治疗的重要目标。
脚注
资助者:Ministero della Salute;DOI: http://dx.doi.org/10.13039/501100003196;格兰特:covid - 2020 - 12371817。
利益冲突:作者声明没有利益冲突
- 收到了2021年8月17日。
- 接受2021年9月1日。
- 版权所有©作者2021。
本版本按照创作共用署名非商业性许可4.0的条款发布。商业复制权利及许可请联系权限在}{ersnet.org















