摘要
“环孢菌素抑制冠状病毒的复制和可能抑制与冠状感染相关的细胞因子风暴”
冠状病毒是已知引起人类和其他哺乳动物的肠道感染呼吸道感染。严重急性呼吸综合征冠状病毒-2(SARS-CoV的-2),这会导致COVID-19,是的第7病毒冠状病毒家庭是已知感染人类。直到2002年,四个冠状病毒感染人类被描述(HCoV- NL63,冠状-229E,HCoV- OC43和HKU1)。这些病毒引起的免疫活性的主机只有轻微的呼吸道疾病。自2002年以来,从这个三口之家高致病性病毒已被确认。SARS-CoV的(也被称作SARS-CoV的-1)是一种有包膜的,正感,单链RNA病毒感染,其肺中的上皮细胞。该病毒通过结合至血管紧张素转化酶2 [进入宿主细胞1]。它感染人类,蝙蝠和果子狸[1]。它的出现2002 - 2003年与大约10%的死亡率,但有限的传输率(大约8100案件,R0 <1)[2-五]。感染者出现流感样症状,其中可能发展为肺炎,急性呼吸窘迫综合征(ARDS)和呼吸衰竭及多器官功能衰竭死亡。中东呼吸综合征冠状病毒(MERS冠状病毒)于2012年出现在沙特阿拉伯和是这个家庭的第二高致病性病毒[6],但用透射率比较低。MERS-CoV的具有比SARS-CoV的(30%)更高的死亡率,但同样的特点是低传输率(大约2500自2012年起的情况下,R0 <1)[6]。典型MERS症状包括发烧,咳嗽和气短。肺炎是常见的,但并不总是存在。胃肠道症状,包括腹泻,也有报道。MERS-CoV感染的一些实验室确诊病例报告为无症状。大多数这些无症状病例已检测到以下积极的接触实验室确诊病例的追踪。单峰骆驼是该病毒的主要储存宿主。
SARS-CoV-2于2019年在中国武汉出现,其特征是比SARS-CoV或MERS-CoV高得多的人际传播能力。导致COVID-19疾病的SARS-CoV-2病毒含有四种主要的结构蛋白。其中的S (spike)糖蛋白是一种跨膜蛋白,存在于病毒的外部,与宿主细胞的人类ACE2受体结合形成同型三聚体[7]。的SARS冠状病毒-2 S蛋白具有与SARS-CoV的-1等价的蛋白质的同源性显著[8,也与ACE2受体结合[9]。然而,SARS冠状病毒2的S蛋白结合具有更高的亲和力与ACE2受体[10]由于弗林蛋白酶样切割位点的存在(682RRAR / S686)插入在S1 / S2蛋白酶切割位点[11]。一种considerable percentage of COVID-19 patients (5–19%) develop ARDS within 24–48 h after onset of symptoms, requiring mechanical ventilation with supplemental oxygen and succumb to the disease. The mortality of patients who develop ARDS is 49% [12]。不少患者COVID-19开发多器官功能衰竭(MOF)。死亡的主要原因是急性呼吸窘迫综合征,与财政部,出血/凝血功能障碍(弥散性血管内凝血,DIC),急性心脏/肝/肾损伤和继发性细菌感染[败血性休克12]。留在重症监护病房的平均长度大约为8天,病情严重的病人有相当大的差异。
大多数受感染的患者没有症状,可以通过携带病毒的飞沫传播的疾病。人在60岁以上的各种健康疾病,如糖尿病,高血压,慢性阻塞性肺疾病,哮喘或损害肾功能很容易受到SARS冠状病毒-2和感染时,制定一个更严重的疾病。有人提出,在所有合并症的一个共同因素是高水平的循环纤溶酶的其裂解病毒的弗林网站增加其感染[存在12]。虽然,一些临床试验正在进行中(约1300干预试验全球认可的时候这篇社论是根据美国国立卫生研究院数据库写入[13])没有有效的治疗可用,患者主要接收支持治疗。
MERS冠状病毒和SARS-CoV的发病已经超过SARS-COV-2更广泛的研究。MERS冠状病毒和SARS-CoV的疾病演变通过两种不同的机制:免疫病理学和病毒逃避[1]。SARS冠状病毒和MERS-CoV的已显示出诱导细胞因子风暴的结果在免疫系统激活的正反馈回路变得独立病毒载量[14-16]。人细胞的转染与含有任一的SARS冠状病毒-1激活PKC的各种同种型和降低(ENaC的)阿米洛利敏感上皮钠通道的活性的S或N蛋白的质粒[17],其可能妨碍肺泡水肿的清除率和恶化该疾病的结果[18]。此外,SARS冠状病毒和MERS-CoV的利用多种机制逃避宿主的免疫检测[1]。SARS冠状病毒和MERS-CoV的复制在缺乏模式识别受体(效绩报告)囊泡[19,20]。此外SARS冠状病毒和MERS-CoV的产生随效绩报告[下游信号级联干扰几种蛋白1]。最后,有证据表明,SARS冠状病毒和MERS-CoV的可以分别抑制I型干扰素的通过SARS-CoV的PLpro和MERS-CoV的PLpro活化[20-23]。SARS-COV-2已经假说认为以类似的方式工作,因为它与SARS冠状病毒和MERS-CoV的密切关系。
Sauerhhering及其同事的这篇论文不仅试图为MERS-CoV提供一种可能的治疗方法,而且还对他们提出的治疗方法——环孢素a的作用机制提供了有价值的见解。
环孢菌素A(CSA)是从真菌中分离多孔木霉1971年,1983年进入医疗领域目前,CsA在美国和大多数西方国家被广泛使用。在美国,CsA被FDA批准用于治疗和预防移植与-host病在骨髓移植和防止排斥反应肾脏,心脏和肝脏移植的。此外,环孢素A被批准用于治疗类风湿性关节炎,以及其他自身免疫相关病症。
CSA已被证明能够抑制体外几个冠状病毒包括SARS冠状病毒和MERS冠状病毒的复制(图。1A)24-26]。下T细胞受体活化后正常条件下,亲环蛋白A(CYP-A)和钙调磷酸酶形成复合物,导致激活的T细胞(NF-AT)的核因子的活化[27,28]。环孢素A的Cyp通过-A的结合和钙调神经磷酸防止NF-AT的激活(施加其免疫抑制作用图。1B)27-29]。环孢素A结合的Cyp-A在其疏水口袋抑制其异构酶的功能,但环孢素A的免疫抑制性质独立于该函数的[三十,31]。环孢素A-的Cyp-A复合物结合钙依赖磷酸酶(T细胞受体的重要下游介质)而不激活它[32],阻断T细胞受体的下游信号传导。此外,环孢素的Cyp-A复合物已被证明是对病毒复制的抑制必需在几个病毒和Sauerhhering和同事提供关于参与的复杂的[此功能的机构的见解33]。CYP-A具有相似的结构的其它亲环和CSA确实形成复合物与它们并影响不同的机制和细胞功能。一个重要的例子是结合的Cyp-d。环孢素A结合到的Cyp-d预防应激条件下的细胞死亡通过抑制线粒体通透性转换孔(MPTP),病理生理学事件胁迫条件下引发的开口(图。1C)27]。
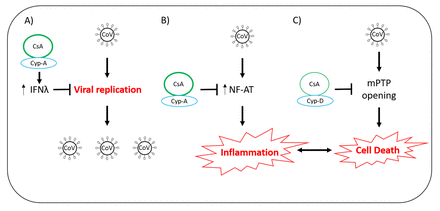
环孢素A(CSA)和冠状病毒的相互作用的示意性概述。一个)的CsA结合于亲环素A(CYP-A)和干扰素上调拉姆达(IFNλ)哪些块病毒复制。B)冠状病毒激活的活化T细胞(NF-AT),其触发炎性细胞因子的释放并引起炎症的核因子。环孢素A-的Cyp-A复合物防止了激活NF-AT减少炎症。c)中冠状病毒引起线粒体通透性转换孔(MPTP),其导致细胞死亡的异常开口。环孢素A在复合体与亲环d(CYP-d)防止的MPTP减少细胞损伤和细胞死亡的开口。
已经发现SARS-CoV的非结构蛋白1可以通过NF-AT诱导IL-2的产生[34,35]。环孢素A已经显示出抑制显著IFN-γ,IL-4,和IL-17从记忆T细胞生产体外在执行后24小时内[36]。这些化合物也抑制T细胞分化成Th1细胞,Th2细胞,和Th17子集,即使在低浓度的6天内使用体外协议 [36]。
首次演出作者环孢素A治疗不仅抑制MERS冠状病毒复制体外但也在鼠体内体内模型。此外,体内建模利用表明改善疾病的结果。这些结果本身是非常重要的。据我们所知,这是第一位体内研究显示对任何高致病性冠状病毒复制的抑制作用。这一发现非常重要,因为它提供了实验证据,证明亲环素抑制剂和CsA不仅在an的孤立设置中是有效的体外设置而且在整个动物的复杂的设置。环孢素处理后呈现肺病理学的减轻成功指示的CsA对MERS-CoV的和潜在的其他冠状病毒的潜在治疗用途。
作者还对CsA的作用机制提供了重要的见解。他们表明,干扰素调节因子1-干扰素lamda (IRF1-IFN -生成物)信号通路的激活对CsA的MERS-CoV抗病毒作用至关重要。IRF1-IFN交互信号轴是一个被广泛研究的途径,已被证明与抗病毒机制有关,尤其是在流感宿主防御中,该途径的故障与病毒感染到慢性感染的进程有关[37,38]。使用的合适组合体内和体外实验研究者发现环孢素上调的IRF1,IFNλ信号通路体内。体外他们发现,抑制IRF1-IFN信号通路阻断了CsA的抗病毒特性,并允许病毒复制。
展望未来,以调查是否改善这将是有趣体内这项研究的结果不仅是由于作者深入研究的抗病毒作用,而且还由于细胞因子风暴的下调,这在冠状病毒感染中是明显的。这项研究的一个可能工具是转基因鼠模型(Ifnlr1- / -和IFNAR1- / -)当前使用的流感研究[37]。CsA是对抗细胞因子风暴的一种适当对策,在许多疾病,特别是ndary噬血细胞性淋巴组织细胞增多症(SHL) [39-41]。此外,该试剂的给药时间的确定是很重要的:早期施用可能使主机易受细菌感染,这是众所周知的显著提高死亡率。政府后来在疾病,可以将细胞因子风暴的发生限制,这有助于从冠状病毒感染的死亡率。即,在感染过程中和之前或“细胞因子风暴”的CsA期间如何早期应适用。
在考虑对环孢素A人体临床试验治疗COVID-19,成本的仔细评估/收益应该发生给出的各种副作用,包括易感性增加感染,恶心,呕吐等癌症发展的触发[42]。此外,环孢素A的气雾化给药已被提出作为在肺移植患者一个闭塞性细支气管炎综合征(BOS)的治疗或潜在的预防性措施[43,44]。这些临床试验的结果提供了有趣的见解和已经表明,当作为气雾剂给药的CsA几乎没有或没有全身毒性。考虑到从疾病的呼吸系统并发症COVID-19的急性生活threating方面,直接的本地应用程序可能是有意义的。然而,这种方法有一个潜在的缺陷。该病毒具有肺系统外的几个水库。环孢素A的本地应用程序可能无法有效地打击这些病毒的水库,导致不可预见的并发症。这也将是确定更具体的目标和治疗药物靶向IRF1,IFNλ信号通路是有用的。这是现在更要归功于由Sauerhhering和他的同事提出的机制非常重要的工作。
考虑MERS冠状病毒,SARS冠状病毒和SARS-COV-2之间的亲属关系,这项研究是在当前COVID-19大流行极其相关。作者提供了有用的见解行动和打击冠状环孢素A的可能的治疗作用的机制。虽然,环孢素A目前尚未批准用于SARS-CoV的2例的用,本研究权证的结果更仔细的调查和临床前研究到尽可能使用环孢素A的对抗COVID-19的治疗剂。
致谢
这项工作得到了抵消计划、美国国立卫生研究院主任办公室(NIH OD)、美国国家神经疾病和中风研究所(NINDS)和美国国家环境健康科学研究所(NIEHS)的支持,批准编号为5UO1 ES026458;3 uo1 ES026458 03 s1;到SM
脚注
支持声明:环境健康科学研究所;DOI:http://dx.doi.org/10.13039/100000066;格兰特:3UO1 ES026458 03S1, 5UO1 ES026458 5UO1 ES027697
利益冲突:MOLYVDAS博士没有透露。
利益冲突:Matalon博士没有透露。
- 收到2020年6月24日。
- 公认2020年7月20日。
- 版权所有©ERS 2020
这篇文章是开放存取并根据知识共享188滚球软件署名非商业许可证4.0的条款分发。