文摘
问题解决的研究2019做三冠状病毒病(COVID-19)疫苗诱导肺移植受者的血清学反应?
方法我们回顾性包括1071名成年人(551人(52%)的男性)在法国九点移植中心。每个收到三个COVID-19疫苗剂量2021年,肺移植。anti-spike蛋白免疫球蛋白反应,定义为一个滴定度> 264 BAU·毫升−1后第三个剂量(中位数(四分位范围(差))3.0(1.7 - -4.1)个月),是主要的结果和不良事件是次要的结果。年龄中位数(差)在第一次疫苗剂量是54(40 - 63)年,中值(差)从移植到第一剂量是64(30 - 110)个月。
结果中值(差)随访后第一剂量为8.3(6.7 - -9.3)个月。开发的疫苗反应173例(16%)患者。独立因素与响应在疫苗接种年轻,时间从移植到疫苗接种和没有皮质类固醇或霉酚酸治疗。疫苗接种后,51例(5%)患者(47无(47/898(5%))和4(4/173(2%))反应)经验丰富的COVID-19,值(差)为6.6(5.1 - -7.3)个月后第三个剂量。没有急救员严重COVID-19与15无相比,其中6人死于这种疾病。
结论一些肺移植受者实现血清学反应三个COVID-19疫苗剂量,表明需要其他防护措施。年龄和使用霉酚酸或皮质类固醇与缺乏反应。COVID-19发病率较低,可能反映了疫苗的保护通过细胞免疫和/或好坚持屏蔽措施。
文摘
三个信使rna COVID-19疫苗剂量很少诱导肺移植患者的血清学反应。COVID-19是罕见的,这表明细胞免疫和/或强烈坚持屏蔽措施。应该寻求其他保护方法。https://bit.ly/3pr9Wox
介绍
2019年全世界重复一波又一波的冠状病毒病(COVID-19)由于严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)需要紧急努力优化疫苗反应免疫功能不全的患者,包括肺移植受者。在法国,这个群体是最早被接种,从2021年1月开始,两个信使rna COVID-19疫苗批准欧洲药品局:mRNA BNT162b2 (Comirnaty;Pfizer-BioNTech)和信使rna - 1273 (Spikevax;现代化)。这两个non-mRNA COVID-19疫苗,ChAdOx1 nCoV-19 (Vaxzevria;AstraZeneca-Oxford大学)和Ad26.COV2。年代(詹森;詹森),后被批准和使用。
最近的报告显示,住院更高的死亡率比非移植患者移植受者调整后并发症。在法国匹配病例对照研究比较非移植病人肾移植受者和的结果,所有人都承认,COVID-19严重COVID的30天的累计发生率两组之间没有差别,而30天死亡率明显高于移植组(17.9%)与分别为11.4%;p = 0.038);然而,通过多变量分析,肾移植并不是独立与死亡率(1]。482年一个国际群移植病人,COVID-19整体死亡率为20.5%,但在30 33%肺移植受者(2]。在法国的35肺移植受者COVID-19经历的头几个月大流行期间,通常需要住院和死亡率为14.3%3]。这些数据支持国际社会的强烈建议心脏和肺移植接种所有移植候选人和接受者,尽管这些排斥从COVID-19疫苗试验的所有阶段4,5]。
数据COVID-19疫苗反应实体器官移植受者出现(6- - - - - -10),大多数研究使用的生产anti-spike或anti-receptor绑定域作为疫苗功效的标记的抗体。这些病人被证明能够生成一个健壮的体液反应自然SARS-CoV-2感染,78%的测试阳性抗体> 3个月后诊断(6]。然而,在一些研究只有40 - 69%积极血清学测试三剂COVID-19疫苗后(7- - - - - -13]。响应COVID-19疫苗可能不同器官移植的类型和数据显示的子群与肺移植仍然是稀疏的11,12]。在先前的研究中,需要注射两剂疫苗血清学反应者的比例是62%在心脏移植受者但只有36%在肺移植受者,反映肺移植后免疫抑制的更大的强度需要(11]。虽然疫苗功效的评价通常依靠血清学,体液和细胞反应,进一步的信息和临床的有效性,在肺移植受者COVID-19疫苗需要制定最佳接种指南。法国是第一批国家推荐助推器剂量在免疫功能低下的患者,包括移植受者,早在2021年4月,根据初步的证据,一个贫穷的前两个反应剂量(14- - - - - -17]。
本回顾性观察性队列研究的目的是评估的蛋白质免疫球蛋白抗体反应和临床保护提供的三个信使rna COVID-19疫苗在肺移植受者。
方法
研究设计和人口
我们进行了一项多中心回顾性观察性队列研究。三个剂量的患者COVID-19疫苗批准在法国被包括在2021年1月1日和2021年8月31日之间。参与者招募九点肺移植中心属于Groupe de阵痛de法国Pneumologie移植de la法国所有的肺移植中心组成的一个网络参与生物医学研究项目在法国。排除标准是年龄< 12年,移植前免疫接种,减少或超过三剂疫苗,接种后没有数据SARS-CoV-2抗体水平,COVID-19感染之前接种疫苗或之前与单克隆抗体血清学检测和治疗前SARS-CoV-2血清学测试。病人单克隆抗体作为预防由于SARS-CoV-2疫苗接种失败被保存在研究如果这种治疗方法是血清学测试后交付。
这项研究是按照法国立法进行生物医学研究和《赫尔辛基宣言》。研究伦理委员会批准的协议是法语的法国德Chirurgie Thoracique et Cardio-Vasculaire (IRB00012919)。书面知情同意之前从每个病人获得研究夹杂物。肺移植过程和细节管理COVID-19是可用的补充材料。
数据收集
数据进入一个安全的和匿名的数据库。我们记录人口特性、特点的移植过程中,药物,疫苗的性质和时间,接种疫苗后COVID-19感染的发生,政府的单克隆抗体治疗或预防COVID-19。维护免疫抑制疗法的疫苗接种是收集,以及是否强化免疫抑制了前6个月内接种疫苗。后续的研究是2021年12月31日结束。
协议和疫苗接种反应评估
从2021年1月开始,所有的法国肺移植中心实施积极的策略,提供合格的肺移植受者COVID-19疫苗接种。由于最初所需的高水平的免疫抑制,第一次疫苗剂量没有早于肺移植后3个月。三个剂量给法国的建议后,至少4周剂量之间的间隔(18]。截止256年绑定抗体单位(BAU)·毫升−1被法国卫生部门分离从无反应者19),基于血清学和临床数据从一个英国阿斯利康疫苗试验做过变体的出现(20.]。符合法国的建议(18滴定度51至264患者,BAU·毫升−1收到第四个疫苗剂量BNT162b2 mRNA辉瑞疫苗的组成;这个剂量的反应并没有研究在当前的研究。患者滴定度≤50 BAU·毫升−1提供对COVID-19单克隆抗体治疗。
SARS-CoV-2突起蛋白免疫球蛋白抗体检测
血液样本收集本地3周,6个月后第三个剂量的疫苗。样本分析使用本地可用ce标记酶免疫测定中以下几点:建筑师SARS-CoV-2(美国雅培,芝加哥,IL),联络(DiaSorin、Saluggia、意大利),Elecsys Anti-SARS-CoV-2(罗氏诊断、巴塞尔、瑞士),NovaLisa (NovaTec Immundiagnostica, Dietzenbach,德国),访问SARS-CoV-2免疫球蛋白(美国贝克曼库尔特,沥青,CA)和Atellica IM SARS-CoV-2(西门子、德国慕尼黑)。所有化验使用和结果转换为BAU·毫升−1如果需要,根据制造商的指示。
结果测量
主要结果是患者的比例飙升蛋白免疫球蛋白抗体滴定度≥264 BAU·毫升−1。
次要结果COVID-19患者的比例,定义为一个积极的鼻咽癌SARS-CoV-2 PCR测试后第三个剂量的疫苗。测试了当时已知的接触病人COVID-19或者当症状符合COVID-19发达。温和COVID-19被定义为肺炎临床症状(发热、咳嗽、呼吸困难、呼吸率高)没有严重肺炎的迹象,特别是与外围血氧饱和度(年代阿宝2室内空气)≥90%。严重COVID-19被定义为肺炎的临床体征加上至少以下之一:呼吸速率> 30次·分钟−1严重的呼吸窘迫和/或年代阿宝2室内空气< 90%。关键COVID-19被定义为急性呼吸窘迫综合征的存在(21]。
统计分析
连续变量被Shapiro-Wilk测试显示有一个偏态分布,因此称为中位数(四分位距(差)和比较两组之间与没有疫苗反应使用Mann-Whitney紫外线测试。被描述为分类变量数(百分比)和通过应用卡方测试相比,与蒙特卡罗模拟计算< 5时。
健壮的Bianco-Yohai过程选择构建一个多变量逻辑回归模型旨在确定疫苗反应的相关因素。向后和向前逐步选择应用于单变量方差分析变量与p值< 0.10。优势比和95%置信区间计算。所有的测试是双面的,假定值< 0.05被送往显示显著差异。进行了统计分析使用R版本3.6.1 (www.r-project.org)。
结果
病人
图1显示病人流程图。1月至2021年8月,2458名患者筛选1071 9参与中心和患者纳入研究(表1)。夹杂物的分布在中心是:Le Plessis-Robinson n = 218 (20%)、Suresnes n = 208(19%)、斯特拉斯堡n = 170(16%),马赛n = 112(10%)、南特n = 109 (10%)、Paris-Bichat n = 97(9%)、波尔多n = 65 (6%)、Paris-Cochin n = 63(6%)和格勒诺布尔n = 29 (3%)。补充表S1报告主要包括和排除患者之间的差异。
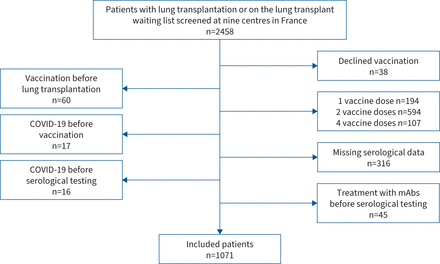
病人流程图。马伯:单克隆抗体。
突起蛋白免疫球蛋白反应(主要结果)
的1071患者中,173例(16%)有一个抗体反应所定义的滴定度> 264 BAU·毫升−1。表1比较了反应者无的主要特点。子群的人员,年龄在疫苗接种是年轻,更多的病人有囊性纤维化肺移植的原因,减少维护免疫抑制患者糖皮质激素和霉酚酸,和更少的患者接受强化在6个月前第一次疫苗剂量免疫抑制。
的细节的时候anti-spike免疫球蛋白化验总人口和子组定义为从肺移植到疫苗接种了补充图S1。随着时间的推移抗体滴定度没有下降。早在子群接种肺移植后,抗体滴定度会随着时间的推移而增加,或许是由于免疫抑制剂治疗强度下降。
表2给疫苗接种协议和血清学测试方法的细节。肺移植是大大延长的时间比无反应者。大多数病人收到一封信使核糖核酸疫苗。
与疫苗相关的因素的反应
表3报告的结果进行单变量和多变量分析来识别抗体反应的相关因素。通过多变量分析,年轻在疫苗接种,时间从肺移植到疫苗接种和不服用皮质类固醇或抗代谢物治疗明显、独立与抗体反应有关。
COVID-19感染和其他活动
中值(差)随访8.3(6.7 - -9.3)个月后第一次疫苗剂量。没有病人失访。777名患者滴定度≤50 BAU·毫升−1第三个疫苗剂量后,221例(28%)有对COVID-19单克隆抗体治疗。COVID-19后发生第三个51例(5%)患者的疫苗剂量:47无和四个反应者,无显著差异(p = 0.12)。47中无经历过COVID-19感染,没有检测到26日anti-spike免疫球蛋白抗体和中值(差)滴定度其余21患者31日(10 - 65)BAU·毫升−1。病情严重,关键在8个和七无分别;没有急救员严重或重要的疾病。六无,都有至关重要的疾病,死于COVID-19,收益率13%的死亡率(6/47)与没有反应相比,虽然差异无统计学意义(表2)。这13%死亡率低于29%的17个病人经历过COVID-19接种疫苗,虽然差异无统计学意义(p = 0.14)。没有患者COVID-19在接种疫苗的协议。
COVID-19患者的比例明显高于的患者被排除在外,因为他们收到了没有,一个或两个疫苗剂量比研究中患者(14%与5%;p < 0.001),而两组的死亡率相似(14%;p = 0.25)。
的1071名患者,12人死亡。除了COVID-19的六名病人死亡,两名患者死于慢性肺部同种异体移植物功能障碍和肺栓塞,肺癌,肾衰竭和感染性休克。
安全
疫苗安全信息收集回顾在每个移植中心。症状主要发生在3天内第二次注射后被认为是与疫苗有关。大多数与疫苗相关的症状发生在第二次注射,温和,最常见的是疲劳(25%)、头痛(16%)、发烧(11%)和发冷(7%)。没有认真的与疫苗相关的不良事件报告。
讨论
我们报告数据的蛋白质免疫球蛋白抗体反应三剂COVID-19疫苗迄今最大的断代的肺移植受者没有COVID-19的历史。接种疫苗的体液反应很差,只有16%的患者产生保护性的anti-spike IgG抗体水平。临床上,严重COVID-19不发生任何反应。无,有1.7%严重COVID-19随访研究,0.7%的人死于COVID-19。
招聘在多个移植中心参与研究和超过1000名患者的样本大小是我们研究的主要优势。没有COVID-19史的患者或anti-SARS-CoV-2抗体疫苗接种前处理,或抗体治疗前血清测试,都包括在内。所有的研究中心使用了相同的接种疫苗的协议。我们的研究没有对照组的健康成人接种疫苗。也没有比较的对照组未接种疫苗的肺移植受者的临床事件,疫苗接种建议所有免疫力低下的个人在法国。Anti-spike免疫球蛋白抗体,但不是中和抗体或记忆t细胞反应,进行了调查。然而,anti-spike免疫球蛋白滴定度与几何平均的中和抗体滴定度密切相关22]。因为患者检测COVID-19只在发生记录接触或兼容的症状,我们可能错过了病例无症状COVID-19。症状的发展,然而,最令人担忧的是,考虑到非常密切监测提出肺移植受者在法国,有症状的情况下很可能已经错过了。虽然anti-spike IgG抗体滴定度与中和抗体,没有阈值或关联的保护已经建立的变异问题。低水平的中和抗体已报告与变异与祖先的应变(23]。抗体滴定度和疾病严重程度之间的相关性的数据是缺乏24]。没有改变在264 BAU·毫升−1anti-spike IgG抗体阈值自出现以来一直推荐的变异问题。使用单克隆抗体在四分之一的无COVID-19病例数下降。几种不同的免疫测定品牌被用来确定抗体滴定度。然而,制造商已经建立了标准化的结果(25]。由于ο波的开始,后续2021年12月31日结束,限制我们的能力来诊断后续COVID-19集。最后,接种疫苗的安全协议没有具体评估,尽管没有严重副作用的疫苗记录和移植排斥反应的频率也非常高。
我们的发现与公布的数据是一致的体液反应三个COVID-19疫苗在实体器官移植受者7- - - - - -13)和添加的信息在肺移植受者6,14- - - - - -16),为谁三剂疫苗的效果尚未报道大量的人群。疫苗有效性的标志是通常anti-spike抗体生产(6- - - - - -8,11- - - - - -13,15- - - - - -17),只有一些研究分析anti-receptor绑定域(10,17)和中和抗体(10]。有两个剂量的信使核糖核酸疫苗,肺移植受者的比例实现了血清学反应只在早期研究[10 - 39%11,15,17]。在实体器官移植受者的数量,大多数人接受了肾移植,急救员三个剂量的比例从40%到69%不等(7- - - - - -13]。在我们的群体中,这一比例仅为16%,形成鲜明对比的高比例反应者在最初的临床试验在免疫活性的个人26,27]。两个因素与减少免疫抑制有关,即。自肺移植的时间较长,目前没有接触皮质类固醇或霉酚酸治疗,明显与更好的反应在我们的研究中,虽然我们的研究设计不允许评估潜在的因果关系。治疗与霉酚酸等抗代谢物也与贫穷相关疫苗反应肺移植受者在两个先前的研究(15,16),这表明这些药物的剂量减少在疫苗接种可能提高免疫反应。符合这种可能性,肺移植术后病人的子群接种早有经验的增加anti-spike免疫球蛋白滴定度随时间(补充图印地)。年轻患者更容易实现疫苗反应,符合其他研究的影响mRNA COVID-19疫苗(6,15,16]。
尽管疫苗反应者的比例较低,COVID-19罕见,发生在5%的病人整体而言,5%的无反应者的2%。这种低发病率可能反映了良好的耐心教育,坚持,防护措施如面具戴和手部卫生,除了有限的总发病率COVID-19在研究期间在法国28]。此外,单克隆抗体SARS-CoV-2 25%的无,可能导致减少COVID-19的风险。单克隆抗体的常规使用COVID-19的早期过程中,从2021年6月开始,可能减少重症和死亡病例的比例。最后,提供免疫接种通过除了anti-spike IgG抗体的生产机制。一个健壮的CD8+t细胞反应是记录1周后的第一剂量BNT162b2信使核糖核酸疫苗在免疫活性的医务工作者29日]。重要的是,t细胞反应两剂疫苗后免疫活性的个人类似规模自然感染后所看到的,尽管他们似乎更有区别30.]。虽然没有观察到在我们的人口(补充图S1),接种疫苗后抗体减弱仍然是一个关注(31日]。T记忆干细胞接种疫苗后可能会更长久的发展。然而,严重或致命COVID-19被认为只有在我们的研究中,无建议可能对细胞免疫保护作用。最后,在研究期间,α和三角洲SARS-CoV-2变异成为主流。尽管最近的数据表明,支持者可能会增加有效性对严重ο变体疾病免疫活性的患者(32),我们的研究结果是否适用于当前和新兴变体在免疫力低下的人群还有待调查。
总之,肺移植受者有受损anti-spike COVID-19三剂疫苗免疫球蛋白反应。年龄较大和较强的免疫抑制治疗方案包括霉酚酸或皮质类固醇与未能达到显著相关疫苗的反应。在研究期间,当α和三角洲SARS-CoV-2变异成为主流,COVID-19非常罕见,尽管疫苗的低频响应,和几只在无致命或非致命的严重病例发生。然而,单克隆抗体预防是可能的保护作用,以及我们的研究结果是否适用于当前和新兴的变异还不清楚。进一步的研究需要阐明这些发现,描述的t细胞反应COVID-19细胞免疫疫苗和确定程度有助于保护对COVID-19免疫功能低下的患者。
补充材料
可共享的PDF
确认
我们感谢Stephane Morisset (Stephane Morisset练习曲和咨询、Perouges、法国)统计分析,a·沃尔夫(肖蒙、法国)修订草案和奥拉夫Mercier (Le Plessis-Robinson式玛丽Lannelongue,法国)支持这个项目。
脚注
数据共享:匿名participant-level数据,研究协议和知情同意的形式,和统计分析计划可以从相应的作者在合理的请求,之后研究出版和签名后的数据共享协议。
作者的贡献:g . Dauriat和j·勒Pavec:研究概念和设计;数据的采集、分析和解释;文章起草和修改。l·博蒙特b . Renaud Picard m . Penhouet b . Coiffard m . Salpin x Demant, n .卡莉·j . Messika和a . m .雷诺•高柏Roux:采集、分析和解释数据;文章起草和修改。第2陈德良阮:研究概念和设计;数据的分析和解释;文章起草和修改。c .圣雷蒙德。丹纳和f . Gallais:数据的采集、分析和解释。相应的作者,j . Le Pavec担保人的研究中,接受全部责任的工作和行为研究。 He had access to the data and controlled the decision to publish. The corresponding author also attests that all listed authors meet authorship criteria and that no others meeting the criteria have been omitted. J. Le Pavec takes responsibility for the content of the manuscript, including the data and analysis, and affirms that the manuscript is an honest, accurate and transparent account of the reported study and omits no important aspects of the study. No discrepancies from the original study protocol occurred.
利益冲突:没有任何作者。
- 收到了2022年3月10日。
- 接受2022年8月11日。
- 版权©2023年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org











