文摘
Dupilumab是良好的耐受性,提高哮喘患者的临床结果和高嗜酸性粒细胞·µL(≥500细胞−1)。改善临床结果与嗜酸性粒细胞计数,展示在那些高嗜酸性粒细胞dupilumab功效。https://bit.ly/3Jxvicb
编辑器:
不受控制,严重哮喘患者高基线·µL血嗜酸性粒细胞(≥500细胞−1)很难治疗1]。全球倡议对哮喘指南建议作为插件生物制剂治疗2型炎症严重哮喘患者,依然不受控制,尽管大剂量吸入糖皮质激素治疗(2]。代理标记2型炎症,如水平升高的血或痰嗜酸性粒细胞和部分呼出一氧化氮(F伊诺)可以用来识别患者2型签名谁可能有资格获得这样的待遇(1- - - - - -3]。现在已经出现了一些生物制剂这一目标不同的分子2型炎症通路,特别是IgE和2型细胞因子(1- - - - - -3]。dupilumab,其中一个是一个完整的人VelocImmune-derived [4,5单克隆抗体,块共享受体组件interleukin-4和-13年,细胞因子是关键和中央司机2型炎症的多种疾病,因此抑制他们的信号6,7]。
在第三阶段自由哮喘探索研究(NCT02414854),附加dupilumab 200毫克和300毫克每2周与匹配的安慰剂显著降低严重哮喘急性加重和改进pre-bronchodilator用力呼气量在1 s (FEV1)在整个人口的不受控制的患者,严重哮喘(8]。在这方面,和其他的研究,这些好处的大小是更大的子组的患者2型签名(嗜酸性粒细胞≥150·µL或≥300细胞−1和/或F伊诺≥25磅或≥50磅)8- - - - - -12]。哮喘控制、评估使用patient-reported 5-item哮喘控制问卷(ACQ-5),与dupilumab也显著提高与安慰剂患者基线嗜酸性粒细胞计数升高(10]。此外,dupilumab是有效地降低2型两气道炎症生物标记(F伊诺)和血液隔间(血清胸腺和activation-regulated趋化因子和血清IgE) (8,10,11]。然而,患者的疗效和安全性的dupilumab高嗜酸性粒细胞水平·µL(≥500细胞−1)是不清楚。
在这个事后分析,我们评估的有效性dupilumab在病人参加探索基线·µL血嗜酸性粒细胞≥500细胞−1。探索阶段3,随机,对照试验,评估的有效性和安全性dupilumab≥12岁的病人不受控制,严重哮喘(8]。探索开放的病人不管最低基准血嗜酸性粒细胞计数或任何其他生物标记的要求。病人被随机2:2:1:1接收与皮下dupilumab 52周的附加治疗剂量200毫克和300毫克每2周或matched-volume安慰剂(分别为1.14毫升或2.00毫升)为每一个活跃的剂量。研究符合赫尔辛基宣言和国际会议协调良好的临床实践指南,并由当地机构审查委员会或伦理委员会批准。之前所有的病人提供书面知情同意参加试验。
分析中的疗效端点折合成年率的严重恶化在治疗期间,意味着改变pre-bronchodilator FEV的基线1随着时间的推移,和改变基线ACQ-5分数在52周的小组基线患者血液嗜酸性粒细胞·µL≥500细胞−1。年化严重的恶化率测定使用负二项模型。最小二乘均值变化pre-bronchodilator FEV的基线1和ACQ-5值来自一个线性混合效应模型与重复的措施。样条回归分析进行整体意向处理(ITT)寻求人口评估治疗的效果通过基线嗜酸性粒细胞计数年严重的恶化率和变化在pre-bronchodilator FEV基线1在12周,52。
ITT公司追求人口由1902名患者。其中,436名(23%)基线≥500个细胞·µL嗜酸性粒细胞计数−1(145随机dupilumab 200毫克每2周,76安慰剂匹配dupilumab 200毫克,141 dupilumab 300毫克每2周和74安慰剂匹配dupilumab 300毫克)。基线人口统计学和临床特征比较四个治疗组。患者的平均年龄范围从46.0到49.0年在治疗组,-63.1%和48.7%是女性。严重发作的平均数量在去年从2.3到2.6不等,基线pre-bronchodilator FEV1从1.70到1.72 L和ACQ-5分数从2.7到2.8在治疗组。基线值水平(四分位范围)的血液嗜酸性粒细胞和基线F伊诺在治疗组范围从690.0(600.0 - -950.0),795.0(630.0 - -1030.0)细胞·µL−1从35.0(22.0 - -61.5)到十亿分之42.5(29.0 - -72.5),分别说明,确认,2型签名的病人。
患者血液中嗜酸性粒细胞·µL≥500细胞−1在基线,dupilumab 200毫克和300毫克每2周与安慰剂显著降低严重恶化了74%和71%,分别(均p < 0.0001与匹配的安慰剂)(图1一个),改善pre-bronchodilator FEV1在52周0.37 L L (95% CI 0.26 - -0.49)和0.30 (95% CI 0.18 - -0.42),分别(p < 0.0001)。所述其他dupilumab研究[8- - - - - -12),FEV的改善1快速,显著差异与安慰剂实现早在第一个评价在2周,然后被持续在52周治疗期的剂量(p < 0.0001与匹配的安慰剂在所有时间点)(图1 b)。样条回归分析显示,对dupilumab剂量,估计的严重发作减少和改善pre-bronchodilator FEV1在12周,52岁的基线水平的增加而增加血液嗜酸性粒细胞(图1 c和d)。哮喘控制,使用ACQ-5评估,也大大改善了52周与安慰剂(最小二乘的意思是改变从基线−0.59 (95% CI -0.88−0.30)和−0.62 (95% CI 0.92−-0.33),分别;p < 0.0001与匹配的安慰剂),实现最小临床重要差异0.5 [13剂量)。
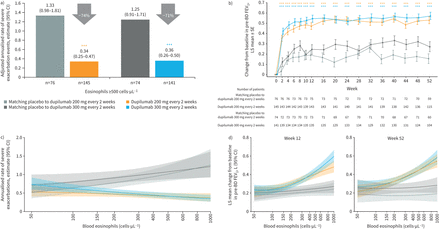
)年严重恶化率在治疗期间和b)最小二乘(LS)意味着改变从基线pre-bronchodilator (pre-BD)在1 s (FEV用力呼气量1随着时间的推移)患者血液中嗜酸性粒细胞·µL≥500细胞−1在基线。c)年严重的恶化率和d) LS意味着改变pre-BD FEV的基线1在整个意向处理人口基线嗜酸性粒细胞计数。* * *:p < 0.001。
不良事件的发生率相近dupilumab——而接受安慰剂的不受控制的严重哮喘患者血液嗜酸性粒细胞·µL≥500细胞−1在基线。最常见的治疗诱发不良事件报告整体在这些患者病毒性上呼吸道感染(20.2%)、注射部位反应(20.0%),上呼吸道感染(12.8%)和支气管炎(12.2%)。患者血液中嗜酸性粒细胞·µL≥500细胞−1,治疗嗜酸性粒细胞(定义为> 3000个细胞·µL−1)据报道10.3%和9.2%的患者接受200和300毫克dupilumab,分别由<匹配的安慰剂组3%的患者。嗜酸性粒细胞升高和临床症状没有联系;一个28 dupilumab-treated患者嗜酸性粒细胞发达与polyangiitis嗜酸性肉芽肿病。
哮喘患者高血嗜酸性粒细胞计数经历更严重的恶化和哮喘差控制;此外,这种关系是连续和线性与哮喘恶化结果逐步增加基线嗜酸性粒细胞计数(14]。发现样条回归分析同意文学,显示dupilumab福利基线嗜酸性粒细胞浓度增高而增强。与之前的数据显示,改善恶化率的大小,肺功能和哮喘控制dupilumab治疗与安慰剂的患者2型签名(更大8- - - - - -12),这里给出的数据表明,dupilumab可能提供最大的利益高2型患者签名,虽然结果进行解释时应特别谨慎,这是一个事后分析。尽管有这样的限制,数据还表明,嗜酸性粒细胞计数基线临床实用程序在指导治疗通过识别患者可能从dupilumab治疗中获益。
可共享的PDF
确认
作者感谢阿曼Altincatal统计支持。医学写作/编辑艾琳·麦克卢尔提供的援助是卡罗尔,博士的摘要,是由赛诺菲安万特Genzyme Regeneron制药,Inc .,根据良好的出版实践指南。
脚注
这是前瞻性临床试验注册在ClinicalTrials.gov标识符NCT02414854。合格的研究人员可能请求访问病人的水平数据和相关研究文档,包括临床研究报告,研究协议与任何修正案,空白的情况下报表,统计分析计划和数据规范。将匿名病人水平数据,研究文件将会修订保护试验参与者的隐私。进一步的细节在赛诺菲的数据共享标准,符合条件的研究,并用于请求访问的过程可以发现:http://www.clinicalstudydatarequest.com/
利益冲突:K.F.瑞芭是一个顾问和发言人费收到阿斯利康,勃林格殷格翰集团、诺华、赛诺菲和梯瓦。身份证Pavord收到Aerocrine AB,议长费Almirall,阿斯利康,勃林格殷格翰的发言,基耶西,葛兰素史克公司,诺华和梯瓦;收到支付从阿斯利康和梯瓦组织教育活动;收到Almirall咨询费,阿斯利康,勃林格殷格翰的发言,奇切尔克西亚,戴伊制药,基因泰克,葛兰素史克,Knopp生物科学,默克,默沙东,Napp制药、诺华Regeneron制药、Inc . RespiVert,赛诺菲,先灵葆雅和梯瓦;收到阿斯利康的国际科学会议赞助,勃林格殷格翰的发言,基耶西,葛兰素史克(Napp制药和梯瓦;收到基耶西的研究经费;和顾问Regeneron制药公司和赛诺菲。m·卡斯特罗接受研究来自美国肺脏协会的支持,阿斯利康、葛兰素史克、NIH,诺华,PCORI, Pulmatrix,赛诺菲-安万特和赢家;基因泰克公司的顾问,诺华公司,赛诺菲-安万特和梯瓦;议长费收到阿斯利康,基因泰克,葛兰素史克,Regeneron制药、公司,赛诺菲和梯瓦; and received royalties from Elsevier. M.E. Wechsler reports personal fees from AstraZeneca, Boehringer Ingelheim, Equillium, Gala Therapeutics, Genentech, Genzyme, Mylan, Novartis, Pulmatrix, ResTORbio, Regeneron Pharmaceuticals, Inc., Sentien Biotechnologies and Teva; and grants and personal fees from GlaxoSmithKline and Sanofi. N. Daizadeh, U. Kapoor, R.R. Johnson, P.J. Rowe and J.A. Jacob-Nara are employees and may hold stock and/or stock options in Sanofi. B. Ortiz, A. Radwan and Y. Deniz are employees and shareholders of Regeneron Pharmaceuticals, Inc.
支持声明:本研究是由赛诺菲和Regeneron制药、公司融资信息本文已沉积的Crossref资助者注册表。
- 收到了2021年9月27日。
- 接受2022年3月17日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org















