文摘
背景治疗的长期疗效和安全性mepolizumab严重嗜酸性的哮喘。在这里,我们审查临床长期使用mepolizumab之后的影响。
方法彗星(NCT02555371)是一个随机、双盲、安慰剂对照、多中心研究与这些相应平行的组织。患者完成了鸽属(NCT01691859)或COSMEX (NCT02135692)和接收连续mepolizumab治疗≥3年随机1:1停止(切换到安慰剂)或持续皮下mepolizumab 100毫克每4周为52周。主要终点:时间第一临床显著的恶化;二次端点:时间先恶化需要住院/急诊服务、时间减少哮喘控制(≥0.5分提高哮喘控制Questionnaire-5得分从彗星基线)和血液嗜酸性粒细胞计数比彗星基线。安全评估。
结果病人停止(n = 151)与继续(n = 144) mepolizumab显著短时间先临床上显著的恶化(风险比为1.61,95%可信区间1.17 - -2.22;在哮喘控制(p = 0.004),减少风险比为1.52,95%可信区间1.13 - -2.02;p = 0.005),和更高的血液嗜酸性粒细胞计数在52周(270与40细胞·µL−1;比(停止与继续)6.19,95%可信区间4.89 - -7.83;p < 0.001)。组之间的疗效差异的结果观察到当评估从第12周(16周后最后mepolizumab剂量)。发作需要住院/急诊服务还很少。不良事件的患者继续mepolizumab是与先前的研究一致。病人停止mepolizumab,安全性与其他嗜酸性哮喘的数量是一致的。
结论病人停止mepolizumab发作的增加和减少哮喘控制与那些仍在继续。
文摘
这个随机研究表明增加恶化风险和减少哮喘控制严重嗜酸性哮喘患者停止mepolizumab治疗长期使用后,相比那些继续治疗。https://bit.ly/3fsxGV2
介绍
长期治疗的有效性和安全性目标,人性化,anti-interleukin 5 (IL)单克隆抗体mepolizumab严重嗜酸性哮喘患者证明长达4.5年以前的双盲(1- - - - - -5)和开放的研究(6- - - - - -8]。Mepolizumab被批准用于治疗严重嗜酸性哮喘全球多个地区,和治疗嗜酸性肉芽肿病polyangiitis成人在美国和日本和治疗≥12岁hypereosinophilic综合症的病人在美国(9,10]。IL-5 Mepolizumab选择性结合,抑制嗜酸性粒细胞的炎症反应(11,12];然而,目前未知是否气道嗜酸性的抑制炎症反应与mepolizumab严重嗜酸性哮喘持续如果患者停止治疗,或长期治疗是否应该建议持续的疾病控制。
之前的12个月观察患者的随访研究停止mepolizumab 750毫克静脉注射治疗后1年建议增加血液嗜酸性粒细胞计数预处理水平和随后回到一个加剧表型(13]。感兴趣的理解反应停止后,作为长期治疗或许有持续的疾病修饰作用,并可能永久减少嗜酸性粒细胞计数(14]。然而,没有数据的影响停止患者mepolizumab > 1年,这是很重要的,因为短期停药可能需要对一些病人在临床实践中。此外,没有数据的影响停止授权mepolizumab剂量在成人和青少年,100 mg皮下注射。
的目的随机、安慰剂对照研究评估的临床影响停止mepolizumab 100毫克南卡罗来纳州。在严重嗜酸性哮喘患者长期(≥3年)暴露评估恶化率和其他临床参数那些停止mepolizumab(和转向安慰剂)与那些仍在继续。彗星的视觉摘要研究提出了补充图E1。
材料和方法
研究设计
彗星(GSK ID 201810;NCT02555371)是一个全球性、多中心、随机、双盲、安慰剂对照,与这些相应平行的组织研究比较停止与继续长期mepolizumab治疗嗜酸性哮喘患者严重。
这项研究由四部分(图1)。筛选后,患者< 3年mepolizumab治疗进入一个部分,一个变量非盲磨合过程的0 - 132周为了确保所有病人收到连续mepolizumab 100毫克南卡罗来纳州。(除了标准治疗)≥3年。一旦患者≥3年mepolizumab接触他们进入了B部分,由4 - 8周的固定的非盲试车期间开放mepolizumab(100毫克南卡罗来纳州。每4周+标准治疗)是管理和基线信息收集。患者≥3年mepolizumab治疗直接筛选进入B部分。B部分后,病人被随机1:1停止mepolizumab治疗和切换到安慰剂(加上标准)或接收继续mepolizumab 100毫克南卡罗来纳州。每4周+标准治疗52周(C)部分。一个或多个患者临床上显著的恶化(补充材料)在部分C被研究人员评估确定病人是否应该继续采取双盲研究治疗(C)部分中继续或恢复开放mepolizumab 100毫克南卡罗来纳州。每4周(切换到D部分;可选的,看到补充材料)研究的其余部分post-randomisation(52周)。没有正式的标准治疗继续向调查人员提供;这个决定是基于的意见治疗医生与患者合作。病人保持在一个稳定的标准治疗哮喘治疗从一开始的B部分研究结束的。报告结果主要集中在盲、随机部分C。
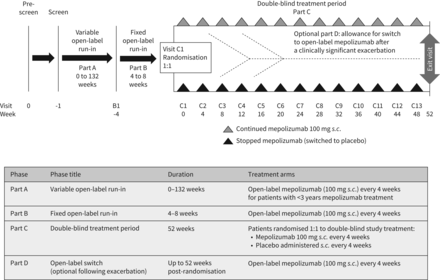
研究设计和描述个人的研究部分。
这项研究是按照国际会议上进行协调好临床实践,所有适用的病人隐私需求,指导原则的当前版本的《赫尔辛基宣言》。之前所有的病人提供书面知情同意参与研究。
病人
严重的嗜酸性哮喘患者完成了前面的开放性研究,鸽属(MEA115666;NCT01691859)[7]或COSMEX (201312;NCT02135692)[8彗星),都有资格(补充材料)。进入研究中,患者必须完成和接受连续mepolizumab治疗(即。没有治疗缺口> 12周(84天,相当于至少两个连续错过剂量)之间的任何两个mepolizumab剂量),和仍然附着在哮喘控制药物/治疗,在前面的非盲mepolizumab研究。
排除标准,随机进入标准C和细节部分中列出的随机和致盲补充材料。
端点和评估
主要终点是时候第一临床显著恶化期间部分C (post-randomisation)。二级终端第一恶化时间需要住院或急诊(ED)访问;时间减少哮喘控制,定义为从基线(双盲治疗开始在彗星)在哮喘控制问卷(ACQ) 5评分≥0.5个单位15];和比基线血液嗜酸性粒细胞计数在12周,24岁,36岁和52岁。其他终端包括第一恶化需要住院时间,意味着从基线ACQ-5分数评估每4周,直到52周,意味着改变基线健康相关的生活质量(如评估圣乔治呼吸问卷(SGRQ)总分)和诊所pre-bronchodilator用力呼气量在1 s (FEV1)在12周,24岁,36岁和52岁。安全终端包括不良事件和严重不良事件,临床实验室参数,12导心电图参数和生命体征。
样本大小和统计分析
样本大小是基于时间第一临床显著恶化的主要终点测试持续mepolizumab治疗的优越性而停止mepolizumab(随机安慰剂)。
intent-to-treat人口,用于所有疗效和安全性数据分析,包括所有随机双盲研究的病人一个或多个剂量治疗。所有改变/比基线端点,基线被定义为双盲治疗开始的(随机)彗星。只有C部分的相关数据被包含在双盲分析周期,停药后的治疗数据审查双盲治疗或切换到非盲mepolizumab在d .进一步的细节部分中提供的样本大小和统计分析补充材料。此外,一个事后分析评估患者基线特征是否能识别更大或降低治疗效果后停止或继续长期mepolizumab治疗和进一步的信息可以在找到补充材料。
结果
患者人群
从先前的研究显示在病人的性格补充图E2。2016年1月至2017年11月,306名患者参加部分A / B和295名患者被随机部分C(安慰剂n = 151;mepolizumab n = 144) (补充图E3)。其中,129名患者,84谁收到了安慰剂部分C和45收到mepolizumab部分C转向非盲mepolizumab (D)部分后哮喘恶化(补充图E4);开关在两组最常见的原因是一个报道缺乏有效性的意见调查(n = 81和n = 42个,其中n = 81和n = 41报道恶化subreason,分别)。这项研究是在2019年7月完成。
人口和疾病特征在第一部分C访问之间相似的安慰剂,mepolizumab组(表1)。几何平均血嗜酸性粒细胞计数两组中均有相似的部分C·µL(安慰剂40细胞−1;mepolizumab·µL 50个细胞−1),以及减少与基线值相比之前mepolizumab治疗梦,门萨·µL和天狼星(230 - 320细胞−1;补充表E2)。此外,人口和疾病特征相似的任何治疗之前mepolizumab彗星每组(如。在梦里,门萨和小天狼星基线;补充表E3)。
随机部分C之前,mepolizumab治疗(范围)持续时间的中位数是44.1(32-59)个月,将1145.2的白细胞数量(表1)。两个病人32个月连续mepolizumab过早暴露是随机偏差随后C和部分确认为协议。在双盲C部分时期,更大比例的患者安慰剂组(56%,84 151)转向开放mepolizumab治疗(D)部分mepolizumab臂(31%,45 144;补充图E3和E4)。因此,总接触双盲治疗更长的时间mepolizumab组(114.6()与安慰剂比较(93.9白细胞数量;表1)。
主要终点
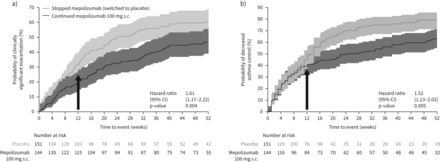
病人停止mepolizumab明显短时间第一临床显著比患者持续恶化;他们增加了61%的风险经历他们的第一个临床显著的恶化(停止/继续mepolizumab风险比(人力资源)1.61,95%可信区间1.17 - -2.22;在52周部分C p = 0.004)时期(图2一个)。更高比例的病人停止mepolizumab(安慰剂组)至少经历了一次临床显著恶化期间部分C与持续mepolizumab治疗(59%与46%;或1.99,95%可信区间1.19 - -3.32;p = 0.009;补充表E4)。kaplan meier累积发病率的病人出现恶化与安慰剂组高出数值与mepolizumab分别在每个时间点:处理间差异被发现从第12周(31.8%和20.2%),并通过24周逐渐变得越来越大(49.3%和32.3%),36(56.0%和40.3%)和每周52(60.7%和47.1%)。总的来说,在安慰剂组22例(15%)患者和19例(13%)患者mepolizumab组在治疗期间经历了两个或两个以上的急性加重部分C。
kaplan meier时间累积发病率曲线第一)临床上显著的恶化;和b)减少哮喘控制,定义为从基线增加哮喘控制Questionnaire-5分数≥0.5个单位的15),和相关的风险比率(停止/继续mepolizumab)治疗;C的一部分;盲目的治疗)。0代表4星期后,最后一次剂量的非盲mepolizumab。阴影区域表示95%的置信区间。箭头表明,群体之间的差异被认为从第12周开始(16周后最后一个剂量的非盲mepolizumab)。
二、其他端点
发作需要住院治疗或ED访问发生在七个(5%)病人停止mepolizumab治疗(九事件;一个病人经历了三个事件需要ED访问和从未变成了D部分;6个病人出现一个恶化需要住院治疗,其中5人立即转向D)一部分。病人继续mepolizumab, 10(7%)经历了单一事件的严重性(8个病人有ED的访问中,七人都变成了D部分;剩下的两个病人需要住院治疗,都立即转向D部分)。
病人停止mepolizumab治疗明显短时间先减少哮喘控制在C的一部分;他们增加了52%的风险减少哮喘控制的12个月里(停止/继续mepolizumab人力资源1.52,95%可信区间1.13 - -2.02;p = 0.005;图2 b)。kaplan meier患者经历的累积发病率减少哮喘控制与安慰剂更高与mepolizumab分别在每个时间点:处理间差异被发现从第12周(44.5%和39.3%),并通过时间延长24(69.5%和49.3%),36(74.9%和56.0%)和每周52(79.0%和63.1%)。恶化哮喘控制,以增加ACQ-5分数表示,被从第12周(16周后最后一个剂量的非盲mepolizumab)停止mepolizumab治疗的病人相比,那些仍在继续,尽管95%置信区间重叠在每个时间点(图3一)。52周,ACQ-5分数的差异(95% CI)病人停止与继续mepolizumab是0.23 (0.02−-0.48;p = 0.067)。
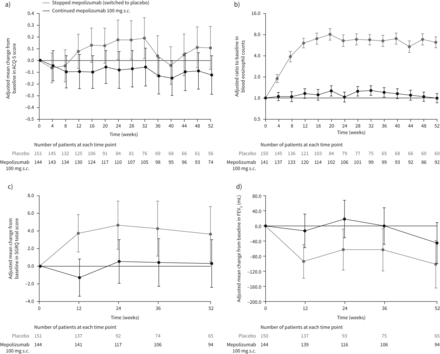
)是指从基线(双盲治疗开始在彗星)在哮喘控制问卷(ACQ) 5分;b)比基线血液中嗜酸性粒细胞计数;c)的意思是改变从基线圣乔治呼吸问卷(SGRQ)总分;从基线和d)意味着改变pre-bronchodilator用力呼气量在1 s (FEV1)(治疗;C的一部分;盲目的治疗)。0代表4星期后,最后一次剂量的非盲mepolizumab。数据提出了最小二乘方法(95% CI)。病人数量在每个给定的时间点每个图如下所示。更高的分数在ACQ-5表明差控制(范围0 - 6);0.5分的变化是最小临床重要的区别(15]。更高的分数的SGRQ表明差函数(范围0 - 100);4点的变化是最小临床重要的区别(16]。
在病人停止mepolizumab,最小二乘(LS)意味着±se日志血嗜酸性粒细胞计数稳步增长从周4(8周后最后一个剂量的非盲mepolizumab),达到270±0.077·µL细胞−1在第12周(16周后患者最后一次剂量的非盲mepolizumab),而患者持续mepolizumab维护LS·µL意味着未来保持血液嗜酸性粒细胞计数细胞−1(第12周停止与继续mepolizumab比率5.21,95%可信区间4.20 - -6.46;p < 0.001)。52周,血液嗜酸性粒细胞计数是270±0.091·µL细胞−1和40±0.077·µL细胞−1病人停止与分别持续mepolizumab(停止与继续mepolizumab比率6.19,95%可信区间4.89 - -7.83;p < 0.001) (图3 b)。绝对血嗜酸性粒细胞计数所示补充表E5。
健康相关的生活质量(SGRQ总分从基线)和肺功能(pre-bronchodilator FEV基线的改变1)测定在12周,24岁,36岁和52岁的两个端点恶化,在患者停止mepolizumab所有时间点;患者持续mepolizumab经历这些结果持续受益,尽管95%置信区间重叠最多时间点(图3 cd)。52周的差异(95% CI) SGRQ总得分和pre-bronchodilator FEV1病人停止与继续mepolizumab是3.3 (0.8−-7.5;p = 0.113)和−56毫升(−139 - 27毫升;p = 0.186)。
事后分析
我们的事后分析表明,急性加重的数量在今年前随机(0,1,≥2)是一个强有力的预后因素的风险恶化在52周的试用期,期间与日益恶化的风险部分C与更多的恶化事件随机前一年。两个或两个以上的患者发作前一年(n = 44)恶化的风险更高与那些没有(n = 185)或(n = 66)恶化(补充图E5)。此外,停止与继续mepolizumab第一恶化的风险增加了74% (HR 1.74, 95%可信区间1.08 - -2.80)和180%(2.80,1.44 - -5.44),分别在病人没有前一年或一个恶化;然而,并没有观察到这种风险增加两个或两个以上的急性加重患者的前一年(0.88,0.46 - -1.67)。没有其他基线特征评估确定微分跨子组治疗效果。
安全
mepolizumab符合先前的试验的安全性(补充表E6)。在C部分,较低的患者比例在安慰剂比mepolizumab报道不良事件(64%与78%);然而,每个patient-year暴露为安慰剂组低于mepolizumab组(93.94与114.60)。Exposure-adjusted率(每1000 participant-years)之间的类似治疗武器(安慰剂3097.77,mepolizumab 2740.01;补充表E7)。类似比例的病人安慰剂和mepolizumab团体报告严重不良事件(7%与6%),所有这些都是被治疗研究者认为是相关的治疗。感染被报道在较低比例的患者相比,安慰剂组mepolizumab组(44%与58%),具有类似exposure-adjusted治疗手臂之间的利率(分别为1373.24和1160.58每1000 participant-years)。本地站点反应发生在安慰剂组的比例较低与mepolizumab-treated患者(< 1%与3%)。有两个死亡报告,一个在C部分(后处理,原因不明),另一个在D部分(治疗,肺炎愿望);死亡都是在C和一部分病人安慰剂都被认为是与学习无关的治疗。
讨论
这是第一个研究随机检查的临床影响停止mepolizumab治疗嗜酸性哮喘患者长期使用后严重。短时间第一临床显著恶化明显对于那些停止mepolizumab相比那些mepolizumab继续治疗。59%的病人停止mepolizumab至少经历了一次临床显著恶化第二年,相比之下,46%的人仍是mepolizumab。ACQ-5恶化和SGRQ分数在第12周(16周后最后一个剂量的非盲mepolizumab),而分数保持那些mepolizumab继续说。这表明亏损哮喘控制和阻止mepolizumab治疗的患者的生活质量,甚至在≥3年使用。因此,mepolizumab的有利影响,明显的基线特征的双盲治疗彗星,停止治疗后不太可能持续。这些结果也强调病人的临床效益持续留在mepolizumab治疗。总的来说,与病人停止mepolizumab相比,持续长期治疗的患者不太可能经历哮喘急性加重和损失控制,持续的好处也健康相关的生活质量和肺功能所示。临床上的概率显著的恶化和减少哮喘控制似乎增加从第12周(16周后最后一个剂量的非盲mepolizumab)的患者停止mepolizumab与那些继续治疗。
有血嗜酸性粒细胞计数差异那些mepolizumab停下,继续,按照mepolizumab[的作用机制9];这些差异被认为早在周4(8周后最后一个剂量的非盲mepolizumab)。血嗜酸性粒细胞计数增加缓慢;第12周(16周后停止mepolizumab)他们有返回值类似于基线开始最初的III期研究(270·µL细胞−1与230 - 320细胞·µL−1)[1,3,4]。这是符合H的出版物aldar等。(13)展示了一个回到预处理血嗜酸性粒细胞计数后停止治疗。之前重要的是,改变血液嗜酸性粒细胞计数分离mepolizumab组和安慰剂组之间的疗效在c部分支持了先前的发现证明mepolizumab的药效学影响血液嗜酸性粒细胞计数不停止治疗后持续13),并进一步证实了临床结果之间的关系和血液嗜酸性粒细胞计数1,3,4,17- - - - - -20.]。
尽管59%的病人停止mepolizumab至少经历了一次临床显著恶化停止治疗后,41%经历过这段期间临床显著恶化。然而,这符合患者的比例没有发作而接受安慰剂过去mepolizumab试验(1,3- - - - - -5),在一个类似的dupilumab[12周试验21]。例如,在门萨,45%接受安慰剂的患者没有经历一个恶化在32周治疗期(4],而等效比例来自天狼星(24周),梦(52周),苍蝇座(24周)和dupilumab试验(12周)分别为32%,33%,59%和56%,分别为(1,3,5,21]。这些发现强调了患者的发作频率严重嗜酸性哮喘表型。一些患者急性加重而接受mepolizumab治疗支持在表型异质性,即非嗜酸性粒细胞因素可能导致急性加重(22]。尽管如此,加剧哮喘表型的稳定在一个给定的时间段是目前未知23- - - - - -26),它是可行的,病人严重恶化的历史在标准的护理治疗可能会恶化免费indeterminant时期然后返回一个加剧表型(27]。
在XPORT研究中,48%的病人停止omalizumab治疗仍然恶化免费在第二年,类似于41%的病人在彗星没有加剧停止mepolizumab [28]。正如前面强调的,这可能是由于恶化的可变性人口严重嗜酸性哮喘发病率。此外,如彗星所示,一个更高比例的患者在omalizumab(67%)没有加重1年的研究期间,相比那些停止治疗(48%)(28]。这是符合54%的病人仍然恶化自由而继续mepolizumab彗星。
它可能是有用的特征或坚持病人没有回复到一个加剧表型在12个月内停止mepolizumab治疗,事实上确定这些患者发作以外的任何其他标记的持续治疗的好处。这些信息可能会被用来确定是否有任何患者可以停止mepolizumab 52周期间没有任何后续的损失控制在持续时间的治疗,尽管需要临床研究证实。利益因此加重的数量在今年前彗星的随机是一个强有力的预后因素,预测未来恶化风险,并是唯一的基线特征评估,确定了通过子组的治疗效果差,停止后发作的风险与继续mepolizumab。该小组的两个或两个以上的患者发作前一年被确认为可能从临床观察少保护重要与mepolizumab发作,没有治疗这个病人中观察到的子群中获益。然而,应该强调,这群病人很小,确认后事后亚组分析,因此这一发现进行解释时应特别谨慎,认为是假设生成。还需要进一步的研究来理解中断的影响在两个或两个以上的急性加重患者mepolizumab去年接受持续治疗。
在这项研究中没有观察到新的安全问题人口相比,这些在之前的研究[1,3- - - - - -8]。此外,不良事件率相似的患者停止mepolizumab然后切换回mepolizumab治疗恶化之后,相比之下,那些收到mepolizumab不断在整个研究。
当前的研究的一个优势是背景治疗的监测和维护整个C部分,建议每协议没有变化。然而,患者选择从一个人完成了先前mepolizumab临床试验;因此,病人招聘是偏向那些回应mepolizumab,和那些没有不良事件导致停药的先前的研究。此外,只有∼50%的病人从鸽属和COSMEX进入了彗星。病人可能一直不愿招收在安慰剂对照研究中,尤其是在那些国家mepolizumab成为彗星的商用开始之前。此外,病人可能也经历了一个长期mepolizumab治疗后疾病的改善活动,这可能导致减少或停用背景药物;病人必须附着在哮喘控制药物/治疗在前面的非盲mepolizumab研究才有资格彗星,这可能减少招生。进一步限制是黑色的非常小的比例的病人包括在彗星的人口由于有限表示父III期试验。此外,尽管ACQ-5恶化和SGRQ分数和FEV恶化1被认为在第12周的病人停止mepolizumab,这项研究没有设计为动力来衡量这些端点统计学意义。
此外,结果是基于低数量的病人与更早的时间点内部分C的一个子集患者从双臂停止双盲治疗和转向部分D。这可能是由于研究设计,呼吁一个调查员评估患者经历了临床显著的恶化在C部分确定切换到非盲mepolizumab D部分将是合适的。这个问题是由使用一个假想的减轻estimand策略应用于处理并发事件的双盲治疗停药。因此,治疗效果报道部分C指结果如果所有患者一直在52周的双盲双盲治疗期。分析恶化年率在双盲治疗期(C)是不可能的,由于病人被允许切换到非盲治疗先恶化后,这意味着重复发作并不期望通过研究设计。
研究者评估期间C也可能导致一部分数量少需要住院治疗的急性加重和/或ED访问,因为患者可能已经转向开放mepolizumab之前发生了更严重的恶化。由于这些更严重的恶化的罕见事件期间部分C,这是符合mepolizumab(之前的试验4,6,8),治疗组之间的任何差异进行解释时应特别谨慎。最后,因为这是一个双盲随机对照试验,决定停止mepolizumab或切换到非盲治疗可能不反映常规临床实践,病人的治疗,病人和医生都是蒙蔽他们是否mepolizumab或安慰剂。因此,45的发现病人接受mepolizumab部分C转向D部分,42切换由于缺乏疗效的报道(在调查员的意见)进行解释时应特别谨慎。这些42例,41也报道恶化为subreason切换。是可能的,调查人员可能将病人在第一个机会(非盲治疗即。后他们的第一个临床显著恶化)所允许的研究设计;这将使病人返回建立有效的疗法,已收到至少前3年。事实上,大多数病人转向D部分继续在非盲mepolizumab设置mepolizumab继续治疗,直到研究结束,很少有取款。
总之,通过12周(16周后最后一个剂量的非盲mepolizumab)患者停止长期(≥3年)mepolizumab治疗有更短的时间第一个临床显著恶化,增加血液嗜酸性粒细胞计数回预处理的水平,和减少哮喘控制、生活质量和肺功能与那些继续mepolizumab相比。这些结果支持继续mepolizumab治疗在严重嗜酸性哮喘患者持续的临床效益,进一步支持血嗜酸性粒细胞mepolizumab适合治疗反应的生物标记。
补充材料
可共享的PDF
确认
医学写作和编辑支持(写作形式的援助,包括基于作者初稿的发展方向,装配表和数据,整理作者的评论,语法编辑和引用)是由伊丽莎白·哈钦森Fishawack邮戳,英国Fishawack健康(由葛兰素史克)的一部分。
脚注
可以从本文的补充材料www.qdcxjkg.com
本研究在Clinicaltrials.gov注册标识符NCT02555371。匿名个人参与者的数据、学习文件可以从www.clinicalstudydatarequest.com要求进一步的研究。
作者的贡献:M.J.吉尔松和R.G.价格参与的概念或设计工作;厕所摩尔,o . Kornmann m·亨伯特c .地方再见贝尔,金子n和m刘参与收购数据;所有作者都参与起草或修订工作至关重要的知识内容(即。数据分析和解释);和所有作者同意提交,并负责所有方面的工作。
利益冲突:厕所摩尔报道,这项研究和写作是由葛兰素史克公司的支持;已经收到了对临床研究的资助和个人费用参与顾问委员会从葛兰素史克,阿斯利康和赛诺菲安万特Regeneron,外提交的工作。
利益冲突:o . Kornmann报道,这项研究和写作是由葛兰素史克公司的支持;和已经收到个人费用从阿斯利康、葛兰素史克诺华,勃林格殷格翰的发言,赛诺菲-安万特和罗氏公司,在提交工作。
利益冲突:m·亨伯特报道,这项研究和写作是由葛兰素史克公司的支持;和收到的个人咨询服务费用在各种会议上发表演讲,并参与临床研究项目与阿斯利康、葛兰素史克、诺华,罗氏公司,赛诺菲安万特Regeneron和梯瓦;外,葛兰素史克的科研补助金,提交工作。
利益冲突:c .地方报道,这项研究和写作是由葛兰素史克公司的支持;和个人费用已收到葛兰素史克、诺华赛诺菲,勃林格殷格翰的发言,在提交工作。
利益冲突:再见贝尔报道,这项研究和写作是由葛兰素史克公司的支持;从葛兰素史克和赠款和梯瓦、个人费用从阿斯利康、葛兰素史克、诺华赛诺菲/ Regeneron,胸骨生物制剂和基耶西,在提交工作。
金子的利益冲突:联合国报告称,这项研究是由葛兰素史克和写作的支持。
利益冲突:信号发生器史密斯报道,这项研究是由葛兰素史克和写作支持;葛兰素史克公司的员工和拥有股票/。
利益冲突:n .马丁报告的研究和写作是由葛兰素史克公司的支持;葛兰素史克公司的员工和拥有股票/。
利益冲突:M.J. Gilson报道,这项研究和写作是由葛兰素史克公司的支持;葛兰素史克公司的员工和拥有股票/。
利益冲突:R.G.价格报告,研究和写作是由葛兰素史克公司的支持;葛兰素史克公司的员工和拥有股票/。
利益冲突:静电的布拉德福德报告,研究和写作是由葛兰素史克公司的支持;和是一个员工在葛兰素史克的研究。
利益冲突:贝拉刘报道,这项研究和写作是由葛兰素史克公司的支持;和获得资助的临床试验勃林格殷格翰的发言,葛兰素史克,落实Mereo BioPharm,轻飘飘的生物,在提交工作。
支持声明:本研究是由葛兰素史克公司(GSK ID: 201810 /NCT02555371)。研究发起人参与研究设计,数据收集、分析和解释,以及报告的编写。赞助商没有地方限制访问数据或报告中陈述。作者有完全访问所有的研究数据和最终责任提交出版。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年2月8日。
- 接受5月23日,2021年。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org