摘要
机制研究表明,生活方式和环境因素通过男性生殖细胞传递的表观遗传变化影响几代人的呼吸健康。来自人类研究的证据非常有限。
我们调查了多代因果关系,以估计吸烟对父系肺功能的因果影响。我们分析了383名成年后代(18-47岁;52.0%女性)及其274名父亲,他们参加了欧洲共同体呼吸健康调查(ECRHS)/北欧、西班牙和澳大利亚呼吸健康(RHINESSA)世代研究,并提供了支气管扩张剂使用前肺功能的有效测量。建立了两个基于反事实的多层中介模型:外公外婆孕期吸烟和父亲青春期前开始吸烟作为暴露;父亲1 s用力呼气量(FEV1)和强迫肺活量(FVC,或FEV)1/FVC z分数作为潜在介质(未观察到的生物机制的代理,是真正的介质);和后代的FEV1以及FVC或FEV1/FVC z-scores作为结果。所有影响都被总结为与父亲和祖母吸烟史相关的预期z得分的差异(Δ)。
父亲在青春期前开始吸烟对两个后代的FEV都有直接的负面影响1(Δz-score - 0.36, 95% CI - 0.63 - - 0.10)和FVC (- 0.50, 95% CI - 0.80 - - 0.20)。祖母怀孕期间吸烟对父亲的FEV有直接的负面影响1/FVC (- 0.57, 95% CI - 1.09 - - 0.05)和对后代FEV的负间接影响1/FVC (- 0.12, 95% CI - 0.21 - - 0.03)与祖母在父亲出生前和父亲童年时期不吸烟相比。
父亲在青春期前吸烟和祖母在怀孕期间吸烟可能导致后代肺功能下降。我们的研究结果支持了这样一个概念,即在这些易感期与生活方式相关的暴露会影响后代的健康。
摘要
父亲的青春期前和祖母的怀孕期是吸烟对后代肺功能不利影响的脆弱时期。在这些易感时间窗口内预防吸烟可能会改善下一代的健康。https://bit.ly/3vvgjsN
简介
哮喘和慢性阻塞性肺病是全世界面临的主要健康挑战[1,2].生活方式和环境暴露是这些疾病的重要危险因素[3.,4],尤其是在幼年接触这种物质时。新出现的证据表明,怀孕前的环境可能损害后代的呼吸健康[5,6],并得到动物研究的支持[7- - - - - -9].与这一假设一致,我们之前发现父亲在15岁(与青春期前期相一致,因为15岁是男孩青春期完成的平均年龄)之前吸烟之间存在负相关[10])及其后代的哮喘表型[11,12].我们还发现了父亲超重的易感性时间窗口。13].
人类健康研究[14],包括呼吸系统疾病[15- - - - - -18],目前更专注于表观遗传学。DNA甲基化的可遗传修饰可能是孕前和早期生活暴露对后代疾病表型影响的关键机制。胎儿期和青春期前对男性生殖细胞系的表观遗传编程有影响,因此是环境暴露敏感性较高的时间窗口[19,20.].这些脆弱时期可能是对男性进行预防性干预的机会之窗,旨在改善今世后代的健康。
因果统计推论[21]有助于阐明从不同世代的接触到随后几代健康结果的易感性时期的途径所涉及的机制。最近提出了一种多暴露、多中介、多结果(MEMMMO)框架,用于识别复杂的多代效应[22].根据这一新的观点,我们调查了父系中父亲在青春期前开始吸烟(G1代)和祖母在怀孕期间吸烟(G0代)对后代肺功能(G2代)的因果关系,以估计其因果影响。作为欧洲队列肺老化研究的一部分(www.alecstudy.org),我们分析了一项正在进行的成年人呼吸健康调查(欧洲共同体呼吸健康调查(ECRHS);www.ecrhs.org(北欧、西班牙和澳大利亚的呼吸健康(莱茵萨);www.rhinessa.net).
方法
研究设计
ECRHS是一项以人群为基础的国际队列研究,研究招募时20-44岁受试者的呼吸健康(ECRHS I;1991 - 1993年)(23].在基线时,每个参与者都收到一份简短的筛查问卷(第一阶段),并从回应者中抽取20%的“随机样本”进行更详细的临床检查(第二阶段)。在第二阶段,还招募了一份具有哮喘样症状的成年人“症状样本”。第二阶段参与者的跟进工作于1998至2002年进行(ECRHS II) [24]及2010-2013年(ECRHS III) [25].这些受试者在所有情况下都进行了标准化的临床访谈、肺功能和实验室检查。莱茵萨是一项关于来自北欧、西班牙和澳大利亚的10个中心的ECRHS参与者后代健康和疾病的国际研究[13].根据适应ECRHS使用的方案,在2013-2016年收集了广泛的问卷调查和肺功能数据。在ECRHS/RHINESSA研究中,每位参与者都获得了书面知情同意。各中心的伦理委员会均已通过伦理批准(补充材料).
肺功能及定义
1秒内支气管扩张剂前最大用力呼气量(FEV)1)和根据美国胸科学会(ATS)的重复性标准测量至少两次技术上令人满意的动作的用力肺活量(FVC) [26,作为ECRHS和莱茵萨临床检查的一部分。最后一次随访接触(ECRHS III)和莱茵萨的ECRHS也测量了支气管扩张剂后的肺活量。在目前的分析中,我们使用了父亲在基线时的肺功能测量(ECRHS I),或者在第一次可用的情况下(ECRHS II或ECRHS III),如果基线时没有进行肺功能测量或没有达到ATS标准。全球肺功能计划z-评分[27],并使用欧洲呼吸学会免费软件(188bet官网地址www.ers-education.org/guidelines/global-lung-function-initiative/spirometry-tools/desktop-sheet-calculator.aspx),以控制肺功能受性别、年龄及身高的影响。
在每次ECRHS考试的面试中,父亲们都提供了自己吸烟史的详细信息,包括他们开始吸烟的时间。父亲吸烟被归类为“15岁前开始吸烟”(即。在青春期前),“15岁或以上开始吸烟”或“从不吸烟”。父亲的教育水平由ECRHS I自行报告,如果在ECRHS研究开始前低于或等于该国的最低离校年龄,则被视为“低”教育水平[28].父亲的职业类别是根据《ECRHS I》和《ECRHS II》之间随访期间任职时间最长的职业而得出的,类别是根据《国际标准职业分类》中的主要类别分类[29].在ECRHS I,父亲们报告了他们的母亲在他们出生之前或之后是否吸烟。因此,祖母吸烟被归类为“父亲吸烟时吸烟”在子宫内、“怀孕前或父亲幼年时期(或未知吸烟时期)吸烟”或“父亲出生前或幼年时期不吸烟”。在ECRHS III中,父亲提供了父母教育水平的信息(如果祖父母双方都只学习到最低离校年龄,则定义为“低”)。在莱茵萨,孩子们报告了自己的吸烟史和教育水平(如果受试者只学习到最低离校年龄,则定义为“低”),以及他们的母亲在他们出生前或出生前是否吸烟,在ECRHS的采访中回答了类似的问题。
研究对象
来自爱沙尼亚(塔尔图)、挪威(卑尔根)、西班牙(阿尔巴塞特和韦尔瓦)和瑞典(哥德堡,Umeå和乌普萨拉)的2302名男性接受了ECRHS I-III的临床检查,其中1241人参加了ECRHS III。其中,913名男性报告至少有一个后代,其中297名至少有一个成年后代参与了RHINESSA临床阶段,因此有资格纳入本分析(图1).这些父亲有有效的肺功能测量,并报告了自己和母亲吸烟史的完整信息。在这297名父亲的420名成年后代中,383人有有效的肺功能测量。这些后代及其274名父亲(来自ECRHS“随机样本”的92.7%)被纳入我们的研究。
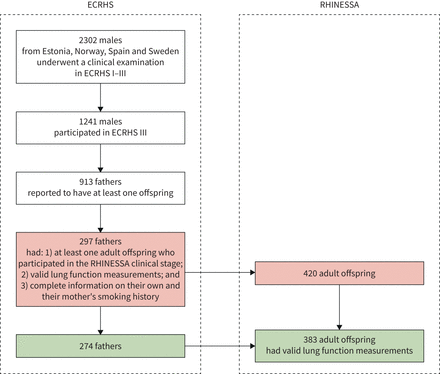
研究对象的选择(父亲及其后代)。欧洲共同体呼吸健康调查;莱茵萨:北欧、西班牙和澳大利亚的呼吸健康。
统计分析
基于反事实的中介分析[30.在一个等级框架内进行了研究,以调查祖母和父亲在脆弱时期吸烟的途径和父亲系内后代的肺功能。我们的数据具有层次结构,因为后代兄弟姐妹(第1级单位)具有相同的生父(第2级单位),并且因为他们的父亲来自不同的中心(第3级单位)。每次暴露对每个结果的总影响被分解为其自然直接影响(即。暴露对结果的影响通过一种不涉及中介的途径)及其自然的间接(中介)效应(即。由于暴露对中介的影响,暴露对结果的影响)[31].调解的主要条件是间接效果在统计上有显著性[32],当观察到的中介效应对某些未测变量的潜在混淆具有鲁棒性时[33].
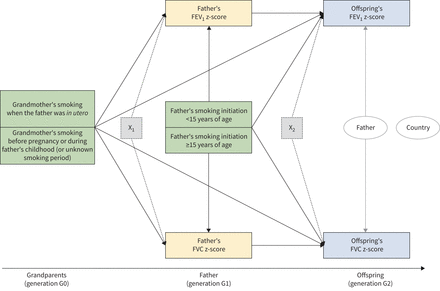
父系中使用了两种多级中介模型。模型1和模型2旨在评估吸烟对支气管扩张剂前FEV的多代影响1及植被覆盖度(图2),或FEV1/ FVC (图3),分别。模型1包括父亲的FEV1和FVC z分数作为正态分布,相关,平行介质,和后代的FEV1和FVC z评分为正态分布,相关,平行结果。模型2包括父亲的FEV1/FVC z分数为正态分布中介和子代FEV1/FVC z-score为正态分布结果。父亲的每个肺功能变量(在成年期测量)被认为是未观察到的生物学机制的代理,这些机制是真正的介质。潜在介质没有包括在模型中,因为我们对每个介质都有一个单一指标,而使用单一指标潜在变量往往会导致模型规范中的识别问题[34].在这两个模型中,祖母和父亲的吸烟情况是兴趣的暴露,祖父母和父亲的教育水平和父亲的职业阶层被分析为潜在的混杂因素。我们验证了这些潜在的混杂因素是否代表“最小充分调整集”(即。通过使用有向无环图(有向无环图),为消除混淆而需要包含的最小测量协变量集[35]在DAGitty (http://dagitty.net;看到补充材料).此外,父亲的年龄、母亲在子女出生前或出生前是否吸烟、子女的性别、年龄、教育程度和是否吸烟被分析为暴露-中介因素-结果关系的调节变量。
1 s用力呼气量(FEV)的中介模型1)和父系内的强迫肺活量(FVC)(模型1)。绿框表示兴趣的暴露,黄框表示介质,蓝框表示结果。虚线框表示中介的潜在混杂因素和调整变量集(X1:祖父母的受教育程度,父亲的年龄、受教育程度和职业阶层),以及结果(X2:父亲受教育程度及职业阶层、母亲在子女出生前后吸烟情况、子女年龄、性别、受教育程度及吸烟情况)。两个椭圆表示第2级单元(父;箭头表示第2级的随机截距项)和聚类变量(国家;没有箭头表明计算了聚类稳健标准误差,以考虑国家内父亲之间的相关性)。
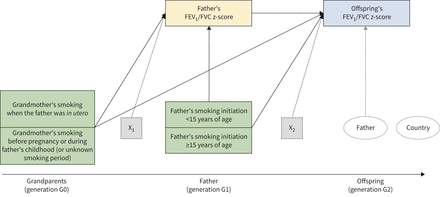
1 s用力呼气量(FEV)的中介模型1)/父系内的强迫肺活量(FVC)(模型2)。绿框代表兴趣暴露,黄框代表中介,蓝框代表结果。虚线框表示中介的潜在混杂因素和调整变量集(X1:祖父母的受教育程度,父亲的年龄、受教育程度和职业阶层),以及结果(X2:父亲受教育程度及职业阶层、母亲在子女出生前后吸烟情况、子女年龄、性别、受教育程度及吸烟情况)。两个椭圆表示第2级单元(父;箭头表示第2级的随机截距项)和聚类变量(国家;没有箭头表明计算了聚类稳健标准误差,以考虑国家内父亲之间的相关性)。
模型1和模型2在2级(父级)具有随机截距项,簇鲁棒标准误差(国家=簇变量)和“2→2→1”配置,即。暴露和介质在第2级(父亲)进行测量,而结果在第1级(后代)进行测量[36].暴露(祖母和父亲的吸烟)对正态分布介质(父亲的z得分)和结果(后代的z得分)的自然(反事实为基础)直接和间接影响被总结为预期z得分的差异(Δ)。自然的直接影响是后代对接触状态变化的Δz-score,当接触不存在时,父亲的z得分保持在其期望值。自然的间接影响是有暴露时后代的Δz-score,但父亲的z得分从没有暴露时的期望值变化到有暴露时的期望值。基于具有稳健标准误差的最大似然估计,计算了直接效应和间接效应的大小及其95%置信区间[36]和产品分配法[37),分别。
Stata版本15 (StataCorp, College Station, TX, USA), Mplus版本8 (Muthén & Muthén, Los Angeles, CA, USA)和R版本3.6.1 (www.R-project.org)进行统计分析。
敏感性分析
进行敏感性分析以评估:1)在纳入两个未测量混杂因素后,估计的效果是否发生变化(U1和你2),通过在Umediation包中使用概率(蒙特卡罗)模拟[38) (https://github.com/SharonLutz/Umediation;看到补充材料);2)这是一个未测量的混杂因素与中介因素和结果之间需要具有的最小关联强度,以测量的混杂因素为条件,以完全解释所观察到的直接或间接影响(中介e值)[39],通过使用Evalue包[40) (https://github.com/mayamathur/evalue_package).通过近似转换,在风险比量表上返回中介e值[41,42];3)当排除了出生后父亲吸烟的182个后代后,父亲在青春期前吸烟的估计影响是否会发生变化;4)当使用后代的支气管扩张剂后肺功能测量时,估计的影响是否会发生变化(可从369个后代中获得)。
结果
研究对象的主要特征
在肺功能评估时,274名父亲及其383名后代(52.0%为女性)的中位年龄分别为37岁和28岁(表1而且2).在我们的样本中,10.2%,8.4%和7.7%的父亲有FEV1, FVC或FEV1/FVC z分数分别低于- 1.645(第5百分位),而其后代的这些值分别为6.0%、3.7%和6.8%。在父亲中,9.1%在15岁前开始吸烟(即。在青春期前)和7.7%的人报告说他们的母亲(本分析中的祖母)在怀孕期间吸烟。在这些后代中,一直吸烟的比例为30.3%,50.7%的人报告说,他们的母亲在他们出生前或出生前吸烟。
父亲在青春期前开始吸烟
父亲在青春期前(G1代)开始吸烟对他们自己的FEV有直接的负面影响1/FVC (Δz-score - 0.36, 95% CI - 0.68 - 0.04)与父亲从不吸烟(表3).这种接触对两个后代的FEV都有直接的负面影响1(−0.36,95% CI−0.63 -−0.10)和FVC(−0.50,95% CI−0.80 -−0.20)(G2代),但我们没有观察到对后代FEV的统计显著影响1/ FVC。未发现父亲在青春期前吸烟对后代肺值的中介作用(仅直接无中介作用)(表4).父亲在较晚的年龄开始吸烟对他们自己的FEV有负面的直接影响1(−0.27,95% CI−0.51 -−0.02)和FEV1/FVC (- 0.20, 95% CI - 0.37 - - 0.04),但我们没有发现对后代肺功能的影响。
祖母在怀孕期间吸烟
祖母吸烟时,父亲在子宫内(G0代)对父亲FEV有直接的负向影响1/FVC (G1代)(- 0.57,95% CI - 1.09 - - 0.05)与父亲出生前和父亲童年时期祖母不吸烟(表3).祖母在怀孕期间吸烟对孙辈的肺功能没有直接影响(第G2代)。这种接触有负面的中介效应,通过未观察到的生物学机制,父亲的FEV1成年期的FVC是孙子的FEV的一个指标1/FVC(−0.12,95% CI−0.21 -−0.03)(仅间接中介)(表4).
敏感性分析
模拟结果表明,可以合理地假设未测量的混杂因素对父亲和祖母吸烟的影响较低(补充数字S4和S5).当各未测混杂因素(U1和你2)在暴露、中介和结果上设定≤5,结果匹配的模拟比例(是否U1和你2均纳入或不纳入模型)为>72.8%,平均效应的平均绝对差值<0.083。U1和你2只更改了非常强的效果的结果(即。对于β回归系数>5)。
青春期前父亲吸烟对后代FEV自然直接影响的中介e值1FVC分别为2.31和2.85,而祖母怀孕期间吸烟对子代FEV自然间接影响的中介e值1/FVC为1.50。因此,一个未测量的混杂因素必须与中介因素和结果相关,其近似风险比至少等于2.31、2.85或1.50(当结果为FEV时)1, FVC或FEV1/FVC)来完全解释所观察到的影响。
排除出生后吸烟的父亲的后代,可以更有力地估计出父亲在青春期前吸烟对后代FEV的直接影响1(−0.55,95% CI−1.18-0.07)和植被覆盖度(−0.77,95% CI−1.61-0.07)。然而,由于数据稀疏,这些估计没有达到统计显著性,因为只有8个后代出生在7个在青春期前开始吸烟并在出生前戒烟的父亲身上。
当使用子代的支气管扩张剂后值时,父亲吸烟对子代FVC的直接影响(−0.35,95% CI−0.62 -−0.07)和祖母吸烟对子代FEV的间接影响1/FVC(−0.09,95% CI−0.17 ~−0.01)降低。然而,父亲吸烟对后代FEV的直接影响1差异均无统计学意义(−0.19,95% CI−0.48-0.11)。
讨论
在本研究中,我们发现父亲和祖母在脆弱时间窗口吸烟可能会对未来两代人的肺功能产生负面影响。这些结果是通过观察数据的因果推断方法获得的,并通过解释未测混杂的敏感性分析得到了加强。我们的新观察是,在青春期前吸烟的父亲的后代可能有较低的FEV1以及FVC值(表明有减少肺总容量的作用)与从不吸烟的父亲的后代相比。另一个关键结果是,当父亲吸烟时,祖母吸烟的间接负面影响在子宫内孙子孙女的FEV1/ FVC。这一发现表明,怀孕期间吸烟(G0代)不仅可能增加G1代气流阻塞的风险,而且还可能对父系内的G2代产生负面影响。我们的研究结果支持了这样一个概念,即男性青春期前和怀孕期间与生活方式相关的接触会影响后代的健康。
父亲在青春期前开始吸烟
在目前的分析中,父亲青春期前吸烟对后代FEV的影响1在孩子出生之前或之后,无论母亲吸烟的影响如何,甚至在排除出生后吸烟的父亲的后代后,FVC也仍然存在。当使用后代的支气管扩张剂后值时,对FVC的影响有所降低,但仍具有统计学意义。此外,父亲较晚开始吸烟对后代的肺功能没有影响。
未测量的基因混淆不太可能解释父亲早期吸烟对后代FEV的直接影响1和FVC,作为少数在遗传研究中确定的尼古丁依赖和肺功能的风险位点(如胆碱能受体尼古丁α5亚基中的rs16969968)CHRNA5基因)[43,44]的相关性比计算的中介e值要弱[39].因此,我们推测我们的发现可能反映了发育中的生殖细胞的表观遗传改变(如DNA甲基化、组蛋白修饰和microRNAs) [45- - - - - -47],导致后代肺容量减少。吸烟对年轻男性的遗传影响在生物学上似乎是合理的,因为男性青春期前是生殖系发育的关键时期[19,20.],这可能使烟草对配子表观遗传特征的影响具有更高的敏感性。此外,观察到父亲在青春期前吸烟对后代FEV的负面影响1FVC可能反映了香烟烟雾对代谢健康相关生物过程的直接毒性作用。父亲在青春期前开始吸烟可能导致青少年肥胖[48]和成年儿子[49],而肥胖成人的肺活量测定模式以较低的FEV为特征1、全肺覆盖度、总肺活量及残余容积[50].
我们的结果得到了之前对同一人群的分析结果的支持,在之前的分析中,我们观察到父亲在青春期前开始吸烟与后代患非过敏性哮喘的风险增加有关[11,12].此外,我们发现父亲在15岁前超重对下一代的非过敏性哮喘有直接影响[13].所有这些结果都加强了男性青春期前的生活方式和环境暴露可能影响未来后代呼吸健康的假设。我们目前的发现可能会对公共卫生产生重大影响,特别是近几十年来,欧洲不同地区11至15岁男孩的吸烟量有所增加[51],以及在幼儿中使用湿润的口服烟草和电子烟。然而,我们承认,男性早期吸烟也可能是其他致病因素的标志,因为几种危险行为可能与青少年吸烟有关。
祖母在怀孕期间吸烟
我们的研究强调,祖母在怀孕期间吸烟可能会对FEV产生负面影响1/FVC在父系内的未来两代。因此,来自英国生物银行的研究结果表明FEV的过度减少1/由于母亲在分娩前后吸烟,导致儿子的植被覆盖度下降,而植被覆盖度下降非常温和[52].产前暴露对父亲肺功能的直接负面影响得到了先前在人类和动物身上的证据的支持[53],因为尼古丁会穿透胎盘屏障,影响肺部发育[54].此外,母亲在怀孕期间吸烟与低出生体重和早产有关[55,56],这些因素与成年后肺功能下降有关[57,58].
我们推测,祖母在怀孕期间吸烟(通过生物学机制,其中父亲成年后的肺功能是一个指标)对孙辈的FEV产生了负面的间接影响1/FVC可通过表观遗传变化来解释[59,60],导致后代的气流受阻[60],这种影响不太可能被未测量的风险位点完全解释,正如计算的中介e值[39].吸烟可引起生殖细胞表观基因组的遗传变化,特别是在产前时期[60,61].多代尼古丁诱发哮喘的动物模型显示,表观遗传修饰可影响第二代后代的肺功能[62].此外,一项针对人类的研究强调了产前暴露于烟草烟雾、DNA甲基化变化和哮喘相关肺功能之间的联系[63].
优势和劣势
关于疾病早期起源的流行病学研究通常侧重于母亲在怀孕前和怀孕期间的接触情况。相比之下,莱茵萨包括了ECRHS中男性和女性参与者的后代,ECRHS调查跟踪了成年男性和女性的育龄期。因此,ECRHS/RHINESSA研究收集了父系和母系两代人在受孕前就已发生的大量暴露数据(以及肺功能的客观测量)。目前分析的另一个主要优势是用于评估因果关系的统计方法,以估计跨代的因果影响。我们使用中介模型[30.],这与流行病学研究中的因果推断越来越相关,以便研究多种暴露、多种介质和多种结果之间的复杂途径(MEMMMO框架)[22].最后,我们的结果得到以下结果的支持:1)对不可测混杂影响的概率模拟[38];2)中介e值[39来量化对未测混杂的稳健性,如。由于尼古丁依赖和肺功能的风险位点[43,44];3)亚组分析,以加强对观察到的青春期前父亲吸烟对下一代肺功能影响的因果解释;4)基于后代支气管扩张剂后肺活量测定的敏感性分析,这是识别不可逆气流阻塞所必需的[2].
我们的分析有许多局限性。首先,主要的限制是ECRHS研究中的父母信息仅适用于一位父母。关于母亲和祖父母的信息分别是子女和父亲报告的,而不是直接评估的,这产生了可能的信息偏见。然而,我们对吸烟队列的验证研究[64]及哮喘[65几代人的研究表明,尽管存在回忆偏差,但它的影响可能有限。其次,主要分析中没有使用支气管扩张剂后肺活量测定法,因为它只适用于ECRHS父亲的一部分。三是暴露对象数量少。由于数据稀疏,我们无法评估后代性别的调节作用[66]和母亲在孩子出生前或出生前吸烟[5) (即。祖母和父亲的风险因素对后代的影响因性别或母亲吸烟情况的不同而不同)。最后,不可测量的混杂因素(如遗传、其他生活方式和三代人的环境因素)可能很重要。特别是,在我们的模型中,我们无法控制遗传因素的潜在混杂效应,因为多态性仅适用于父亲的一个子集,而祖母、祖父、母亲和后代的基因型也需要分离基因遗传的影响与生活方式/环境暴露的影响[67].然而,我们估计未测量的混杂对我们分析中确定的效应的影响有限。
结论
与从不吸烟的男性相比,15岁前开始吸烟的男性的后代肺功能可能较低。祖母在怀孕期间吸烟可能会对儿子的肺功能产生负面影响,这种影响可能会延续到他们的孙辈身上。这些结果支持这样一个概念,即男性青春期前和怀孕期间与生活方式相关的接触会影响后代的健康。在这些易感时间窗口预防吸烟可能对几代人都有潜在的好处。
补充材料
可共享的PDF
确认
目前的分析是挪威研究理事会FRIPRO项目(由C. Svanes领导)和ALEC研究(www.alecstudy.org;由D.贾维斯领导)。目前的手稿有助于ALEC工作包2(由C. Svanes领导)。莱茵萨首席研究员(pi)/副pi和ECRHS pi /团队成员列在补充材料.
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:所有作者都构思和设计了这项研究。A. Johannessen, B. Benediktsdóttir, R.J. Bertelsen, L. Bråbäck, S.C. Dharmage, B. Forsberg, F. Gómez Real, M. Holm, C. Janson, N.O. Jõgi, R. Jõgi, A. Malinovschi, J. Martínez-Moratalla Rovira, J.L. Sánchez-Ramos, V. Schlünssen, K. Torén和C. Svanes收集数据。S. Accordini和L. Calciano进行了统计分析。S. Accordini, L. Calciano, D. Jarvis和C. Svanes撰写了手稿的第一个版本。所有作者都对结果进行了评论并对手稿做出了贡献。
利益冲突:S. Accordini没有什么可透露的。
利益冲突:卡尔卡诺没有什么可透露的。
利益冲突:A. Johannessen没有什么可透露的。
利益冲突:B. Benediktsdóttir没有什么可披露的。
利益冲突:R.J.贝塔森没有什么可透露的。
利益冲突:L. Bråbäck没有什么可披露的。
利益冲突:S.C.损害保险公司没有什么可透露的。
利益冲突:B.福斯伯格没有什么可透露的。
利益冲突:F. Gómez皇马没有什么可透露的。
利益冲突:J.W. Holloway报告了欧盟地平线2020研究和创新计划以及挪威研究委员会在研究期间的资助。
利益冲突:霍尔姆先生没什么可透露的。
利益冲突:C. Janson没有什么可透露的。
利益冲突:N.O. Jõgi没有任何可披露的信息。
利益冲突:R. Jõgi报告爱沙尼亚研究委员会(个人研究资助号562)的资助,在研究期间;GSK、勃林格和诺华的咨询和讲座的个人费用,GSK和勃林格在提交工作之外的差旅/住宿/会议的个人费用。
利益冲突:A. Malinovschi没有什么可透露的。
利益冲突:A.马尔康没有什么可透露的。
利益冲突:J. Martínez-Moratalla Rovira没有什么可透露的。
利益冲突:J.L. Sánchez-Ramos没有什么可透露的。
利益冲突:V. Schlünssen没有任何可披露的内容。
利益冲突:K. Torén没有什么可披露的。
利益冲突:D. Jarvis在研究期间报告了来自欧盟的资助。
利益冲突:C. Svanes没有什么可透露的。
支持声明:ALEC研究获得了欧盟地平线2020研究和创新计划(资助633212)的资助。莱茵萨获得了来自挪威研究委员会(赠款214123、228174和274767)、卑尔根医学研究基金会、挪威西部地区卫生当局(赠款911631、911892和912011)、挪威劳动监察局、挪威哮喘和过敏协会、丹麦木材基金会(赠款444508795)、丹麦工作环境管理局(赠款20150067134)、瑞典肺部基金会、瑞典哮喘和过敏协会的资助,爱沙尼亚研究委员会(资助PUT562)。ALEC研究和莱茵萨研究都得到了澳大利亚国家健康和医学研究委员会的资助。ECRHS的协调工作得到了欧洲委员会(ECRHS I和II)和医学研究理事会(ECRHS III)的支持补充材料.资助者在研究设计、数据收集、分析和解释或报告的撰写中没有任何作用。通讯作者拥有对所有数据的完全访问权,并对是否发表的决定负最终责任。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年7月15日。
- 接受2021年3月11日。
- 版权所有©作者2021。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org