摘要
肺组织和循环中几种内皮标记物的升高,包括CD31、VEGFR-2、ICAM-1、VCAM-1、e -选择素、p -选择素和vWF,支持肺内皮在局部和全身COVID-19病理中发挥重要作用https://bit.ly/3eQObIR
给编辑:
严重的急性呼吸综合征冠状病毒2(SARS-COV-2)导致目前的冠状病毒病(Covid-19)大流行[1].近几个月来,发表了大量涉及该疾病多个方面和表现的新颖研究文章。越来越多的证据表明,内皮细胞在SARS-CoV-2感染中发挥着核心作用[2- - - - - -5].早期研究已经表明,COVID-19肺组织中血管和炎症因子(如血管细胞粘附分子(VCAM)-1、白细胞介素(IL)-8或单核细胞趋化蛋白(MCP)-1)的表达增加[2].这些内皮功能障碍和内皮细胞完整性改变的标志物是SARS-CoV-2感染预后不良的重要预测因素[6],并与肺水肿、血管内血栓形成和急性呼吸窘迫综合征(ARDS)有关。肺内皮细胞在调节血管张力、炎症反应、凝血/纤溶和维持血管稳态和通透性方面起着至关重要的作用。对这些受到严格管制的过程的干扰可能直接导致发病率和死亡率。然而,导致COVID-19肺血管病变的确切机制仍不清楚。在这里,我们提供了几个与炎症反应有关的重要血管标志物(e -选择素,细胞间细胞粘附分子(ICAM)-1, VCAM-1),微血管完整性的维持(CD31,血管内皮生长因子受体(VEGFR)-2),血小板活化和凝血(p -选择素,在新冠肺炎患者肺组织和血浆中检测von Willebrand因子(vWF)。
采集肺组织标本事后剖析从19名批判性患者和11名年龄和性别匹配的尸检控制没有潜在的肺病。Covid-19和75年的中位年龄为各自的尸检控制(图1一个).研究方案和组织使用得到格拉茨医科大学伦理委员会的批准(EK-number: 32-362 ex 19/20)。从均质肺组织中分离RNA,如前所述进行cDNA合成和实时定量PCR [7].免疫荧光染色对来自相应的COVID-19患者和尸检对照的福尔马林固定石蜡包被的肺组织进行了免疫荧光染色,使用vWF (1:1000, #M0616,安杰伦,Santa Clara, CA, USA)和CD45 (1:50 50, #10558, Abcam, Cambridge, UK)和Alexa Fluor 555或Alexa Fluor 488标记的二抗(1:50 00,Thermofisher Scientific, Waltham, MA, USA)。从德国汉诺威医学院和德国吉森贾斯图-李比希大学临床免疫学和输血医学系采集的21名COVID-19重症患者和22名健康对照者的血浆样本。COVID-19患者的中位年龄为59岁,对照组为61岁。90%的患者和89%的对照组为男性。所有COVID-19患者均病情严重,需要使用血管加压药和机械通气(图1 b).调查由当地伦理委员会批准(汉诺威样本:SEPSIS/ARDS Registry 8146_BO_K_2018;Giessen样本:05/00),并获得所有参与者或其近亲的书面知情同意。采用LEGENDplex法检测血浆e -选择素、p -选择素、ICAM-1、VCAM-1和CD31水平。采用Sandwich高灵敏度ELISA试剂盒定量vWF (#EHVWF, Thermofisher Scientific)和IL-6、IL-8、肿瘤坏死因子(TNF)-α和MCP-1 (Biolegend, San Diego, CA, USA)血浆水平。在R(版本号4,www.r-project.org).数据表示为单个数据点,箱线图覆盖指示中位数和四分位数范围。各组比较采用Wilcoxon Mann-Whitney u检验。相关性采用Spearman秩相关。
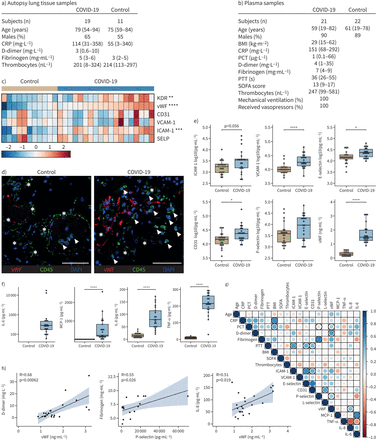
a) 2019冠状病毒病(COVID-19)患者特征及对照肺尸检样本。中位数(范围)值显示。b)用于评估血浆内皮细胞和炎症标志物水平的COVID-19队列患者特征和临床参数。中位数(范围)值显示。c) COVID-19 (n=19)和对照组(n=11)肺组织匀浆中重要内皮标记物的实时定量PCR分析。相对表达式变化的热图表示。z得分。d)对照组和COVID-19肺组织血管性血友病因子(vWF)(红色)和炎症标志物CD45(绿色)免疫荧光染色。白色箭头表示炎症细胞。白色星号表示自体荧光细胞外基质。 Scale bar: 50 µm. Circulating levels of e) endothelial markers intercellular adhesion molecule (ICAM)-1, vascular cell adhesion molecule (VCAM)-1, E-selectin, CD31, P-selectin and vWF, and f) inflammatory mediators interleukin (IL)-6, monocyte-chemoattractant protein (MCP)-1, IL-8 and tumour necrosis factor (TNF)-α in the plasma of COVID-19 patients (n=21) and healthy controls (n=22). g) Correlation matrix of clinical parameters and ICAM-1, VCAM-1, E-selectin, CD31, P-selectin, vWF, IL-6, IL-8 and MCP-1 circulating levels in COVID-19 patients. Dot size and colour correspond to the correlation coefficient, circled dots indicate significance using a threshold of p<0.05. h) Selected correlations as calculated in (d). *: p<0.05; **: p<0.01; ***: p<0.001; ****: p<0.0001. KDR/VEGFR2: vascular endothelial growth factor receptor 2; CD31/PECAM1: platelet and endothelial cell adhesion molecule 1; SELP: P-selectin; CRP: C-reactive protein; PCT: procalcitonin; PTT: partial thromboplastin time; BMI: body mass index; SOFA: sequential organ failure assessment score.
基因表达分析显示,与对照组织相比,COVID-19肺组织中ICAM-1、vWF和VEGFR2 (KDR)上调(图1 c).用于炎症细胞标志物CD45和VWF的免疫荧光染色显示出炎症细胞的渗入增加和突出的,突出的差异VWF信号(图1 d)。后者可能反映了vWF的排出增加,这一假设得到了循环vWF水平升高的支持(图1 e).除vWF外,我们还发现COVID-19血浆中VCAM-1、e -选择素和CD31水平显著升高(图1 e),提示COVID-19时内皮细胞激活/失调。此外,COVID-19血浆中炎性细胞因子IL-6、IL-8、MCP-1和TNF-α水平显著升高(图1 f).详细的相关性分析揭示了一些内皮衍生标记之间的强烈关联,而是仅具有与年龄或一般炎症参数(如C-反应蛋白)的薄弱关联(图1 g).d -二聚体水平与可溶性vWF密切相关,而部分凝血活酶时间的增加与表面标志物ICAM-1、e -选择素和CD31的脱落相关(图1 g和h)。纤维蛋白原水平与p -选择素的增加相关(图1 h).此外,血浆IL-8水平与循环vWF水平密切相关(图1 h).总之,在COVID-19患者中,局部和全身循环炎症标志物与显示内皮激活和损伤的各种标志物一致。
肺内皮细胞是一个受到严密调控的器官,在生理和病理条件下都具有多种功能。炎症细胞向肺募集是由内皮细胞表面表达的选择素(e -选择素、p -选择素)和细胞粘附分子(ICAM-1、VCAM-1)介导的。这些分子要么储存在细胞内释放出来(p -选择素),要么从新创合成(ICAM-1,VCAM-1,E-SELETIN)响应于特异性细胞因子Milieu [8].此前曾有报道称,在严重的COVID-19中,过度产生促炎细胞因子,即所谓的“细胞因子风暴”[9- - - - - -11.并在此确认。细胞因子风暴有助于从保护性内皮细胞表型转变为炎性内皮细胞表型,并与血管渗漏、组织损伤和免疫血栓形成相关。粘附分子的脱落表明内皮细胞高度活化,而血浆CD31水平升高与内皮细胞凋亡相关[8].考虑到循环中黏附分子(e -选择素、VCAM-1、ICAM-1)和CD31水平的增加,我们的数据表明,在严重的COVID-19中,内皮细胞高度炎症并部分受损。vWF mRNA和蛋白水平的局部改变以及其在COVID-19肺部的斑片状和弥漫性分布证实了这一观点。我们的数据显示,vWF和IL-8的相关性表明,Weibel-Palade体伴随释放这些蛋白,确保了对炎症细胞的损伤和招募的快速反应,进一步突出了COVID-19危重患者的内皮应激和激活。同时上调VEGFR-2表达可能显示代偿性血管生成,这已在各种疾病严重程度的COVID-19患者中观察到[2].值得注意的是,与流感引起的ARDS相比,肺组织中VCAM-1、IL-8和MCP-1表达的增加已被证明对COVID-19具有特异性[2].总的来说,我们的数据显示的是本地数据新创内皮激活和损伤标志物的合成表明肺参与了血浆中这些蛋白的积累。然而,肺相对于其他器官的贡献的大小和速率必须在未来的研究中加以解决。
一般来说,静息的肺内皮支持维持纤维蛋白溶解[9].然而,促炎介质的存在会导致一种促凝状态,最终导致凝血和血栓过度激活,就像COVID-19患者中所看到的那样。我们发现,在重症COVID-19患者中,不仅vWF的循环水平,而且其在肺中的表达也强烈升高。当内皮细胞损伤时,vWF储存在Weibel-Palade体中并迅速释放出来。它在局部促进血小板粘附和血栓形成[8].最近的一些出版物表明vWF在COVID-19血管病变中发挥重要作用[12.,13.]及急性肺栓塞后残留的肺阻塞[14.].重要的是,据报道vWF水平升高与SARS-CoV2感染患者的病情严重程度和死亡率相关[12.].d -二聚体是COVID-19重症患者凝血激活和预后不良的标志,而循环vWF与d -二聚体之间存在强正相关关系,支持了与COVID-19重症患者内皮功能障碍直接相关的促凝过程和抗凝过程之间的不平衡。最近的一项研究也强调了使用IL-8来区分高死亡率的COVID-19患者[11.].最近的发现表明,与非Covid-19 ARDS相比,Covid-19 ARDS中的循环细胞因子水平降低,而伴随着严重的Covid-19患者中的溶次纤维蛋白溶解的局部癌细胞增加增加[15.].在一起,累积评估内皮细胞活化/损伤和炎症的几个标志物可能是评估免疫血栓形成状态的有价值的工具,从而抑制Covid-19住院患者栓塞血管闭塞的风险估算。
本研究受到缺乏非Covid-19疾病对照的限制;然而,我们的数据有利于肺内皮在底层Covid-19的全身免疫病理学中的重要作用。符合其他报告,我们的作品在严重的Covid-19患者中看到内皮功能障碍和肺凝血病之间的联系。虽然需要进一步的研究来充分了解疾病的发病,进展和解决的内皮变化,但我们参与炎症细胞招生,维持内皮细胞完整性和凝血在批判性的Covid-19患者中的疾病的数据衰减内皮细胞标记。在将这些标记集成到临床实践中可能允许更好地预测Covid-19结果,因此需要使用较大的群组进行进一步的前瞻性研究。
可共享的PDF
致谢
我们要感谢西蒙娜·蒂施勒和托马斯·福克斯出色的技术援助。作者感谢吉森和马尔堡大学肺中心临床免疫学和输血医学研究所(UGMLC)获得并提供了对照血浆样本。
脚注
利益冲突:A. Birnhuber无需披露。
利益冲突:E. Fliesser没有什么可透露的。
利益冲突:G. Gorkiewicz没有什么可披露的。
利益冲突:M. Zacharias没有什么可透露的。
利益冲突:B. Seeliger无需披露。
利益冲突:S. David报告了德国研究基金会和细胞吸附剂的资助,在提交的工作之外。
利益冲突:T. Welte报告了德国研究和教育部在进行研究期间的拨款;罗氏(Roche)、诺华(Novartis)、葛兰素史克(GSK)、阿斯利康(AstraZeneca)和勃林格(Boehringer)的个人费用。
利益冲突:施密特没有什么可披露的。
利益冲突:H. Olschewski报告了来自拜耳和诺华的顾问委员会工作和非财政支持的个人费用,来自Actelion的拨款拨款,来自MSD的顾问委员会工作和研讨会支持的拨款和个人费用,辉瑞的裁决和非财政支持的个人费用,Inventiva和Algorithm Sciences的拨款,顾问委员会工作、讲座和差旅费的个人费用,勃林格的非财政支持,Chiesi、Menarini、阿斯利康和葛兰素史克的顾问委员会工作的个人费用,MedUpdate的讲座的个人费用,提交作品之外;他还是奥地利格拉茨路德维格·玻尔兹曼肺血管研究所的联合主任。
利益冲突:M. Wygrecka没有什么可透露的。
利益冲突:G. Kwapiszewska没有什么可披露的。
支持声明:E. Fliesser由奥地利研究促进局(FFG,项目编号:34926649)资助,并在格拉茨医科大学分子医学博士项目框架内接受培训。M. Wygrecka获得了德国研究基金会(DFG, sf - tr84, A2项目)的资助。
- 已收到2020年11月27日。
- 接受2021年4月26日。
- 版权所有©作者2021。
此版本在Creative Commons归因非商业许可证4.0的条款下分发。用于商业再现权和权限联系权限在}{ersnet.org