摘要
结核病(TB)预防性待遇(TPT)的扩大规模必须加快,以实现联合国结核病和结束结核病战略的联合国高级别会议设定的目标。有效的TPT的扩大率受到对运营挑战的担忧阻碍了实施Tb感染的现有测试。新的更简单的测试可以促进TB感染的测试扩大。我们提出了一种评估新的免疫因素试验来检测Tb感染的框架,旨在促进其标准化评估,并加快通过全球和国家政策和随后的扩展。该框架描述了在评估TB感染的新测试时要考虑的原则,并为制造商,研究人员,监管机构和其他用户提供指导,研究设计,人口,参考标准,样本量计算和数据分析,并且它也与全球相一致世界卫生组织在2020年通过的结核病研究与创新策略。此外,我们简要介绍了在评估新测试时应考虑的技术问题,包括皮肤测试的安全性,患者和卫生系统产生的费用,以及运营特征。
摘要
应加快评估新的,改进的结核病感染测试,以加快通过进入政策和随后的扩展来加速通过。描述了这种评估的框架。https://bit.ly/38chjbe.
介绍
治疗结核病(TB)感染,也称为结核病预防治疗(TPT),是实现2016-2035终止策略的雄心勃勃的目标所需的关键组成部分[1].TB感染的管理也对追求结核病的影响也至关重要[2].如果在可预见的未来可以在全球范围内开发和扩大全球疫苗的前景,持续措施扩大有效的TPT仍然是至关重要的。此外,在2018年第一次联合国TB的高级会议上,会员国致力于在2018-2022:600万人患有艾滋病毒(Plhiv),400万名儿童<5岁的儿童家庭接触到TB的人和2000万家庭接触者[3.].在TB患者联系人中扩大TPT覆盖的进展已经非常限于2019年的大约有大约500万次的触点[4.].没有诊断结核病感染的黄金标准方法[5.].世界卫生组织(世卫组织)目前推荐结核病皮肤测试(TST)或干扰素-γ释放测定(IGRA)以测试TB感染[6.].这种检测有助于识别出罹患结核病风险较高的人群以及可能从TPT中获益的人群,因为在大多数已发表的研究中,结核病感染检测呈阳性的人群的这种风险高于检测呈阴性的人群[7.].然而,Tb感染的目前的测试在预测感染与活性TB疾病中的进展风险有限[8.].
通过更高的预测能力(称为进展测试)的测试的开发和评估是研究的高优先级。2018年,世卫组织出版了关于此类试验特征的指导文件[9.].根据由世卫组织定义的目标产品简介,用于预测TB疾病的发展的这种测试的最佳敏感性和特异性是⩾90%[9.那10.],远高于现时可用的尖沙咀资助计划或政府资助计划[11.].直到在现场条件下可用的更好的测试可用于使用,在包括TST和IGRA的现有测试,包括TST和IGRA,仍然是选择的标准测试。
在结核病负担高的国家,来自高危人群(如艾滋病毒感染者和5岁以下的家庭接触者)的人开始TPT之前不需要进行结核病感染检测(图1)[6.].对于来自其他高危人群的人,建议进行结核病感染检测,以确定哪些人将从治疗中受益最大,并避免有不良事件风险的不必要治疗(图1)。然而,对Tb感染的测试的实施充满了困难,包括缺乏质量保证的纯化蛋白质衍生物,需要进行培训和阅读TST的需求,实验室设置不足,以便在分散的设置和高成本中进行IGRA测试(IGRA)。这需要具有更好的操作特性的新测试。
用于测试和治疗不同群体的结核病(TB)感染的算法,被认为有风险。#:如果年龄<10岁,当前任何咳嗽或发烧或与诊断为结核病的人有接触史,或报告体重下降或自上次就诊以来体重下降>5%,或生长曲线平坦或年龄< - 2 z-scores的体重。1岁以下的无症状艾滋病毒感染婴儿只有在家庭中接触过结核病的情况下才能接受结核病感染治疗。结核菌素皮肤试验(TST)或干扰素-γ释放试验(IGRA)可以确定艾滋病毒感染者(PLHIV)谁将从预防性治疗中获益最大。在开始治疗结核病感染之前,胸部x线摄影(CXR)可用于抗逆转录病毒治疗的PLHIV。¶:咳嗽、发烧、盗汗、咯血、体重减轻、胸痛、气短或疲劳。在5岁以下的儿童中,他们也应该没有厌食症,不能茁壮成长,饮食不好,活动减少或玩耍被认为是无症状的。+:包括矽肺病,透析,抗肿瘤坏死因子剂治疗,制备移植或国家指南中的其他风险。§:包括急性或慢性肝炎,外周神经病变(如果使用异烟肼)或常规和重度饮酒。怀孕或以前的结核病历史不是禁忌症。ƒ:保养法选择基于年龄,应变(药物敏感或其他),毒性,有效性和偏好风险的考虑。##:CXR可能已更早地进行,作为强化案例发现的一部分。TPT:TB预防治疗。再现和修改[6.经允许)。
新版的TST和IGRA已经上市或正在研发中,都使用了ESAT6和CFP10抗原。Diaskintest(属,莫斯科,俄罗斯)[12.]和ESAT6-CFP10(安徽治肺Longcom生物制药有限公司,安徽,中国)13.],这两者都是IGRA样皮肤试验TB感染,是市售的,并且一个新的IGRA样皮肤测试,C-Tb的(印度血清研究所,印度Pune)14.那15.],最近已开发出来。Qiagen(Venlo,荷兰),IGRA Test Quantiferon-TB Gold Plus的制造商和SD Biosensor(Suwon-Si,韩国)的IGRA都开发了IGRA的简化版本,可以使用更严重的实验室支持(M。Ruhwald;“TB感染的未来测试”,在51号联盟世界肺部健康会议上提出; 20-24 10月20日)。
由于缺乏参考标准,结核病感染检测的评估并不简单。在这里,我们提出了一个评估用于检测结核病感染的新的免疫诊断检测方法的框架,目的是促进其标准化评估,并加速纳入全球和国家政策,并随后扩大规模。该文件的主要目的是指导诊断制剂制造商、研究人员、资助者、监管机构、结核病规划协调员、民间社会和其他利益攸关方的工作。该框架由世卫组织召集的一个技术专家组制定,并听取了该领域专家的意见[16.].
这一框架的重点是评价结核病感染检测的诊断性能。此外,我们还简要概述了在评估结核病感染的新检测方法、评估皮肤试验的安全性、患者产生的成本以及卫生系统和操作特点时应考虑的技术问题。
评估结核病感染的新试验框架
缺乏适当的金标准使评估灵敏度和特异性变得复杂,而灵敏度和特异性是评估新诊断试验性能的标准方法。因此提出了替代参考标准。世卫组织在审查有关使用IGRA的证据时制定了一套参考标准(图2)[11.].
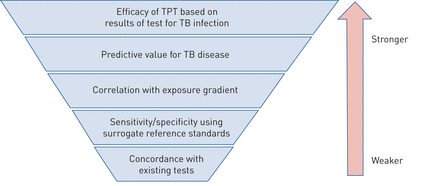
用于评估结核病(TB)感染测试的证据基础的参考标准的层次结构。TPT:TB预防治疗。再现和修改[16.经允许)。
等级等级较高的参考标准应为测试的准确性提供更强的证据,以确定将从TPT受益的人。目前在管道中的TB感染的新测试基于与TST和IGRA的类似概念;也就是说,引发免疫反应结核分枝杆菌特异性抗原要么在活的有机体内(皮肤硬结大小)或在体外(细胞因子释放的幅度)[17.].因此,预计它们在预测结核病进展风险方面不会提供显著优势。总的来说,任何新的结核病感染检测方法的预测性能都不应低于当前的技术。考虑到测量预测价值的挑战(见下文),比较新检测和现有检测之间的敏感性、特异性和一致性的研究可能是最好的可行选择。在这种情况下,一种新的结核病感染检测方法与世界卫生组织认可的作为TPT规则检测方法的至少一种现有检测方法相比,根据预先规定的界限或一致性,可以显示出非劣的敏感性和特异性。因为有越来越多的证据表明IGRA比TST具有更高的特异性和可能更高的敏感性[18.那19.], IGRA应优先作为新试验的比较指标[14.那20.].旨在实现预测性能显着改善的任何新测试应遵循评估框架,以预测TB疾病的进展[9.那10.].
学习设计与人口
研究设计1:预测性能
预测值的预测纵向研究是比较TB感染测试性能的最合适的方法,因此可以为未来的使用新测试(图3)。使用TST或IGRA测试TB感染的世卫组织建议基于对这种类型的研究进行审查[6.那21.].使用这项研究设计,筛选TB疾病的TB感染阳性或阴性试验的人;然后,那些没有结核病疾病的人进行χ12个月以进行TB疾病的发展。建议⩾12个月的随访,以确保进展的足够长的时间。这种设计的主要道德问题是,应在TPT上开始患有Tb感染阳性测试的TB风险的人们干扰诸如TB发病率或死亡率的主要终点。虽然TB发病率可以测量测试阳性的TB感染但没有接受治疗的人来衡量,但这将减少研究权力,也可能引入偏见,因为开展的人们可能与那些与那些人的终点相关的特征不同采取治疗。此外,研究设计可能妨碍研究科目的掩蔽(如。将新的TST与IGRA进行比较)。此外,不遵守提供商的建议的人更有可能停止,这可能会严重危及队列设计的完整性。然而,如果在同一队列中同时评估两个或更多个测试,则仍可导出测试预测性能的相对(不是绝对)估计。有关如何进行此类研究的详细指导,请参阅进展测试的框架[9.那10.].

研究结核病(TB)感染检测评价的研究。研究1和2包括用于简单性的图中的单一测试,但应将新测试与参考测试进行比较。研究设计1基于kIK.et al。[9.];详情见其中。红外光谱:发生率;RR:风险率;IRR:发病率比。
研究设计2:使用临床参考标准的敏感性和特异性
敏感性可以使用培养证实的结核病作为参考标准进行评估。这对减少估计准确性的偏差很重要。即使是儿科结核病和倾向于临床诊断的肺外结核病,也应鼓励使用这种方法。仅基于临床或放射学标准的诊断应该是例外的。在这种情况下,重要的是不要在诊断标准中包括结核病感染检测,因为这将虚假地高估感染检测的敏感性。
特异性取决于用于诱导免疫应答的抗原。通过使用重叠肽抗原中是高度结核分枝杆菌-特异性,例如ESAT6和CFP10,目前的IGRA测试不受Bacille Calmette-Guérin(BCG)疫苗接种的影响,与TST不同,它们的特异性基于在不太可能的低风险群体中进行的研究,它们的特异性高97-99%已被TB感染。但是,ESAT6和CFP10的表达由一组非泛骨分枝杆菌物种,包括海分枝杆菌和M. Kansasii.众所周知,导致对这些物种感染的人们的假阳性测试结果。对于特异性的估计,人口是预先接触的非常低的可能性结核分枝杆菌.重要的是通过BCG疫苗接种状态进行亚组分析,并通过暴露于不泛骨分枝杆菌的可能性来评估交叉反应的影响;例如,基于地理和人口统计学信息[22.].对于基于BCG疫苗本身(例如ESAT6或CFP10)中未发现的TB特异性抗原的TB感染的测试,不需要考虑参与者的疫苗接种状态。
试验应在相同的时间作为延迟它们之间可以引入偏压来执行。作为临床评价22.].这可能是队列研究的一部分,但纵向随访并不重要。此外,重要的是在不同的Tb流行病学环境中进行测试,尽管在具有高患TB感染的环境中不能测量特异性。如前所述,敏感性和特异性的估计需要两种不同的队列,有活跃的TB的人和具有非常低的TB感染的人。注册时应随机或连续选择每个群组的参与者。避免在可能影响可能影响测试性能的临床或疾病特征的基础上,避免从较大的潜在符合条件的人群中选择研究人群(尽管这是对新测试评估的早期阶段是可接受的)。
该测试应由参考测试和新测试的程序中经历的良好训练的人员进行。表演和评估测试的人应蒙蔽其他测试的结果。监督,监测和质量控制方法应充分且清楚地描述。这些要点也适用于协调的研究。
研究设计3:测试的一致性
这种设计基本上与新基准测试协议的研究,是用于诊断测试评估证据的最低水平。应当指出的是,一致性可能是低时,新的测试被认为具有较高的预测性能和灵敏性和特异性。因此,当新的测试提供了超过现有的测试运营优势,但在诊断性能没有收获,预计这样的设计是适当的。
学习参与者应该代表一般人群。例如,重要的是包括非常年轻或老年人,孕妇,患有更严重的疾病或具有严重合并症的人的人(如。艾滋病,糖尿病,肾功能衰竭,营养不良),因为这些可能会影响测试性能。留学不同结核病流行病学设置和非结核分枝杆菌的预期负担协议鼓励。
当进行两项检测时,应在同一时间进行,最好是在同一样本上(如果基于血液或尿液)。如果分析皮肤试验,应同时在每组进行参考试验和指数试验。收集血液或尿液标本在体外TB感染的测试应同时或在管理TST以避免升压效果之前进行[23.].
样本量计算
样本尺寸的原理确定:优越性与非
如果参考测试具有次优性能,则优越性设计和相关样本量计算是合适的。例如,判断Tb感染的当前测试的敏感性是次优。患有患儿和免疫引起的人群的敏感性特别是疾病风险增加的免疫因素,因此是测试结核病感染的优先考虑。因此,如果它具有卓越的敏感性,特别是在这些高风险的人群中,新测试将具有很大的兴趣。
如果参考测试具有优异的特异性,例如当前IGRA的97-99%特异性,则需要大的样本量来展示优越性(表1)[24.].然而,一个新的检测可能具有不逊于现有检测的特异性,并且由于其他优点而成为首选。如果选择了非劣效性设计,那么这些其他重要的优势,如降低病人或卫生系统的成本,增强的可行性,或护理点的可用性,必须预先指定,并仔细衡量。同样值得注意的是,当标准或参考试验具有非常好的性能时,非劣效设计应保留用于测试性能,例如IGRA试验的特异性的例子。这是必要的,以避免随着时间的推移,测试性能逐渐恶化的风险,如果新出现的技术相继使用非劣效标准与上一代测试进行比较[25.].
样本容量的一般决定因素
在设计一项研究时,特别重要的是预先指定效应大小,或预期差异,无论是优势设计还是非劣势设计。一般来说,效应量越大,样本量越小。重要的是要认识到,更大的效应量可能是不现实的,可能导致错误的结论。在参与者太少的研究中,一种新的测试具有更好的性能,但与参考测试有一点不同,可能无法显示出优越性,因为跨越空值的置信区间很宽。用于样本量计算的参考检验的性能估计应该基于最近进行的高质量的系统评估,以确保其准确性。
特定的样本量计算和研究分析
预测性能
理想情况下,新检测方法具有良好的敏感性和合理的特异性。然而,结核病感染的新检测方法预计不会大幅提高预测价值,大多数进展预计将出现在操作方面。因此,在预测性能方面证明非劣效性是可以接受的。
样本量计算必须考虑未来TB疾病的可能性,因为这决定了事件的数量,目前测试在预测这些事件时的敏感性,以及新测试和随访时间的敏感性的差异。虽然更长的随访时间减少了所需的样品大小,但可能导致随访的损失更大,并导致高传输设置中重新凝集的风险更高,这可能使对初始测试的解释复杂化。因此,不鼓励更长的后续行动时间,至少用于主要分析和样本量计算。
队列研究中的事件发生率通常计算为每100人年随访的事件数,这解释了大规模队列中不同的随访时间。由于同一个人将进行两次或两次以上的结核病感染检测,事件发生率的差异可以直接计算出来,既可以作为风险差异,也可以作为风险比。发病率比率可估计为检测阳性者的发病率/检测阴性者的发病率。
敏感性和特异性
结核病感染电流试验通常具有次优的灵敏度。灵敏度是儿童,艾滋病毒感染者和其他免疫力低下的人群低。在这些人群中,一个新的测试的优势将是优选的非劣效性设计。
目前的IGRA检测具有很好的特异性。因此,优越的特异性既没有必要也不可能被证明。因此,当参考标准试验是IGRA或未接种过bcg的人群中的TST时,非劣效设计足以具有特异性。如果参考标准是接种卡介苗人群的TST,那么推荐一种优越的设计。
可以使用基于上述参考标准的标准配方来计算灵敏度和特异性。然而,在具有非常低的Tb流行率的人群中,可以使用作为分母的人数的人数来近似特异性,而不是没有结核病感染的人数,如下:所有测试负面/所有人在非常测试的人- 流行人口。
一致
如果预计新测试具有与参考测试相似的诊断准确性,但具有操作优势,如成本更低或更大的可行性,那么显示高度一致的测试是有价值的。应计算κ统计量,并给出相应的95%置信区间。κ-统计解释了偶然性校正的一致性,这在阳性检测流行率非常低或非常高的情况下尤其重要。k的最大可接受宽度95%置信区间、潜在的阳性真实比例和k的期望值决定样本量26.].
技术问题
免疫测定是一种复杂的测定方法,受多种可影响结果的可变性的影响。表2列出了在在体外结核病感染的检测,如IGRA,应优先由开发人员在技术描述的分析。完整名单可在其他地方查阅[16.].
由于免疫测定检测连续刻度的响应,通过使用阈值(截止)将其转换为正或负作为正或负面的二进制结果(截止),对该截止的可变性的描述特别相关。为了确定任何新测试的截止阈值周围的可变性程度,我们建议使用足够数量的参与者评估IGRA结果的变化,其中没有积极的结核病,其中代表群组中正常生理范围的正常生理范围。感染很可能,重新感染事件很少见。例如,近期成人移民从高结核病发生率到低对中发病率国家的研究,其中TPT未常规启动阳性IGRA结果,可以检验初始IGRA阳性的可重复性,从重新感染的影响最小。同样,IGRA结果的再现性通常在医疗工作者中进行了评估,证明了结果的波动[27.].还可以对最近转为阳性检测的结核病患者的接触者进行随访,以评估逆转的可能性。样本应使用预定义的检测阳性临界值来估计IGRA转换/逆转的速率。在IGRA转换的情况下,可以收集第三个样本来评估使用预先定义的截止是否由于一个结核分枝杆菌感染事件,而不是截止截止围绕变异性的虚假效果。在定义不确定性区域的范围时,应排除来自这些参与者的样本。
The QuantiFERON-TB Gold In-Tube and QuantiFERON-TB Gold Plus assays report considerable variability around the assay cut-off of 0.35 IU·mL-1[28.].虽然任何新的IGRA的临界值应根据与现有测试(如QuantiFERON-TB Gold Plus)的一致性来定义,但制造商应谨慎地在这个不确定区域报告测试结果。任何新的IGRA评估也应报告IU·mL-1对于有丝分裂原,分别以抗原和未刺激对照。每一个新的IGRA都需要研究不确定性区域。只有二进制读数的结核感染检测应该提供额外的数据,以确认重现性,而不会导致大量无效结果。来自结核病感染可能性极低的人群以及确诊的结核病患者的参与者样本,应用于建立一系列临床相关样本预期的干扰素-γ应答。
对皮肤测试安全的评估
新皮肤测试的安全性应根据新测试的目标群体的群体代表参考皮肤测试(TST)进行评估,以表明注射部位反应和其他不良事件类似于或少于TST。应在各种群体中评估安全,如Plhiv,儿童和孕妇和哺乳期。TST是安全给孕妇和哺乳期妇女管理。同样,在给予怀孕或哺乳期妇女时,Tb感染的新皮肤测试不太可能对Tb感染的新皮肤试验导致对胎儿或护理婴儿的不利影响。
研究设计应力求在查明局部不良反应偏差最小化。一种方法是,得到在同一时间的新的基准测试中在双盲方式各前臂。以评估安全性的另一种方法是比较不良事件的随机对照试验报告。然而,审判不太可能足以检测罕见的不良反应和上市后监测是必不可少的。方法记录不良事件应充分和明确的记载,如。使用MedDRA分类(www.meddra.org/)。随着皮肤测试的设计诱导局部反应,重要的是预先定义如何将反应解释为相关的诱导或不良事件。
经济评价
与现有测试相比,新测试应理想地具有较低的卫生系统和患者成本。为了评估这方面,应考虑在评估新测试的研究中考虑与新测试的启动和常规操作相关的成本。理想情况下,应将经济评估纳入研究现场或独立研究研究的研究。无论研究设置如何,重要的是努力记录实施新测试的“真实”成本(即正如它将在实践中使用)。应考虑下列费用:实验室设备和开办;计算机和软件;供应;冷链要求;人员时间适用于不同方面的测试;初期和持续培训;质量控制与监督;以及检查呈阳性或阴性的病人到卫生设施就诊。在考虑实施时,应采用最佳的护理组织模式(如。“一站式服务”,当天协调并提供对检测呈阳性的人的后续护理)。关于在评价期间要考虑的具体费用的更多细节载于补充表.
操作特征
结核病感染的新检测方法还应解决与现有检测方法相关的业务挑战。在医疗系统的最低层次部署的能力尤其重要。需要无需仪器的测试,或可以用小型、便携式或手持的由电池或太阳能供电的仪器进行的测试。快速测试(如。<1小时的结果)也提供了一个巨大的优势。皮肤测试和在体外试验,应根据适用于素质预算标准的不同条件建立试剂的稳定性[29.].试剂在高温和潮湿条件下保持足够长的稳定时间是可取的,并且不需要冷链来运输它们。不需要抽取静脉血样本的检测将是首选。
结束言论
TPT的吸收在全球范围内非常缓慢,部分原因是关于与当前测试相关的性能和运营挑战的担忧。结核病感染的新测试提供了促进规模和瞄准TPT的机会,以便更有效地使用。他们还支持改善TB预防性治疗的其他举措,例如2020年发布的新目标产品概况。该框架的实施用于评估TB感染的新测试将有助于对新测试的标准化评估,并将加快他们的国家政策。在实现全球目标所需的规模中。
补充材料
可分享的PDF.
致谢
我们感谢以下个人对世卫组织发表的原始文件的关键审查:塞维利亚·埃姆·梅多夫(美国国际发展局),Claudia Denkinger(Heidelberg大学),Darragh Duffy(Institut Pasteur,法国),纳粹Ismail(国家传染病,南非),AfrânioKritski(联邦里约热内卢大学,巴西),Elisa Nemes(开普敦,南非大学)和Molebogeng X. Rangaka(英国伦敦大学学院)。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
利益冲突:滨田没有什么可披露的。
兴趣冲突:S. DEN BOON没有什么可披露的。
利益冲突:D.M.奇里洛有没有透露。
利益冲突:A.佩恩 - 尼科尔森:找有几个临床研究项目,以评估对已经通过协商一致的过程定义公布目标产品简介多个新的诊断测试。这些研究是由私营公司提供谁进入发达国家诊断产品的技术诀窍,设备/试剂,并通过无限制的捐款按FIND政策和外部审核SAC贡献。FIND还没有分配的任何金融价值诀窍或接入设备通过这些项目获得的。目前的项目在www.finddx.org上市以获取更多信息。此外,A.佩恩-尼克尔森具有专利WO2016123058A1 WIPO(PCT)(生物标志物检测结核病的风险2016年8月4日)的未决的和专利WO2017081618A9 WIPO(PCT)(生物标志物用于确定预期的风险为积极开发结核2017年7月13日)悬而未决。
兴趣冲突:M.Ruhwald:查找有几个临床研究项目可以评估通过共识过程所定义的发布目标产品简介的多个新的诊断测试。这些研究是由私营公司提供谁进入发达国家诊断产品的技术诀窍,设备/试剂,并通过无限制的捐款按FIND政策和外部审核SAC贡献。FIND还没有分配的任何金融价值诀窍或接入设备通过这些项目获得的。目前的项目在www.finddx.org上市以获取更多信息。此外,M.Ruhwald还有一个授予血清研究所的专利WO2017084671A1,并发给达龄血清研究所的专利O2008028489A2。
利益冲突:D.孟席斯没有什么可透露的。
利益冲突:O. Oxlade没有什么可披露的。
利益冲突:D.法尔松没有什么可披露的。
利益冲突:A.坎查尔没什么可透露的。
利益冲突:A. Korobitsyn没有什么可以披露的。
利益冲突:M. Zignol有没有透露。
利益冲突:A. Matteelli无需披露。
利益冲突:T. Kasaeva无需披露。
- 收到2020年11月4日。
- 接受2021年1月2日。
- 版权所有©作者2021。
此版本在Creative Commons归因许可证4.0的条款下分发。
















