摘要
在普通人群中,肺功能加速下降与心血管疾病(CVD)风险增加有关,但对慢性阻塞性肺疾病(COPD)的相关性知之甚少。我们调查了初级保健COPD人群中肺功能加速下降与CVD结局和死亡率之间的关联。
临床实践研究数据链(CPRD)-GOLD初级保健数据集确定无CVD病史的COPD患者(n=36 382)。1秒内用力呼气量(FEV)加速下降1)的定义是使用COPD人群下降最快的四分之一。用Cox回归评估基线加速FEV之间的关系1下降和随访中心血管疾病的综合结果(心肌梗死、缺血性卒中、心力衰竭、房颤、冠状动脉疾病和心血管疾病死亡率)。根据年龄、性别、吸烟状况、体重指数、哮喘史、高血压史、糖尿病史、他汀类药物使用史、改良医学研究委员会(Modified Medical Research Council, mMRC)呼吸困难评分、发作频率和基线FEV对模型进行了调整1%预测。
6110名COPD患者(16.8%)在随访期间发生CVD事件;平均随访时间为3.6天 年(四分位间距(IQR)1.7-6.1年)。FEV的中位发病率1下降幅度为-19.4 毫升·年−1(差-40.5 - -1.9);9095例患者(25%)FEV加速1下降(> -40.5毫升·−1), 27287(75%)未发生(≤ -40.5 mL·年)−1).CVD风险和死亡率在有和没有FEV加速的患者之间相似1下降(人力资源邻接的相应的风险估计值:心力衰竭为0.99(95%CI 0.83-1.20),心肌梗死为0.89(95%CI 0.70-1.12),中风为1.01(95%CI 0.82-1.23),心房颤动为0.97(95%CI 0.81-1.15),冠心病为1.02(95%CI 0.87-1.19),冠心病为0.94(95%CI 0.71-1.25)相反,CVD风险与mMRC评分相关≤2和前一年的两次或两次以上恶化。
CVD结局和死亡率与病情加重的频率和严重程度以及mMRC呼吸困难评分的增加有关,但与FEV加速无关1下降。
摘要
在COPD患者的初级保健人群中,CVD结局和死亡率与FEV加速无关1下降,但伴有慢性阻塞性肺病频繁和严重的恶化,呼吸困难加剧https://bit.ly/35APXL6
介绍
用力呼气量1 s(FEV1)从成年初期开始随年龄增长而下降。之前的一项荟萃分析发现,在普通人群中,FEV的平均比率1老年人的下降幅度为-9.9 毫升·年−1至–56.0 毫升·年−1中位下降-29.4 mL·年−1[1].然而,慢性阻塞性肺疾病(COPD)患者以加速的速度失去肺功能,约为-33.2 mL·年−1根据V埃斯特博等.[2].COPD的下降率是高度异质性的,有~ 38%的患者> -40 mL·年下降−1在-21毫升·年的价格下,则为31%−1和–40 毫升·年−1, 31%为< -21 mL·year−1[2].有几个因素与COPD患者肺功能变化速率相关,包括COPD急性加重(AECOPD)的频率和严重程度、吸烟和COPD严重程度[3.- - - - - -8].然而,对COPD患者肺功能下降率与共病之间的关系知之甚少。
COPD患者最普遍的合并症之一是心血管疾病(CVD) [9].COPD和CVD都有共同的危险因素,如。吸烟与老化[10,11].具体来说,接触香烟烟雾中的有毒颗粒会导致系统性炎症加剧,这是慢性阻塞性肺病和心血管疾病的特征[12,13].目前还不完全了解COPD和CVD除了共同的风险因素外是如何联系的,但研究人员已经确定了一些可能的机制,如缺氧和氧化应激,可能涉及[9,10].此外,许多研究报告了各种测量肺功能受损(包括低FEV)之间的关联1、强迫肺活量(FVC)和FEV1/FVC,发展心血管疾病的可能性增加,以及心血管疾病继发住院和死亡的风险增加[14- - - - - -20.].
最近,有人提出肺功能丧失的速度与心血管疾病的风险有关。在一项针对社区动脉粥样硬化风险(ARIC)研究参与者的一般人群研究中,FEV加速下降1在3年的基线期间内,与因心力衰竭和中风而住院和死亡的风险增加相关[21]到目前为止,还没有研究调查FEV感染率和死亡率之间的关系1慢性阻塞性肺病患者心血管疾病转归和死亡率的下降和风险,这些患者的心血管疾病风险已经高于普通人群[9].因此,我们调查COPD患者是否存在FEV加速1在英国的初级保健人群中,COPD患者更有可能发展为CVD。
方法
研究人群和设计
临床实践研究数据链(CPRD)-GOLD是一个初级保健电子医疗记录数据库。它包含了英国全科医生(GP)实践的信息,包括会诊、患者人口统计、处方治疗和临床诊断。CPRD约占英国人口的7%,在年龄、性别和种族方面可泛化[22].CPRD为英国患者的这项研究提供了来自医院事件统计(HES)和国家统计局(ONS)的关联假名数据。数据由NHS Digital连接,使用仅由NHS Digital持有的可识别数据。全科医生在执业水平上同意这一过程,患者个人有权选择退出。HES和ONS数据用于确定心血管疾病住院和死亡病例。
符合以下最低纳入标准的患者被纳入:1)符合HES连锁标准,2)诊断为COPD, 3)年龄在35岁或以上,4)吸烟者或戒烟者,5)数据从2004年开始记录。具体而言,纳入日期为患者首次FEV的日期1在他们被诊断为慢性阻塞性肺病、向目前的全科医生注册、年龄35岁以及该实践被认为是研究质量的日期之后进行测量(图1) [22].
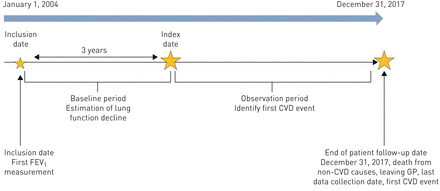
研究设计。FEV1:1小时用力呼气量 s、 心血管疾病:心血管疾病;全科医生:全科医生。
在纳入日期之后,患者需要进行3年的基线随访,至少两次FEV1至少6个月的间隔测量,以估计患者的FEV速率1下降;应在较长时间内估计肺功能的变化,以得出长期肺功能下降的结论,并减少可能的测量误差[23].指数日期是基线期结束的日期,表示随访开始(图1).因此,从患者的索引日期到2017年12月31日,或以下事件的第一个日期,对患者进行随访:转移到非CPRD GP机构,最后一个数据收集日期,死于非CVD原因或有CVD事件。此外,要求患者无中风、心力衰竭、心肌梗死史在索引日期之前记录的心律失常、心房颤动或冠状动脉疾病。
慢性阻塞性肺病和FEV1下降
使用CPRD-GOLD中经过验证的COPD算法识别COPD患者[24].年龄在35岁及以上,且至少有一项临床诊断为慢性阻塞性肺病且有吸烟史(以前或现在)的患者被认为患有慢性阻塞性肺病。由于COPD与哮喘的潜在分类错误,从不吸烟的人被排除在外。FEV加速了感兴趣的暴露1下降。对于每个研究合格患者,所有绝对FEV1CPRD-GOLD中记录的从纳入日期到指标日期之间的测量值和FEV速率进行了识别1使用随机截距和随机斜率的混合线性回归模型估计的下降。加速下降定义为FEV1下降速度是下降速度最快的四分之一。患者分为有或没有加速FEV1在最近的一项验证研究中,肺活量测量的质量被发现很高[25].
心血管疾病的结果
主要结果是一项综合指标,定义为随访中第一次心血管事件发生的时间。CVD事件包括心肌梗死、心力衰竭、卒中、房颤、冠心病(不包括急性心肌梗死)和CVD死亡率。这些事件是通过初级保健记录(CPRD-GOLD)、住院数据(HES)和死亡率统计(ONS)确定的。国际疾病分类第10版(ICD-10)代码用于确定住院(初级诊断)和CVD死亡。进一步探讨CPRD-GOLD、HES和/或ONS中同一天记录的CVD事件,以避免重复事件。在这些情况下,优先考虑死亡事件,其次是住院事件,然后是gp记录事件。次要结果包括首次心肌梗死、心力衰竭、卒中、房颤、冠状动脉疾病或CVD死亡率的时间。
统计分析
基线特征用比例、中位数和四分位范围(IQR)描述。Cox回归研究首次复合CVD事件发生的时间,比较有和没有加速FEV的患者1下降,调整性别、年龄(连续)、吸烟状况(当前或曾经吸烟)和气流阻塞水平(轻度:FEV)1≤80%预测值;中等:钒铁150% - -80%的预测;严重:FEV130%–50%预测;非常严重:FEV1< 30%的预测;基于患者最后一次FEV基线1改良医学研究委员会(mMRC)的呼吸困难评分(0-4)和体重指数(BMI)(体重不足、正常、超重、肥胖)被定义为在3个基线期内最接近指数日期的测量值 年。在3年的基线期内确定有高血压、糖尿病或哮喘病史 年。他汀类药物的使用被定义为在指数日期前一年内至少有一种处方。AECOPD的频率和严重程度(中度:GP记录的AECOPD;重度:AECOPD住院)也使用指数日期前一年记录的信息进行定义,并分类为无;一个中度和零重度;两个中度和零重度;三个或更多中度和零重度;一个重度和任意数量的中度;以及两个或更多重度和任意数量的中度。该分类与上一年的分类类似CPRD-GOLD中AECOPD事件的详细调查[26].二次分析研究了加速FEV之间的关联1和每一个单独的心血管疾病事件即。心肌梗死、心力衰竭、中风、心房颤动、冠心病和CVD死亡率。
还进行了以下敏感性分析:1)FEV的相对变化率1FEV的变化1%预测值用于分类加速下降(与绝对FEV相反)1);2)比较加速FEV患者CVD结局和死亡率的风险1另外三个四分位数分别为下降和患者;3)FEV率之间的线性关系1研究心血管疾病的下降和风险;4)使用不同的截止值(> −20 mL·年)−1(参照组),−20 - −40 mL·year−1, −40– −60 毫升·年−1和< −60毫升·−1)来定义四组FEV速率1下降;5)样条回归分析加速FEV之间的非线性关系1使用第10、50和90个百分位数的FEV可以降低CVD结局的风险1下降;6)将有哮喘病史的患者排除在COPD误诊病例之外;7)仅调查住院心血管事件作为结果;8)仅调查gp记录的CVD结果作为结果;9)只调查心血管疾病死亡作为结果;10)按性别、年龄、吸烟情况、AECOPD频率和气流阻塞程度(即。基线FEV1%预测);11)加速FEV1使用FEV速率对下降进行分类1使用至少四个FEV估算的下降1基线期间的测量;12)加速FEV1使用FEV速率对下降进行分类1下降估计使用至少两FEV1测量间隔至少2年;13)加速FEV之间的关联1随访第一年复合心血管疾病、心力衰竭、心肌梗死、卒中、房颤和冠状动脉疾病的下降和风险;14)随访期间所有的CVD事件都被确定(不仅仅是第一次事件),泊松回归用于模拟重复事件。所有分析使用STATA v16.0 (StatCorp, College Station, TX, USA)进行。
后果
病人的特点
我们确定了132个 923名CPRD-GOLD患者符合我们的最低资格标准。在应用进一步的纳入标准后,36 382名患者被纳入最终研究人群(图2).中位随访时间为3.6年(IQR 1.7-6.1年)。FEV的中位速率1下降幅度为-19.4 毫升·年−1(差-40.5 - -1.9毫升·−1),因此患者被归类为FEV加速1如果他们有FEV,就拒绝1下降速度快于-40.5 mL·年−1.这意味着9095名患者(25%)被归类为加速衰退,27287名患者(75%)被归类为未加速衰退。患者中位FEV为3 (IQR 2-4)1三年基线期间的测量。补充图E1、E2举例说明FEV的数量1基线期间的测量和测量之间的时间间隔。
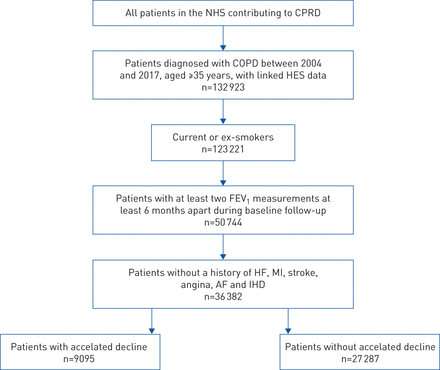
符合纳入标准的患者。NHS:国民保健服务;CPRD:临床实践研究数据链;COPD:慢性阻塞性肺疾病;HES:医院事件统计;FEV1: 1秒内用力呼气量;心力衰竭:心力衰竭;心肌梗死:心肌梗塞;房颤:心房颤动;缺血性心脏病。
表1报告了有和没有加速FEV的患者的基线特征1下降。加速下降的患者多为男性,有严重的气流阻塞(FEV较低1%患者在所有其他心血管疾病特征方面(糖尿病和他汀类药物的使用)相似。
心血管疾病的风险
在随访期间,6110名患者发生了心血管事件,这相当于每100人年4.6个事件(95% CI 4.5-4.7事件每100人年)。我们没有发现复合CVD事件的风险与加速FEV之间存在关联的证据1在我们未经调整的分析(HR未调整0.99, 95% CI 0.93-1.05)或在完全调整分析(HR邻接的0.98, 95%可信区间0.90-1.06)(图3).然而,我们确实发现了AECOPD和呼吸困难(mMRC)的频率和严重程度增加与CVD结果之间的关联(图3)此外,与对照组相比,年龄、男性、吸烟、高血压和他汀类药物的使用增加了心血管事件的风险(补充表E1).
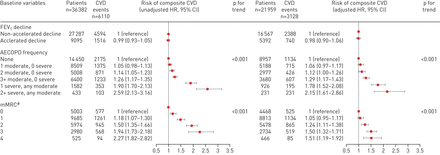
危险比(95% CI)显示1秒内用力呼气量(FEV)加速下降之间的关联1)、慢性阻塞性肺疾病(AECOPDs)急性加重频率、改良医学研究委员会(mMRC)评分以及心血管疾病(CVD)结局和死亡率的风险。#:mMCR分数在12中缺失 215名患者。
在随访期间有心血管疾病事件的6110名患者中,记录了1220名心衰患者、788名心肌梗死患者、1039名中风患者、1427名房颤患者和1636名冠状动脉疾病患者。有556例心血管病相关死亡。加速FEV之间没有关联1下降和心力衰竭(HR邻接的0.99, 95% CI 0.83-1.20)、心肌梗死(HR邻接的0.89,95%可信区间0.70–1.12),卒中(HR邻接的1.01,95%可信区间0.82–1.23),心房颤动(HR邻接的0.97,95%可信区间0.81–1.15),冠心病(HR邻接的1.02, 95% CI 0.87-1.19)和CVD死亡率(HR邻接的0.94,95%可信区间0.71-1.25)(图4).而加速的FEV之间未发现关联1在未调整的模型中,单个CVD结局的下降和风险、AECOPD的频率和严重程度的增加和mMRC的增加与所有CVD结局单独相关。补充表E2-E7分别提供心衰、心肌梗死、卒中、房颤和冠状动脉疾病各模型中所有协变量的危险比。
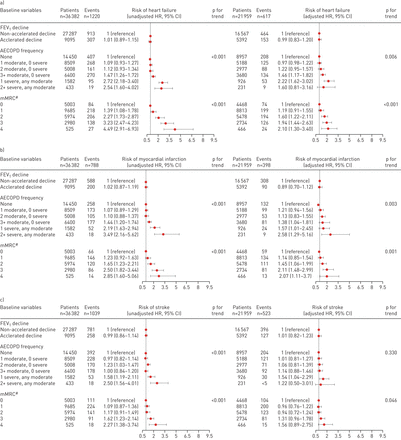
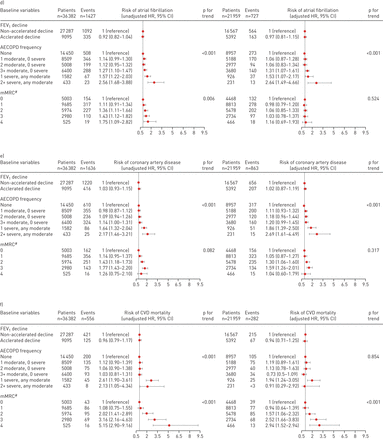
危险比(95% CI)显示1秒内用力呼气量(FEV)加速下降之间的关联1)、慢性阻塞性肺疾病(AECOPDs)急性加重频率、改良医学研究委员会(mMRC)评分和a)心力衰竭、b)心肌梗死、c)中风、d)心房颤动、e)冠状动脉疾病和f)心血管疾病(CVD)死亡率的风险。#:“调整”分析中mMCR评分缺失的患者比例;看到表1为进一步的信息。
敏感性分析
无论肺功能丧失率(FEV)用于对患者进行分类的定义和临界值是什么,CVD的风险在有无加速衰退的患者之间是相似的1).当以FEV来量化加速下降时,这一发现仍未改变1%预测FEV或相对变化1与基线相比,FEV线性速率之间没有相关性1心血管疾病的下降和风险(补充表E8)此外,FEV患者的CVD风险没有差异1最慢四分位数和所有其他四分位数的下降(补充表E8),在FEV患者之间1拒绝> −20 毫升·年−1以及感染FEV的病人1幅度下降−20– −40 毫升·年−1, −40– −60 毫升·年−1和< −60毫升·−1(补充表E9),或介于加速和非加速FEV之间1样条回归(补充图E3).
当分析仅限于无哮喘史的COPD患者时,有和没有FEV加速的患者之间的CVD风险没有差异1下降(补充表E10).将分析限制在初级保健记录的事件(gp诊断的CVD)和CVD住院治疗中,并没有对我们的效果估计产生实质性影响(补充表E11).没有发现加速FEV之间的关联1按性别、年龄、吸烟状况、AECOPD频率和气流阻塞(基线FEV)分层后,CVD和死亡率的下降和风险1%预测)(补充表E12).
只包括那些至少有四次FEV的患者1测量或仅测量至少两个FEV1间隔至少2年的测量也没有产生加速FEV之间关联的危险比的可察觉的变化1下降和心血管疾病风险(补充表E13和E14).我们也没有观察到加速FEV之间的关联1心衰、心肌梗死、中风、房颤和冠状动脉疾病的下降和风险,作为随访第一年的单独结果或综合结果(补充图E4).最后,在敏感性分析中,我们考虑了随访期间的多个CVD事件(发生率为每100人年9.5事件,95% CI 9.2-9.8事件/ 100人年),我们发现,在有和没有加速FEV的患者之间,复合CVD的发生率及其个体成分是相似的1下降(补充图E5).
讨论
这是第一个大型观察研究,以调查加速FEV之间的关联1慢性阻塞性肺病患者心血管疾病预后和死亡率的下降和风险。我们发现在cvd患者中,那些FEV加速的患者1无论CVD事件的类型如何,下降与没有加速下降的患者有相似的CVD结局和死亡率风险。其他疾病特征与CVD结局和死亡率更密切相关,包括频繁的中、重度AECOPD病史和呼吸困难增加。
先前的研究
之前没有研究调查COPD人群中肺功能下降和CVD之间的关系。Silvestreet al。[21]使用ARIC研究对居住在美国的一般人群进行了调查。作者发现FEV加速的人1在17年的时间里,下降速度更快的人比没有加速下降的人患心血管疾病的风险更大。CVD被定义为一个复合终点,包括因心力衰竭、中风和冠心病(包括心肌梗死)而住院或死亡。当对每一种CVD成分分别进行分析时,他们发现了加速FEV1衰退与心力衰竭和中风事件密切相关,但与冠心病事件无关。
我们的研究与S的研究有许多不同之处ilvestre等.[21可以解释观察到的差异。ARIC是一项队列研究,从1987年开始跟踪参与者,以了解动脉粥样硬化的原因和其他临床结果,包括CVD危险因素。这些参与者的数据是由经过培训的医疗保健人员在随访的四个阶段系统收集的。这与CPRD-GOLD不同,CPRD-GOLD是一个定期收集的医疗信息数据库,记录了全英国初级保健全科医生的实践。虽然这两种类型的数据库都有优点,但研究结果可能是不同的。此外,年代ilvestre等.[21使用FEV的相对变化1从基线到估计加速FEV的预测百分比1下降。我们的研究使用了FEV的绝对变化1调整基线FEV1.此外,我们利用FEV的变化进行敏感性分析1%绝对FEV的预测和相对变化1结果与我们的主要结果一致。最后,虽然年代ilvestreet al。[21]调整基线FEV1,其他诊断如慢性阻塞性肺病或气流阻塞未被考虑在内。有可能COPD患者混淆了FEV与FEV之间的关系1下降和心血管疾病结局。同样重要的是要注意,在有和没有加速FEV的人群之间,与心血管疾病结局的关联程度1在美国,它的规模很小ilvestreet al。研究[21],表明他们的风险(HR)略有增加邻接的1.14, 95%可信区间1.06-1.23)。
其他研究发现,肺功能低下(FEV和1和FVC)与一般人群晚年心血管疾病的风险有关[14,18- - - - - -20.].例如,在ARIC研究中,最低分位数的参与者因心力衰竭住院或死亡的风险比最高分位数的参与者高。这一风险在气流阻塞(FEV)的参与者中也较高1/FVC <70%),不论男性还是女性[14].同样,这可能是由通常FEV较低的COPD患者造成的1比同龄健康的人要多同样,健康、衰老和身体组成(ABC)研究[15]和年轻人冠状动脉风险发展(CARDIA)研究[16,美国两项基于社区的研究发现,FEV之间存在线性关联1%预测和事件的心力衰竭和中风住院。然而,总体而言,几乎没有证据表明,与肺功能较高相比,COPD患者肺功能较低与心血管疾病预后和死亡率相关。最近的一次事后对SUMMIT试验数据的分析发现,FEV1在CVD风险增加的COPD人群中,预测的%与CVD事件无关[27].这与我们的调整结果一致,即FEV基线1与心血管疾病风险和死亡率无关。FEV之间的联系1, FEV1非慢性阻塞性肺疾病一般人群和慢性阻塞性肺疾病人群之间的下降和CVD存在差异。
COPD加重、mMRC评分和CVD
在我们的COPD患者队列中,AECOPD的频率和严重程度以及mMRC评分的增加与CVD结局和死亡率的风险增加相关。这表明,疾病严重程度的其他标志物,而不是肺功能下降率,可能与CVD结局和死亡率更密切相关[28].这一观察结果与先前的观察性研究一致,即AECOPD发生心血管事件(如心肌梗死和中风)的风险相对于更稳定的疾病时期是极高的。例如,Rothnie等.[29]使用相关的英国初级保健数据(CPRD-GOLD和HES)来研究AECOPD(中度和重度)与心肌梗死和卒中(AECOPD后91天)之间的关系。AECOPD后发生心肌梗死和卒中的风险增加,且AECOPD越严重的患者发生心肌梗死和卒中的风险更高。另一项英国初级保健患者的观察性研究(THIN数据库)发现,COPD患者在AECOPD后5天内出现心肌梗死的风险更高[30.].同样,一个事后SUMMIT研究的数据分析报告了AECOPD与心血管疾病结局(包括死亡、心肌梗死、中风、心绞痛和短暂性缺血发作)风险增加之间的关联,该风险在AECOPD后长达1年,在严重AECOPD后升高[31].
很少有研究调查AECOPD频率与心血管疾病结局之间的长期相关性indsor等.[32]使用英国初级保健全科医生数据(CPRD-GOLD)进行了一项病例对照研究,比较了频繁发作(指标日期前一年两次或两次以上AECOPD)和非频繁发作患者发生中风的几率。他们发现,在最长9年的时间里,AECOPD频率与中风之间没有关系[32]然而,本研究没有使用二级护理数据,导致潜在的重大错误分类,因为它们不能包括更严重的AECOPD或中风。先前的验证研究强调了使用与CPRD相关的二级护理数据识别事件的重要性[33].特别是Windsoret al。研究[32]很可能错过了相当大比例更严重的aecopd或中风。相比之下,我们的研究采用了HES和CPRD-GOLD相关数据的队列设计,发现在最长13年的随访中,aecopd的频率和严重程度都与CVD结局风险密切相关。
优势和局限性
这是第一个研究COPD人群中肺功能下降率和CVD结局风险之间关系的研究。通过使用电子医疗记录,我们能够确定具有不同疾病严重程度的大量慢性阻塞性肺病患者(N=132 923),从而创建一个更具有广泛性的慢性阻塞性肺病患者群体。我们纳入了广泛的CVD终点(基于gp治疗或住院的CVD事件,包括中度和重度),以捕捉不同程度的CVD事件严重程度。而绝对FEV的变化1是我们的主要暴露,在之前关于肺功能下降的研究之后,我们纳入了基线FEV1%在我们的模型中预测为混杂因素,并使用FEV的相对变化进行了敏感性分析1[2,8,34].由于患者内部的绝对FEV变异高1, FEV1%在小于5%的研究中,预测被认为在估计肺功能变化方面更好 多年的后续行动[35].我们利用FEV的变化进行了敏感性分析1%预测结果与我们的主要分析结果一致。
为了确定基线时肺功能下降的速率,最大限度地减少测量误差的影响,并准确总结患者的肺功能下降,根据先前的研究,要求患者至少进行3次测量 开始随访前的基线随访年数[21]因此,该设计可能会导致永久性的时间偏差。然而,基线轨迹可能会保持不变,任何疾病改变都不可能改变患者从加速下降到非加速下降的轨迹,也不会影响CVD的风险,因为没有发现与另一个潜在问题是COPD患者可能被误诊为哮喘和哮喘反之亦然.这在40岁以上的患者中更为常见[36].这是数据的局限性,因为我们依赖于全科医生记录的诊断和症状。我们进行了敏感性分析,试图排除可能被误诊为COPD的患者。此外,并不是所有的患者特征或生活方式因素都记录在初级和二级护理中,如。体育锻炼,所以残留的混淆是可能的。最后,他汀类药物的使用被用作胆固醇水平的替代指标,由于其可靠性较差,没有使用包年吸烟。尽管如此,稳健的敏感性分析与主要发现是一致的。
结论
我们进行了首次观察研究,以研究加速FEV之间的关系1COPD患者心血管疾病预后和死亡率的下降和风险。我们没有发现FEV率之间的联系1心力衰竭、心肌梗死、卒中、房颤和冠心病(不包括心肌梗死)作为单独的结局。相反,频繁和严重的aecopd和呼吸困难的增加与CVD结局和死亡率的风险相关。
补充材料
可共享的PDF
确认
本研究的方案由MHRA数据库研究的独立科学咨询委员会(ISAC)批准(方案编号19_258),经批准的方案在同行评审期间提供给杂志和评审员。这项研究部分基于临床实践研究数据链(CPRD)的数据,该数据链获得了英国药品和保健产品监管局的许可。这些数据由患者提供,由NHS收集,作为其护理和支持的一部分。本研究中所包含的解释和结论仅为作者个人的观点。CPRD为本研究提供了链接的假名数据。数据由法定的可信任第三方NHS Digital链接,使用仅由NHS Digital持有的可识别数据。选择全科医生同意这一过程的实践水平与个人患者有选择退出的权利。国家统计办公室(ONS)是包含在CPRD数据中的ONS数据的提供者,并保持版权©2019,在卫生和社会保健信息中心的许可下重新使用,保留所有权利。可向CPRD索取资料。他们的条款要求购买许可证,而我们的许可证不允许我们向所有人公开它们。 We used data from the version collected in January 2018 and have clearly specified the data selected in our Methods section. To allow identical data to be obtained by others,通过购买许可证后,我们将按要求提供代码清单。牌照可向CPRD (www.cprd.com):英国伦敦E14 4PU金丝雀码头南柱廊10号药品和保健品管理局临床实践研究数据链集团。
脚注
这篇文章的补充材料可从www.qdcxjkg.com
利益冲突:H.R.Whittaker报告了GSK、阿斯利康和BI在提交工作之外提供的资助。
利益冲突:C. Bloom报告了来自阿斯利康、Chiesi和哮喘英国的资金,在提交的工作之外。
利益冲突:摩根没有什么可披露的。
利益冲突:D. Jarvis报告了来自欧盟和囊性纤维化信托基金的拨款,在提交的工作之外。
利益冲突:S.J. Kiddle报告了医学研究理事会在进行研究期间的拨款(拨款号MR/P021573/1);以及罗氏诊断和DIADEM在提交作品之外的个人费用。
利益冲突:J.K. Quint报告了英国肺脏基金会的拨款,在进行研究期间;阿斯利康(AstraZeneca)、BI、拜耳(Bayer)和葛兰素史克(GSK)的拨款和个人费用,以及哮喘英国(Asthma UK)、医学研究理事会(Medical Research Council)和Chiesi的拨款。
支持声明:这项工作是由英国肺基金会资助的。这项研究得到了国家卫生研究所帝国生物医学研究中心的支持。所表达的观点是作者的观点,不一定是国家卫生和社会福利部的观点。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年3月30日。
- 接受2020年9月8日。
- 版权©2021人队
这个版本是在知识共享署名许可证4.0的条款下发布的。















