摘要
给药120mg·kg-1α1一个每两周抗胰蛋白酶是安全和耐受性良好http://ow.ly/CVbz30lUBum
致编辑:
α1抗胰蛋白酶(α1-AT)缺乏症是一种遗传性疾病,其特征在于功能性α的异常的低浓度1-AT在血液和组织中[1]。α的主要作用1-AT的作用是保护含弹性的组织,尤其是肺,免受蛋白水解酶的破坏[2]。重症患者α1——缺乏与血清α同在1——浓度< 11μM容易破坏肺部组织,通常开发呼吸道症状和肺气肿在第四或第五个十年的生活3,4]。
三十年来,与静脉注射α治疗1-AT已问世,但仅在最近是RAPID(增强治疗的随机试验中α-1蛋白酶抑制剂缺乏)-Randomised对照试验(RCT),在180α2年安慰剂对照试验1——deficiency patients, able to demonstrate that weekly therapy with 60 mg·kg-1体重α1-AT降低肺组织的损失[五],并减缓疾病进展[6]。快速开放标签延长(OLE)研究对其中的130名患者进行了2年的随访[6]。
目前指南推荐的许可剂量是每周注射60 mg·kg-1体重α1——(7-9]。该方案可能耗时、成本高且不方便,已经有人提出了替代剂量方案[10]。然而,临床试验数据支持的替代给药方案的功效,安全性和耐受[一个缺乏11]。
在一个事后我们调查了60 mg·kg的安全性和耐受性-1和placebo infusions to 120 mg·kg-1在RAPID-RCT施用输注;biweekly infusions of either placebo or 120 mg·kg-1用来支付计划中的毒品假期。此外,合并比较所有双周120mg·kg-1在4年的快速计划期间进行了输液。
治疗中出现的不良事件(TEAE的)进行了分析和分级为轻度严重程度(不与日常活动干扰),中度(干扰日常活动)或严重(无法进行日常活动)。严重不良事件(SAE)定义为导致住院危及生命的TEAE,住院时间延长,显著残疾或死亡。
分别计算两种不同的措施来比较不良事件发生率。Ťhe exposure-adjusted event rates (EAERs) divided all TEAEs during the study conduct by the cumulative exposure of the respective group (60 or 120 mg·kg-1α1-AT或匹配的安慰剂)。Ťhe infusion-adjusted event rates (IAERs) compared the TEAE rates occurring in the 7-day period prior to and following a biweekly 120 mg·kg-1输注或匹配的安慰剂,即注入序列。
EAERs的差异采用正态近似检验进行评估。使用McNemar试验对第一次双剂量前7天的TEAEs发生情况进行个体内比较(即后60 mg·公斤-1),并在7天后的最后一个120mg·kg-1α1——剂量。报告的p值是双边的,没有调整多次测试。
75(α的80.6%1——集团)的93名患者至少有一两周一次的α的注入1-在进行快速rct时,87名患者中有70名(80.5%)接受了双周安慰剂注射。基线特征列于图1。
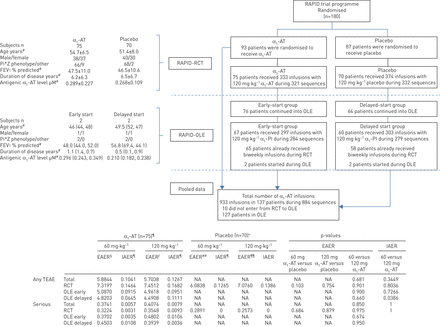
至少每两周接受一次120mg·kg的患者的基线血流、人口统计学特征和疾病特征-1α1抗胰蛋白酶(α1-AT)注入或匹配的安慰剂在快速(alpha -蛋白酶抑制剂增强治疗的随机试验不足)的随机对照试验(RCT)或RAPID-Open标签扩展(OLE),α和安全1——infusion sequences compared to placebo in RAPID-RCT occurring 7 days prior to and within 7 days after the administration of 120 mg·kg-1。数据以均数±表示SD或n.如果只有两个数据点可用,则个别数据显示在括号内。EAER:暴露调整事件率(每受试者年的事件数),该参数考虑了试验期间所有治疗紧急不良事件(TEAEs),但未考虑输注量未知的时期除外(29 076次输液中64次);IAER:输注调整事件率(每n个输注序列的事件数),包括已接受120 mg·kg的个体的teae个体内比较-1双周输注。一个n infusion sequence consisted of a 60 mg·kg-1weekly infusion or matching placebo followed by one or more infusions of biweekly 120 mg·kg-1或安慰剂。一世n this analysis the number of TEAEs occurring within the 7-day period prior to a double-dose infusion while exposed to 60 mg·kg-1or matching placebo was compared with those occurring in the 7-day period following the biweekly 120 mg·kg-1注射或匹配安慰剂;π* Z:α1——缺乏;FEV1:用力呼气1 s;PI:蛋白酶抑制剂;拿拿淋:不适用。#:在RCT的基线得到的数据。¶:每周两次的注入与α序列1-在RCT n=321和OLE n=563期间,总n=884。+:RCT N = 332时,与安慰剂输注每两周序列。§:药物暴露于α1-快速rct组每周60 mg为158.20年;输液次数(I) 8098次;快速- ole早期治疗组135.02人-年,I=6948;快速- ole晚期治疗组113.27例,I=5814。ƒ:药物暴露于α1-在快速rct中,每周摄入120毫克的受试者年龄为14.09岁,I=333;快速- ole早期治疗组12.50例,I=297;速效晚期治疗组12.69例,I=303。##:drug exposure for placebo group 120 mg weekly in RAPID-RCT was 134.92 subject-years, I=6845.¶¶:安慰剂组每周120 mg的快速- rct药物暴露为15.55受试者-年,I=374。
每两周输注包括所有α的4.3%1-AT和在两个研究都安慰剂主管部门的5.2%。Ťhe calculated drug exposure for 60 mg·kg-1infusions weekly was >10 times higher than for the biweekly 120 mg·kg-1注入(α1——158.20与14.09受试者年,安慰剂134.92与15。五五 subject-years). When all α1-两周剂量的快速- rct和-OLE共检测了137例患者中超过884个输液序列的933例(均数±±)SD6.45±4.26,范围1-21)(图1)。
该EAERs为7.32与6.08每周60 mg·kg-1α1-AT和安慰剂(p值= 0.103)和7.45与7.08每两周120 mg·kg-1α1-AT和安慰剂注射(p=0.754) (图1)。Ťhe proportion of patients who experienced a TEAE during the infusion sequences was 33.3% in the biweekly 120 mg·kg-1group compared to 35.7% in biweekly placebo and 37.3% in weekly 60 mg·kg-1或每周服用安慰剂37.1%。相应的IAER为0.1682与120 mg·kg为0.1386-1α1-AT和安慰剂注射(p值= 0.754)和0.1464与0.1265 for 60 mg·kg-1α1——与每周安慰剂(p值= 0.103)。Within 24 h of infusion, when volume-related TEAEs would be expected, IAERs were 0.0374 for 120 mg·kg-1α1——与两周安慰剂0.0301,60 mg·kg 0.0343-1α1——与每周服用安慰剂0.0361例。延迟启动OLE亚组的IAERs在60 mg时为0.0645,而在120 mg时为0.1111 (p=0.0386)。在所有双剂量输注程序中,有4个teae与每两周120 mg·kg相关-1输注(一个患者报告关节疼痛和头痛,一个有一个加重和头痛的人抱怨;累积IAER = 0.0125)相比,在每两周方案(IAER = 0.0030)安慰剂皮疹的单一治疗相关的报告。
During RAPID-RCT and -OLE 16% of patients reported a TEAE within 24 h of infusion and 25% reported TEAEs within 72 h in either treatment group. A higher proportion of patients experienced a TEAE within 7 days following a biweekly 120 mg·kg-1infusion (43.8%) than 7 days prior to double-dosing (34.3%). The number of TEAEs per infusion was 0.1267 for 120 mg·kg-160 mg·kg为0.1041-1。中号ost TEAEs were mild or moderate in intensity: 94.6% with 60 mg·kg-192.9%,每两周120 mg·kg-1。通过系统器官分类的TEAE的分析在所有亚组显示出相似的分布(数据未显示)。
在快速rct中,在注射序列中报告了四个sae,三个sae,每两周120 mg·kg-1(恶性肿瘤膀胱,前列腺和小肠梗阻的经尿道切除术);one SAE was reported with 60 mg·kg-1(胸痛);没有报告使用安慰剂。急性期发生8例SAEs(加重n=4;1例患者出现3例不良事件(肺炎、脓肿、肺叶慢性肥厚),脑血栓n=1。12例SAEs中有1例被认为与药物相关(慢性肉食)。
据我们所知这是第一个系统分析不良事件率和概要文件的两个不同的α1相比匹配的安慰剂给药-AT图案。的TEAE率均为亚群之间的可比性。一世n particular, there was no difference in event rates within 72 h after infusion or causally related events, demonstrating that doubling the dose and infusion volume is not associated with adverse volume effects in the investigated population. The significant difference in the OLE delayed-start group in favour of the 60 mg group was driven by a low rate of reported TEAEs compared to 60 mg RCT and early-start subgroups in an analysis that was not adjusted for multiple testing.
每两周给药,剂量为120 mg·kg-1α1-AT是一个方便的替代建议每周给药模式,并且其显着地降低每周输注的组织和药用负担如。到输液点的旅行,生活方式的中断和所有与输液有关的程序,包括调度,设置和管理。这项研究是支持双周120mg·kg的安全性和耐受性的最大证据-1模式。在报告的TEAEs的类型、频率、持续时间和严重程度方面没有变化的迹象。这与之前发表的关于>60 mg·kg剂量下增强治疗安全性的报告一致-1在较小的群组[获得12,13]。
群体药代动力学模拟预测数据槽水平高于11µM保护阈值将保持两周一次的患者在大多数120毫克公斤-1输注[14],这是考虑其他给药方案的重要前提。然而,每两周120 mg·kg-1由于计划中的药物假期,所以在RAPID计划中输液并不频繁,而且是零星的,而且对于双周方案对肺密度下降率的影响也没有得出结论。长期每周评估120 mg·kg-1对功效,安全性和耐受性结果输注目前正在临床试验[评价15]。
一世n conclusion, biweekly infusions of 120 mg·kg-1α1-AT的安全性和耐受性与60mg·kg相似-1和都与安慰剂的患者严重的α1抗胰蛋白酶缺乏症。每两周一次给药预期增强治疗与α便利1——。
致谢
Michael Riley和Barbara Boggetti (Trilogy Writing and Consulting GmbH, Frankfurt, Germany)代表CSL Behring提供医学写作支持。
脚注
本研究注册于ClinicalTrials.gov用标识符数字NCT00261833和NCT00670007。CSL Behring之前已经发布了RAPID和RAPID OLE协议《柳叶刀》并乐意在此出版物一起提供这些索取。这是一个简单的,事后这些试验的安全性分析。目前,CSL Behring不打算公布进行这些分析所依据的已去识别的个别患者数据。
快速试验。澳大利亚:J.G.W.伯顿,R.爱德华兹,A.格兰维尔,M.霍姆斯,P.汤普森,M.菲利普斯,P.A.沃克。加拿大:R.T. Abboud, K.R. Chapman, R.K. Elwood, P. Hernandez。捷克共和国:j.c Chlumsky。丹麦:N. Seersholm, T. Skjold。爱沙尼亚:a . Altraja。芬兰:r . Makitaro。德国:J. Ficker, J. f . Herth, K. Schulze, H. Teschler。爱尔兰:净收益McElvaney。波兰:J. Chorostowska-Wynimko, M. Sanak, A. Szczeklik, W.Z. Tomkowsk。 Romania: P.I. Stoicescu. Russia: T. Martynenko. Sweden: E. Piitulainen. USA: M. Campos, T.J. Craig, R.A. Sandhaus, J.M. Stocks.
利益冲突:T.格罗伊利希报道阿斯利康和葛兰素史克(讲课费),勃林格殷格翰,基耶西,CSL Behring公司和诺华(讲课费,顾问委员会和旅游支持),以及Mundipharma(讲课费和顾问委员会)的个人费用;从GRIFOLS(AATD工党,讲课费和旅行支援)以外的所有提交的作品补助和个人费用。
利益冲突:J.赫卢姆斯基报告由CSL Behring公司举办的讲座酬金,以及由勃林格殷格翰组织,提交作品外讲座。
利益冲突:M. Wencker报告说,在研究进行期间,conresp作为顾问向CSL Behring提供了支持。
利益冲突:O.维生素从杰特贝林报告的支持,作为研究的雇主和赞助商。
利益冲突:M.薯条报告从杰特贝林支持,作为研究的雇主和赞助商。
利益冲突:T.涌报告支持CSL Behring公司,作为研究的雇主和赞助商。
利益冲突:A. Shebl报告来自CSL Behring作为研究的雇主和赞助者的支持。
利益冲突:C. Vogelmeier报告了来自阿斯利康(AstraZeneca)、勃林格(Boehringer)、葛兰素史克(GlaxoSmithKline)、Grifols和诺华(Novartis)的资助和个人费用;CSL Behring、Chiesi、Menarini、Mundipharma、Teva、Cipla的个人费用;以及拜耳-先灵葆雅、MSD和辉瑞的资助,所有这些都不包括在提交的研究报告之内。
利益冲突:k·r·查普曼报告来自阿斯利康、勃林格殷格翰、CSL Behring、Grifols、赛诺菲、Genentech、卡马达、罗氏和诺华的赠款和个人费用;百特(Baxter)、葛兰素史克(GlaxoSmithKline)、安进(Amgen)、夏尔(Shire)和奥克塔帕玛(Octapharma)的资助;默克的个人费用;以及CIHR-GSK呼吸保健服务提供研究主席UHN,所有这些都是在研究过程中进行的。
利益冲突:N.G. McElvaney报告说,在研究进行期间,CSL Behring为进行最初的快速和快速OLE研究提供了研究资助;以及CSL Behring(顾问委员会)提交作品之外的个人费用。
支持声明:资金从杰特贝林接收。本文资金的信息已交存Crossref资助者注册表。
- 收到了2018年2月28日。
- 公认2018年9月10日。
- 版权©2018人队
这篇文章是开放获取的,并在知识共188滚球软件享署名非商业许可4.0的条款下发布。