摘要
囊性纤维化(CF)是由囊性纤维化跨膜调节基因(雌性生殖道)导致经上皮负离子转运减少。CF肺的特征是气道表面液体(ASL)脱水、慢性感染/炎症和中性粒细胞增多。功能失调的CFTR可上调上皮Na+(ENaC),进一步加剧脱水。我们先前证实,短腭肺和鼻上皮克隆1 (SPLUNC1)在正常气道上皮中负向调控ENaC。
在这里,我们使用肺组织样本、痰和人支气管上皮细胞(HBECs)来确定SPLUNC1是否可以在cf样环境中调节ENaC。
我们发现CF分泌物中内源性SPLUNC1减少,重组SPLUNC1 (rSPLUNC1)被CF分泌物快速降解。正常痰中含有SPLUNC1和SPLUNC1衍生肽,在正常和CF HBECs中都能抑制ENaC。相反,CF痰液激活ENaC, rSPLUNC1不能逆转这一现象。此外,我们观察到人CF支气管ENaC蛋白水平上调。与SPLUNC1不同,新型SPLUNC1衍生肽SPX-101抵抗蛋白酶降解,与HBECs顶端结合,抑制ENaC,并在CF痰延长预孵育后防止ASL脱水。
我们的数据表明CF粘膜分泌物驱动ASL的高吸收,蛋白酶抗性肽,如。SPX-101可以逆转这种作用,使CF ASL再水化。
摘要
细胞外囊性纤维化(CF)环境在调节经上皮离子转运中起着关键作用。CF分泌物降解SPLUNC1并激活ENaC,导致气道脱水。http://ow.ly/6WJA30lnDyC
简介
囊性纤维化(CF)是一种由囊性纤维化跨膜电导调节基因(雌性生殖道),导致经上皮负离子转运缺陷[1].在气道中,上皮细胞钠+通道(ENaC)是控制经上皮钠的速率限制步骤+吸收(2].CFTR的缺失导致ENaC活性和Na含量的增加+高吸收,结合阴离子分泌不足导致ASL脱水,从而减少粘液纤毛清除[3.- - - - - -5].综上所述,这些变化预计会导致脱水腔内粘液塞的积累,从而成为后续细菌感染的病灶。未能解决这些感染导致慢性炎症/中性粒细胞增多和肺腔蛋白酶水平升高。这些蛋白酶,包括中性粒细胞弹性蛋白酶(NE)和组织蛋白酶B和S,然后引起支气管扩张,最终破坏肺[6,7].最近报道了NE活性与CF肺病严重程度之间的相关性[8].
短腭肺和鼻上皮克隆1 (SPLUNC1)是一种多功能的25 kDa先天防御蛋白,可分泌到气道表面液(ASL)中[9- - - - - -12].SPLUNC1是一种变构调节因子,与细胞外结合,引起ENaC构象变化。该结合事件之后是nedd4.2依赖的α-ENaC泛素化和随后的通道内化,这有助于还原Na+和ASL吸收[11- - - - - -13].SPLUNC1晶体结构的分辨率允许它的功能被分配到不同的区域。例如,n端“S18”区域抑制ENaC调节ASL体积[11,12].
CFTR和ENaC之间的相互作用在异源表达系统中已被报道[4,14,15].然而,这些相互作用的性质和潜在的机制+高吸收是未知的。因此,ENaC在CF肺病理生理中的作用仍存在争议[16,17].SPLUNC1在正常ASL中抑制ENaC。然而,由于存在一系列pH敏感盐桥,SPLUNC1在中酸性CF ASL (~ pH 6.5)中无法发挥作用[11].因此,在天然ASL积聚的薄膜条件下,SPLUNC1可以在正常而非CF上皮中自发抑制ENaC。由于缺乏pH敏感性盐桥,SPLUNC1的ENaC抑制结构域的肽是pH不依赖的,并在cf影响的上皮中抑制ENaC [12].例如,SPLUNC1类肽SPX-101目前正在进行用于治疗CF肺病的临床试验[18].我们之前关注的是CF中的启动事件[5,11].然而,考虑到CF气道中高水平的中性粒细胞和蛋白酶活性,我们假设内源性SPLUNC1在CF肺中容易发生非ph相关的降解,如果发生在S18区域,将阻止ENaC抑制。因此,使用患者来源的样本,我们测试了以下假设:1)SPLUNC1在CF气道中降解,导致ENaC活性增加;2) SPX-101可以克服这一缺陷,诱导ENaC抑制并使CF ASL再水化。
方法
中提供了所使用方法的详细描述补充材料.
正常/CF痰液及粘液脓性物质上清
诱导和自发痰样本的获取如所述[9].如上所述,从切除的人CF肺的气道中收集粘液脓性物质(SMM)上清[19].捐赠者的人口统计数据显示在补充表S1、S2和S3.
免疫印迹
内源性NE和SPLUNC1蛋白水平测定使用18个捐赠者的干净痰样本。降解实验中,PBS、NE、正常或CF痰液(每组来自n=6个供体)和SMM(来自n=3个供体)与10µM rSPLUNC1在37℃下共孵育。在适用的情况下,抑制剂在rSPLUNC1孵育前与痰预孵育1小时。
NE活性测定
使用NE敏感肽su - ala - ala - ala -7-氨基-4-甲基香豆素(MCA)测定NE活性水平,如文献所述补充材料.
ENaC和Na+/ K+- atp酶在人支气管中的表达
如上所述获得人肺;捐赠者的人口统计数据显示在补充表S3.从下层组织中解剖支气管;CF支气管选自相对无病变区域。用乳酸林格氏溶液冲洗组织,用含NP40的裂解缓冲液提取蛋白质[20.].
质谱法测定rSPLUNC1和SPX-101裂解
将10µM的rSPLUNC1和SPX-101与混合的正常或CF痰孵育(每组n=6个供体)。样品在−80°C下快速冷冻,并通过过滤辅助样品制备用于蛋白质组学[21].利用Q Exactive (Thermo Scientific, Waltham, MA, USA)质谱仪耦合到UltiMate 3000 (Thermo Scientific)纳米高效液相色谱系统注入溶解肽材料进行无标签定量蛋白质组学分析,并按所述进行数据采集[22].
HBEC文化
根据北卡罗来纳大学(UNC)协议#03-1396,从不适合移植(非CF捐赠者)或移植后(CF捐赠者)的人类肺部采集细胞。按照所述在可渗透支架上培养,并在改良的支气管上皮生长介质中保持在气液界面[20.].在播种后21-28天对细胞进行研究。
美国手语高度测量
将30µM的rSPLUNC1或SPX-101与PBS或混合的正常/CF痰液(每组n=6个供体)在37℃联合或不联合sivelestat孵育过夜,然后添加到HBEC粘膜表面。ASL高度的测量方法如前所述[11].
SPLUNC1和SPX-101与HBECs的结合
将细胞根尖暴露于胺反应性Dylight-633 rSPLUNC1或5-TAMRA-SPX-101与PBS、正常或CF混合的痰液预孵育。使用钙黄素乙酰氧基甲基(AM)对细胞进行反染色,并使用SP8共聚焦显微镜(Leica Microsystems, Wetzlar, Germany)成像。
经上皮电位差
单管经上皮电位差(Vt)传感微电极通过微操作器定位于ASL,并与浆膜溶液中的宏观电极联合使用来测量Vt使用电压表(World Precision Instruments, Sarasota, FL, USA),如所述[11,23].
统计数据
对正态分布数据进行方差分析,然后进行Tukey检验或t检验。当数据非正态分布时,采用非参数等价检验(Mann-Whitney U检验、Kruskal-Wallis检验和Dunn’s多重比较检验)。对于SPLUNC1随时间的退化,曲线采用单指数拟合,并使用额外平方和F检验进行分析。使用GraphPad Prism 7.0 (GraphPad Software, La Jolla, CA, USA)进行数据分析。
结果
CF痰中SPLUNC1蛋白水平降低
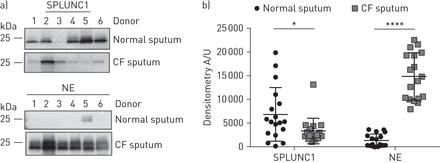
与之前的研究一致,我们通过Western blot检测了正常痰样本中的SPLUNC1水平[9,24].我们检测到CF痰中内源性SPLUNC1蛋白水平显著降低(图1).因为NE可以降解SPLUNC1 [24],我们接下来测定NE蛋白水平。与以往的研究一致[25],我们发现CF痰中NE水平升高(图1).接下来,我们将rSPLUNC1与正常捐赠者和CF捐赠者的痰液混合孵育。全长rSPLUNC1被CF痰呈指数级降解(t1/2=26分钟),但与正常痰孵育后仍保持稳定(图2一个, b).由于CF肺病会增加ASL蛋白含量,我们将rSPLUNC1与体积调节后的正常和CF痰液共同孵育,以测试rSPLUNC1的降解不受蛋白浓度的影响。仅在CF痰中rSPLUNC1水平显著降低(图2 c, d).为了证实SPLUNC1的降解是蛋白质介导的,将痰样本与正常或CF痰在4℃或热变性的正常和CF痰(95℃/β-巯基乙醇)孵育。这两种方法都减弱了CF痰中rSPLUNC1的降解(补充图S1a, b).鉴于正常痰液和CF痰液的收集方法不同(即。诱导与我们确认了rSPLUNC1的稳定性不受收集方法的影响,并且我们发现在自发收集中SPLUNC1的稳定性没有差异与诱导痰(补充图S2).
囊性纤维化(CF)痰中SPLUNC1蛋白水平显著降低。a)具有代表性的Western印迹显示,每组n=6名捐赠者的正常和CF痰样本中SPLUNC1和中性粒细胞弹性蛋白酶(NE)的内源性表达。在剥离前对膜进行NE探测,并重新探测SPLUNC1。b)每组18名供者正常和CF痰中SPLUNC1和NE蛋白丰度的密度分析。数据以均数±表示sd.数据采用韦尔奇修正t检验进行分析。*: p<0.05, SPLUNC1正常与CF痰;****: p<0.0001,网元正常与CF痰。
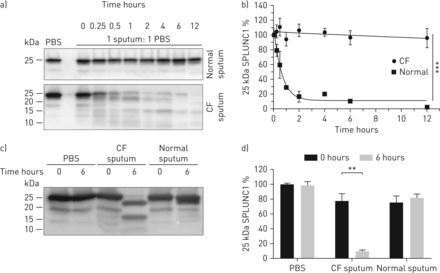
rSPLUNC1在囊性纤维化(CF)痰中迅速降解。a) 37°C下,与CF和正常痰液(来自n=6名捐赠者)孵育后,具有代表性的Western印迹显示SPLUNC1丰度。b)密度分析显示rSPLUNC1降解迅速。数据以均数±表示sdn= 3-4个独立实验。PBS的速率常数(k)之差与用额外平方和f检验分析黏脓物质(SMM) rSPLUNC1降解上清液;* * *: p < 0.001。CF痰:t1/2= ~ 26分钟,k=1.57;痰液正常:t1/2= ~ 4 h, k=0.02。c)代表性Western blot显示,37°c孵育6小时后,CF痰中含有15µg总蛋白,10µM rSPLUNC1显著降解,d)相关密度测定;数据以均数±表示扫描电镜n= 3-5个独立实验。数据分析采用Mann-Whitney U检验;* *: p < 0.01。
CF痰中的NE是SPLUNC1降解的部分原因
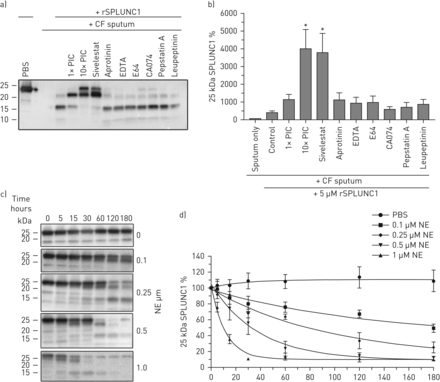
我们将rSPLUNC1和CF痰液与几种蛋白酶抑制剂(它们各自的抑制剂和用于抑制多种蛋白酶的无edta蛋白酶抑制剂混合物(PIC))共同孵育[19].只有sivelestat和10× PIC显著降低了rSPLUNC1的降解(图3一, b).由于NE在CF痰液中升高,而SPLUNC1的降解对sivelestat敏感,我们将rSPLUNC1与NE共孵育,后者以浓度依赖的方式降解rSPLUNC1 (图3 cd).由于这些发现的潜在重要性,我们将rSPLUNC1暴露于正常或CF痰中,并在蛋白酶抑制剂的存在下延长时间。令人惊讶的是,sivelestat在延长潜伏期后无法阻止rSPLUNC1的降解(图4一, b)。
Sivelestat可部分减弱rSPLUNC1降解。a)与1×/10×蛋白酶抑制剂鸡尾酒(PIC)或10 μ M蛋白酶抑制剂和囊性纤维化(CF)痰(来自n=6个捐献者)共孵育6小时后,代表性Western blot显示25 kDa rSPLUNC1丰度;b)来自n=8个个体实验的相关密度测定;数据以均数±表示扫描电镜, % 25 kDa的SPLUNC1表达与CF单独痰液比较。数据显示,10µM sivelestat和10× PIC对rSPLUNC1降解有显著抑制作用。数据分析采用Kruskal-Wallis检验;*: p < 0.05。c)将rSPLUNC1暴露于中性粒细胞弹性蛋白酶(NE)一段时间后的代表性Western印迹和d)相关密度测定,来自n= 4-6个单独实验。数据以均数±表示扫描电镜.数据分析采用额外平方和f检验;p<0.0001,速率常数(k)各网元数据集之间的差异。
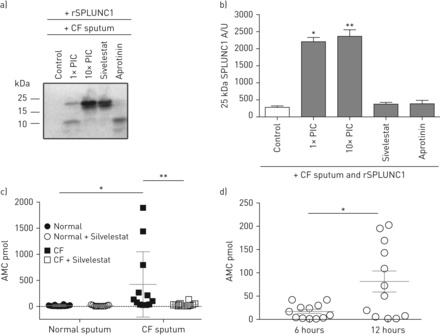
Sivelestat不能长期阻止囊性纤维化(CF)痰对rSPLUNC1的降解。a)具有代表性的Western blot显示,在1×/10×蛋白酶抑制剂鸡尾酒(PIC)、10µM sivelestat或10µM抑肽酶和CF痰(来自n=6个捐献者)共孵育后,25 kDa rSPLUNC1丰度;b)来自n= 3-4个个体实验的相关密度测定;数据以均数±表示扫描电镜.% 25 kDa SPLUNC1与单纯CF痰液进行Kruskal-Wallis试验比较;*: p < 0.05;* *: p < 0.01。c)在37°c±10µM sivelestat下,正常和CF痰液孵育6小时后,100µM荧光底物suca - ala - ala - ala - mca裂解后形成7-氨基-4-甲基香豆素(AMC)。数据以均数±表示sd来自n=12个正常供体和n=12个CF供体。Kruskal-Wallis检验与Dunn多重比较为正常与CF, *: p<0.05;对CF与CF+sivelestat, **: p<0.01。d) CF痰经6或12 h +10µM sivelestat裂解100µM含氟底物suca - ala - ala - ala - mca后AMC形成的变化。数据以均数±表示sd来自n=12个正常供体和n=12个CF供体。数据分析采用Mann-Whitney U检验;*: p < 0.05。
为了确认高NE蛋白水平转化为升高的NE活性,我们在痰液±sivelestat中添加了NE敏感底物,并测量了荧光产物AMC的形成,暴露于CF后AMC显著升高,但正常痰液中没有(图4 c).Sivelestat无法减少CF痰暴露12小时后AMC的形成(图4 d),无法恢复SPLUNC1调节ASL高度的能力(补充图S3a, b).此外,我们还检测了组织蛋白酶B、K、S、L在CF痰中是否有活性。使用蛋白酶特异性荧光底物,我们观察到CF中组织蛋白酶B、组织蛋白酶K和组织蛋白酶S/L活性明显高于正常痰(补充图S4a- c)。我们还检查了MMP-2/9活性,其在CF痰中显著升高(补充图S4d).由于这些酶的抑制剂未能减弱rSPLUNC1的降解,我们得出结论,尽管许多蛋白酶在CF痰中具有功能活性,NE是rSPLUNC1降解的主要原因。
α-, β-和γ-ENaC和Na的上调+/ K+CF支气管中atp酶α1蛋白表达表明ENaC活性增加
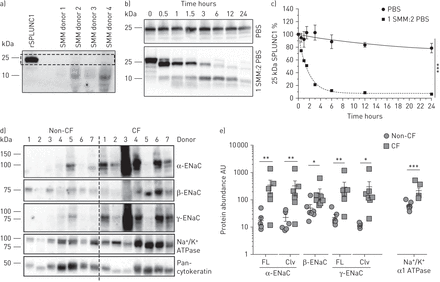
从切除的CF肺收集的SMM中未检测到SPLUNC1 (图5一个).同样,SMM和rSPLUNC1共同孵育导致rSPLUNC1 (图5 b, c).因为SPLUNC1影响ENaC的蛋白平衡[13],我们测量了ENaC水平。从非CF和相对无病变区域的CF肺中收集支气管,我们用Western blot检测蛋白质水平[11].我们观察到CF支气管中所有ENaC亚单位均显著增加(图5 d, e). α-和γ-ENaC必须在ENaC传导Na之前被蛋白水解裂解+[26].有趣的是,我们检测到CF支气管中分裂的ENaC亚基显著增加,这表明ENaC活性上调(图5 d, e).与ENaC水平升高一致,Na+/ K+atp酶α1亚基在CF支气管中也增加(图5 d, e)。
SPLUNC1被降解,α-, β-和γ-上皮Na+通道(ENaC)亚单位在囊性纤维化(CF)支气管中上调。a) Western blot显示从n=4个移植后获得的CF供体肺中提取的粘液脓性物质(SMM)上清中内源性SPLUNC1水平。b)具有代表性的Western印迹显示10µM rSPLUNC1在PBS中或SMM在PBS中稀释为1:2 (SMM池n= 3-4个供体)。c)来自n=3个独立实验的25 kDa SPLUNC1的相关密度测量;数据以均数±表示sd.PBS的速率常数k与采用额外平方和f检验分析SMM rSPLUNC1降解;* * *: p < 0.001。PBS: t1/2=14.6 h, k=0.05;社交媒体:t1/2=1.2 h, k=0.60。d) Western blot显示大量全长(FL)和cleaved (Clv) α-, β-和γ-ENaC,以及Na+/ K+从n=7例非CF肺和n=7例CF肺中解剖支气管,发现atp酶和泛细胞角蛋白事后剖析或者移植后。e)相关密度测定;数据以均数±表示sd、日志10改变了。每个个体供体的蛋白质丰度归一化为泛细胞角蛋白表达。正常的与采用Mann-Whitney U检验分析CF表达;*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
CF痰液切割SPLUNC1的enna抑制结构域
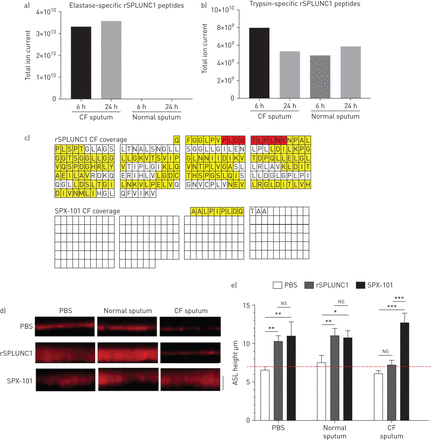
NE主要裂解缬氨酸和丙氨酸残基。事实上,rSPLUNC1与CF而不是正常痰共同孵育产生弹性酶特异性肽(图6).作为对照,我们进行了胰蛋白酶消化,并检测了与基因型无关的肽(图6 b).覆盖分析显示SPLUNC1的S18区(GGLPVPLDQTLPLNVPA)发生缬氨酸特异性裂解,并形成PLDQTLPLNV,这可能无法调节ENaC (图6 c).我们最近开发了一种新型的抗ne的SPLUNC1拟肽体SPX-101 [18].暴露于CF痰液后,SPX-101肽的ENaC相互作用区域保持完整(图6 c).为了确定rSPLUNC1和SPX-101在CF痰中是否仍保持活性,我们将PBS或痰与rSPLUNC1或SPX-101共孵育一夜,并将其添加到正常供者的HBECs中。rSPLUNC1和SPX-101在PBS和正常痰液存在时增加ASL高度(图6 d, e).与质谱数据一致,只有SPX-101能够在CF痰存在时调节ASL高度(图6 d, e)。
囊性纤维化(CF)痰劈裂SPLUNC1的上皮Na+通道(ENaC)抑制区。a, b)弹性酶特异性(a)和胰蛋白酶特异性(b) SPLUNC1肽与CF和正常痰液在37°C孵育后的总离子色谱强度。c)弹性蛋白酶特异性肽蛋白组学分析后SPLUNC1覆盖。被鉴定为PLDQTLPLNV的肽表明SPLUNC1的S18区域被破坏,以红色突出显示。d)将人支气管上皮细胞(HBECs)与PBS、正常痰液或CF痰(合并n=6个供体)孵育2小时后的代表性气道表面液(ASL)高度±30µM rSPLUNC1或30µM SPX-101。e)从n= 4-5个个体供体培养的n= 12-15个转孔测量ASL高度,表示为平均值±扫描电镜.数据采用Tukey's双因素方差分析事后分析;*: p < 0.05;* *: p < 0.01;* * *: p < 0.001;ns:不重要的。
CF痰液可阻止SPLUNC1结合并提高ENaC活性
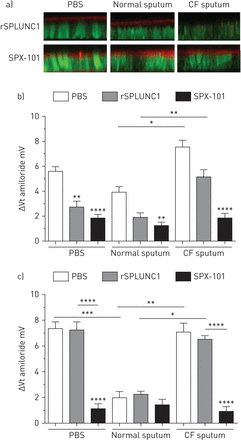
由于ENaC在根尖表达,SPLUNC1也必须在根尖结合,作为抑制过程的一部分[13].因此,在根尖加入HBECs之前,我们将荧光标记的rSPLUNC1和SPX-101与PBS或痰共孵育。我们观察到Dylight633-rSPLUNC1和5-TAMRA-SPX-101在PBS和正常痰处理HBECs的根尖结合(图7).暴露于CF痰液后,SPX-101而不是SPLUNC1能够在根尖结合(图7).此外,暴露于NE后,SPX-101(而不是SPLUNC1)仍保持功能活性并内化α- enc - gfp (补充图S5).
囊性纤维化(CF)痰阻止SPLUNC1结合到人支气管上皮细胞(HBEC)粘膜表面,并提高阿米洛利敏感的上皮电位差(Vt).a)将Dylight633-rSPLUNC1和TAMRA-SPX-101与PBS、正常痰和CF痰在37℃孵育2小时,并在成像前将其粘膜添加到HBECs中2小时。XZ共聚焦显微照片显示Dylight633-rSPLUNC1和TAMRA-SPX-101(红色)与正常HBECs的根尖结合。用钙黄素-乙酰氧基甲基(绿色)染色HBECs。b, c)将30µM rSPLUNC1和SPX-101与PBS、正常或CF痰液(来自n=6个供体)在37℃下孵育12小时,并将其粘膜添加到HBECs中再孵育2-3小时。然后通过微操作器和氨酰洛利敏感V将电压传感微电极放置在气道表面液(ASL)中t测量。所有Vt测量是在底侧10 μ M布美他尼存在下进行的,以抑制Cl−分泌。ΔVt阿米洛利然后按指示测量正常(b)和CF (c) HBECs。数据以均数±表示扫描电镜从n= 5-8个个体供体中培养出16-24个HBECs。数据经Tukey's方差分析事后分析;*: p < 0.05;* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001。
接下来,我们确定CF分泌物对SPLUNC1的降解是否与ENaC活性亢进有关。我们之前曾报道过原发性CF HBECs中ENaC活性的增加[23].而传代HBECs则没有这种现象。以相似的经上皮电压(Vt),我们将传代的正常和CF HBECs暴露于正常或CF痰液或PBS(对照)中,并测量由此产生的amiloridsensitive Vt作为ENaC活性的标志。基线阿米洛利敏感Vts在正常HBECs和CF HBECs之间无显著差异(图7 b, c).但加入正常痰液可降低Vt而CF痰明显升高Vt,独立于HBEC基因型。PBS中rSPLUNC1的加入显著降低了Vt与我们之前的发现一致,SPLUNC1不能在CF HBECs中发挥作用[11].rSPLUNC1对已经还原的V没有进一步影响t这表明内源性s18样肽的数量足以抑制ENaC,如所述[12].正常而非CF痰能显著降低CF Vt(图7 c),提示正常痰中存在自发产生的生物活性肽,而CF痰中不存在。为了进一步检验这一效果,我们将正常痰液通过尺寸排除柱去除≥10 kDa的多肽和蛋白质。然后将该滤液添加到正常HBECs中,6 h后测量ASL高度。该滤液显著增加了ASL高度,在滤液中添加30µM rSPLUNC1没有进一步的效果(补充图S6).与我们之前观察到的全长SPLUNC1在CF气道中不活跃一致,rSPLUNC1未能降低氨洛利德敏感Vt存在CF痰。SPX-101能显著抑制阿米洛利德敏感Vt暴露于PBS或CF痰后的正常和CF HBECs (图7 bc)。
讨论
肺粘膜环境含有约1000种蛋白质,其中约5%为蛋白酶及其抑制剂[27].在正常情况下,抗蛋白酶可防止气道内过度的NE活动[28].总体而言,SPLUNC1在正常痰液中相对稳定(图1),但在某些情况下,我们确实观察到一些退化现象(如。补充图S2).然而,降解产物的大小接近全长SPLUNC1 (>20 kDa),并且与我们之前将SPLUNC1暴露于胰蛋白酶后观察到的SPLUNC1降解产物的大小相似[29].因此,我们推测存在于正常ASL或痰中的丝氨酸蛋白酶可能会在翻译后影响SPLUNC1。然而,慢性中性粒细胞在CF肺腔内显著增加游离NE水平[8,28,30.].同样,我们发现CF痰中NE蛋白水平和活性明显高于正常健康捐赠者的痰(图1).我们还观察到CF痰中SPLUNC1蛋白水平显著降低,rSPLUNC1在CF痰中迅速降解(图1而且2).为了证实SPLUNC1被降解,我们进行了蛋白质组学分析。CF痰中ne特异性SPLUNC1覆盖率显著增加,提示炎症诱导降解。关键的是,完整的s18样肽可以抑制ENaC在CF痰中是不存在的。尽管被NE分裂,SPLUNC1在分离前仍能聚集数小时[31].然而,CF痰中缺乏SPLUNC1的覆盖以及rSPLUNC1在CF痰中相对较短的半衰期表明,在稳定状态下,SPLUNC1在CF气道分泌物中不作为一个功能实体存在。
NE抑制剂此前曾在CF患者中进行过试验,效果甚微。例如,AZD9668在CF患者中进行了测试,对炎症或肺功能没有影响[32].同样,重组α1抗胰蛋白酶也不能影响肺部炎症[6].我们的数据表明,sivelestat在防止CF痰中的SPLUNC1降解方面仅部分有效,而且这种效果随着时间的推移而消失。ENaC是高度混杂的,可被多种蛋白酶裂解。因此,可能有两个原因导致NE抑制剂在临床上的失败:1)在没有NE的情况下,SPLUNC1和其他蛋白质仍然被CF分泌物降解;2) ENaC仍可被CF肺内的其他蛋白酶激活,导致ASL持续脱水。因此,虽然较新的广谱抗蛋白酶如QUB-TL1可能更有效地阻止ENaC切割[33],它们在CF肺中是否完全有效仍有待确定。
我们的工作假设是SPLUNC1导致ENaC从质膜上去除,阻止其裂解和激活。我们最近开发了SPX-101,一种尺寸优化的肽,可以抑制CF HBECs和CF样动物模型中的ENaC [18].由于SPX-101目前正在进行治疗CF的临床试验,我们测试了SPX-101在CF痰样本中是否稳定有效。SPLUNC1和SPX-101在正常痰中孵育过夜后,ASL高度均升高。然而,暴露于CF痰液后,SPLUNC1降解,不能调节ASL高度,而SPX-101保持完整和活性。作为对照,我们还将SPLUNC1和SPX-101与NE孵育过夜,并探测α- enc - gfp的减少,作为内化的指示。尽管SPLUNC1失去了抑制ENaC的能力,但SPX-101在长时间暴露于NE后仍然保持活跃(补充材料).
SPLUNC1在来自中央气道的CF痰中被降解。然而,通过使用SMM,我们也观察到在CF肺的更多远端区域SPLUNC1降解。与SPLUNC1缺失一致的是,我们观察到全长α-、β-和γ-ENaC亚基显著增加,这表明SPLUNC1未能内化ENaC。至关重要的是,α-和/或γ-ENaC必须通过蛋白裂解才能活化[26,34,35],我们还检测到CF气道中裂解的α-和γ-ENaC亚基显著增加。基底外侧Na+/ K+- atp酶用来泵出钠+进入细胞通过ENaC,以保持细胞内钠+约23毫米[36].该泵先前已被证明在CF气道中有功能性上调[37].同样,我们观察到Na的显著增加+/ K+- atp酶蛋白水平在CF气道中,与分裂的α-和γ-ENaC亚单位的增加一致。威尔士和他的同事[38,39]提出电生理学检测到的ENaC活性增加是由阿米洛利德诱导的根尖膜超极化引起的人为现象。然而,我们的生物化学数据表明,cleaved (即。活性)ENaC以及必需的Na+/ K+- atp酶在CF上皮细胞中上调,提示事实并非如此。
虽然有缺陷的离子转运被广泛认为是CF肺病发病机制中的初始事件,但ENaC的作用仍然存在很大争议[17].许多研究表明电钠增加+可归因于ENaC活性增加的CF气道上皮的通量和液体变化[3.,40].相比之下,其他研究未能在CF仔猪和培养的气道上皮中发现差异[38,39,41].我们的数据显示,在CF痰预孵卵后,rSPLUNC1未能与HBEC根尖膜结合,而n端标记的SPX-101在暴露于正常或CF痰后结合得同样好。rSPLUNC1被DyLight633标记,这表明有多个残基被标记。因此,虽然CF蛋白酶可能已经去除了一些染料标记的残留物,但我们将SPLUNC1/CF痰预孵卵限制在2小时内,在这一点上应该保留了20%的蛋白质。
在我们的微电极研究中,我们首先添加了布美他尼,以避免阿米洛利德诱导Cl的任何混淆效应−非cf HBECs的分泌[23].SPLUNC1降低了阿米洛利德敏感Vt而SPX-101降低了Vt不管基因型如何。在这里,CF HBECs中碳酸氢盐分泌的减少有助于防止SPLUNC1功能所需的适度酸化。功能性CFTR对SPLUNC1抑制ENaC的要求可能是由于SPLUNC1三级结构中存在pH敏感盐桥,使其在pH值低于7时失去活性。相反,分离出的enac抑制肽,如SPX-101,缺乏盐桥,与pH无关[11].令人惊讶的是,非CF型和CF型HBECs对阿米洛利德敏感的V均显著降低t在接触正常的痰2小时后。这可能是由于内源性s18样enna抑制肽的存在[12].确实,在将正常的痰液通过尺寸排除柱去除≥10 kDa的蛋白质,包括全长为~ 25 kDa的SPLUNC1后,滤液能够显著增加ASL高度。在滤液中加入rSPLUNC1没有进一步的效果(补充图S5),表明滤液与SPLUNC1具有相似的靶点(即。博)。因此,虽然我们不能说SPLUNC1/S18是ASL中唯一的ASL调节肽,但我们的数据表明,正常痰中存在小的ASL调节肽。相比之下,加入CF痰液可显著提高阿米洛利德敏感Vt与正常痰相比,非CF和CF HBECs均有明显差异。与ASL高度和结合实验一样,由于过度降解,SPLUNC1在改善这些影响方面无效。但SPX-101仍有活性,可显著降低阿米洛利德敏感Vt.这些变化可能是由于CF痰中含有丰富的蛋白酶,其中许多蛋白酶可以裂解和激活ENaC,同时缺乏功能性SPLUNC1或SPLUNC1衍生肽。综上所述,这些发现表明CF粘膜环境(即。(ASL分泌物)影响已确诊的CF肺病中的离子转运。先前的研究证实了CFTR和ENaC之间的细胞相互作用[4,14,15].然而,我们的研究是第一个测试CF气道分泌物对ENaC活性影响的研究,我们的数据有力地表明,细胞外环境驱动CF气道ENaC活性增高。
总之,我们已经证明了在CF气道分泌物中SPLUNC1缺失或显著减少,这有助于增加CF HBECs中的ENaC活性和ASL脱水。这些数据表明,在存在CF痰液的情况下研究CF HBECs将作为一个更现实的CF气道模型,同时也表明,在存在CF分泌物的情况下,应该测试新的治疗方法的有效性。
补充材料
确认
我们感谢卡罗莱纳大学(UNC)囊性纤维化中心组织核心提供细胞和组织,Colin Bingle(谢菲尔德大学,谢菲尔德)提供SPLUNC1结构,Debbie Baines(圣乔治,伦敦大学)提供α-ENaC-GFP结构,Thomas Kleyman(匹兹堡大学)和M. Jackson Stutts (UNC)提供β-和γ-ENaC结构,Michael Miley和Ricard Feng (UNC)纯化SPLUNC1。最后,我们要感谢布莱恩·巴顿(北卡大学)允许在这个项目中使用他的设备。
脚注
作者贡献:M.J. Webster, B. Reidel, C.D. Tan, A. Ghosh和R. Tarran设计并执行研究并分析数据。N.E. Alexis, S.H. Donaldson和C.M.P. Ribeiro提供了痰液和SMM样本,设计了实验并解释了数据。M. Kesimer设计实验并分析数据。M. J. Webster, B. Reidel和R. Tarran撰写了手稿。所有其他作者编辑并批准了手稿。
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究由美国国立卫生研究院R01HL108927、P30DK065988、英国囊性纤维化基金会(INOVCF)、囊性纤维化基金会R026-CR11和TARRAN17G0资助。本文的资助信息已存入交叉参考基金注册.
利益冲突:M.J. Webster没什么可透露的。
利益冲突:B. Reidel没有什么可透露的。
利益冲突:C.D. Tan没有什么可透露的。
利益冲突:A.高希没有什么可透露的。
利益冲突:N.E.亚历克西斯没什么可透露的。
利益冲突:S.H. Donaldson报告了来自Vertex Pharmaceuticals和Parion Sciences的资助,来自Nivalis Pharmaceuticals的资助和个人费用,以及来自Pulmatrix, Novartis Pharmaceuticals和PTC Therapeutics的个人费用,在提交的工作之外;此外,S.H. Donaldson拥有“PLUNC蛋白调控钠通道”专利,并已支付专利使用费。
利益冲突:M. Kesimer没有什么可透露的。
利益冲突:C.M.P. Ribeiro是Irex Pharma的创始人并拥有股权。
利益冲突:在提交的工作之外,R. Tarran是Spyryx Biosciences的创始人和董事会成员;此外,R. Tarran拥有“PLUNC蛋白调控钠通道”专利,并已支付专利使用费。
- 收到了2018年4月8日。
- 接受2018年8月6日。
- 版权所有©ERS 2018