摘要
出于安全考虑,在阻塞性睡眠呼吸暂停(OSA)中使用催眠药物是禁忌的。最近的研究表明,根据病理生理学的差异,一夜的催眠药物使用加重了一些人的低氧血症,并降低了另一些人的OSA严重程度。然而,长期的临床试验数据缺乏。本研究旨在确定佐匹克隆1个月对低-中呼吸唤醒阈值且无严重夜间低氧血症患者OSA严重程度、嗜睡和警惕性的影响。
69名参与者用会厌导管完成生理筛选,以量化唤醒阈值。30例符合条件的患者(呼吸暂停-低通气指数(AHI) 22±11事件·h−1然后,完成了标准的实验室多面体摄影(基线),并在1个月,双盲,随机的并行试验期间接受了每晚ZOPICLONE(7.5mg)或安慰剂后,返回两种额外的隔夜睡眠研究(夜晚1和30)(ANZCTR标识符ANZCTRN12613001106729)。
从基线到30晚,佐匹克隆的AHI变化没有差异相对安慰剂组(−5.9±10.2相对−2.4±5.5事件·h−1;p = 0.24)。同样,低氧血症、第二天嗜睡和驾驶模拟器的表现也没有区别。
1个月的Zopiclone在没有重大过夜缺氧血症的情况下,在选定患者中不会恶化OSA严重程度,嗜睡或警觉性。作为评估催眠效果对OSA严重程度和睡眠超越单夜研究的效果的研究,这些发现提供了重要的安全数据和洞察OSA病理生理学。
摘要
在低-中度唤醒阈值个体中,每晚服用1个月的佐匹克隆不会加重OSA严重程度或症状http://ow.ly/9JD230khJpl
介绍
使用催眠药物很普遍,3-5.5%的一般人口曾在过去一个月内报告使用过催眠药物[1,2].肥胖者(7.2%)和老年人(9.1%)的使用频率更高[1]是导致阻塞性睡眠呼吸暂停(OSA)的两个主要危险因素。OSA是一种日益常见的与睡眠有关的呼吸障碍,对健康和安全造成严重的不良后果[3.- - - - - -5].超过40%的OSA患者也有失眠症状[6,7].
从历史上看,催眠药在OSA禁止。主要担心中枢神经系统抑郁症将损害“救命”唤起呼吸刺激,恶化咽部肌肉收缩性以促进呼吸事件延长和低氧血症[8].实际上,一定的催眠剂在高剂量或非常严重,肥胖个体可以恶化低氧血症[9- - - - - -11.].然而,理解OSA发病机制的最近进步表明频繁的唤醒令人厌倦的睡眠和呼吸,并为OSA做出贡献[12.,13.].在气道狭窄(低呼吸唤醒阈值)期间太容易醒来可能是高达50%或更多OSA患者发病机制的关键因素[12.- - - - - -17.].与以往的观点相反,标准剂量的普通催眠药(替马西泮、曲唑酮、佐匹克龙和唑吡坦)并不会系统地减少咽部肌肉的收缩力或增加上呼吸道的塌陷性[11.,18.,19.].然而,在最近的两个小生理学研究中,曲唑酮和唑酮没有改变呼吸暂停 - 低尿症指数(AHI),ZOPICLONE在具有严重OSA的个体中增加1%的平均过氧血症[11.,19.].相比之下,在单晚研究中,埃佐匹克隆和曲唑酮已被证明可以促进睡眠并减少AHI,而不会恶化事件持续时间或低氧血症[14.,20.].在eszopiclone研究中,低唤醒阈值个体AHI的减少是不变的[14.].Eszopiclone联合氧也显著降低AHI,唤醒阈值较低和解剖损伤较少的患者降低更大[21.].
鉴于> 50%的OSA患者未能遵守第一线疗法,连续正气道压力[5,17.,22.],二线治疗的疗效多变且不可预测[23.],而针对阻塞性睡眠呼吸暂停(OSA)的个人化药物治疗方法也越来越受到关注[24.].因此,为了获得重要的安全知识,并了解某些催眠药物对选定的OSA患者的潜在治疗效用,有必要确定AHI的下降是否随时间稳定。因此,本研究的主要目的是确定与安慰剂相比,在低-中呼吸唤醒阈值和轻度夜间低氧血症患者中,1个月的佐匹克隆夜间治疗是否能降低OSA严重程度。由于催眠药有可能在第二天残留睡意,次要目的是评估睡眠参数、白天睡意和警惕性的变化,以建立这组患者长期使用催眠药的安全概况。最后,要推进临床转译,在二级事后我们评估了最近开发的一种临床工具,用于评估标准多导睡眠描图(PSG)变量的呼吸唤醒阈值,是否产生了与黄金标准(但有一定侵入性)压力导管方法相似的结果[16.].
方法
参与者
其他健康的18-65岁的未治疗或疑似OSA患者被招募通过在当地的告示板上用传单做广告。新诊断的患者或其他治疗失败的患者也从位于澳大利亚悉尼的NeuRA研究志愿者数据库或当地睡眠诊所转诊(威尔士王子医院和Woolcock睡眠诊所)中招募。要进行随机化,患者必须有AHI≥5事件·h−1,Nadir动脉血氧饱和度(年代aO2)≥75%,呼吸唤醒阈值≥- 25 cmH2O(在夜间筛选生理学研究中确定,稍后概述)。其他排除标准包括任何可能影响呼吸、睡眠或咽部肌肉活动的药物,孕妇或哺乳母亲以及已知的对安眠药过敏。参与者还被要求在为期一个月的试验期间不饮酒,并在服用研究药物后每晚留有充足的睡眠时间。
知情同意由东南悉尼地方卫生区人类研究伦理委员会批准。这项研究是注册ANZCTR标识符编号ANZCTRN12613001106729。
协议和主要测量
最初,一项通宵筛选生理学研究(Spike 2;使用标准PSG设备(见后文)加上会厌压力导管(Millar, Houston, TX, USA)和鼻面罩来量化唤醒阈值以确定合格性[11.].符合条件的参与者(AHI≥5个事件·h)−1,最低点年代aO2≥75%和呼吸唤起阈值≥-25cmh2o)然后完成标准过夜PSG,没有外延压导管。包括记录设备:脑电图,电动图,心电图,表面底次电象,脉搏血氧镜,胸部和腹部运动,位置监测和鼻压和热敏电阻气流传感器(Remlogic; Natus Medical,Pleasanton,USA,USA)重新确认资格标准和量化基线睡眠特征和OSA严重程度在没有外延压导管的情况下。在筛选生理学研究和基线PSG之后,根据双盲,并行设计()将参与者随机分为1个月的夜间安慰剂或ZOPICLONE(7.5mg)(图1).在为期1个月的试验中,参与者在第一个晚上(第1晚)和最后一个晚上(第30晚)返回进行标准的多导睡眠监测,以调查不同条件之间的基线睡眠参数的潜在变化。服用30夜的药片数来评估依从性。每次就诊前1.5 h,采用Epworth嗜睡量表(ESS)、睡眠功能量表(FOSQ)和Karolinska嗜睡量表(KSS)进行评分。KSS、利兹睡眠评估问卷(Leeds Sleep Evaluation Questionnaire, Leeds)和一项30分钟的驾驶模拟器任务在每天早上醒来30分钟后进行,以评估第二天的困倦和警觉性[25.].在试验结束时,参与者还被问了几个问题,包括他们在研究期间的感受,以及他们是否相信自己服用了佐匹克隆相对安慰剂臂。
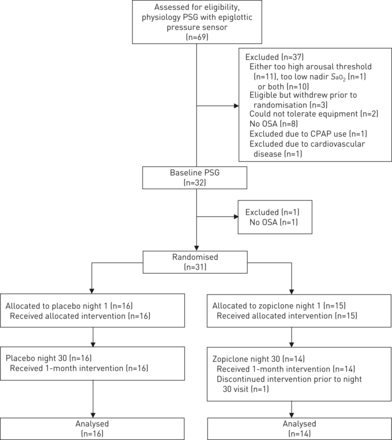
CONSORT流程图显示了该双盲、安慰剂对照平行试验的纳入、随机化、分配、随访和分析程序。一开始,被确诊患有阻塞性睡眠呼吸暂停综合症或临床怀疑患有阻塞性睡眠呼吸暂停综合症的参与者会对研究广告做出回应或被联系通过一个研究志愿者数据库。参与者参加了一个实验室生理学筛选PSG,以确定试验的资格。符合条件的患者(未经治疗的OSA(呼吸暂停-低通气指数≥5事件·h)−1一夜之间),最低点年代aO2≥75%和低-中呼吸唤醒阈值(≥- 25 cmH)2O)其他方面健康的)参加了标准的实验室基线PSG。如果仍符合基线条件,则将患者随机分为安慰剂组或佐匹克隆组。参与者要么每晚服用一次安慰剂,要么在睡前服用7.5毫克佐匹克隆,持续1个月。参与者在治疗的第一个晚上(第1晚)和最后一个晚上(第30晚)参加了两个标准的实验室psg。1例患者在基线PSG后被排除在研究之外,因为他们被发现没有阻塞性睡眠呼吸暂停。一名患者在30夜结束前因无关的个人问题而停止参与研究。PSG:多导睡眠描记术;年代aO2:动脉血氧饱和度;OSA:阻塞性睡眠呼吸暂停;CPAP:持续气道正压。
数据分析
所有的分析都是在研究干预的情况下进行的。睡眠分期、呼吸事件和唤醒评分由一位经验丰富的睡眠技术人员根据美国睡眠医学学会推荐标准2.1版进行[26.].在最初的生理筛选PSG过程中,随机选择20个(或尽可能多的)与会厌压力波动增加(伴有阻塞性呼吸暂停或低通气)同时发生的皮层唤醒,以计算每个参与者的唤醒阈值。具体来说,每个呼吸事件(图2),并取平均值来量化唤起阈值,如前所述[11.,14.].作为探索性事后分析,简单验证临床工具的效用来估计标准PSG变量的唤醒阈值[16.]用来确定是否能够准确地识别基线处的低-中度唤醒阈值人群。
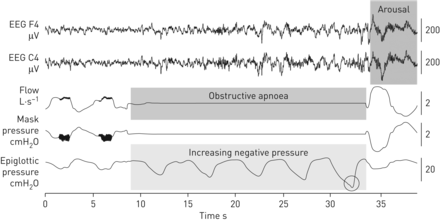
一个病人的多导睡眠图记录显示如何获得呼吸唤醒阈值测量。本例显示35岁男性患者N2期非快速眼动睡眠约40秒(呼吸暂停-低呼吸指数20事件·h)−1;体重指数32.2 kg·m−2)经历了一个约25秒的呼吸事件(呼吸流通道的阴影区域,标记为“阻塞性呼吸暂停”),最后从睡眠中唤醒皮质(两个脑电图通道的阴影区域,标记为“唤醒”)。呼吸唤醒阈值被量化为唤醒前呼吸努力时的会厌压力最低点(会厌压力通道上的圆圈区域,在本例中约为−32 cmH2o)。流量是测量的鼻孔通过口罩和呼吸测速仪;口罩压力是用压力传感器测量鼻罩上的压力。脑电图:脑电图。
结果
参与者的特征
在69名参与夜间筛选生理学研究的个体中,有38人因其唤醒阈值≤- 25 cmH而不符合条件2O和/或他们的最低点年代aO2≤75%,或不符合其他纳入标准。在这38名患者中,27人有严重的OSA (AHI 48±25事件·h)−1),九个没有OSA(AHI <5事件·H.−1)和AHI在两名参与者中无法量化,因为在生理筛选的夜晚,记录设备无法入睡(见图1为进一步的细节)。31人随机分组;30人完成了试验的所有4个晚上,并被纳入最终分析(图1).基线人体测量和睡眠参数在安慰剂组和佐匹克隆组之间匹配良好(表1).在1个月的试验期间,人体测量特征没有改变(补充表E1).佐匹克隆组和安慰剂组对研究干预的依从性均较高(分别为93.7±9.7%和93.4±11.0%)。在1个月的试验期间,不良事件不常见,除1例外,其余均为轻微事件,且与研究用药无关(表2).表3总结了在1个月试验结束时对研究药物(安慰剂或Zopiclone)的参与者的看法。在与安慰剂相比,Zopiclone期间,79%相对56%的人说睡眠改善了,36%相对31%的人表示,如果有条件,他们将继续使用研究药物,79%的人表示相对69%正确察觉他们正在服用它们的研究药物。
呼吸事件和睡眠参数
从基线到夜间30的AHI的变化在唑酮和安慰剂条件之间没有差异(P = 0.24)(图3.).佐匹克隆治疗组30夜AHI较基线平均降低为- 5.9±10.2 (p=0.048)。相对−2.4±5.5事件·h−1在安慰剂组(p = 0.098)。佐匹克隆在中度< - 15和> - 25 cmH患者中降低AHI的百分比相似2o)和低(≥-15cmh2O)呼吸唤醒阈值(29%)相对21%)(表4).
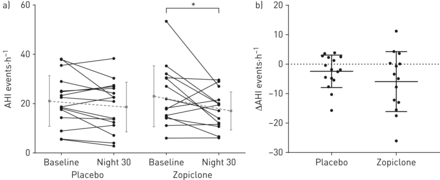
a)呼吸暂停-低呼吸指数(AHI)散点图,代表安慰剂组每个个体的AHI (n=16)相对佐匹克隆(n=14)条件下基线和夜间30。灰色线和误差条表示平均值±SD..*:与基线有显著差异。b)散点图,显示两种情况下每个个体从基线到30夜AHI (ΔAHI)的变化。直线和误差条表示平均值±SD..
两种情况下的基线和第30晚PSG数据汇总在表4.从基线到第1晚,佐匹克隆的睡眠效率显著高于安慰剂(8.8±0.1%)相对1.2±0.1%;p = 0.02)(补充表E2).佐匹克隆组的睡眠效率从基线到第30晚增加了6.9±0.1%,但没有达到统计学意义(p=0.06)。从基线到30晚的delta变化在不同条件下没有差异(表4).使用佐匹克隆后,睡眠开始后的清醒时间从基线减少到第1晚相对安慰剂(−41±45相对−8±38分钟;p = 0.004) (补充表E2),但与30夜(表4).其他大多数睡眠参数之间没有条件差异,包括睡眠开始潜伏期、非快速眼动(REM)或快速眼动睡眠(REM)中总睡眠时间(TST)的百分比、唤醒指数、TST仰卧百分比、仰卧AHI或呼吸事件持续时间。的意思是年代aO2在基线睡眠期间,ZOPICLONE组的~1%较低(P = 0.03)。但是,佐科酮没有改变卑鄙或纳迪尔年代aO2.第1夜的睡眠和呼吸参数与第30夜相似(补充表E2).
嗜睡和警觉性
从基线到30晚,安慰剂和佐匹克隆的嗜睡和警惕性数据总结在表5.在睡意或警觉性方面,包括ESS、FOSQ、Leeds、KSS或AusEd驾驶模拟器的表现,在不同条件下没有差异。与安慰剂相比,佐匹克隆驾驶任务中从基线到第1晚车道位置中值的标准差增加了(6.7±8.4)相对-5.4±12.1厘米;p = 0.004) (补充表E3),第1夜的警觉性和困倦程度在不同条件下没有差异。
简单的临床评估唤醒阈值的工具
在纳入1个月试验的患者中,使用已发表的算法,100%被正确地确定为合格[16.结合我们的唤醒阈值≥- 25 cmH的纳入标准2o和nadir.年代aO2≥75%。为所有筛选的参与者应用这些标准,其中数据在n = 60中提供数据,我们发现只有15%的注册就会被错误。其中,所有都有高唤起阈值,用外延导管测量(-32±4 cmh2O),被算法低估(−21±2 cmH)2O)。这些患者均有中度至重度OSA (AHI 45±13事件·h)−1).
讨论
本研究的主要发现是,标准7.5 mg剂量的佐匹克隆在1个月的疗程中,并没有恶化OSA患者的AHI、低氧血症、日间嗜睡或早晨警惕性,低-中呼吸唤醒阈值(≥- 25 cmH)2o)在基线(Nadir)和温和 - 中度过夜过夜缺氧年代aO2≥75%)。此外,在该患者人群中佐匹克隆使用无重大不良事件发生。这些新发现扩展了最近的单夜催眠研究,并挑战了早期关于催眠药会系统性地恶化OSA的担忧。
佐匹克隆夜服1个月对OSA严重程度的影响
尽管没有系统化相对安慰剂,AHI内部群体内部减少25%从基线与ZOPICLONE有超过1个月,与最近的次夜概念的概念临床研究一致,主要与埃斯特替斯替斯洛酮和曲唑酮,主要是未选择的患者(分别为23%和26%)[14.,19.].然而,在佐匹克隆的两项小型生理学研究中,AHI没有变化相对安慰剂和曲唑酮相对基线(11.,19.].与其立体异构体Eszopiclone不同,其中AHI的不变减少在具有低唤醒阈值的个体中发生(总体〜45%)[14.但在目前的研究中佐匹克隆并非如此。相反,在低和中度唤醒阈值的个体中观察到类似的AHI降低。这些研究之间明显差异的确切原因尚不清楚。然而,阻塞性睡眠呼吸暂停的原因因患者而异[12.,24.].因此,在当前的研究中未测量的觉醒阈值之外的因素,如患者之间上呼吸道折叠性和肌肉反应性的差异,可能起到了作用。虽然eszopiclone被认为在药理学上与zopiclone相当,但两种药物之间的细微差异也可能起到了作用[27.].然而,标准剂量的伊佐匹克隆(3mg)和佐匹克隆可将唤醒阈值提高到类似的程度(约30%)[11.,14.,18.].最后,只有一名低唤醒阈值的参与者在佐匹克隆治疗后AHI增加。虽然该组的仰卧睡眠从基线到第30晚没有系统性差异,但该个体在第30晚的仰卧睡眠>增加了20%。相反,佐匹克隆组AHI降低最大的受试者在30夜仰卧睡眠>下降20%。因此,在个人层面上,夜间身体姿势的变化可能是一个重要的混杂因素[28.].
阻塞性睡眠呼吸暂停患者使用催眠药物的另一个问题是延长呼吸事件持续时间,加重血气紊乱。事实上,以前的研究表明,某些安眠药会加重低氧血症,特别是大剂量安眠药或患有严重OSA的肥胖患者[9,11.,21.].相反,与目前的研究结果一致的是,其他几项催眠研究显示,未选择的患者和根据基线低氧血症选择的患者的事件持续时间或低氧血症没有变化[10.,11.,13.,14.,19.,20.,29.- - - - - -32.].
睡眠参数
可与先前的催眠研究相媲美[10.,11.,14.,30.,32.[与我们研究的OSA中的个体相比,标准剂量的ZOPICLONE倾向于将睡眠效率提高7-8%。这也反映在研究结论中的主观睡眠质量报告中。增加的睡眠效率与OSA严重程度的变化相结合而不会导致血气扰动可能是有益的,因为大量比例(〜40%)OSA患者也经历睡眠中断和失眠症的症状[6,7].然而,与以往的欧卓霉素研究不同,其中从N1到N2睡眠和减少唤起指数的显着变化,这可能导致OSA严重程度的改善[14.],在本研究中,佐匹克隆对非快速眼动和快速眼动阶段所花费的时间比例及唤醒指数均无显著影响。这可能是由于上限效应,因为在目前的研究中,主要是轻-中-重度患者的睡眠阶段比例在基线时处于或接近正常范围相对埃佐匹克隆研究中病情越严重的患者[14.,33.].因此,纳入基线睡眠质量较差的患者,佐匹克隆可显著改善睡眠参数。另外,佐匹克隆的标准剂量可能在药理学上与之前的OSA研究不同[14.,21.].因此,尽管可能会增加第二天不必要的副作用,但在OSA患者中,可能需要更高剂量的佐匹克隆来产生临床相关的睡眠参数变化,包括AHI。
嗜睡和警觉性
由于担心中枢神经系统的抑制作用会对睡眠呼吸暂停患者造成伤害,包括可能加剧第二天嗜睡和警惕性等不良后果,催眠药通常被禁止用于治疗阻塞性睡眠呼吸暂停患者。然而,关于催眠药对阻塞性睡眠呼吸暂停患者睡意和警觉性的影响的数据有限。如果催眠药被认为是治疗某些阻塞性睡眠呼吸暂停患者的一种手段,那么至关重要的是,它们不会使第二天的症状恶化。目前的研究是第一次检验长时间使用催眠药对阻塞性睡眠呼吸暂停患者第二天困倦和警觉性的影响。与我们之前在未选择的主要严重OSA患者中使用标准剂量佐匹克隆的单晚试验一致,我们发现第二天的嗜睡没有变化通过KSS [11.].与苯并二氮卓尼硝普兰感知嗜睡[30.]和第二天的警惕性和注意力与褪黑素受体激动剂雷米特恩[34.在对阻塞性睡眠呼吸暂停患者的急性单晚研究中也没有变化。此外,本研究中对ESS、Leeds和FOSQ的测量均未因佐匹克隆而改变。
此外,在1个月的试验期间,佐匹克隆对使用30分钟驾驶模拟器性能测试评估的警觉性的客观测量没有变化。从安全的角度来看,这是至关重要的,因为未经治疗的阻塞性睡眠呼吸暂停患者发生交通事故的可能性已经高达6倍[3.].在目前的研究中,驾驶模拟器的表现没有受到损害,这与之前在健康参与者中进行的研究形成了对比。在之前的研究中,标准剂量的“z-药物”唑吡坦和佐匹克隆在一项约60分钟的任务中恶化了道路驾驶表现,以及第二天的认知和精神运动表现[35.,36.].已经提出,健康个体可能夸大了急性安眠药的残余影响,不存在于长期催眠用户或个人睡眠质量差的失眠症患者和患有阻塞性睡眠呼吸暂停综合症等,作为潜在的负面的残余影响可能超过有睡眠质量的提高(37.].实际上,在〜60分钟的驾驶任务期间,在旧的失眠症期间的道路驾驶性能在繁殖的ZOPIClone的标准剂量经常或不经常使用催眠药[37.].另外,当驾驶模拟器任务中警觉性随时间下降时[38.],它仍然可能发生与ZOPICLONE的驱动损伤可能发生在当前研究中测试的30分钟内。未来的研究,纳入其他客观的警觉性评估(如。保存的清醒测试)将提供额外的洞察力。同样重要的是要注意,目前研究人口中的大多数人在基线上没有特别困倦,并被要求避免在试验期间避免睡眠机会和酒精不足的混杂因素。因此,昏迷使用后的下一天嗜睡可能在困扰患者和其他混乱中不同。
安眠药和表现型
我们的第二项研究发现,在目前1个月的佐匹克隆试验中,AHI较基线略有降低,这提高了该药物对一些OSA和失眠患者的帮助可能性。然而,这仍然需要在这一人群中进行测试,作为失眠之前的症状相对试验后没有进行系统评估。此外,对大多数患者来说,AHI较基线的降低幅度不足以作为一个临床相关的治疗选择,作为单药治疗OSA。这与单晚标准剂量的埃佐匹克隆形成对比,后者总能降低低唤醒阈值患者的AHI(总体降低约45%)[14.],在未选择的阻塞性睡眠呼吸暂停患者中,与氧气联合使用可提高约45% [21.].与阻塞性睡眠呼吸暂停潜在病理生理原因的重要性相一致,对埃佐匹克隆和氧气有反应(定义为>降低50%至AHI <15事件·h的患者)−1)的上呼吸道可折叠性较低,OSA较轻,上呼吸道肌肉效能较高[21.].这些患者也倾向于具有低唤起阈值[21.].因此,这些研究为催眠药物的潜在使用提供了支持,当结合其他靶向辅助治疗时,这些患者是根据其OSA的潜在原因根据表型方法精心选择的[23.,24.].然而,具有催眠药的进一步的长期研究,包括额外的表型测量措施,例如上气道顽固性,以确定AHI还原是否随时间稳定并且适用于其他临床相关的目标种群(如。睡眠患者和睡眠障碍的年龄> 65岁是常见的)。因此,对于安全性和有效地实施催眠药,简化的工具允许准确识别OSA的潜在病理生理原因的基本原因[39.].根据该目的,使用最近开发的工具来估计基线唤起阈值,使用来自诊断PSG的易于可获得的变量与Nadir饱和标准结合以确定适合安全使用Zopiclone的合适候选事后在当前的研究分析。这些发现强调了正确估计轻度阻塞性睡眠呼吸暂停(OSA)患者唤醒阈值的潜力。而重度OSA伴AHI患者>30事件·h−1将在具有压力导管的另外的PSG中受益于压力导管,以准确地确定其催眠药靶向治疗之前的唤起阈值。
摘要和临床意义
在18-65岁的OSA患者中,标准剂量的佐匹克隆每晚服用1个月,不会加重OSA的严重程度、第二天嗜睡或警惕性,基线时无严重低氧血症或嗜睡。在二次分析中,佐匹克隆也有降低AHI ~ 25%和提高睡眠效率的趋势。这项随机临床试验的发现挑战了先前关于催眠药对阻塞性睡眠呼吸暂停患者的影响的假设。事实上,美国睡眠医学学会对原发性失眠症的治疗指南警告有阻塞性睡眠呼吸暂停症状或体征的患者使用催眠药物[40].目前的研究结果表明,通过筛查排除严重的夜间低氧血症,结合使用最近通过PSG数据验证的临床工具来估计唤醒阈值,可能有助于准确识别哪些人可以安全地使用佐匹克隆治疗轻度-中度OSA。特别是,这可能与大量OSA患者同时存在失眠症状,或未能遵守持续气道正压或其他治疗相关。相反,对于觉醒阈值高、长时间呼吸事件和/或基线严重低氧血症的OSA患者,应避免使用催眠药物,因为这些患者可能经历更长事件持续时间,并因此在使用催眠药物后出现更多低氧血症。当前研究的新发现强调了对OSA患者针对性使用不同剂量的不同催眠药物以及与其他疗法联合使用的必要性。
补充材料
确认
作者感谢研究药剂师Bandana Saini(悉尼大学,澳大利亚悉尼)协调了随机过程和盲性隐藏。作者还想感谢Benjamin Tong (neuroa, Randwick, Australia)和Anna Mullins (Woolcock Institute of Medical Research, Glebe, Australia)分别为夜间生理学和PSG研究打分。
脚注
本文提供了补充材料www.qdcxjkg.com
这项研究是注册ANZCTR标识符编号ANZCTRN12613001106729。
作者贡献:S.G. Carter和D.J. Eckert撰写了手稿,所有的作者都对最终版本和数据解释做出了贡献。S.G.卡特、L.P.费舍尔和C.M.罗洛收集并分析了这些数据。G. Cho, D.J. Stevens和A.L. D'Rozario协助数据收集。D.J. Eckert和J.C. Carberry协助进行数据收集和分析,并与R.R. Grunstein和D.K. McKenzie合作,负责研究的概念和设计。
利益冲突:S.G.卡特报告了国家健康和医学研究委员会(NHMRC;nmrc卓越研究中心NeuroSleep提供的个人费用(研究生研究补足奖学金)和澳大利亚神经科学研究(NeuRA)提供的个人费用(补充奖学金)。在提交的工作之外,从ResSleep兼职工作的个人费用。
利益冲突:J.C. Carberry报告了NHMRC(授权1042493)和NeuroSleep(授权1060992)在研究进行期间的拨款。
利益冲突:G. Cho报告了NHMRC(批准1042493)和NeuroSleep(批准1060992)在研究进行期间的拨款。
利益冲突:L.P. Fisher报告了NHMRC(1042493)和NeuroSleep (NHMRC卓越研究中心(1060992))在研究进行期间的拨款。
利益冲突:C.M. Rollo报告了NHMRC(1042493)和NeuroSleep (NHMRC卓越研究中心(1060992))在研究进行期间的拨款。
利益冲突:D.J.史蒂文斯报告了NHMRC(授权1042493)和NeuroSleep(授权1060992)在研究进行期间的拨款。
利益冲突:R.R. Grunstein报告授权NHMRC(授权1042493)和NHMRC卓越研究中心NeuroSleep(授权1060992),在研究进行期间,以及默克和Teva在提交工作之外的当地顾问委员会活动的个人费用。
利益冲突:D.J.Eckert报告NHMRC(授予1042493和奖学金1116942)和Neurosleep,NHMRC研究卓越中心(Grant 1060992),以及澳大利亚联邦政府的赠款合作研究中心补助金(工业伴侣opentus医疗)拜耳咨询委员会活动和咨询的个人费用,在提交的工作之外。
利益冲突:A.L. D’rozario报告了NHMRC(授权1042493)和NeuroSleep(授权1060992)在研究进行期间的拨款。
支持声明:该研究由澳大利亚国家健康和医学研究委员会(NHMRC)项目资助(1042493)和国家健康和医学研究委员会卓越研究中心(1060992)资助。D.J. Eckert获得NHMRC高级研究奖学金(1116942),R.R. Grunstein获得NHMRC高级首席研究奖学金(1106974),A.L. D’rozario获得NHMRC- arc研究奖学金(1107716)。本文的资金信息已存入Crossref资助者注册表.
- 收到了2018年1月24日。
- 接受2018年5月23日。
- 版权©2018人队