抽象的
非分化的气道上皮细胞显示初级纤毛,它们的数量与COPD特征相关联http://ow.ly/wiGH30jDbeG
到编辑:
慢性阻塞性肺病(COPD)是全球主要的经济和社会问题,因为它对死亡率和发病率的影响[1].COPD的特征在于气道上皮重塑,一种失去的气道上皮塑性的标志[2].目前还没有可用的治疗方法来恢复上皮的完整性和功能。因此,新的研究来源对于理解COPD发病的根本变化变得至关重要。非运动性初生纤毛是在细胞周期控制、增殖、极性和分化中起关键作用的单个感受器,尤其是具有运动性纤毛的纤毛细胞[3.那4.].初级纤毛聚集在不同类型的人类细胞上,这取决于它们的状态和响应细胞静止的活动,它们传递细胞外信号,并在细胞周期重新进入时收缩[5.].原发性纤毛结构和功能的改变是患有纤毛病的责任[6.那7.].初级纤毛可能对测定气道上皮细胞分化期间的结果至关重要,因此我们假设原发性纤毛存在于成人上皮细胞中,并且可能在气道可塑性中发挥关键作用。首先,我们研究了支气管上皮中原发性纤毛的存在和定位。其次,我们分析了非COPD和COPD患者的原发性纤毛和临床,功能和组织学特征之间的关系。
患有癌症肺部切除的患者(大学雷斯,Reims,法国)审查了机构审查委员会批准的标准(IRB Reims-Chu-20112612)。知情同意是从所有患者获得的。进行临床评估和肺功能试验。在视觉上以前描述的胸椎计算断层扫描在视觉上进行了肺气肿定量,如前所述8.那9.].福尔马林固定的石蜡嵌入(FFPE)远离肿瘤的肺组织用Haematyxylin和eosin染色,用于支气管上皮分析。用以下初级抗体对FFPE肺组织进行免疫荧光:抗ARL13B(1:200; Proteintech,Rosemont,IL,USA);抗γ-小蛋白(1:200; Sigma,St.Louis,Mo,USA);抗乙酰化-α-微管蛋白(1:1000; sigma),抗GT335(1:500;脂肪原,义峰,瑞士)和抗P63(1:100;研发系统,Minneapolis,Mn,Mn,USA)。通过Confocal Zeiss LSM710显微镜(Oberkochen,德国,目标63x / 1.40油DIC(差动干扰对比)采取图像。每次染色载玻片的10个随机场分析原发性纤毛。使用T确定组之间的差异-检验或Fisher精确检验,用Spearman秩相关检验分析变量之间的相关性。p值<0.05被认为是显著的。
36例患者被纳入:19例COPD患者(全球慢性阻塞性肺疾病倡议(GOLD) 1: n=5;黄金2:n = 12;黄金3 - 4:n = 2;年龄(中位数(四分位范围(IQR)) 66岁(59-73);1s用力呼气量(FEV)1,中位数(IQR):71%(62-81))和17名非COPD患者(69岁(66-76); FEV1:89%(83-102))。与非COPD组相比,COPD组的COPD叶片的COMPERCOMICOMEMA评分显着高(0(0-0)相对1(0-2);P <0.0001)。
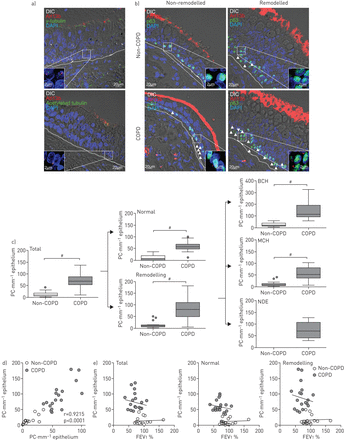
在上皮内鉴定和局部地鉴定纤毛,具有纤毛轴突和膜(GTPAse AR113b)和基体/中心体(γ-管蛋白)的特定染色(图1A).在指向腔的上皮细胞表面的表面上容易鉴定Motile Cilia,而在小鼠肺部发育期间,在假疗化上皮的非分化细胞上发现孤立性纤毛(原发性纤毛)[10].我们证实鉴定初级纤毛的鉴定轴突的两个另外和良好表征的标记(乙酰化α-小管蛋白和GT335)(图1A和数据未显示)[11].
原发性纤毛存在于成人支气管上皮细胞上,并在慢性阻塞性肺病(COPD)患者中改变。a)最大强度Z堆突起的实例显示两次吸烟者COPD患者的支气管上皮细胞上皮细胞的初级纤毛的存在:DIC(灰色),ARL13B(红色)和γ-微管蛋白(上,绿色)或乙酰化小管蛋白(下,绿色)。虚线表示基底薄层。盒装区域显示为放大倍数。核用DAPI(蓝色)染色。b)代表性的最大强度Z堆Z堆投影比较原发性纤维对非COPD和COPD患者对DIC(灰色),ARL13B(红色)和P63(绿色)的共焦型和COPD患者的非重组和COPD患者的重新耦合区域。箭头显示初级纤西本地化。虚线表示基底薄层。盒装区域显示为放大倍数。 Nuclei are stained with DAPI (blue). c) Box and whiskers plot showing median with interquartile range of the numbers of primary cilia (PC) per epithelium types in non-COPD patients and COPD patients on the epithelium as a whole (total), normal epithelium (normal), remodelled areas (remodelling), basal cell hyperplasia (BCH), mucous cell hyperplasia (MCH) and non-differentiated epithelium (NDE). d) Graph depicting the repartition of non-COPD and COPD patients according to the number of primary cilia per mm of normal (x axis) and remodelled (y axis) epithelium; e) Graphs depicting the repartition of non-COPD and COPD patients according to forced expiratory volume in 1 s (FEV1)%(x轴)和每毫米上皮(y轴)的初级纤毛的数量作为整体(左图),正常(中间图)或改造(右图)区域。线表示线性回归。#:P <0.0001。
由于已经表明,原发性纤毛不存在于成年肺组织[10[虽然它们存在于休息阶段的其他人体细胞上[12],我们考虑区分组织学“正常”上皮和“重塑”上皮细胞[13].普通上皮定义为呈现三种主要细胞类型(基础,纤毛和杯状细胞)的伪变性上皮。b)缺乏增生或细胞增生;c)在表面上显示至少50%的纤毛细胞。
我们分析了非COPD组和COPD组的支气管上皮(图1B.).作为整体,COPD患者与非COPD患者相比,COPD患者呈现巨大增加(中位数(IQR))(68.1(52.2-88.2)相对9.5(6.1-18.3);P <0.0001)(图1C.).有趣的是,与非COPD患者相比,COPD患者的正常上皮细胞原发性纤毛数量增加(56.5(48.2-67.1))。相对6.2(2.9-19.5);P <0.0001),改造地区(80.7(51.1-109.4)中更明显相对10.7(7.9-14.8);P <0.0001)。它在基础细胞增生中特别引人注目(116.9(91.2-188.2)PROPD患者每毫米上皮的原发性纤毛相对15.5(8.9-32.5)非COPD患者;P <0.0001)。除了一个受试者的数目在正常上皮每毫米40初级纤毛和重塑上皮每毫米50初级纤毛的被确定为截止COPD和非COPD状态之间(R = 0.9215,P <0.0001)(图1D).有趣的是,原发纤毛的显著增加与吸烟状态(p=0.01)有关,但与吸烟史(p=0.08)、呼吸困难评分(p=0.0003)、慢性支气管炎(p=0.04)、气道阻塞的严重程度(FEV)无关1:p = 0.002和fev1/强制生命能力:P = 8.7×10-7)、是否存在肺气肿(p=0.008)和严重程度(p=0.0009)。这些患者的临床或功能特征,加上对COPD患者原发性纤毛的分析,如。FEV.1(%pred;图1E.,线性回归升高之间的差异对于非COPD中的每个参数非常重要相对COPD组;P <0.0001)。
肺中初级纤毛的定位与它们的已知功能一致,包括极性获得、迁移、分化和细胞周期控制[14].来自非COPD患者的上皮内皮患者稀有的原发性纤毛患者罕见,表明原发性纤毛未稳定足够长,或者只有几种细胞是静态的。COPD患者中原发性纤毛的增加可能在这种疾病的背景下铺平了对对细胞可塑性的新理解。1)如果原发性纤毛是细胞周期进展指标,则基底细胞是否不再能够分开以更新上皮?2)是负责原发性纤西幻影的COPD的发作,也是反之亦然?3)初级纤毛的增加可以被认为是异常和功能失调支气管上皮的标志物,可参与气道阻塞和/或肺气肿,特别是关于气道再生异常的发育?
有趣的是,在正常和重组区域之间改变了原发性纤维数,表明在更新或修复上皮或修复过程中可能出现原发性纤毛的区域[10].这也与原发性纤毛在细胞迁移和组织稳态中的作用一致[15].支气管上皮伤口闭包的异常已显示在严重的COPD中,并且与气道阻塞和肺气肿的严重程度相关[8.].同样,原发性纤毛的异常可能参与这种现象。
在我们的研究中必须指出一些局限性。尽管这些发现是新颖的,但这些分析是探索性的,并且是在单中心研究中进行的,包括相对较少的患者。因此,样本选择和队列大小代表了偏见,以及“正常对照”的缺乏,这在肺切除术组织的研究中是无法避免的。此外,还需要进一步的研究来明确原发性纤毛改变的潜在机制。
总之,我们已经显示出与定义COPD的临床,形态学,功能和组织学参数相关的支气管上皮细胞纤毛的增加。由于原发性纤维素的存在与代表COPD的临床特征相关,理解原发性纤毛表达和功能的缺点将提供在这种复杂病理学中的额外线索,其中上皮的作用表现越来越重要。据我们所知,它是第一次观察人类成人气道上皮的非运动原发性纤毛。原发性纤毛细胞的积累是否是疾病驱动过程或上皮改变的后果将需要进一步调查。
脚注
作者贡献:学习理念:V. Dormoy;研究设计:J-M。Perotin和V. Dormoy;数据采集:J-M。Perotin,E. Lagonotte,G.Elageine,G.deslée和V. Dormoy;分析和数据解释:J-M。Perotin,G.deslée,M.Polette和V. Dormoy;修订稿件:C.Coraux,P. Birembaut,M.Polette和G.deslée;稿件写作:J-M。Perotin和V. Dormoy
利益冲突:没有宣布。
支持声明:这项工作得到了RégionChampagne-Ardenne和法国卫生和医学研究所(内在)的支持。本文的资金信息已存入Crossref资助者注册表。
- 已收到2018年1月19日。
- 公认2018年4月11日。
- 版权所有©ers 2018