摘要
在死于呼吸衰竭的新冠病毒-19患者中发现开放性肺内支气管肺吻合(IBA)。IBA可能是导致新冠病毒-19严重低氧血症的肺内右向左分流的微观解剖学基础。https://bit.ly/3e2GajO
致编辑:
严重急性呼吸综合征冠状病毒2(SARS-CoV-2)的传播导致了一种毁灭性的全球大流行性疾病,称为2019年冠状病毒病(COVID-19)。COVID-19导致急性缺氧性呼吸衰竭(COVID-ARF),这是死亡率和发病率的主要原因,其病理生理机制尚不完全清楚。G阿提诺尼等[1.]指出,COVID-19急性低氧呼吸衰竭患者的肺部疾病往往表现为保存相对良好的肺力学(包括肺顺应性)与严重低氧血症之间显著分离。这些发现与肺顺应性高的通气患者发生严重低氧血症的概念是一致的,这可能是由于肺灌注调节的丧失和低氧肺血管收缩受损。早期尸检研究表明,肺循环是冠状病毒感染的主要靶点,不同程度的血栓形成、细胞凋亡、水肿、炎症和血管生成导致严重的肺血管疾病[2.–4.].这些变化导致肺血管的失调,从而导致灌注异常,并导致COVID-19肺炎中报告的生理表型。此外,计算机断层扫描显示小肺动脉有一种独特的“树状芽状”外观[3.而对COVID-19低氧血症患者的经颅刺激盐水微泡多普勒研究表明,这些泡存在肺内分流,且经肺泡转运的存在和程度与低氧血症程度相关[5.]尽管进行了这些研究,但在相对正常的肺顺应性条件下,在新冠病毒-19患者中,严重低氧血症和分流的组织病理学相关性在很大程度上是缺乏的。
连接肺动脉和绕过肺泡的支气管动脉的突出肺内支气管肺吻合术(IBA)的特点是组织切片的三维(3D)重建,并被确定为几种肺部疾病中严重低氧血症的右向左分流的潜在来源,包括特发性肺动脉高压和慢性血栓栓塞性肺动脉高压[6.–13].IBA代表支气管和肺血管树之间预先存在的血管连接,这些血管树通常在胎儿期突出,在出生时似乎关闭,但在出生后可能出现,特别是在疾病时[14].这些分流血管的生理作用尚不完全清楚,但似乎是由于运动、缺氧和儿茶酚胺刺激导致从右到左分流,从而导致低氧血症[15–17].这些毛细血管前吻合口的直径在15-500之间 μm能够将脱氧血液重定向至肺微血管床,从而导致远端肺灌注不良[18]尚未研究这些血管连接是否在新冠病毒-19肺中显著,反映分流血管的募集。我们假设IBA在死于新冠病毒-19并伴有严重低氧血症的急性呼吸衰竭患者的肺中募集。
这项研究得到了西奈山伊坎医学院机构审查委员会的批准。我们收集了三名COVID-19患者的存档尸检肺组织。我们回顾了每个患者肺的两个组织块的苏木精-伊红(HE)染色片。常规HE切片结合三色染色和免疫组化染色(CD31,平滑肌肌动蛋白染色)确定肺结构和显微解剖。我们的研究聚焦于肺远端血管,这是气体交换的位置,因此研究的血管是邻近的终末和呼吸细支气管(气道直径范围为250-600 μm)和远端空气空间。进一步研究了IBA的结构和路径,建立了Z-stack,然后使用三维重建自由-D计算机软件程序[19].
所选患者的人口统计学反映了典型的新冠病毒-19患者群体,死亡时的年龄范围为69-86岁 年,男女比例为2:1,高血压、糖尿病和慢性肾病的常见相关共病,以及新冠病毒-19(2-10)阳性检测后的短期低氧血症病程 所有患者均接受与新冠病毒相关的药物治疗,包括阿奇霉素和羟基氯喹。所有患者的胸片均显示斑片状阴影。
病理组织学检查结合3D重建显示所有三名患者均存在显著的IBA。IBA显示肺血管和支气管血管之间广泛开放的吻合血管连接,通过3D重建证实(图1).扩张的支气管微血管和IBA,大小可达75 所有患者的直径均为μm。我们没有发现内皮炎、毛细血管微血栓或动静脉畸形的组织学证据。一名患者在远端肺静脉内有血栓。两名患者出现肺气肿改变。在所有样本中均观察到与急性肺损伤相关的组织病理学变化,包括病毒性肺炎、气道和间质炎症、aedema和透明膜疾病的可变组合
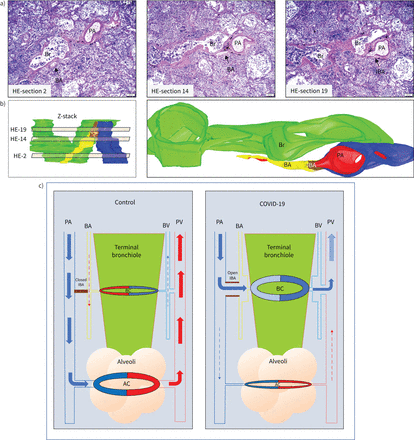
系列苏木精-伊红(HE)切片和三维(3D)图像重建相结合,可识别2019年冠状病毒病(COVID-19)中的肺内支气管肺吻合(IBA)患者。a)分析30个连续HE切片的三个代表性图像。首先创建显示支气管动脉束区域的HE切片Z叠层(图b,左侧:虚拟浅棕色切片表示Z叠层中编号HE切片的近似区域),并重建具有倾斜表示的3D图像(图b,右侧)。有一个大开口的IBA(3D图像中为棕色,第19节中为小箭头),连接肺动脉(PA,蓝色)和支气管动脉(BA,黄色)。细支气管(Br)为绿色,BA、IBA和PA的内皮细胞以红色突出显示。比例尺:200μm.c)肺内右向左分流的显微解剖示意图。在COVID-19患者中,末梢细支气管水平的远端肺血流重新排列。在正常肺(左图)中,肺动脉(PA)中的脱氧血(蓝色箭头)进入肺泡毛细血管床(AC)用于气体交换,并收集含氧血液(红色箭头)通过肺静脉(PV)进入左心。少量含氧血液(红色虚线箭头)供应末梢细支气管(绿色)通过支气管动脉(BA)和细支气管毛细血管网(BC)。去氧血(蓝色虚线箭头)由支气管静脉(BV)收集,随后是进入左心的肺静脉。IBA(棕色)闭合,肺和支气管血管树之间不存在血流。在新冠病毒-19肺(右图)中,远端肺动脉中的大部分脱氧血液没有到达肺泡毛细血管网络进行气体交换(蓝色虚线箭头),而是通过开放的IBA重定向(蓝色箭头)至支气管动脉和支气管微循环,绕过肺泡毛细血管床。由于来自右心的大量血液,支气管动脉、毛细血管和静脉被动扩张。血液保持脱氧状态,由支气管静脉收集并进入左心通过肺静脉,导致新冠病毒-19患者出现严重的全身性低氧血症。
尽管冠状病毒-19感染者严重低氧血症的确切病理生理机制尚不确定,但最近的临床、影像学和尸检研究发现肺血管异常[2.–4.]肺内右向左分流[5.]我们的研究结果不仅与最近影像学研究中发展的肺血管病范式一致,而且在发展为无症状、深度和无反应性低氧血症的过程中发挥了关键作用,导致了新冠病毒-19患者群体的显著发病率和死亡率[3.,5.],但进一步表明,显著的IBA可能是新冠病毒-19相关低氧血症的微观解剖相关因素。通过严格的组织学评估和计算机三维图像重建,我们确定了突出和招募的IBA,并认为这些是肺内右向左分流的潜在组织学相关性。肺血栓形成在新冠病毒-19患者中很常见[2.–4.].虽然我们没有发现微血栓,但我们确实在一位患者中发现了血栓形成的肺静脉。在患有慢性血栓栓塞性肺动脉高压的成年患者中,已经描述了支气管血管与肺血管的连接以及异常的肺静脉,这表明血栓事件与COVID-19患者中IBA的招募之间存在联系[13].炎症和传染性呼吸道疾病已被证明可诱导IBA的招募,在COVID-19呼吸衰竭和低氧血症患者中可能存在该病毒[20,21].
我们认为,缺氧的血液通过扩张的支气管微血管从右向左流动,绕过肺泡毛细血管网络,影响气体交换(图1)我们的发现支持了最近的搅动盐水超声研究,该研究表明肺内右向左分流是新冠病毒-19患者严重低氧血症的病理解释[5.].这种最初的低氧血症伴梗阻和远端毛细血管床灌注不良可能会因IBA募集而恶化,从而导致血液从右至左严重分流。这种分流进一步减少远端肺灌注,阻碍气体交换,导致难治的低氧血症和死亡。对IBA的调控进行重点研究可能会产生独特的策略,从而降低感染SARS-CoV-2患者的发病率和死亡率。
可共享PDF
致谢
作者要感谢西奈山伊坎医学院病理学系的Fumiko Dekio和Rachel Brody的支持。
脚注
利益冲突:C.Galambos无需披露任何信息。
利益冲突:D.布什没有什么要披露的。
利益冲突:S.H.Abman无需披露任何信息。
支持声明:这项工作得到了国家心脏、肺和血液研究所(授权:NIH RO1#2RO1HL06702-13A1)的支持。本文的资助信息已存放在交叉参考基金登记处.
- 收到2020年12月3日。
- 认可的2021年4月5日。
- 版权所有©作者2021年。
本版本根据知识共享署名非商业许可4.0的条款发布。有关商业复制权利和许可,请联系权限{at}ersnet.org