文摘
慢性阻塞性肺疾病(COPD)是一种已知的患肺癌的危险因素,但潜在机制仍然未知。我们假设,慢性阻塞性肺病基质包含支持tumourigenesis分子机制。
我们进行了一次无偏multi-omic分析来识别基因表达模式,区分COPD患者基质或没有肺癌。我们从COPD患者肺组织获得和肺癌(肿瘤和相邻的良性组织)和患有慢性阻塞性肺病没有肺癌蛋白质组的分析和信使rna(细胞质和polyribosomal)。我们使用了关节和个体变异解释(假的)方法整合和分析三个数据集。
JIVE确定八个潜在的模式,强劲杰出和分离的三组组织样本(肿瘤、毗邻和控制)。预测变量与肿瘤有关,与相邻的基质相比,主要是在转录组数据,而预测变量与邻近组织,控制相比,在translatomic代表水平。路径分析显示细胞外基质和phosphatidylinositol-4 5-bisphosphate 3-kinase-protein激酶B信号通路中重要的信号肿瘤邻近的基质。
multi-omic方法区分肿瘤邻近的基质在肺癌和揭示了两种基质表达模式与癌症有关。
文摘
multi-omic方法识别基因表达项目区分COPD肺间质与肺癌有关http://ow.ly/j1Da30jWH1X
介绍
独立于吸烟,慢性阻塞性肺疾病(COPD)是一种已知的危险因素的发展肺癌(1,2]。这种模式支持的进一步观察肿瘤更有可能出现的与肺气肿的领域(3,4]。中心气流梗阻的病理生理学COPD肺细胞外基质(ECM)的改造与失去弹性和气流阻力增加。这ECM重塑伴随着小气道纤维化和炎症,潜在的基质环境促进tumourigenesis曾产生致癌突变的上皮细胞接触烟草或其他致癌因素。
它也承认癌症启动发生基因突变的过程。然而,它正变得越来越明显,肿瘤是整体与他们的微环境5,6]。这个微环境由ECM组成的基质成纤维细胞、内皮细胞和居民免疫细胞促进肿瘤进展。这些基质细胞不获得基因突变,然而,它是承认癌症相关的成纤维细胞,产生ECM的主要基质细胞,在肿瘤进展的主要因素。最近的证据也将成纤维细胞和ECM的中心肿瘤起始。人类衰老成纤维细胞已被证明刺激和恶性癌变前的上皮细胞增殖,而“正常”的上皮细胞不受影响(7]。在小鼠模型的乳腺癌,成纤维细胞缺乏的肿瘤抑制基因PTEN大大加速癌症启动的方式部分依赖于纤维母细胞分泌的因素(8]。我们的研究试图确定具体改变COPD-stroma促进肺部致癌作用,当这些仍然未知。
创造一个pro-malignant基质环境的机制可能是复杂的。尽管蛋白质效应分子,他们的监管可以出现在多个水平包括转录、翻译和翻译后修饰。在早期,转录调控研究的主要焦点;然而,翻译监管已经成为一个重要的机制对于致癌作用[9- - - - - -11]。因此,全基因组的方法理解致癌作用的复杂性是必要的。在这方面,我们试图理解的角色使用multi-omic COPD肺间质在肺癌的方法。
材料和方法
研究人口和肺组织样本
明尼苏达大学的机构审查委员会人体试验委员会批准了这项研究。外科肺组织样本从梅奥诊所获得与COPD肺标本从个人注册阶段I或II腺癌(接受手术切除表1)。肿瘤和邻近肺组织样本包括来自32个腺癌和慢性阻塞性肺病患者。控制来自美国国立卫生研究院(NIH LTRC)和肺组织研究财团包括来自32个COPD患者的肺组织没有肺癌(表1)。所有样品都获得了NIH LTRC使用相同的过程。所有主题,例和对照组现任或前任吸烟者。这些肺组织活检被称为“肿瘤、毗邻和控制”。总共有32个组织样本共享转录组,translatome和蛋白质组数据(10和11例肿瘤控制和一个相邻的组织;表2)。样品的数量为每个数据类型所示是可用的表3。
蛋白质组学和RNA序列
肺组织为等压标签处理相对和绝对定量(iTRAQ)标签遵循制造商的建议和之前发表(12]。肺组织处理总量和polysomal mRNA隔离和测序如前所述13]。详细的实验设计信息是可用的补充材料。蛋白质质谱在蛋白质组学数据可用识别(骄傲)数据库(www.ebi.ac.uk骄傲/归档/;加入PXD007919)。RNA序列基因表达数据的综合(GEO)数据存储库(www.ncbi.nlm.nih.gov /地理/;加入GSE106899)。
统计分析
所有数据分析使用R统计计算环境(www.r-project.org/;3.3.2 R版本)。之前数据集成、数据进行预处理和独立筛查中描述的补充材料(14- - - - - -16]。预处理后蛋白质组有1486,5989个转录组和8014个translatome基因或蛋白质。接下来,我们确定一个综合复合生物标记样本状态(肿瘤、毗邻和控制)三种不同的数据类型(蛋白质组学、转录组和translatome)使使用多步方法前面描述的(17]。
对于每个数据类型,我们首先进行了单变量线性建模步骤为每个基因或蛋白质过滤变量预测能力。过滤后,我们进行了一个综合降维的变量使用联合和个体变异解释(假的)方法(18,19]。隐语是主成分分析的扩展multi-omic之间共享数据,它能够识别潜在的结构和表达多种高通量数据类型。“联合组件”定义样本模式解释跨多个数据类型和实质性的变化“单个组件”样本模式解释实质性的变化在一个数据类型而不是其他人(17]。
执行JIVE之后我们使用了肺癌样本类型(肿瘤、毗邻和控制),我们在多项逻辑回归结果使用JIVE组件作为预测因子。组件所包含或排除在模型逐步(向前或向后)选择算法最小化Akaike信息标准(AIC) [20.]。这给了一个复合模型来预测组织样本被癌变的机率,tumour-adjacent,或发生慢性阻塞性肺病从所有三个组学数据集。
评估拟合模型的准确性我们进行n次(离开)交叉验证,一个组织样本被作为一个测试用例,模型参数估计使用剩下的(n = 31)样本作为训练集,由此产生的模型的预测评估使用的测试用例。这个过程被重复每个样本作为测试用例。
要确定哪些人是最有影响力的基因或蛋白质,JIVE组件映射回原变量空间给meta-loadings每个变量(17]。这些可以解释为给线性重量(即。每个变量的系数)为每个比较拟合模型。我们进行了路径分析使用meta-loadings确定哪些生物功能是最常见的拟合模型。这些基因的绝对meta-loading大于或等于绝对的均值meta-loading对于一个给定的比较作为活跃基因设置为每个数据类型。基于web的基因集分析工具包(WebGestalt;www.webgestalt.org/)[21)是用来执行一个代表使用KEGG通路富集分析中描述补充材料。
结果
样本和数据采集
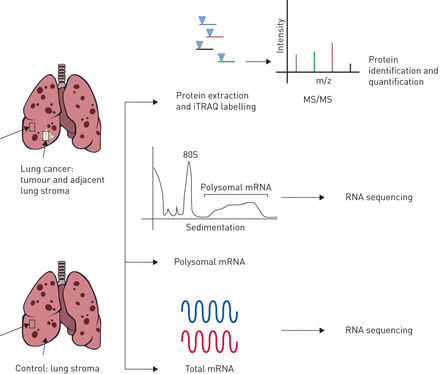
我们比较肺肿瘤和非肿瘤邻近肺组织从COPD患者COPD患者但没有肺癌组织(图1)。蛋白质组学分析用于32 COPD和肺癌患者和32的控制。肺功能更严重的声带良性对照组平均%预计在1 s (FEV用力呼气量1)在肺癌患者(18%至53%表1)。蛋白质组学分析包括iTRAQ-based定量质谱在16分,获得平均27 432光谱匹配12 457 2105不同的肽和推断蛋白质1%全球错误发现率(罗斯福)。21个学科(11例和10控制)样本足够的蛋白质组学分析和信使rna序列,总量和polyribosomal (表2),平均24 484 971读和平均读38的质量。这导致阅读映射的百分比52.6,识别平均5602个基因样本总mRNA的信使rna序列(转录组)和polysome-associated mRNA(成绩单受三个多核糖体)。后者标识有效地翻译mRNA,以下简称translatome。较低的映射是由于相对比较小的样本质量要求额外的放大。
肺肿瘤的multi-omic分析方法,相邻发生肺组织和肺组织慢性阻塞性肺疾病控制。相对和绝对定量iTRAQ:等压标记;女士/小姐:串联质谱分析。
独立的筛选
在单变量筛选下,translatome数据并未产生显著的独立与癌症生物标记关联状态下罗斯福阈值为0.1。转录组数据达到五个重要的独立与癌症生物标记关联状态和蛋白质组数据达到1116重要的独立的生物标志物协会。更多的社团发现的蛋白质组学数据,部分原因是其更大的样本量为蛋白质组(n = 96与n = 33 mRNA),收益更多的统计能力检测独立协会在这里使用的严格的多个测试标准。
维恩图展示的数量为每个比较重要的蛋白质(罗斯福< 0.1)(图2)。蛋白质组独立协会内的结果,大多数的生物标志物协会为比较重要的肿瘤样本配对相邻样本和比较肿瘤样本和控制(图2 b)。少数蛋白质区分相邻样本的控制。的转录组数据,一个基因(DDIT4)是一个共享的重要独立生物标志物之间的癌症状态关联的肿瘤和控制以及相邻和控制(图2一个)。使用更严格的阈值,罗斯福< 0.05,没有转录组关联仍和314年总蛋白质组学协会仍然显著。
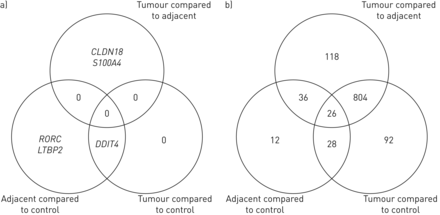
维恩图之间的)共享记录和b)蛋白样品比较使用成对t(错误发现率(罗斯福)< 0.1)。
的转录组数据,35基因与% FEV预测有显著相关性1translatome数据的内部控制,而18基因与% FEV预测有显著相关性1内部控制(罗斯福< 0.1)。这些基因没有重叠与基因与癌症的地位图2。未发现其他重要协会与% FEV预测1转录组和年龄,translatome或蛋白质组学数据,在控制或在癌症患者。
数据集成和预测模型确定了八个潜在的数据结构
将这三个数据集整合到一个有用的预测模型我们JIVE算法用于多源数据18,19]。隐语是主成分分析的扩展multi-omic数据和识别潜在的结构(即。组件)之间共享,并表示在多个高通量数据类型。接头组件定义样本模式解释大量的可变性跨多个数据类型和各个组件示例模式解释实质性的变化在一个数据类型而不是其他人(17]。
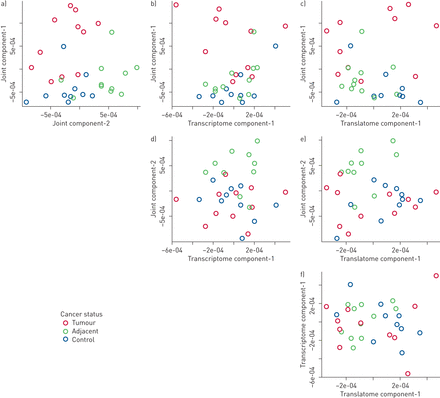
过滤后一元多项式回归我们有612,1108和574个基因的蛋白质组学、转录组和translatome数据,分别。蛋白质或基因的数量在每个阶段的过滤和转录组之间的重叠和translatome给出在每个阶段图3。排列测试确定了两个联合JIVE组件,零显著的额外的蛋白质组学数据的单个组件,三个单个组件的转录组和三个单个组件translatome总共八个潜在潜在的模式。三个样本组(肿瘤、毗邻和控制)是有区别的两个接头组件,见的左上的面板图4。
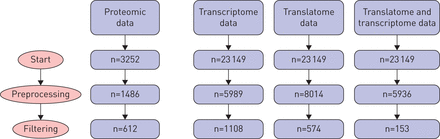
图的数量基因或蛋白质在不同阶段的预处理和过滤前关节和个体变异(假的)分析解释。预处理细节中可用补充材料。右侧栏给基因的数量后的转录组和translatome数据共享的每一个步骤。
散点图的关节和个体变异解释(假的)得分为两个接头组件和转录组数据的第一个单个组件和translatome数据。每个点代表一个肺组织样本和颜色给癌症的地位。第一个关节组件共享的三种数据类型(a - c)显示了一个非癌症(控制和相邻)和癌症之间分离样本。第二个关节组件(d, e)显示了一个区分邻样品和其他样品。分别为个体结构(转录组和translatome)没有显示强烈的癌症分化状态(f)。
接下来,我们符合多项逻辑回归模型来预测样本组使用JIVE组件作为预测指标确定的八。即日志优势比样本属于某一组加权线性组合模型的两个接头组件,三个转录组的单个组件和三个translatome单个组件。每个样本的概率预测组n次交叉验证以下所示图5。该模型区分样本三个组。使用类的概率预测0.5作为阈值,三个样本分类错误(90.6%的准确率):肿瘤样本分类为肿瘤邻近(10的11正确分类),相邻样本并被错误地归类为一个控制(10的11正确分类)和一个控制样本并被错误地归类为肿瘤(9的正确分类)。日志预测概率没有%预测FEV显著相关1或在控制年龄患者在癌症患者(p > 0.05)。
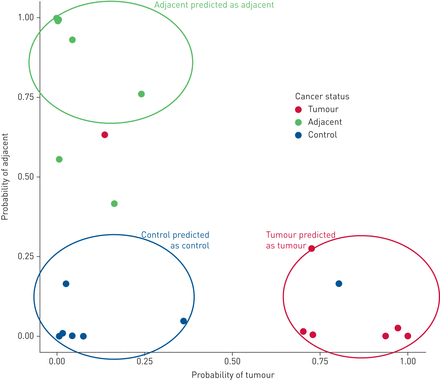
集团为多项式概率逻辑回归预测使用n次交叉验证(n = 32)。
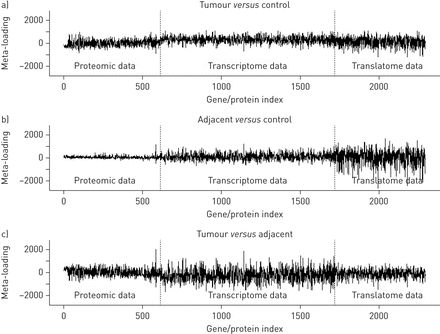
多项式回归模型(补充图S1JIVE成绩总结)系数补充表S1。由此产生的基因和蛋白质meta-loadings每个比较(肿瘤所示与控制,相邻与控制和肿瘤与相邻)图6。这些情节显示meta-loading对变量(基因或蛋白质)指数,揭示了每个变量的贡献大小和方向的预测模型进行比较。为肿瘤相比,很明显,预测变量控制组织均匀分布在蛋白质组学、转录组和translatomic数据。预测变量与癌症相关的慢性阻塞性肺病基质与相邻的慢性阻塞性肺病基质与癌症无关translatomic中主要是数据(polyribosomal-associated mRNA),而肿瘤的预测变量与邻近主要是在转录组数据(总mRNA)。这种模式表明,肺组织毗邻肺癌,但不包含肺癌,显示独特的签名,体现在不同级别的监管。这些数据表明,不仅彻底审讯的蛋白质组,转录组和translatome,提供分子的洞察力,否则将被丢弃。
Meta-loadings三种数据类型的变量(蛋白质组,转录组和translatome)每个样本的比较认为:a)肿瘤与控制,b)相邻与控制和c)肿瘤与邻边。
KEGG途径分析
的通路富集分析meta-loadings从JIVE预测分析显示几个重要途径获得跨越三个数据类型(为每一个比较表4)。蛋白质组数据的六个途径对肿瘤具有重要意义与相邻的比较和五个是重要的肿瘤与控制的比较。然而,对于translatome数据,相邻的六个途径是重要的与控制的比较。对于所有其他分析校正后所有通路都是无关紧要的多重比较(罗斯福> 0.1)。这些发现符合translatome最相关的邻近的区别与控制样本,而蛋白质组数据更相关的其他两个比较。然而,一些途径共享不同的比较和数据类型。ECM-receptor交互,粘着斑和phosphatidylinositol-4 5-bisphosphate 3-kinase-protein激酶B (PI3K-Akt)信号是非常重要的三个分析产生了显著的结果。
一个类似的途径分析基于单变量t统计量而不是JIVE meta-loadings为每个数据集和比较也执行。的途径实现意义又发现只有三个以上分析(肿瘤与相邻的蛋白质组学数据,肿瘤与控制蛋白质组学数据和相邻与控制translatome数据)。那些相似的结果表3(见补充表S2)。
讨论
COPD和肺癌之间的关系被描述在三十年前(1,2];然而,这个观察的分子基础仍然是难以捉摸的。在这项研究中,我们利用一个multi-omic方法在肺部组织,包括肿瘤、相邻良性肺组织和COPD肺组织主题没有肺癌肺间质中发现3信号。这种multi-omic方法包括定量质谱蛋白质组学以及总细胞质RNA序列(RNA-Seq) mRNA(转录组)和polysomal-associated mRNA (translatomics)。整合我们的multi-omic数据集,利用联合和个体变异解释(假的)方法(18,19),同时模型共享的组件在所有的数据集。从这些我们构造一个multi-omic预测模型,给统计可靠的分离的三种组织类型(即。肿瘤,non-tumour邻近组织和控制慢性阻塞性肺病组织)。
在我们的数据集的蛋白质组学数据集的最大样本量由于原样品质量的限制。我们观察到最大的差异表达比较肿瘤和non-tumour组织时,相邻组织或慢性阻塞性肺病,从控制。这并不奇怪考虑癌症取代正常的肺结构创建一个独特的分子背景。有趣的是,我们发现显著变化从附近组织基质蛋白质组肺癌之间控制组织相比,即。不是与肺癌有关。
探索和集成三个multi-omic数据集之后,我们利用JIVE算法过滤由一元多项式回归。JIVE算法减少了大型数据集变量到八潜在的模式。这三个样本组(肿瘤、毗邻和控制)大多数由两个接头组件。六个额外的单个组件或模式识别转录组和translatome(三)。使用这些组件,我们生成了一个模型来预测样本组的身份,强劲杰出和分离样本三个组。接下来,我们决定每个变量的大小和方向对模型的贡献。预测变量的肿瘤相比,邻近肺间质被发现主要在转录组数据集。这并不奇怪,因为nonsmall细胞性肺癌(NSCLC)由上皮细胞发生了基因改变往往体现在改变转录(22]。然而,对没有恶意的基质的预测变量,即。肿瘤邻近的基质与控制基质,体现在polyribosomal mRNA数据集或translatome [23),这表明监管发生在翻译的水平(24,25]。这些发现与其他报告一致,基因表达在癌症控制发生和发展层面的转化(26- - - - - -28]。
通路的基因分析表明相邻的变化组织translatome确定ECM和PI3K-Akt信号作为潜在3通路。ECM和PI3K-Akt代表是常见的肿瘤及邻近组织,但不同于控制。蛋白质组的变化也与ECM和PI3K-Akt信号通路,但这些差异表明代表肿瘤组织相对于相邻的组织和控制。这表明,异常ECM和PI3K-Akt 3信号中发挥作用。
翻译是一个严格监管的过程,这个过程的失调是许多癌症的发展和进展,包括肺癌(26]。真核翻译起始因子4 e (eIF4E)形式复杂,使翻译。然而,在稳态条件下,eIF4E隔离刺激通过雷帕霉素(mTOR)的PI3K-Akt-mammalian目标途径导致装配eIF4E复杂,增加了翻译的29日]。高浓度的eIF4E相关实验和人类癌症,包括肺癌(26,29日]。与这些发现,我们的数据是一致的肿瘤样本演示的增加表示PI3K-Akt信号通路与相邻的组织和控制。然而,eIF4E在前期恶性病变的作用是减少定义。l我et al。(28)确定eIF4E阳性细胞在相邻,良性组织与口腔鳞状细胞癌。我们确定了PI3K-Akt信号通路在组织的席位附近肿瘤控制基质相比,这种模式主要表达在translatome或polyribosomal分数。因此,肺间质,是肺癌的组织学检查免费3增加了翻译的信号通过PI3K-Akt信号通路。
一种蛋白激酶的作用在慢性阻塞性肺病是鲜为人知的。在一项研究H奥斯古德et al。(30.),单核苷酸多态性(SNP)PTEN基因被发现与慢性阻塞性肺病。PTEN是一个重要的细胞循环发展和细胞生存和监管机构也AKT的负调节功能。的损失PTEN与癌症有关启动,因此它被指定为肿瘤抑制基因。在小鼠模型的乳腺癌,损失的PTEN在基质成纤维细胞显著加速癌症起始和进展(8]。这些发现表明,AKT监管可能是慢性阻塞性肺病和癌症之间的联系开始。
肿瘤间质包括良性细胞,如成纤维细胞、间充质细胞和免疫细胞以及血管和ECM。在过去的二十年里,它已成为明显的肿瘤基质中发挥着积极的作用在肿瘤细胞招聘、发展和传播(6,31日,32]。然而,ECM 3信号的作用仍不清楚。异常发现以来的ECM仍然是慢性阻塞性肺病的标志elastolytic升高和其他相关蛋白酶破坏ECM在慢性阻塞性肺病33,34]。这些基质降解蛋白酶是由良性细胞,但是一旦发布就可以掌握在恶性或3细胞援助micro-invasiveness或信号通路的激活35]。像预期的那样我们发现ECM区分肿瘤和邻近组织的证据,但是也发现差异时比较相邻良性肿瘤间质和COPD肺组织与癌症无关。这些发现是受到慢性阻塞性肺病严重程度的差异之间的控制和那些有癌症,但是强调了重要的和ECM有点隐蔽的作用可能在慢性阻塞性肺病和3间质。
限制我们的研究慢性阻塞性肺病严重程度的差异在肺癌相关的慢性阻塞性肺病与控制(即。控制有更严重的慢性阻塞性肺病相对于那些肺癌)。由于我们的数据并不足以控制慢性阻塞性肺病严重,我们无法确定是否观察到的一些差异与慢性阻塞性肺病严重程度相关。然而,相同的路径(如。ECM和PI3K-Akt)在肿瘤组织的区别与邻近组织,这表明它们与致癌作用而不是慢性阻塞性肺病严重程度有关。此外,确定基因和多项式模型的预测并没有与慢性阻塞性肺病严重程度内控制或癌症人群。虽然我们相邻的良性肺组织并没有恶性肿瘤的组织学证据,我们不能保证肿瘤间质表型在远处通过分泌因素的影响。此外,我们不能保证对照组没有携带3变化体现在稍后的时间点。然而,如果真的这将引入噪声和削弱我们的统计分析,这不是建议的健壮的区别在我们的研究中发现。
总之,我们开始探索慢性阻塞性肺病癌症相关的支持tumourigenesis基质分子信号。我们发现附近COPD肺组织,但不包含,腺癌表达不同的分子信号相比,肿瘤和良性慢性阻塞性肺病组织(控制)。具体来说,分子信号在肿瘤组织中被体现在翻译水平和丰富ECM和PI3K-Akt信号。这表明异常ECM和PI3K-Akt信号作为潜在3通路。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
补充方法和表erj - 02665 - 2017 - _supplement
补充图S1。多项适合逻辑回归模型预测癌症从八JIVE组件状态。erj - 02665 - 2017 - _figure_s1
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:没有宣布。
支持声明:本研究得到了美国国家心脏,肺和血液研究所(NHLBI)授予R01-HL107612。资金信息,本文已沉积的Crossref资助者注册表。这种材料是工作的结果支持在明尼阿波利斯VAMC资源和设施的使用。内容不代表美国退伍军人事务部的观点或美国政府。
- 收到了2017年12月20日。
- 接受2018年5月6日。
- 这个工作的内容不受版权。设计和品牌版权©2018人队