抽象
临床环境下nintedanib在IPF患者中的安全性和耐受性与产品标签一致http://ow.ly/Nulb30jPAld
编辑器:
Nintedanib已被包括美国在内的60多个国家批准用于特发性肺纤维化(IPF)的治疗[1]。在两期三期肺搏试验中,nintedanib通过减少强制肺活量的下降来减少疾病进展[2]。大多数患者能够控制nintedanib的副作用,19.3%的患者接受nintedanib治疗与13.0%接受安慰剂治疗,因不良事件永久停止研究用药。最常见的不良事件是胃肠道,特别是腹泻。有一次或多次严重不良事件的患者比例与nintedanib和安慰剂相似(30.4%)与30.0%)。
随着nintedanib作为IPF的治疗手段的推出,我们收集了其在现实环境中的安全性和耐受性信息通过上市后监测。在这里,我们对2014年10月15日和10月31日,2015年的数据对IPF患者不良事件报告的推出尼达尼布之间在美国收集的数据进行分析与处理尼达尼布,不论因果关系,收集通过与专业药店和自发报告系统积极主动的交流。此外,收集不良事件的报告通过与患者和护理人员的直接接触是患者支持计划的一部分(开门)。不良事件根据医学规范活动词典(MedDRA)进行编码。根据nintedanib的作用机制和灌胃试验的数据,上市后监测数据中感兴趣的不良事件被定义为腹泻、出血、肝脏疾病、动脉高血压、主要不良心血管事件(MACE)、心肌梗死和卒中。出于上市后安全性分析的目的,这些不良事件的发生率采用与INPULSIS试验相同的定义进行评估。有关腹泻(在一般人群中)发病率和其他相关不良事件(在不匹配的IPF患者中)的流行病学数据来自于文献[3.- - - - - -9],然后从患者代表美国的商业保险人口的专有研究数据库(在文件中的数据,Optum研究数据库)。
我们的上市后监测数据来自6758例患者带着IPF与尼达尼布处理。Median duration of exposure was 113 days (range 6–390 days). Estimated cumulative exposure was 2715 patient-years. Diarrhoea (2858 events, not individuals reporting at least one event), nausea (1476 events) and vomiting (705 events) were the most frequent adverse events. Most (95.0%) adverse events were not serious. A total of 4062 adverse events defined as of interest in the post-marketing surveillance data were reported. Of these, 322 had a fatal outcome, including 27 cases of MACE, eight of myocardial infarction, three of stroke and two of bleeding. In 123 cases, the cause of death was not reported. The most frequent causes of death that were reported were progression of IPF (81 cases), respiratory failure (27 cases) and pulmonary fibrosis (18 cases).
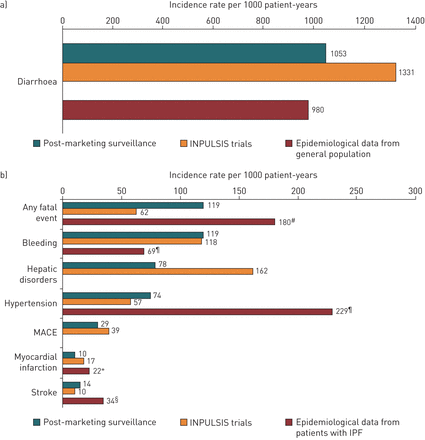
The incidence of diarrhoea in the post-marketing surveillance data was 1053 per 1000 patient-years. Understanding that diarrhoea is a very common side-effect of nintedanib therapy, this was lower than the rate reported in INPULSIS (1331 per 1000 patient-years) and similar to the rate in epidemiological data from the general population (980 per 1000 patient-years) [5,8)(图1一个)。
nintedanib抑制血管内皮生长因子受体,可能增加出血风险。已知有出血风险的患者,包括接受全剂量抗凝剂或高剂量抗血小板治疗的患者,均被排除在临床试验之外。美国产品标签规定,只有当预期收益大于潜在风险时,已知有出血风险的患者才应接受nintedanib治疗[1]。在上市后监测数据出血事件的发生率类似于INPULSIS(119与每1000个病人年有118人)。大多数出血事件并不严重;最常见的是鼻出血、挫伤和直肠出血。基于医疗保健索赔数据的IPF患者出血事件发生率低于上市后监测数据(图1 b)。这并不是意料之外的,出血事件并不严重到病人需要就医的程度(如。鼻出血)通常不包含在基于索赔的数据中。不出所料,已知的抗凝药物在出血患者中的使用比非出血不良事件中要多。在上市后监测的324例出血病例中,报告37.7%的患者同时使用抗凝药物,34.3%的患者不知情。在4739例无出血的不良事件中,有25.4%的报告同时使用抗凝药物,46.3%的病例未知。
在灌血试验中,接受nintedanib和安慰剂治疗的患者中分别报告了10.0%和10.6%的心脏疾病不良事件,但在基于标准化MedDRA查询“心肌梗死”的心肌梗死患者比例中存在数量失衡(2.7%)与分别为1.2%)(10]。nintedanib在美国的产品标签上说,心血管风险较高的患者应谨慎对待[1]。The incidence of myocardial infarction in the post-marketing surveillance data (10 per 1000 patient-years) was lower than in INPULSIS (17 per 1000 patient-years) or in epidemiological data from unmatched patients with IPF (22 per 1000 patient-years) (from references [4,7]和文件数据,Optum研究数据库)。MACE的发生率低于肺脏(29例)与每千名病人年39名(图1 b)。The incidence of hypertension in the post-marketing surveillance data was similar to that in INPULSIS (74 and 57 per 1000 patient-years, respectively) and lower than in epidemiological data from unmatched patients with IPF (229 per 1000 patient-years) (data on file, Optum Research Database). The incidence of stroke reported in the post-marketing surveillance data was similar to that reported in INPULSIS (14 and 10 per 1000 patient-years, respectively) and lower than in epidemiological data from unmatched patients with IPF (34 per 1000 patient-years) (from references [7,9]和文件数据,Optum研究数据库)。肝脏疾病的发生率(每1000个病人年78例)低于肺脏疾病的发生率(每1000个病人年162例),这可能反映了较少的肝酶测量。
随机对照临床试验提供特定患者人群药物的安全性和耐受性最可靠数据,但必然是持续时间短,并在人口并不完全代表潜在的药物收件人进行。上市后监测研究提供了药物的安全性和耐受进一步的数据,并帮助量化罕见的不良反应发生率[11- - - - - -13]。然而,上市后监测研究,有一些限制,包括漏报无严重不良事件[12,14以及缺乏关于不良事件、不良事件的结果(包括剂量调整和永久性停用)和报告不良事件的患者特征的全面文件。这组上市后数据中相对较短的暴露时间中值(113天)应作为一个限制,但数据仍在继续收集。方法上的差异意味着应该谨慎地比较上市后监测、临床试验和流行病学研究的数据。此外,临床医生在提供处方时可能存在安全偏差,导致临床实践中某些不良事件的发生率低于临床试验。
我n conclusion, post-marketing surveillance data collected for ∼1 year after the US launch of nintedanib as a treatment for IPF suggest that the safety and tolerability profile of nintedanib in the real-world clinical setting is consistent with the product label. As in clinical trials, the most frequent adverse events reported in clinical practice were non-serious gastrointestinal events, particularly diarrhoea.
确认
作者感谢Alexandar Allinger, Boehringer Ingelheim Pharma GmbH & Co. KG(德国莱茵Ingelheim)在数据采集和分析方面的贡献。医学写作援助由FleishmanHillard Fishburn(英国伦敦)的Julie Fleming和Wendy Morris提供,该项目由Boehringer Ingelheim Pharmaceuticals, Inc.签订合同并提供资金。所有作者都参与了数据的解释和本信函的撰写,并批准了最终版本。
脚注
利益冲突:M. Kaul是Boehringer Ingelheim的雇员。
利益冲突:C.S. Conoscenti是Boehringer Ingelheim的雇员。
利益冲突:G. Raghu报告从Boerhinger Ingelheim、Sanofi和Vercyte收取个人和其他费用,以及从BMS、Fibrogen、Gilead、Promedior、Roche-Genentech和UCB收取作为提交工作之外的IPF研究顾问的其他费用。
利益冲突:一,诺斯接受赠款,以及个人费用研究合同,扬声器局的成员,顾问委员会成员,并从勃林格殷格翰咨询报告;补助金,并为研究合同,扬声器局的成员,顾问委员会成员,并从基因泰克咨询个人费用;个人费用从ImmuneWorks咨询;和个人的费用提交作品外赛诺菲安万特公司的顾问委员会成员。
支持声明:本INPULSIS试验和尼达尼布的上市后监测方案是由勃林格殷格翰资助。本文资金的信息已交存Crossref资助者注册表。
- 收到2017年7月3日。
- 接受2018年4月20日。
- 版权所有©ERS 2018