抽象的
不正常DNA甲基化模式区分气道平滑肌细胞功能在哮喘和哮喘严重程度http://///wly/ctrk30icwvk.
编辑器:
哮喘是一种慢性气道炎性疾病,其特征在于气道高反应性,炎症和重塑,包括气道平滑肌细胞(ASMC)增生和耻骨滑道纤维化[1,2].来自严重哮喘的ASMC是过度增殖的,释放更多的促炎细胞因子,与来自健康个体和非严重哮喘患者的人相比,皮质类固醇不敏感[3.,4].遗传和表观遗传过程如MiRNA表达和DNA甲基化已涉及哮喘发病机制[5].实际上,DNA甲基化在哮喘血细胞中改变[5]并且可能是Atopate的生物标志物[6].
我们假设与改变的mRNA和miRNA表达相关的DNA甲基化的全基因组分析将揭示对疾病的途径,特别是在疾病中的功能异常的ASMC中。我们分析了DNA甲基化状态差异的互连和功能性相关性以及从五个健康受试者中获得的支气管活组织检查培养的ASMC中的MRNA和MIRNA的表达,5例非严重哮喘患者(NSA)和5名严重哮喘患者(SA),在基线和后续刺激胎儿小牛血清(FCS)和转化生长因子(TGF)-β(1ng·mL−1)[3.,4].已知该刺激诱导ASMC增殖,并以严重程度的依赖方式增强炎症介质的释放[3.,4].SA和NSA定义如前所述[1,2].健康受试者既往无哮喘史和刺激浓度导致1 s >16 mg·mL用力呼气量下降20%−1.完整的患者人口统计学显示在表格1.该研究得到了皇家Brompton和Harefield Hospital NHS信任的伦理委员会的批准,所有科目都提供了书面知情同意书。
使用Illumina 450 K阵列(人甲基化450k.2,San Diego,Ca,USA)鉴定了1283个差异甲基化的位置(DMP)(由> 20%平均甲基化差异),通过临床指定聚类(图1一个).分析组之间的DMP揭示了15个枢纽网站(图1 b)除了TRPV1.,与与哮喘病理生理学相关的重要过程/途径相关的新型哮喘基因相关,包括来自SA的ASMC中的炎症,代谢和增殖途径。
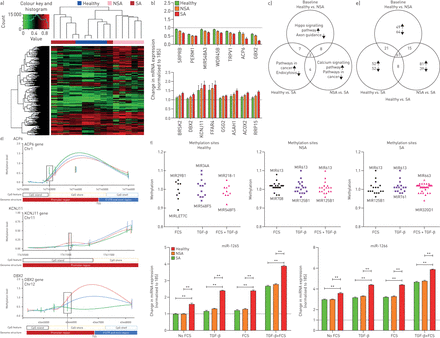
严重哮喘气道平滑肌细胞的DNA甲基化位点和miRNA调控。a)气道平滑肌整体甲基化模式的热图。12 383个差异甲基化DNA位点的非监督分层聚类。红色代表高甲基化,绿色代表低甲基化。b)通过逆转录酶PCR检测15个“枢纽”基因的RNA表达变化。c)差异甲基化位置(DMPs)相关基因的通路分析。d)通过加权基因共表达分析(WGCNA)和bumphunter分析,显示了三个枢纽dmp的基因组位置。的kcnj11.DMP位于CPG岛和推动者地区,而ACP6.和DBX2.同时位于CpG shore和启动子区域。e)维恩图,显示组间与基线相关的差异甲基化位点的比较。f)用胎牛血清(FCS)(2.5%)和转化生长因子(TGF)-β (1 ng·mL)刺激后健康、非严重哮喘(NSA)和严重哮喘(SA)气道平滑肌中差异表达的miRNAs位点的图示−1),均在甲基化水平和miRNA水平。
路径分析使用g:Profiler [7]表示,与健康受试者的DMP相关的基因与基线的NSA参与了细胞增殖和凋亡(河马信号通路)和轴突引导的调节,而SA和对照之间的差异与ASMC收缩(钙信号通路),增殖(癌症相关途径)和内吞作用相关联(图1 c).刺激健康受试者ASMCs激活的通路与在NSA和SA细胞中看到的通路相似(河马通路和内吞作用)。这表明,来自NSA和SA的ASMCs尽管在培养了几代后,仍保留着与细胞增殖和哮喘有关的表观遗传特征。刺激的NSA ASMCs增加了与抑制先天免疫反应(eb病毒感染)相关的dmp,而在SA细胞中,Notch信号通路被最显著激活。这一数据强调了先天免疫改变和Notch增殖信号在严重哮喘ASMCs中的重要性。
我们使用了不同的方法来检查严重程度相关的DMP的重要性,即加权基因共表达分析(WGCNA)[8]和Bumphunter分析[9].我们确定了19个模块中的五个与疾病严重程度有明显相关(图1 d).过滤这些表型相关的CPG位点的显着和连通性,得到15个表型DMP,其更加富集在基因组CPG岸边或立即侧翼的CPG岛中并确认了先前识别的重要性DBX2.,ACP6.和kcnj11.作为集线器DMPS。这些基因与改变的脂肪酸代谢和增殖有关(ACP6.)代谢综合征中的G蛋白偶联受体信号传导(kcnj11.)和神经元模式(DBX2.).
该分析还证实了先前报告的基线减少PDE4D(磷酸二酯酶4d)哮喘致哮喘的启动子区域,调节哮喘的Asmc增殖[10.].然而,当FCS/TGF-β刺激细胞时,这一效应被逆转,表明ASMC DNA甲基化状态在细胞激活时不稳定,从而导致功能后果。表型相关dmp的通路分析证实了Hippo信号传导、轴突引导和内吞通路的重要性,但也描述了包括内源性大麻素信号传导在内的新通路,这通常存在于大脑中[11.]并且在病毒诱导肿瘤[12.].进一步调查这些途径在SA中的作用。
DNA甲基化不仅调节基因表达,还可以调节miRNA。MiRNA的改变表达调节许多生理过程,包括炎症和重塑,并涉及哮喘[3.].我们检测了这里描述的dmp是否也可以控制miRNA的表达,特别是作为15个枢纽dmp中的一个与之相关mir-548a-3(图1 b).我们发现,如前所述的诸如逆转录酶(RT-)PCR的许多miRNA的表达改变了[3.,13.,14.])在基线和刺激之后,迄今为止在哮喘的ASMC中与DMPS与DMP相关联。观察到与miRNA基因座相关的113dMP比较健康受试者和NSA患者;104比较NSA和SA ASMC时比较健康受试者和SA样品和120时(图1 e).与最高和最低的甲基化CpGs相关的miRNAmir137.和mir372.分别在健康受试者的ASMC,mir548q.和MIR575国安局的样本,还有mir1265.和mir1266.在SA的ASMC中。mir137.,mir372.和MIR575据报道,曾经在ASMCS中表达过异常表达[13.]和哮喘肺活检[14.].然而,我们第一次证明mir-1265.和mir-1266.在SA ASMC中过度表达。
FCS/TGF-β刺激对SA细胞中DMPs的影响更大,健康ASMCs中10个miRNAs的DMPs显著改变,在NSA中18个miRNAs, SA ASMCs中50个miRNAs的DMPs以错误发现率(图1 f).分别在健康受试者ASMC中分别最高和最低甲基化的位置与MIR218-1和MIR548F5, 和mir613.和mir125b1.在NSA样品中,并与MIR663和mir320d1.(图1 f).利用RT-PCR,我们证实了与甲基化状态的增加或减少相关的成熟mirna表达的预期变化。表达量最高的miRNA为mir-320d-1,确认我们之前在两个ASMC的报告[13.]和哮喘肺活检[14.](图1 f).总之,我们的数据表明,来自SA患者的ASMC的增殖性/凋亡途径的调节是异常的,并且这可能是对具有多疑代谢过程的控制,特别是与脂肪酸代谢有关的患者。
总体而言,这里报告的DNA甲基化型材的〜80%重叠和来自健康受试者和NSA的基因表达谱,如前所发表的[5,13.,14.].这不仅证实了我们在mRNA水平上的重点分析,也表明了饮食和生活方式等已知因素会影响DNA甲基化状态[15.,不太可能在这里造成重大偏见。为了解决这些问题,需要进行更大规模的重点研究。
我们确认DNA甲基化的不同模式与哮喘有关本身还有疾病严重程度。这些甲基化反过来变化与可能影响ASMC功能的基因表达和miRNA表达的变化相关。实际上,我们描述了SA中ASMC功能障碍的新机制,并提供了描绘去甲基化试剂的潜在治疗作用的理由(即。佐剂治疗)。我们还突出了新型途径的潜在作用,例如Endannabinoid信号传导在SA中的ASMC功能中。因此,这项研究不仅扩展了我们对控制SA ASMC表型的调节机制的多层或综合性质的理解,但它应该刺激在SA中ASMC功能的功能调节的工作,具有更新的潜力更有效疗法旨在不仅缓解气道调增加,而且是严重哮喘的过度增殖和促炎疗效。
脚注
作者的贡献:m.m.Perry计划实验,培养了ASM细胞,分析了数据并准备了稿件;P.薰衣草ran ran甲基化阵列;C.H.S.Kuo分析了数据;F. Galea,C. Michaeloudes和J.M.Flanagan负责焦点训练;K.F.涌招募患者并进行支气管活检;I.M. Adcock资助了这项研究。毫米。 Perry, K.F. Chung and I.M. Adcock designed the study. Consent for publication: All authors have read the manuscript and consent to it being published. Availability of data and material: All data and material are included in the manuscript.
利益冲突:未申报。
支持声明:来自哮喘英国(08/041)和Wellcome Trust(085935)(K.F.Chung)的补助金支持这项工作。该项目是皇家Brompton和Harefield NHS基金会信托和伦敦帝国学院的NIHR呼吸疾病生物医学研究单位的支持。本出版物中表达的观点是作者的观点,不一定是NHS,国家卫生研究所或健康部的NHS。K.F.Chung是英国NIHR的高级调查员。I.M.Adcock和K.f.Eu-Innovative Medicines倡议联合开展项目U-Biopred(115010)支持涌。毫米。佩里,即adcock和K.f.Chung是一位环境景点的成员 - 比利时国家 - 比利时科学政策 - 项目P7 / 30。 Funding information for this article has been deposited with theCrossRef Resder注册表.
- 已收到2016年9月21日。
- 接受2018年2月8日。
- 版权所有©ers 2018
本ERJ开放文章在知识共享署名许可4.0条款下开放188滚球软件访问和发布。