摘要
成人新发哮喘的预后尚不清楚。横断面研究提示,这些患者可能在1 s内出现用力呼气量(FEV)加速下降1).然而,肺功能加速衰退的危险因素尚未确定。
我们旨在对200名新诊断为哮喘的成年人进行为期5年的前瞻性随访研究,以确定这些危险因素。在目前的研究中,每年对临床、功能和炎症参数进行评估,持续5年。线性混合效应模型用于识别预测因子。
可评估的141例患者肺功能集可用。支气管扩张剂后FEV的中位数(四分位范围)变化1−17.5(−54.2至+22.4)mL /年。FEV加速下降1由下降的较低四分位数(>54.2 mL /年)定义。鼻息肉、血液和痰中嗜酸性粒细胞数量、体重指数和呼出一氧化氮水平与肺功能下降呈单变量相关。只有后两者是独立相关的。使用临界值来确定最高风险的患者显示FEV加速下降1在所有合并呼出一氧化氮分数(F伊诺)≥57 ppb,体重指数(BMI)≤23 kg·m−2.
我们得出的结论是,伴有高水平的呼出一氧化氮和低BMI的新发哮喘的成年人有肺功能加速下降的风险。
摘要
呼出一氧化氮和BMI预测FEV加速下降1新发哮喘的成年人http://ow.ly/1yDz30hE5YE
简介
哮喘是一种异质性疾病,包括几种具有不同临床、炎症和功能特征的亚表型[1,2].发病年龄似乎是这些亚表型的一个重要的独特特征,因为研究表明,成人发病的哮喘患者在许多方面不同于儿童发病的哮喘患者[3.].由于成人发病哮喘占新诊断哮喘的50%以上[4,5这是一种重要的临床表型。成人发病哮喘与更多(持续性)嗜酸性气道炎症和更多慢性鼻窦疾病相关[6,7].横断面和纵向研究也表明,这些患者的FEV下降更快1[8,9].
吸烟已被证明是导致一般哮喘人群肺功能加速衰退的潜在因素[10],反复发作[11]和1 s内低基线用力呼气量(FEV1) [12].然而,炎症的严重程度也可能是诱导气道重塑的重要因素[13].
早期识别有肺功能加速下降危险的患者很重要,因为已知不可逆气流阻塞与发病率和死亡率增加有关[14,15].此外,确定危险因素的性质可以帮助确定最适合特定患者的预防性治疗。
在这项研究中,我们假设在诊断时可以识别患有成人发作哮喘的肺功能加速下降的风险。本研究的目的是确定加速FEV的临床、功能或炎症危险因素1在新诊断哮喘的成年人中进行的一项前瞻性5年研究。
方法
主题
总共有200名成年人被纳入ADONIS研究(成人发病哮喘和炎症亚表型),他们被前瞻性随访了5年。年龄在18-75岁之间的患者,如果他们最近(<12个月)被诊断为哮喘,则符合条件。哮喘诊断基于典型症状,至少200毫升,FEV改善12%1%预测值或存在气道高反应性[16].目前吸烟或吸烟史>10包年,如果没有气流阻塞(FEV1/用力肺活量(FVC) <0.7)和正常扩散能力(肺对一氧化碳的扩散能力,经血红蛋白和肺泡容积>80%校正)。排除儿童时期有哮喘或慢性呼吸道疾病史的患者。该研究已获得AMC医学伦理委员会的批准,并在荷兰试验登记册(NTR1846)注册。所有参与者提供书面知情同意书。
研究设计
研究设计包括5年内7次访问。在基线时,患者接受了临床、功能和炎症参数的综合评估。每年随访一次,6个月后再进行一次随访。在最后一次访视时,重新评估所有基线测量值。
研究测量
在基线时,收集了以下数据:人口统计数据;病史;药物使用;哮喘控制(哮喘控制问卷-6)[17];标准化支气管扩张剂前后肺活量测定法(FEV1及植被覆盖度)[18];气道高反应性,定义为使FEV下降20%所需的乙酰胆碱刺激浓度1(如果没有下降,浓度为32 mg·mL−1使用);特异反应,定义为IgE >0.35 kU·L−1至少一种常见航空过敏原(ImmunoCAP, ThermoScientific, Uppsala,瑞典);外周血细胞计数;呼出的一氧化氮分数(F伊诺) (NIOX系统,Aerocrine,瑞典)[19];根据国际标准进行的痰细胞鉴别[20.];鼻息肉,根据鼻内窥镜检查和/或鼻息肉切除术的患者的历史。在随后的随访中,药物使用参数、ACQ、哮喘生活质量问卷、加重(定义为前一随访期间口服皮质类固醇的疗程)、支气管扩张剂(pb)后FEV1,外周血细胞计数和F伊诺被评估。在最后一次就诊时,除特应性状态和存在鼻息肉外,重复所有基线评估。
加速下降的定义
年度pbFEV1以个体pbFEV回归线的斜率计算每位患者的下降1随时间的测量。年度pbFEV1在较低的四分位数(≤25百分位数)对每位患者的下降进行了二分。低于这个较低四分位数的值被定义为加速下降。
统计分析
仅参加基线随访且未进行随访的患者的数据被排除在外。纵向pbFEV的线性混合效应模型1使用随时间变化的值(mL /年)来确定年度pbFEV之间的关系1衰退和协变量。pbFEV变化1随时间(年)的变化被建模为线性函数。在线性混合效应模型中,将患者个体截距和随时间变化的斜率作为随机效应。在混合效应模型中,我们通过纳入预测因子的相互作用项与随访时间(年)来评估这些个体回归线的斜率在变量水平之间是否不同。
使用单变量混合模型为多变量混合模型(p<0.10)选择变量,其中包含连续或二分预测变量。在多变量连续和二分模型中采用逆向选择,所有模型都对基线pbFEV进行了调整1(表示为pbFEV1%的预测),包括这个变量作为主要影响。此后,随访期间的病情加重被添加到多变量模型中。
随后,基于混合效应模型的结果,采用加速pbFEV进行受试者工作特性分析1衰落是结果。我们将预测变量的截止值定义为每个预测变量的特异性为90%的阈值。
p值<0.05为有统计学意义。SPSS软件(版本23;IBM SPSS, Armonk, NY, USA)和Rstudio (Version 1.0.136;自由软件基金会,公司,波士顿,MA,美国)用于统计分析。
结果
在纳入研究的200名患者中,141名患者(71%)在5年内进行了重复肺功能测试。资料不完整的59例患者多为女性(71%)与50%;P <0.01),使用低剂量吸入糖皮质激素(250µg·d)−1与313µg·−1;P =0.02)优于数据集完整的患者(表E1).141例新发哮喘成人患者的基线特征见表1.从哮喘诊断到基线就诊的中位时间为2个月(四分位数范围1-5个月)。均值±sd随访时间4.6±1.4年,中位数5(5 - 6)次。中位恶化率为0(0 - 0.25)/年;68%的患者在随访期间没有报告任何加重,19%的患者仅经历了一次加重。pbFEV的中位数变化1−17.5 mL /年。下四分位数的极限为- 54.2 mL /年,上四分位数的极限为+22.4 mL /年。
肺功能加速衰退的预测因子
单变量线性混合效应分析显示,鼻息肉的存在,身体质量指数(BMI)较低,血液嗜酸性粒细胞数量较多,痰嗜酸性粒细胞百分比较高,血清嗜酸性粒细胞水平较高F伊诺与pbFEV的急剧下降显著相关1(表2,图1).男性也往往与pbFEV的急剧下降有关1, (p = 0.08)。其他变量与肺功能下降无关。
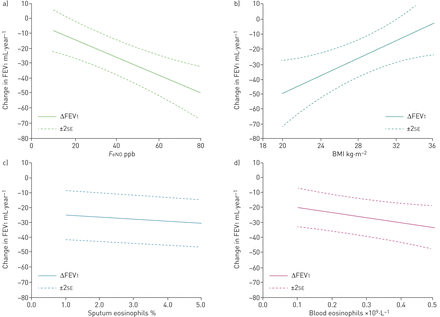
1 s用力呼气量(FEV)的单变量模型1)随着不同的生物标志物而下降。一)F伊诺(p < 0.001);b)体质指数(BMI) (p=0.011);C)痰中嗜酸性粒细胞(p=0.022);d)血液嗜酸性粒细胞(p=0.044)。实线:支气管扩张剂(pb)后FEV变化1(mL /年,每增加一个生物标志物);虚线:±2se.
当所有来自单变量分析的显著性(p<0.10)连续变量被放入逆向选择多变量模型时,仅较高F伊诺BMI降低与pbFEV下降显著相关1,每ppb每年为- 0.55 mL (p=0.001),每kg·m为2.20 mL−2每年(p=0.049)。将计算出的变量截点值放入逆向选择多变量模型中,F伊诺(≥57 ppb)和BMI(≤23.05 kg·m−2)与pbFEV变化显著相关1−37.9 mL /年(p=0.015)和−49.9 mL /年(p=0.003),表3).
的负预测值F伊诺≥57ppb或BMI≤23.05 kg·m−2的比例相当不错,分别为77%和79% (表4的阳性预测值F伊诺≥57 ppb或BMI≤23.05 kg·m−2比例较低,分别为45%和41%。然而,当F伊诺≥57 ppb, BMI≤23.05 kg·m−2两者联合,肺功能加速衰退的阳性预测值为100%。
当在连续模型中加入加重时,BMI和F伊诺仍与肺功能下降有关,但加重与肺功能下降之间似乎没有关联(p=0.253)。此外,在使用截止变量的模型中没有发现关联。
讨论
这项研究表明,在新发哮喘的成年患者中,发病率更高F伊诺水平和较低的BMI与FEV的快速下降独立相关1.当我们使用临界值来确定肺功能加速衰退风险最高的患者时,(定义为FEV下降的最低四分位数1)时,似乎所有患者合并F伊诺≥57 ppb, BMI≤23.05 kg·m−2显示加速下降。目前或曾经吸烟或气道高反应性对肺功能下降无影响。这些结果表明,在新发哮喘成人患者中,非肥胖且气道炎症相对严重的患者未来肺功能受损的风险最高。
这项前瞻性纵向研究特别关注成人新发哮喘的预后,特别强调临床、功能和炎症标志物的预测价值。另一项针对芬兰成人哮喘人群的研究报告称,吸烟史>10包年与FEV加速下降有关1[21],这没有得到我们数据的证实,可能是由于本研究中较少的包年数和很少的当前吸烟者,以及我们排除了特别容易受到吸烟影响的患者(即。FEV患者1/FVC <0.7或肺对一氧化碳扩散能力降低)。我们也不能证实气道高反应性增加或哮喘加重率是FEV加速下降的危险因素1,这在以前的几项研究中有所报道,但并非全部[11,21- - - - - -24].这些差异可能是由于研究人群的差异,即。我们研究中的成人哮喘人群与其他研究中的普通哮喘人群。这强调了在哮喘研究中考虑发病年龄的重要性[2].关于BMI,在一项研究中发现了与我们相似的结果,显示FEV更快1非肥胖患者与肥胖成人哮喘患者相比下降[25].值得注意的是,在普通人群中,却出现了相反的结果,发现高BMI与肺功能下降之间存在关联[26].高F伊诺在之前的研究中,长期成人哮喘患者的肺功能过度下降与该水平相关[27,28],我们的研究提供的证据表明,即使在疾病开始时也很高F伊诺该水平预示着前5年肺功能的严重丧失。
我们研究的优势在于关注相对暴露不足和研究不足的哮喘表型,研究的前瞻性设计,以及患者的广泛临床、功能和炎症特征。此外,由于每位患者的访视率相对较高(中位数:7次访视中有5次),以及随访研究的参与者比例较高,因此有可能进行可靠的统计分析。事实上,线性混合效应模型,其中所有可用的年度肺功能测量都被考虑在内,保证了FEV过程的真实和准确的表示1下降超过5年。
不幸的是,我们无法从所有患者中获得足够的痰细胞样本,这可能降低了该生物标志物作为预测指标的潜力。这与痰中嗜酸性粒细胞百分比在单变量分析中与肺功能下降相关,但在多变量分析中不相关的观察相吻合。这并不适用于嗜酸性粒细胞,这意味着,与嗜酸性粒细胞相比,F伊诺与肺功能下降的相关性更强。我们的研究没有包括一个对照组,这可以被视为一个限制。然而,关于健康志愿者(每年22毫升)和哮喘患者(每年38毫升)肺功能下降的可靠纵向数据是可用的[10].在本研究中,我们选择肺功能下降的较低四分位数来定义pbFEV的加速下降1(每年54.2毫升)。因此,这一定义似乎与临床相关。
我们如何解释两者之间的联系F伊诺肺功能加速衰退?一个明显的解释是,患有高水平F伊诺由于依从性差或治疗不足,没有使用足量的抗炎药物。吸入糖皮质激素已被证明会降低F伊诺值(29],并预防新诊断哮喘患者的肺功能随着时间的推移而恶化[30.].然而,当我们比较肺功能加速下降和没有加速下降的患者时,吸入糖皮质激素剂量、哮喘症状或气道高反应性方面没有差异,这意味着高F伊诺水平与哮喘控制较差或存在气道功能障碍无关,因此没有临床理由假设患者不坚持或需要增加哮喘治疗。另一种解释可能是F伊诺水平由鼻息肉引起[31].虽然鼻息肉病与肺功能丧失没有独立的联系,但这可能是因为有一半被诊断患有这种疾病的患者使用了局部皮质类固醇治疗。因此,我们不能完全排除鼻息肉与肺功能下降相关的可能性,这与观察到的鼻息肉是一种特定的严重成人发作哮喘表型的特征相吻合[32].事实上,高F伊诺这些患者的水平可能反映了一种导致肺功能丧失的“无声”机制。许多研究都表明这个数字很高F伊诺水平与嗜酸性气道炎症相关[33- - - - - -35],而普遍认为持续的气道炎症导致气道重塑是导致肺功能加速衰退的原因[13].值得注意的是,以主要嗜酸性气道炎症为特征的哮喘通常与成人发作的哮喘和低症状评分相关[1],这符合我们的概念F伊诺是该人群无症状气道炎症的标志。
基线时较低的BMI与FEV的加速下降独立相关1这是一个意外的发现,我们只能推测可能的机制。在以前的研究中,体重增加与肺功能下降之间的联系已经在哮喘患者[25]和一般人群[26,36].然而,这种关联在随访期间肥胖的患者中最为明显[36].在我们的研究中,BMI较低的患者并没有变胖;在5年的随访中,该组的平均BMI仅略高于基线。另一种可能性是,BMI非常低的患者由于缺乏锻炼而肌肉质量较低,或者患有与持续炎症相关的轻度消瘦综合征。这与我们观察到的低BMI和高BMI合并的患者相吻合F伊诺肺功能加速衰退的风险最大。最后,肥胖和非肥胖哮喘患者可能代表不同的哮喘表型,不仅在临床和炎症机制方面,而且在气道重塑和长期预后方面[37,38].最近的一项聚类分析也指向了这一方向,表明肥胖患者合并哮喘的肺功能下降程度低于瘦人患者[39].
我们的研究具有临床意义,因为它提供了一个新的和重要的作用F伊诺在日常实践中。我们的研究结果表明F伊诺是一种易于测量的、非侵入性的生物标志物,用于持续的嗜酸性气道炎症,即使在疾病得到控制而没有恶化的患者中也是如此。这也说明了高F伊诺哮喘诊断水平应被认真对待,特别是对于已经接受初始治疗的患者,因为它可能反映了长期持续或难治性炎症和肺功能丧失。F伊诺-指导治疗目前只提倡用于频繁哮喘加重的成人和儿童[40,41],但这一建议是基于没有考虑肺功能衰退速度的研究。因此,研究是否F伊诺引导治疗能否预防肺功能加速衰退应被列为重要研究议程。
总之,我们的研究表明F伊诺是近期诊断为哮喘的成人肺功能加速下降的预后生物标志物。特别是非肥胖患者高F伊诺水平似乎是最危险的。高F伊诺该水平可能代表难治性嗜酸性粒细胞性气道炎症导致气道重塑,即使在控制哮喘的患者中也是如此。F伊诺可能成为临床医生在日常实践中指导哮喘治疗的重要生物标志物。
补充材料
披露的信息
确认
我们要感谢所有参与ADONIS研究的患者。我们感谢收集数据的医科学生,感谢协助进行所有测量的所有肺功能和实验室技术人员。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究由葛兰素史克(SAS117256)资助。本文的资助信息已存入交叉参考基金注册.
临床试验:本研究注册于www.trialregister.nl编号为NTR1846。
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2017年8月31日。
- 接受2017年11月23日。
- 版权所有©ERS 2018















