摘要
慢性但不间歇性铜绿假单胞菌感染导致囊性纤维化肺菌群失调http:///wly/cdko30eonx5
编辑器:
慢性肺部感染铜绿假单胞菌触发慢性气道炎症和结构肺损伤仍然是囊性纤维化患者发病率和死亡率的关键危险因素(CF)[1]。以前,基于培养的诊断方法认为纤维化患者的气道感染是单病原性的,但最近采用非培养方法的方法表明,纤维化肺的细菌感染涉及一个多菌群[2- - - - - -4]。典型CF病原体的慢性感染如铜绿假单胞菌与肺功能下降相关,并与肺部微生物群的多样性的降低相关。然而,病原体和微生物群之间的相互作用仍然难以理解,并且已经假设微生物群的消化不良可能预先存在并促进病原体的生长铜绿假单胞菌在CF肺中。目前的研究的目的是评估影响的影响铜绿假单胞菌肺纤维化菌群生态失调的感染。
本研究获得了海德堡大学伦理委员会的批准,并获得了研究对象的知情书面同意。在每季度例行门诊就诊(n=336)和住院(n=56)期间采集CF患者的气道样本。CF的诊断依据已制定的标准[5和感染铜绿假单胞菌如前所述,分为负性、间歇性或慢性[6]。71例年龄较大的CF患者共392份痰标本(平均值±)sd年龄21±11岁,范围3-70岁,病情严重程度(平均±)sd1 s内用力呼气容积(FEV)1)在各个阶段分析55.7±24.9%,包括来自50个受试者的纵向样品,包括纵向样品。铜绿假单胞菌感染;纳入154例阴性、88例间断性和150例慢性感染样本。此外,对71例CF患者(268例为阴性,77例为间歇性感染,63例为慢性感染)的408例咽喉拭子进行了分析。提取DNA, 16S rRNA V4区扩增,测序,计算统计分析,如前所述[7]。
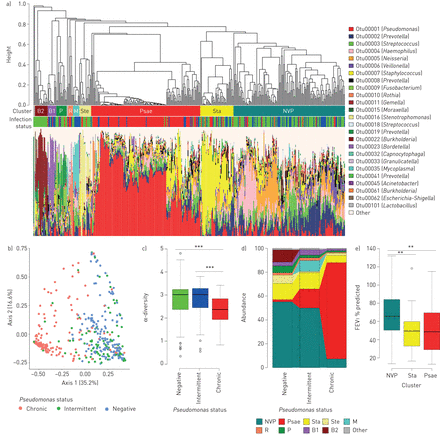
慢性病人的痰样本铜绿假单胞菌在主坐标分析中,感染(Psa慢性)与未感染(Psa阴性)组和间歇感染(Psa间歇)组不同(图1一个b) PERMANOVA显示,只有Psa慢性组与其他两组有显著差异(p<0.01)。Psa慢性痰标本的多样性显著降低(p<0.01) (图1 c),比Psa阴性组和Psa间歇吐痰组更显著(p<0.01),细菌总生物量比Psa阴性组增加(p<0.05)。分层聚类显示12个聚类最有效地模拟了人口(图1一个)。大部分PSA慢性样品(80.0%)在一个聚类中发现,其特征在于高丰度铜绿假单胞菌(簇PSAE)。鉴定了另外两种主要集群,其特征在于高度丰富奈梅里亚,韦永氏球菌属和普氏菌(簇NVP),口咽部的已知共生体,或支配葡萄球菌集群(Sta)。其他少数聚集的特征是其他经典呼吸道病原体的优势,包括Stenotrophomonas(Ste),洋葱(B2),支原体(m),Bordetella.(B1)或上呼吸道的共生体(普氏菌(P),罗思氏菌属(R))。总的来说,54.5%的Psa阴性样本和51.1%的Psa间歇样本聚集在NVP簇中(图1 d)。采用多因素分析(包括年龄、性别和加重状态)对三个主要组(NVP、Psae和Sta)进行FEV比较1% pred和体质指数(BMI)之间的标准差评分。在患者的痰中有微生物群聚假单胞菌和葡萄球菌组,FEV1与携带以nvp为主微生物组的患者相比,% pred显著降低(p<0.01) (图1 e)。此外,包括所有有肺功能评价的样本(68例患者292例),FEV呈负相关1占优势关系的%(这是最丰富的运作分类单位(OTU)的相对丰富(伯格 - 帕克指数[8]),r2= -0.26,p <0.001)和与α-多样性的正相关性(非参数香农指数考虑到OTU的数量和丰度分布[9), R2可以显示= 0.33,P <0.001)。来自三种不同簇的CF患者之间的BMI没有显着差异。在喉咙中,对微生物组的没有变化被观察到假单胞菌感染状态。
囊性纤维化患者痰菌群的聚集。a)簇以颜色表示,并以树状图表示的莫里西塔-角距离为基础。底部为25个最丰富otu的相对丰度的叠加条形图。集群以最丰富的属命名:NVP:奈梅里亚/韦永氏球菌属/普氏菌,sta:葡萄球菌Psae:假单胞菌Ste:Stenotrophomonas,m:支原体R:罗思氏菌属P:普氏菌,B1:Bordetella.B2:洋葱。感染状态铜绿假单胞菌由颜色表示:绿色负,蓝色和慢性的间歇性。b)主要坐标分析,代表患者的样品与患者的莫里锡角距离铜绿假单胞菌感染(阴性)和患者间歇和慢性铜绿假单胞菌感染。c)与感染状态相关的α-多样性铜绿假单胞菌由非参数化Shannon指数评估。d)每个感染状态(负,间歇性和慢性)的每个簇属于每簇的样品的百分比。e)1 S强迫呼气量(FEV1) NVP、Sta和Psae三组患者的预测。统计分析采用多变量分析(包括年龄、性别和恶化状态)。* *: p < 0.01;* * *: p < 0.001。
我们的研究表明,慢性但不间歇性感染铜绿假单胞菌与纤维化患者肺部生态失调有关。慢性铜绿假单胞菌感染后,菌群的多样性在全球范围内呈下降趋势普氏菌,奈梅里亚和韦永氏球菌属。这些属是ecotype NVP(各自线性鉴别分析(LDA)-score: 3.92, 4.65, 4.30)的主要组成部分,这是一种高度多样化的微生物群,与本研究中观察到的咽喉微生物群密切相关(数据未显示),在健康人群中也是如此[10.]。这一结果与目前的理论一致,即肺菌群是口咽菌群平衡迁移/清除的结果[11.]。尽管有报道认为该菌群在CF中具有促进疾病的作用,但也有报道认为这些共生体反映了正常的肺微生物群,甚至可能通过与CF病原体的生态竞争而获益[3.,10.,12.,13.]。这种生态型主要在缺乏或间歇性感染的患者中发现铜绿假单胞菌。间歇性感染可以被解释为第一次遭遇或新的重新感染铜绿假单胞菌根据我们的数据,这并不伴随着CF肺中潜在的微生物群的改变。这些发现与一个模型是一致的殖民与铜绿假单胞菌是导致纤维化患者肺部微生物异常发展的主要驱动因素,这种异常与疾病严重程度的增加有关[1,14.]。患者间歇铜绿假单胞菌感染并没有在肺菌群中显示出主要的改变,反驳了微生物群的改变是肺感染的前兆的假设假单胞菌感染。这一系列的变化突出了及早发现和消除铜绿假单胞菌可能限制甚至阻止严重的生态失调的进展,从而在CF肺中建立促进疾病的微生物组。
与观察到的变化相似铜绿假单胞菌,其他属的优势聚类包括葡萄球菌,寡养单胞菌,伯克霍尔德氏菌,支原体和Bordetella.还与肺部微生物组的多样性和增加的优势增加有关。值得注意的是,如前一项研究所述,优势与肺功能呈负相关[3.,15.]。此外,FEV1% pred在以。为主的患者中显著降低假单胞菌和葡萄球菌感染比来自NVP集群的感染。这些数据表明,一种物种的主导地位改造了肺部微生物群,可以促进CF肺病的严重程度,而高度多样化的NVP群可能是保护性的,并且可以与更好的结果相关。
我们研究的一个局限性是16S扩增子测序不能识别导致慢性感染的机制铜绿假单胞菌或在我们的聚类分析中鉴定的其他病原体,以及CF肺中的诱导功能性。将需要进行分析分析偏心组织和转录组织的研究,以更好地了解这些改变的潜在机制。我们的集群分析可以帮助选择定义的样本以获得这种方法。
总之,本研究表明间歇性铜绿假单胞菌慢性纤维化肺疾病和慢性阻塞性肺疾病均有感染,但无生态失调铜绿假单胞菌感染触发肺中的消化不良。因此,我们假设早期根除铜绿假单胞菌间歇期可保留更多样化和有益的肺微生物群,从而有助于CF患者的临床获益。
披露的信息
补充材料
美国BoutinERJ-01086-2017_boutin.
A.H. Dalpkeerj - 01086 - 2017 - _dalpke
如。Dittrich.erj - 01086 - 2017 - _dittrich
确认
我们感谢Jessica Panitz, Selina Hassel, David Ibbersson和Bioquant的技术团队对我们的卓越技术支持。我们也感谢Iris Kuhbandner的病人招募和样本收集。作者贡献:本研究的构思与设计:S. Boutin, S. y . Graeber, M. Stahl, A.S. Dittrich, M.A. Mall, A.H. Dalpke;数据的获取、分析和解释:S. Boutin, S. y . Graeber, M. Stahl, A.S. Dittrich, M.A. Mall, A.H. Dalpke;为重要的知识内容起草或批判性地修改文章:S. Boutin, S. y . Graeber, M. Stahl, A.S. Dittrich, M.A. Mall, A.H. Dalpke。
脚注
支持声明:本研究部分得到了德国教育和研究部(82DZL00401, 82DZL004A1)和欧盟委员会(第七框架计划项目编号603038,CFMatters)的支持。迪特里奇获得HRCMM(海德堡分子医学研究中心)职业发展奖学金。本文的资金信息已存入Crossref资助者注册表。
利益冲突:披露可以在这篇文章旁边找到www.qdcxjkg.com
- 收到2017年3月14日。
- 接受2017年7月4日。
- 版权所有©2017