抽象的
在COVID-19肺炎中,双能量计算机断层扫描显示了两种疾病过程中的肺灌注模式:灌注血容量(PBV)增加伴毛玻璃影和PBV减少伴实变https://bit.ly/2zh0xci.
给编辑:
血管受累2019年(Covid-19)已经提出了几种观察结果,例如肺栓塞的高率[1]、血栓前状态和促炎生物学特性[2,3.],以及严重内皮损伤和弥漫性血栓形成的病理结果[4].双能量计算机断层扫描(DECT)可以对碘造影剂在肺内的分布进行特定成像,这已被证明是肺灌注的替代标记[5,6].因此,我们的目标是评估体内采用DECT检测COVID-19肺炎患者肺部微血管病变情况,并确定疾病过程中血管变化是否变化。
这项单中心研究由我们的制度伦理委员会批准。我们对住院患者进行了对Covid-19肺炎的患者进行了回顾性分析(通过RT-PCR为严重的急性呼吸综合征冠状病毒2),他接受了增强的DECT,用于寻找肺栓塞的症状和/或低血量症的临床恶化。
肺部计算机断层扫描(CT)血管造影数据在双层DE CT系统(iQon®;(飞利浦医疗保健公司)使用大剂量跟踪技术,在肺动脉主动脉的阈值为110 HU,可进行碘图像重建,并由一名资深放射科医生和一名资深肺科医生进行评估。主要的肺病变如毛玻璃影(GGO)和肺泡实变,以及每叶的容积扩张(0:无;1: 0 - 25%;2: 26 - 50%;3: 51 - 75%;4:76 - 100%)。与远端实质相比,每叶灌注血容量(PBV)的增加或减少是评价灌注异常的存在和方面。大叶PBV与肺动脉干碘浓度相关,通过计算肺叶平均碘浓度与肺动脉干平均碘浓度的比值。由于肺灌注可能与注射时间有关,记录左心房上肺动脉主动脉内碘浓度的比值,并以中位数(四分位数范围)表示。
使用D'Agostino-Pearson测试测试PBV分布的正常性。未配对的T检验用于PBV在具有主要GGO和固结的裂片之间的PBV比较。使用多元线性回归用于将幼瓣PBV与延伸的函数进行比较。统计显着性设定为P <0.05。
2020年3月15日至4月30日共纳入5例患者。患者均为男性,年龄45-88岁,中位年龄70岁。无慢性呼吸道疾病史。3例患者(60%)入院,1例患者(20%)死于急性呼吸衰竭。在DECT成像时,4例患者(80%)进行了氧补充治疗(室内空气氧饱和度<90%),2例患者(40%)进行了预防性抗凝治疗,而其余3例患者(60%)进行了长期抗凝治疗。没有患者有细菌感染的迹象。d -二聚体水平为3107±3053 μg·L−1,纤维蛋白原6.5±1.6 g·L−1, c反应蛋白水平为93±45 mg·L−1血小板计数为390 000±234 000毫米−3.
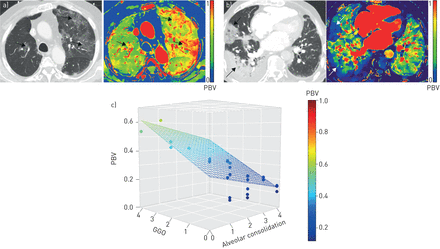
在两名患者(第7天和第8天)的症状发作期间,在三名患者(第17天和第18天)后,在第一周进行DECT。没有病人有肺栓塞。临床期患者患有主要的GGO病变(图1一个),而临床晚期患者以巩固为主(图1 b).肺动脉主动脉与左心房碘浓度的中位数比值为1.4(1.3-3.1)。各叶灌注异常,与相应的实质病变相匹配。均值±SD.以GGO为主的肺叶PBV为0.48±0.09,以实变为主的肺叶PBV为0.22±0.08 (p<0.0001)。病灶周围及正常实质区均未见灌注异常。多元线性回归分析显示PBV与实质病变显著相关(R=0.84, p<0.0001), PBV与GGO呈正相关(Pearson's R= 0.83), PBV与实变负相关(Pearson's R=−0.51)(图1 c).
微血管血管疾病微血管疾病的关键成像特征2019(Covid-19)使用肺血管造影双能计算断层扫描。灌注血容量(PBV)定义为主要肺动脉肺叶中碘浓度与碘浓度的比例。a)早期临床相的代表性成像特征:PBV增加(黑色箭头,右图),与地面玻璃透射件(GGO)(黑色箭头,左面板)相匹配,相对于没有GGO的区域。b)晚期临床阶段的代表性成像特征:看到PBV(白色箭头,右图),与肺泡整合(黑色箭头,左面板)相对于未经整合的区域匹配。c)Lobar PBV的三维图作为GGO和肺泡固结的存在和延伸的函数。每个点对应于叶片,其坐标由PBV表示z-轴,GGO扩展中x-轴和固结延伸在y-AXIS(体积扩展分数,0:无; 1:0-25%; 2:26-50%; 3:51-75%; 4:76-100%)。颜色网格代表多个线性回归平面。
该试点研究表明,DECT可用于评估肺血管受累体内在Covid-19肺炎患者中。观察到两种不同的肺灌注模式。
在患有症状发作以来的第一周发生的早期临床阶段,主要的实质病变是弥漫性双侧GGO,并且与相应的叶片中的肺灌注增加相关。该观察结果表明,这些患者的低血量症可能是由于通风/灌注失配导致肺分流。我们推测,低通风/灌注比率可能与病毒性肺炎的通气减少有关,以及正常或增加的灌注,这可能是由于炎症细胞因子引发的生理缺氧血管收缩。这些血管变化可以对应于近期尸检研究中发现的肠套血管生成的组织病理学发现[4].
在疾病的后期,发生在2周后,主要实质病变为双侧肺泡实变,并与受累叶肺灌注减少相关。在未检测到肺栓塞的情况下出现肺灌注不足是COVID-19的一个显著特征,可能是由于内皮功能障碍和血栓前细胞因子的释放,通常被称为“细胞因子风暴”,可能导致急性呼吸窘迫综合征。这些血管变化被病理结果证实为内皮功能障碍、影响小血管的弥漫性凝血病变和微血栓的形成[4].所有患者均有增加的炎症和癌细胞生物标志物。虽然抗凝治疗,但仍然存在下低血灌病的病变也是值得注意的。注意,先前已经报道了使用DECT的Covid-19肺炎的肺血管表现的描述[7,8].影像学表现为镶嵌型灌注,肺内外血管增大,周围灌注缺损伴周围灌注增加晕[7,8].这些结果在一定程度上与我们的研究结果一致。然而,我们的研究为疾病过程中肺灌注的时间变化以及与实质CT特征的关系提供了新的见解[9,10.].
我们的研究有一些局限性,包括患者数量少和回顾性设计。尽管DECT扫描主要表现为肺动脉混浊,但仍不能排除肺炎区域可能存在全身动脉供血。没有在同一患者中进行序贯DECT研究。然而,CT扫描是为了现实生活中的临床目的而进行的,考虑到肾脏和辐射的风险。
总之,DECT成像显示COVID-19肺炎中肺部微血管受累有两种不同的模式。它可能被用来更好地了解COVID-19的病理生理学和预示治疗试验的新目标。
可共享的PDF
致谢
我们感谢Valerie Leitman(里昂大学)对手稿编辑的贡献,以及Adeline Mansuy(里昂市民临终关怀院)提交的研究提案。
脚注
兴趣冲突:S. Si-Mohamed报告来自Boehringer Ingelheim的顾问的个人费用和非财政支持在提交的工作之外的Guerbet出席Guerbet。
利益冲突:N. Chebib报告了来自CSL Behring、Actelion、GSK、勃林格殷格翰、罗氏和MSD的非财务支持,除了提交的工作外。
利益冲突:M. Sigovan没有什么可披露的。
利益冲突:L. Zumbihl没有披露。
利益冲突:S. Turquier没有什么可透露的。
利益冲突:S. Boccalini没有什么可披露的。
利益冲突:布塞尔没有什么可透露的。
利益冲突:J-F。Mornex报告CSL Behring和LFB,个人费用和非财政支持的赠款,个人费用和非财政支持,从CORCHE,Boehringer Ingelheim,GSK,Novartis,Chiesi和Elivie提供的个人费用,在提交的工作之外。
利益冲突:V. Cottin报告了咨询委员会工作和讲座的个人费用,Actelion对出席会议的非财政支持,拨款,咨询和讲座的个人费用,以及勃林格殷格翰(Boehringer Ingelheim)对出席会议的非财政支持,拜耳/MSD和加拉帕戈斯咨询委员会和数据监测委员会工作的个人费用,诺华咨询委员会工作和讲座的个人费用,数据监测和指导委员会工作、咨询和讲座的个人费用,以及罗氏/Promedior出席会议的非金融支持,赛诺菲(Sanofi)和阿斯利康(AstraZeneca)演讲的个人费用、Celgene和Galecto数据监测委员会工作的个人费用、盐野义(Shionogi)咨询委员会工作的个人费用、纤维原(Fibrogen)指导委员会工作的个人费用。
利益冲突:P.杜克没有什么可透露的。
- 收到了2020年7月2日。
- 接受2020年9月2日。
- 版权所有©ers 2020。
本版本在知识共享署名非商业性许可4.0条款下发布。