文摘
肺大细胞神经内分泌癌(LCNEC)是罕见的。小细胞肺癌化疗的转移LCNEC范围从(SCLC)方法nonsmall细胞肺癌(NSCLC)化疗方案。我们分析的结果为LCNEC化疗。
荷兰癌症登记处和荷兰病理学注册(PALGA)寻找四期患者放疗LCNEC (2003 - 2012)。207名患者,病理组织学的幻灯片是用于小组审查。一线以铂为基础的联合化疗是集群“NSCLC-t”,包括吉西他滨、多西他赛,紫杉醇或vinorelbine;“NSCLC-pt”,培美曲塞治疗;和“SCLC-t”,依托泊苷组成的化疗。
小组检查诊断LCNEC成立于128年的207例。NSCLC-t化疗在46% (n = 60)管理,NSCLC-pt 16% (n=20)和SCLC-t 38% (n=48)的患者。中位数(95% CI)总体生存NSCLC-t化疗为8.5(7.0 - -9.9)个月,明显长于NSCLC-pt,患者平均生存5.9(5.0 - -6.9)个月(危险比为2.51,95%可信区间1.39 - -4.52;SCLC-t患者p = 0.002)和化疗,生存中值为6.7(5.0 - -8.5)月(危险比为1.66,95%可信区间1.08 - -2.56;p = 0.020)。
患者LCNEC, NSCLC-t化疗导致更长的NSCLC-pt相比总体存活率和SCLC-t化疗。
文摘
治疗肺LCNEC讨论;我们为标准吉西他滨NSCLC化疗结果有利http://ow.ly/2Xt730a0PK0
介绍
肺大细胞神经内分泌癌(LCNEC)是一个肺癌亚型与神经内分泌形态、免疫组织化学神经内分泌分化,有丝分裂率高(> 10有丝分裂·2毫米−2)和nonsmall细胞的细胞学特征1]。LCNEC很少见,占∼3%的肺癌,但肺癌诊断的比例LCNEC似乎增加(2]。因为LCNEC重叠的组织学特性与nonsmall细胞肺癌小细胞肺癌(NSCLC)和偶尔(SCLC),组织学诊断是很困难的(3,4]。
诊断LCNEC因为困难及其罕见,最佳的全身治疗尚未充分建立(5]。在当前欧洲社会医学肿瘤学非小细胞肺癌指南,没有特定的治疗LCNEC描述(6]。在美国临床肿瘤学会(ASCO)准则,platinum-etoposide化疗治疗(SCLC类型)或同一方案nonsmall细胞nonsquamous癌(非小细胞肺癌类型)是LCNEC建议。然而,SCLC-type化疗是被专家意见认为是最合适的7]。
一些观测表明LCNEC应该最好应对SCLC-type治疗。例如,最近的研究表明,基因组的LCNEC对应与SCLC (8,9]。此外,我们报道的预后和转移模式诊断LCNEC明显与SCLC (2,10]。然而,重要的差异响应SCLC-type化疗治疗LCNEC和SCLC(已报告5]。两个单臂LCNEC二期试验(n=29日和n = 30)显示客观反应率(ORR)依托泊苷或伊立替康联合顺铂(从31%到47%不等11,12),大大低于SCLC III期试验评估etoposide-cisplatinum化疗(奥尔≈66%)(13]。因为报告更高的阻力在LCNEC SCLC-type化疗,一些临床医生倾向于NSCLC-type化疗治疗。
因为这些感知差异,我们调查了患者的化疗治疗转移性LCNEC从2003年到2012年在荷兰。此外,我们回顾相关的整体生存和无进展生存(PFS)和化疗患者类型LCNEC panel-reviewed组织学诊断。
材料和方法
数据源和道德规则
数据检索来自荷兰癌症登记处和荷兰病理学注册(PALGA,全国注册表病理学在荷兰的14])。执行的研究是根据癌症登记处和病理学注册指南和国家隐私法规和医学伦理委员会批准的马斯特里赫特大学医学中心(METC azM / 14-4-043, 2014年11月20日)。
病人的选择
所有患者诊断为四期LCNEC记录在癌症登记处或病理学注册中心之间的1月1日,2003年和2012年12月31日被包括在内。从癌症登记处选择LCNEC国际疾病分类肿瘤第3版代码M8013使用。之前我们已经观察到一个广泛的诊断术语是用来描述LCNEC [15]。确定另外LCNEC例癌症登记处,被诊断出患有替代术语,额外的诊断代码M8246(神经内分泌癌)和M8574与神经内分泌分化(NSCLC)都包括在内。数字病理报告的摘要从病理学注册中心检索筛选诊断LCNEC,正如前面报道(15]。病人诊断为转移性LCNEC,包括肿瘤患者诊断为命名可能指LCNEC,接受化疗治疗从国家数据库,检索被包括在内。数据类型的化疗治疗回顾性更新在2015年由合格的癌症登记数据管理员。化疗患者被排除在外,如果细节是不可用的。
首先,我们分析了所选择的类型的化疗病人研究小组(目标1)。然后,我们对所有病人进行病理学检查。基于细胞学诊断患者和患者来说,最初的组织病理学幻灯片不能检索被排除在外。患者的总体生存和确定PFS的panel-confirmed诊断LCNEC(目标2)。
数据收集
收集的数据包括阶段(肿瘤、节点和转移(TNM)阶段6或7)和时间从诊断到死亡或后续审查了36个月的总生存期。PFS是计算从诊断日期直到第一次进展的证据,死亡或后续的最后一天。治疗亚型数据包括化疗,化疗周期数和二线治疗。一线化疗是集群分成三组,如下所示。1)“非小细胞肺癌化疗类型”(NSCLC-t),由吉西他滨、多西他赛,紫杉醇或vinorelbine;2)“培美曲塞NSCLC类型”(NSCLC-pt),培美曲塞治疗;和3)“SCLC类型”(SCLC-t),依托泊苷组成的化疗。铂组件都是顺铂或卡铂。在诊断转移性网站从记录的临床数据检索(cTNM)。病理数据包括病理历史,病理标本类型和诊断根据数字病理报告总结。
病理学修订
收集肿瘤组织学幻灯片,包括至少一个免疫组织化学(包含IHC)神经内分泌染色(CD56 / NCAM chromogranin-A或synaptophysin)和苏木精和伊红染色。审查是由三个病理学家(e . Thunnissen r . van Sulyen和m .)他窝,他们盲目的临床结果和最初的诊断。包含IHC染色模式神经内分泌标记、细胞角蛋白、TTF1和p63和ki - 67(如果可用)被j . Derks评估之前,r . van Sulyen中央审查会议。评估人员评估苏木精和伊红在多线程显微镜幻灯片;提供了信息包含IHC表达模式(j . Derks)。LCNEC成立至少两个病理学家同意诊断时,称为panel-consensus LCNEC。世界卫生组织(世卫组织)2015年所有panel-consensus建立诊断标准进行评估。额外的病理学检查的详细信息可以在网上找到补充病理数据文件。
统计分析
卡方和费舍尔准确测试是用于比较分类数据。连续变量进行了测试使用Mann-Whitney u测验和中位数和四分位范围(差)报道。总体生存和PFS审查在截止日期(2014年2月1日)。总生存期估计根据使用生存率较kaplan meier和测试方法。多变量Cox回归分析进行了协变量包括重要的单变量分析。非线性被log - log块视觉评估。双面的假定值< 0.05被认为是重要的。使用SPSS分析(Windows版本22;美国芝加哥,IL)。
结果
以人群为基础的化疗治疗随着时间的变化
数据从癌症登记处1627名患者和1172名患者的病理注册中心检索。355名患者接受化疗了四期疾病。排除患者来说,细节的化疗治疗不能检索,化疗治疗分析294例(图1)。检索的完整概述诊断和化疗治疗提出了在线补充表S1。LCNEC NSCLC-t化疗治疗显著降低随着时间从59%(2003 - 2009)到31% (2010 - 2012)(p<0.001);NSCLC-pt化疗类型从10%上升到16% (p = 0.29);和SCLC类型从31%上升到53% (p = 0.002)。
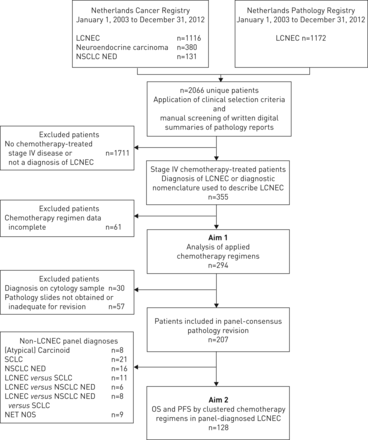
配偶(合并报告的标准试验)图显示的病人和病理学检查执行。LCNEC:大细胞神经内分泌癌;非小细胞肺癌NED: nonsmall细胞与免疫组织化学神经内分泌分化肺癌;SCLC:小细胞肺癌;净:神经内分泌肿瘤不是另有规定;操作系统:总体存活率;PFS:无进展生存。
Panel-consensus诊断LCNEC
组织病理学幻灯片从207名患者被检索。128年病人LCNEC诊断的共识,2015年与108例会议所需的所有标准(在线补充表S2) [16]。患者panel-confirmed LCNEC诊断(n = 128)的平均年龄65(56 - 71)年,59%是男性,67%是由(核心)穿刺活检标本(诊断表1)。在肝脏转移(53%)、骨(27%)和nonmediastinal淋巴结(22%)是最常见的。转移仅限于单个器官中48%的病人。至少四个化疗周期(中值(差)4(2 - 4))在62%的病人管理。二线化疗在23%的病人管理。超过三个转移患者在不同器官更频繁收到SCLC-t化疗。总的来说,NSCLC-t化疗在46%的病人管理,主要platinum-gemcitabine NSCLC-t病人(76%)。NSCLC-pt和SCLC-t化疗在16%和38%的患者管理,分别。panel-consensus LCNEC诊断病人的特点完成所有必需的标准并没有不同,描述在网上补充表S3。
总体生存panel-consensus诊断LCNEC集群通过化疗
3例患者在随访期间死亡。中位数(95% CI)总生存期是7.3个月(6.3 - -8.2个月)。NSCLC-t化疗患者的中位总生存期8.5个月(7.0 - -9.9个月),这是大大超过NSCLC-pt化疗患者(5.9个月,5.0 - -6.9个月;p = 0.011),并显著长于SCLC-t化疗患者(6.7个月,5.0 - -8.5个月;p = 0.012) (图2一个)。协变量的多变量分析,包括重要,单变量分析(性别、年龄、肝转移和转移的器官在诊断)(在线补充图S2),结果仍显著NSCLC-t与NSCLC-pt治疗(危害比(人力资源)2.51,95%可信区间1.39 - -4.52;p = 0.002), NSCLC-t与SCLC-t治疗(1.66,1.08 - -2.56;p = 0.020) (图3)。Cisplatinum与carboplatinum化合物没有显著影响治疗结果数据(在线补充图S3)。相应结果LCNEC患者总生存期和PFS 108年确诊的肿瘤样本中所有2015标准在网上补充描述数据S3, S4和S5。
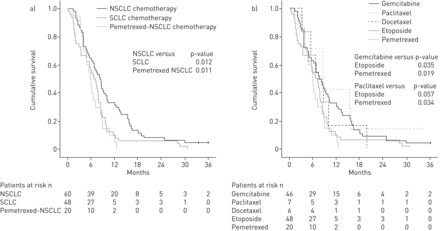
总体生存panel-consensus诊断大细胞神经内分泌癌患者相比)化疗集群和b)亚型的化疗(vinorelbine除外)。n = 128。非小细胞肺癌:nonsmall细胞肺癌疗法;SCLC:小细胞肺癌疗法。
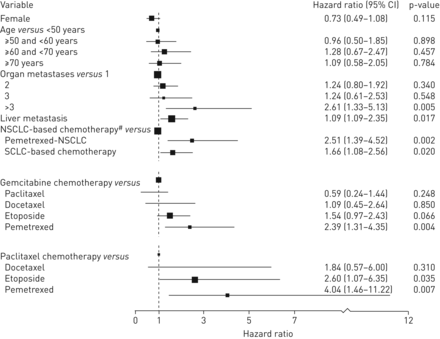
提出了三种多元模型用于集群化疗,platinum-gemcitabine和platinum-paclitaxel panel-consensus大细胞神经内分泌癌的化疗。n = 128。非小细胞肺癌:nonsmall细胞肺癌;SCLC:小细胞肺癌。#:排除vinorelbine。
总体生存panel-consensus LCNEC根据化疗亚型
platinum-gemcitabine化疗患者的中位总生存期(95% CI) 7.8个月(5.9 - -9.6个月),这是大大超过platinum-pemetrexed(5.9个月,5.0 - -6.9个月;platinum-etoposide化疗p = 0.019)和(6.7个月,5.0 - -8.5个月;p = 0.035) (图2 b)。在多元分析总体存活率为吉西他滨化疗优于培美曲塞(HR 2.39, 95%可信区间1.31 - -4.35;观察p = 0.004)和一个强大的趋势相比,依托泊苷(1.54,0.97 - -2.43;p = 0.066) (图3)。Paclitaxel-treated患者的中位总生存期为8.7个月(95% CI 2.7 - -14.7个月),大大超过对培美曲塞化疗(p = 0.034),和一个强大的趋势观察依托泊苷化疗(p = 0.057) (图2 b)。在多变量分析紫杉醇化疗显示总体存活率优于培美曲塞(HR 4.04, 95%可信区间1.46 - -11.22;p = 0.007)和依托泊苷化疗治疗(HR 2.60, 95%可信区间1.07 - -6.35;p = 0.035) (图3)。
在panel-consensus PFS LCNEC根据化疗亚型
在119名患者PFS的数据是可用的;除了一名患者在研究期间进展或死亡。PFS (95% CI)中值为4.7个月(4.2 - -5.3个月)。只有NSCLC-pt化疗治疗病人显著恶化PFS(4.1个月,3.8 - -4.5个月;p = 0.040)相比NSCLC-pt化疗患者(图4一)。吉西他滨化疗患者有显著延长PFS 5.2个月(4.1 - -6.2个月)NSCLC-pt化疗患者相比(p = 0.034) (图4 b)。所有其他比较特定亚型的PFS的化疗没有显著差异。
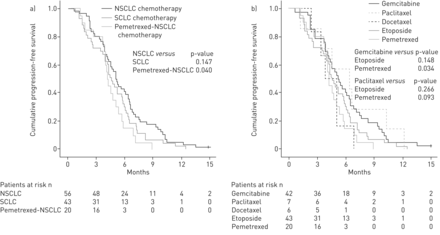
无进展生存相比)化疗集群和b)亚型的化疗(不含vinorelbine)在panel-consensus大细胞神经内分泌癌。n = 119。非小细胞肺癌:nonsmall细胞肺癌化疗方案;SCLC:小细胞肺癌化疗方案。
讨论
双重联合化疗的患者转移LCNEC生存和最佳的化疗治疗不佳LCNEC仍未查明的。这里我们NSCLC-t化疗,患者报告,主要是吉西他滨,有优越的患者总生存期与NSCLC-pt化疗。此外,NSCLC-t的组合方案,排除那些包含培美曲塞显示优越的生存与依托泊苷(SCLC-t)化疗。这些结果与ASCO的建议治疗指南(7]。
化疗治疗患者LCNEC显著改变了从2003年到2012年,在荷兰,与减少NSCLC-t化疗和增加SCLC-t化疗。这个观察与数据积累2014年的问卷调查中传阅21荷兰肺内科医生。在这个调查中绝大多数的医生(80%)将与SCLC治疗LCNEC化疗(在线补充图S6)。我们找不到具体的解释为什么治疗LCNEC已经改变了。治疗的偏好可能是受到2005年发表的一项研究描述LCNEC SCLC-type化疗(有利的反应的17]。
在LCNEC几项研究评估化疗,但报道研究异构的病理学诊断的病例选择和确认(表2)。两个二期试验,都与病理检查报告。欧洲试验(11)报告了8.0个月的中位总存活数(95% CI 3.7 - -7.9个月),PFS的5.0个月(95% CI 4.0 - -7.9个月),或者在29 platinum-etoposide化疗患者的34%。在日本试验(12),中位总生存期为12.6 (95% CI 9.3 - -16.0)个月,PFS 5.8 (95% CI 3.8 - -7.8)个月,据报道47%的奥尔platinum-irinotecan治疗(n = 30)。在回顾性评估群LCNEC病人,platinum-etoposide化疗的报道或者范围从37%到73%,整体生存范围从8.4到16.5个月(17- - - - - -20.]。治疗结果为SCLC和NSCLC-type LCNEC此前被评估化疗;27个病人显示改善生存platinum-etoposide化疗相比,非小细胞肺癌的组合方案(17]。相反,评价一个额外的26个病人表现出显著降低总体生存platinum-etoposide化疗相比,非小细胞肺癌的组合方案(19]。因为非小细胞肺癌治疗经常结合进行分析,缺乏数据subtype-specific整体生存和PFS。的报道或者铂金与吉西他滨相结合,多西他赛和紫杉醇是41% (n = 17), 77% (n = 9)和81% (n = 11),分别为(18,21]。
Platinum-pemetrexed化疗建议作为一线治疗转移性nonsquamous NSCLC患者(7]。然而,platinum-pemetrexed化疗显示差结果相比platinum-etoposide SCLC (22),肿瘤生物LCNEC密切相关。培美曲塞治疗反应差可能是由于报道thymidylate合成(TS)的高表达基因LCNEC。增加TS表达建议与抵抗培美曲塞治疗(23- - - - - -25]。培美曲塞阻力的增加趋势,加上报道临床观察表明,培美曲塞在LCNEC患者不应使用。
分子LCNEC和描述了SCLC的变化。SCLC的特点是RB1和TP53基因突变,而LCNEC是特点是互斥RB1和TP53基因失活与结合STK11 /喀斯特KEAP1基因突变(9,26]。在将来的研究中会分析这些模式感兴趣的分子背景调查是否符合反应不同的化疗方案9]。
本研究也有一些局限性。首先,它是一个回顾性研究和化疗的数据不能被检索所有的病人。然而,排除患者随机而不是选择,正如排除类似的整体存活率和年龄的患者相比,分析患者队列(在线补充表S4和S5)。第二,信息缺乏表现分,这可能使得报告总体存活率。没有观察到的差异总体存活率与cisplatinum治疗或carboplatinum化疗(在线补充图S2)。第三,完成化疗周期NSCLC-t和SCLC-t治疗之间略有不同。然而,多达62%的病人完成4个或多个周期的化疗治疗组之间没有明显不同。第四,报道总体生存放疗亚型可能被混淆,强大的二线治疗的疗效。然而,在提出队列二线治疗的频率相对较低(23%),而不是统计不同集群化疗中亚型(表1)。二线治疗的频率低于报道日本二期试验(86%)(12),但不是远低于日常临床实践的报道肺癌(32%)(27]。最后,PFS回顾性获得数据并不能正式评估RECIST(固体肿瘤反应评估标准)标准,这是一个真实的分析设置和临床试验。反应评估在40%的病人没有标准化的和不完整的;因此,这些数据没有报道。
总之,我们现在最大的系列pathology-reviewed患者转移LCNEC迄今为止,表明NSCLC-t方案,主要platinum-gemcitabine化疗,优于platinum-pemetrexed和platinum-etoposide治疗。这些结果需要前瞻性评估,最好是在随机试验中,在集中LCNEC确认。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
补充病理数据erj - 01838 - 2016 - _supplementary_pathology_data
辅助临床数据erj - 01838 - 2016 - _supplementary_clinical_data
补充图S1。协变量的单变量分析的整体存活率panel-consensus LCNEC (N = 128)。LCNEC:大细胞神经内分泌癌;非小细胞肺癌:非小细胞肺癌;SCLC:小细胞肺癌。erj - 01838 - 2016 - _figure_s1
补充图S2。总体生存panel-consensus LCNEC (N = 128)根据cisplatinum治疗或carboplatinum双重化疗。erj - 01838 - 2016 - _figure_s2
补充图S3。总体生存LCNEC凡2015标准的可评价的(N = 108)的化疗相比集群(A)和化疗(B)的亚型。无进展生存比较化疗集群(C)和亚型的化疗(D) (N = 101)。* Vinorelbine排除在外。LCNEC:大细胞神经内分泌癌;SCLC-t: platinum-etoposide小细胞肺癌化疗方案;NSCLC-t:非小细胞肺癌化疗方案的铂和吉西他滨、紫杉醇、多西他赛或vinorelbine;platinum-pemetrexed NSCLC-pt:非小细胞肺癌治疗方案。erj - 01838 - 2016 - _figure_s3
补充图S4。协变量的单变量分析的整体存活率panel-consensus LCNEC凡2015标准的可评价的(N = 108)。LCNEC:大细胞神经内分泌癌;非小细胞肺癌:非小细胞肺癌;SCLC:小细胞肺癌;谁:世界卫生组织。*多元分析排除由于小尺寸效应。erj - 01838 - 2016 - _figure_s4
补充图S5。多变量分析的整体存活率panel-consensus LCNEC凡2015标准的可评价的(N = 108)。LCNEC:大细胞神经内分泌癌;非小细胞肺癌:非小细胞肺癌;SCLC:小细胞肺癌;谁:世界卫生组织。erj - 01838 - 2016 - _figure_s5
补充图S6。概述的问卷调查在荷兰医生(N = 21)在支持一线治疗一个病人被诊断为四期LCNEC疾病根据肝脏转移。这个问卷是教育肺癌会议期间流传“Wengen op德瓦登2014”。LCNEC:大细胞神经内分泌癌;非小细胞肺癌:非小细胞肺癌;SCLC:小细胞肺癌。erj - 01838 - 2016 - _figure_s6
确认
的成员PALGA(全国网络和注册表的组织和细胞病理学在荷兰)组织如下。l . Arensman:河曲Medisch中枢Klinische Pathologie(阿默斯福特);远东Bellot: Klinische Pathologie Hoofddorp (Hoofddorp);J.E. kg: Isala Klinieken(兹沃勒);:范菜:Klinische Pathologie Groene哈特Ziekenhuis(英国);K.E.S. Duthoi: Amphia Ziekenhuis(布雷达);M.J. Flens: Symbiant(样子);J.M.M. Grefte: Gelre Ziekenhuis Klinische Pathologie(克);M.C.H.法眼:Labpon(亨格罗);r .色织席纹绸:混合Ziekenhuis(海牙); A.F. van Hamel: Pathologie SSZOG (Groningen); P.J.J.M. Klinkhamer: Stichting PAMM (Eindhoven); J.W.R. Meijer: Ziekenhijs Rijnstate (Arnhem); J.C.C. van der Meij: Pathologie Friesland (Leeuwarden); F.H. van Nederveen: Laboratorium voor Pathologie (PAL) (Dordrecht); E.W.P. Nijhuis: Onze Lieve Vrouwe Gasthuis (Amsterdam); M.F.M. van Oosterhout: St. Antonius Ziekenhuis (Nieuwegein); S.H. Sastrowijoto: Pathologie Sittard (Sittard); K. Schelfout: Stichting Pathologisch en Cytologisch Laboratorium West-Brabant (Bergen-op-Zoom); J. Sietsma: Pathologie Martini Ziekenhuis (Groningen); F.M.M. Smedts: Reinier Haga MDC (Delft); M.M. Smits: Laboratorium voor Klinische Pathologie (Deventer); J. Stavast: Laboratorium Klinische Pathologie Centraal Brabant (Tilburg); W. Timens: Pathologie UMCG (Groningen); M.L. van Velthuysen: NKI-AVL (Amsterdam); A. Vink: Universitair Medisch Centrum Utrecht (Utrecht); C.C.A.P. Wauters: Canisius Wilhelmina Ziekenhuis (Nijmegen); S. Wouda: VieCuri Medical Centre (Venlo).
这项工作已经在欧洲社会医学肿瘤学海报讨论,哥本哈根,丹麦,10月7 - 11,2016(文摘1122)和欧洲神经内分泌肿瘤学会会议上,巴塞罗那,西班牙,2017年3月8 - 10日。
脚注
可以从本文的补充材料www.qdcxjkg.com
支持声明:这项工作是由荷兰癌症协会的资助(7110号)。资金信息,本文已沉积的Crossref资助者注册表。
利益冲突:没有宣布。
- 收到了2016年9月19日。
- 接受2017年3月5日。
- 版权©2017人队
这收获打开文章是开放和分布式根据创作共用署名非商业188滚球软件性4.0许可证。















