摘要
支气管炎代表了对儿科重症监护单位(ICU)的非选择性录取的最常见原因。
我们评估了2002年至2014年在澳大利亚和新西兰ICU收治的患有细支气管炎的<24个月婴儿的入院率、呼吸支持和预后的变化。
在研究期间,34829例非选择性ICU住院患者中有9628例(27.6%)为毛细支气管炎。据估计,因毛细支气管炎而以人群为基础的ICU住院率每年增加11.76 / 10万人(95%可信范围8.11-15.41)。毛细支气管炎患者需要插管的比例从2002年的36.8%下降到2014年的10.8%(调整后OR 0.35, 95% CI 0.27-0.46),同时观察到高流量鼻插管治疗的使用显著增加到72.6% (p<0.001)。我们观察到在不同科室之间的实践中存在相当大的差异,在风险调整插管率方面存在6倍的差异,这些差异不能用ICU类型、大小或主要患者因素来解释。2014年,由于严重毛细支气管炎导致的年度直接住院费用增加到3000多万美元。
我们观察到由于严重的毛细支气管炎而增加的医疗保健负担,在管理实践中从有创支持到无创支持的重大改变,提示毛细支气管炎患者进入ICU的门槛已经改变。未来的研究应该评估icu外毛细支气管炎的治疗策略。
摘要
改变毛细支气管炎患者入住PICU的门槛对成本和资源利用产生了重大影响http://ow.ly/AVA630a08rx
介绍
细支气管炎是一种常见的病毒性下呼吸道感染,主要表现为急性小气道炎症,是婴儿出生后一年内住院的主要原因[1.].在高收入国家,因细支气管炎住院的婴儿中,约有八分之一因呼吸衰竭和低氧血症导致的进行性呼吸窘迫而需要进入重症监护病房进行呼吸支持[2.,3.].尽管总体住院人数呈下降趋势,但细支气管炎相关的住院费用最近有所增加,在美国每年达17.3亿美元[4.].在过去的几十年中,药理学干预措施未能出现任何好处,因此,共识指南强调支持性治疗方案[2.,3.,5.–8.]尽管传统上认为有创通气是重症监护病房治疗严重毛细支气管炎的基石,但近年来,越来越多的单中心研究报告了早期使用无创通气(NIV)和高流量鼻插管(HFNC)的益处减少毛细支气管炎插管和有创通气需求的治疗[9–13].
本研究的目的是描述澳大利亚和新西兰重症监护室新生儿以人群为基础的入院率和毛细支气管炎的严重程度,确定有创通气的危险因素,并评估入院率、管理、2002-2014年13年期间的成果和相关直接保健费用。
方法
关于研究方法的进一步信息可以在补充材料中找到。对澳大利亚和新西兰小儿科重症监护(ANZPIC)登记处的所有患者的多期面,融合,回顾性研究[14]该研究得到了人类研究和伦理委员会(澳大利亚布里斯班Mater Health Services HREC)的批准,包括放弃知情同意。ANZPIC登记处前瞻性记录了年龄小于16岁儿童的人口统计学、入院时的生理变量、重症监护支持、儿科ICU和普通ICU入院的诊断和结果 澳大利亚和新西兰的年龄[14, 92% - 94%的儿科ICU住院病例。
纳入和排除标准
年龄<729天的婴儿被诊断为毛细支气管炎[8.]并于2002年1月1日至2014年12月31日期间在澳大利亚或新西兰入住儿科ICU(PICU)或普通ICU。排除选择性入院和已有气管造口术的婴儿。
成果和定义
主要结果定义为需要插管和有创通气的婴儿比例。NIV定义为持续气道正压通气(CPAP),有或没有通过鼻罩、全脸面罩或鼻咽管提供压力支持。机械通气定义为有创通气和/或无创通气。自2010年以来,ANZPIC注册中心一直在前瞻性地记录HFNC氧疗的使用情况。HFNC定义为>1 L·kg−1.·Min.−1.气体氧混合物通过鼻插管的流动,并与机械通气支持分开编码[12,13].因此,数据分析被分为两个阶段:HFNC治疗广泛应用前(2002-2009年)和HFNC治疗广泛应用后(2010-2014年)。2010年以前,除一个儿科ICU外,HFNC在主要儿科ICU和ICU中未常规使用。
补充材料中提供了费用估计方法。
统计数字
数据以百分比和数字或带有标准偏差的平均数表示。采用T检验对各亚组进行比较。计算以人群为基础的入院率估计值。我们评估了13年期间呼吸支持的线性趋势。此外,通过比较风险调整后的有创通气需求,评估了13年研究期间的趋势。我们构建了有创通气需求的多变量预测模型。对于多变量模型,使用了来自单变量分析的所有显著预测因子。我们使用了一种基于p>0.05的逆向逐步消除程序来消除不显著的预测因素。
在整个研究期间,澳大利亚和新西兰的所有儿科ICUs都参与了ANZPIC的注册。在研究期间,参与登记的普通ICUs数量从6个增加到19个。为了解释潜在的报告偏差,进行了以下预定义的亚组分析:1)专门的儿科icu;2)一般(成人和儿童混合)ICUs;3)在整个研究期间为ANZPIC注册做出贡献的儿科和普通ICUs。
关于风险预测模型的更多细节在补充材料中提供。
所有分析都使用Stata(版本12.1,Stata公司,College Station, Texas, USA)进行。p值小于0.05被认为是显著的。
结果
在研究期间,毛细支气管炎是ICU住院的最常见原因,2岁以下婴儿非选择性住院的34 829例中有9628例(27.6%)是毛细支气管炎的原因。324名婴儿做了气管切开术原位被排除在入院时。早产(20%)、慢性呼吸系统疾病(10%)和先天性心脏病(7%)是最常见的潜在疾病(表1).2010-2014年期间(在广泛引入HFNC后),5670名婴儿因毛细支气管炎入院,而2002-2009年期间为3634名(表2)近年来,入住ICU的毛细支气管炎患儿年龄较大,不太可能需要院间转移,更可能入住普通ICU,也不太可能有潜在疾病(p<0.001)。以平均死亡概率(PIM2)衡量的疾病平均严重程度显著降低,ICU和住院时间(LOS)也相应减少。整个研究期间的粗死亡率为0.38%(35/9304)。重新校准的PIM2标准化死亡率从2002-2009年的1.53(0.99–2.26)下降到2010-2014年的0.54(0.26–0.98)。
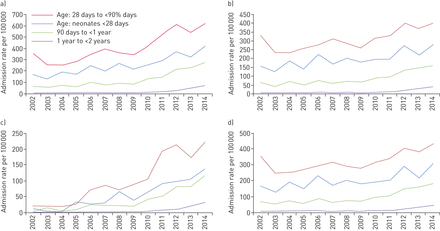
每年入ICU(包括儿科和普通ICU)的毛细支气管炎患儿数量由2002年的383例增加到2014年的1528例(表2,图1).在此期间,每年非选择性ICU住院总人数从1933年增加到4115人。在研究期间,估计以人群为基础的年龄标准化细支气管炎住院率增加,24个月以下的婴儿平均每年增加11.76例(95%可信区间8.11-15.41)。入院率的变化在普通icu中最明显,2014年需要重症监护的毛细支气管炎住院患者中有40%是普通icu (p<0.0001)。当限制对儿科icu(每年增加5.80例/ 10万,95%可信区间3.68-7.90)和对整个研究期间的登记有贡献的icu(6.21例/ 10万,95%可信区间3.80-8.63)进行分析时,入院率的增加没有那么明显。毛细支气管炎的增加高于任何其他呼吸道感染的住院,也高于所有儿科ICU的年度住院,从1933年增加到4115 (表2).
毛细支气管炎引起的估计人群重症监护病房(ICU)入院率。每100人的ICU入院率 000名婴儿<24 a)澳大利亚和新西兰儿科重症监护登记处记录的所有ICU住院患者的年龄和年份;b) 儿科PICU入院;c) 入住普通重症监护病房(ICU);d)在2002-2014年的整个研究期间,儿科重症监护室和重症监护室的入院率为注册提供了帮助。
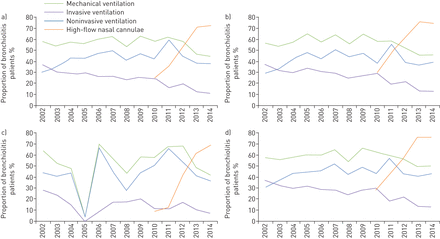
2002年,37%的毛细支气管炎患者进行了插管/有创通气,而2014年只有11%(p<0.001,图2和补充表S1)。考虑到伴随的细支气管炎相关ICU住院率的急剧增加,我们计算了基于人群的插管率(补充表S2)。在研究期间,毛细支气管炎患儿的绝对插管数和以人群为基础的插管率没有显著下降(p>0.05)。我们观察到在入院后1小时进行ICU插管的比例从2002-2009年的66.2%(674/1018)下降到2010-2014年的43.6%(394/903)。在研究期间,未在入院后1小时内插管的婴儿进行插管的时间没有变化(p=0.840;补充图S1)。同期内,机械通气(有创通气和/或NIV)的持续时间从平均109小时显著减少至69小时(每个机械通气患者每年平均减少3.4小时;95%可信区间2.25 - -4.56)。2010-2014年期间,在大多数儿科icu中引入HFNC治疗后,毛细支气管炎患儿HFNC的使用增加到72.6%;同时也减少了NIV的使用。 The findings observed in the entire cohort were confirmed in subgroup analyses restricted to paediatric ICUs only, and to paediatric ICUs and ICUs that had contributed to the registry for the entire study duration (图2以及补充表S1和S2)。
2002 - 2014年婴儿呼吸期间呼吸支持模式的变化,婴儿患有支气管炎的重症监护单位(ICU)。机械通气定义为插管和/或非侵入性通风。每位患者使用的呼吸支持模式的比例(允许多种方式)显示为a)澳大利亚和新西兰小儿科重症监护登记处所捕获的所有ICU入学;b)招生儿科ICU;c)录取一般ice;d)向小儿德卢比和ICU的入场,为整个研究持续时间2002-2014提供了贡献。
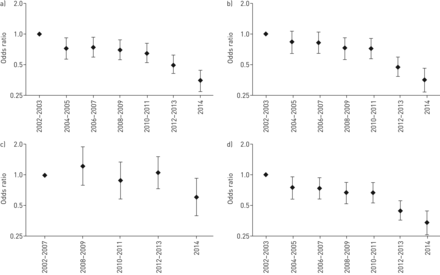
在多变量分析中,年龄、院间转运、主要慢性疾病、早产和严重指标(如低收缩压)被确定为插管的重要预测因素(表3;AUC 0.76, 0.75 - -0.77)。每年插管风险降低0.9% (95% CI 0.81-1.00%)。从2002/2003至2014年,插管的总调整优势显著下降(OR 0.35, 95% CI 0.27-0.44;p < 0.001) (图3).该模型适用于到达儿科ICU时未插管的婴儿(补充表S3A)。在HFNC治疗的儿童中,年龄偏小、支气管肺发育不良、先天性心脏缺陷、低血压和负基过量升高是插管的主要预测因素(p<0.01)(补充表S3B)。
研究期间毛细支气管炎患儿插管/有创通气的调整风险。优势比根据年龄、院间转运、慢性呼吸和神经疾病、早产、先天性心脏病、特异性呼吸道病毒、低收缩压进行调整,并显示a)澳大利亚和新西兰儿科重症监护登记处记录的所有重症监护病房(ICU)入院情况;b) 儿科重症监护病房住院;c) 普通重症监护病房入院;d)在2002-2014年的整个研究期间,儿科重症监护室和重症监护室的入院率为注册提供了帮助。
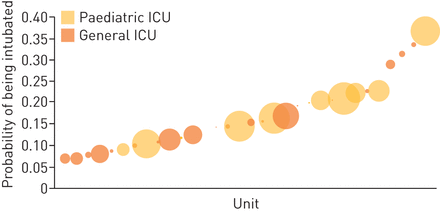
当比较婴儿患有支气管炎的婴儿的风险调整率时,注意到单位之间的重要差异(图4).与仅截取的混合效应模型相比,该模型控制了年和患者风险因素(表3)表明随机效应的方差减少了39.1%。这一差异表明,60.9%的插管率变化既不能用病例组合解释,也不能用时间趋势解释,而可能反映了单位与单位实践的潜在差异。使用插管的平均风险曲线,细支气管炎患儿插管的概率在各个单位之间从6.9%到36.7%不等。
比较不同儿科和普通重症监护病房(ICU)毛细支气管炎患儿接受有创通气的可能性。气泡面积表示相对入院人数。
我们评估了需要ICU住院的婴儿的直接住院相关总费用,包括ICU和病房费用。虽然2002 - 2014年期间的成本有所减少,但年度总成本从2002年的1140万澳元增加到2014年的4430万美元(补充表S4和图5).同期,专科儿科重症监护室收治的与细支气管炎有关的总费用从1 070万美元增加到3 110万美元。
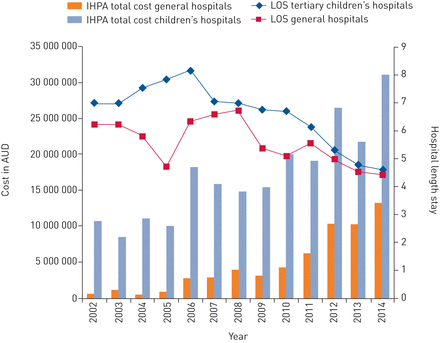
由于澳大利亚和新西兰的重症监护室入学,2002 - 2014年,年度直接住院费用(2014年澳元)。住院时间(LOS)和独立医院定价管理局(IHPE)估计的相关费用(IHPE)有效的价格确定显示儿童医院和综合医院。
讨论
这项包括9000多名患有细支气管炎的危重婴儿的大型两国研究表明,严重的细支气管炎造成了巨大的疾病负担,在澳大利亚和新西兰每年造成超过3000万美元的直接成本。毛细支气管炎对ICU资源消耗有重要影响,>占婴儿非选择性PICU入院人数的25%。在ICU治疗毛细支气管炎缺乏高水平证据的情况下,我们观察到澳大利亚和新西兰因毛细支气管炎入院重症监护的儿童数量显著增加,同时HFNC治疗的使用增加。鉴于婴幼儿重症细支气管炎的死亡率接近于零,这些发现表明迫切需要进一步研究是否有一部分患者可以在ICU外得到安全管理,从而降低相关的医疗成本。
通过估算以人群为基础的ICU住院率,我们能够记录过去十年中实践中的一个重大变化,即不需要有创通气的细支气管炎患儿的ICU住院人数显著增加。由于近年来更多的一般ICUs为研究数据库提供了数据,一般ICUs观察到的增加可能由于报告偏倚而增强。然而,这些发现在局限于儿科icu的亚组分析中得到了再现,并且局限于那些在整个研究期间提供了数据的中心。近年来ICU收治的毛细支气管炎患儿有潜在合并症的可能性较低,年龄较大,预测死亡率较低,提示ICU住院阈值有所改变。与此同时,我们观察到科室之间存在相当大的差异,风险调整插管率的差异超过6倍,不能用ICU类型、大小或主要患者因素来解释。我们的发现支持了最近一项关于细支气管炎的北美研究,该研究观察到儿科icu之间插管风险的>3.5倍的差异,以及暴露于其他非循证干预的患者比例的高变异性[15].而毛细支气管炎住院率和住院时间已被建议作为基准,在NHS的医疗保健变异图集(www.chimat.org.uk变异),尚未调查ICU资源使用情况。值得注意的是,在研究期间,主要儿科医院实施了快速反应小组和早期预警工具(EWT),其次是地区医院。而EWT已被证明可以预测ICU入院的需要,并减少病房环境中的心肺骤停[16],据我们所知,它们还没有被证实专门用于毛细支气管炎。事实上,患有严重毛细支气管炎的婴儿通常表现为心动过速、呼吸急促和呼吸功增加,并可能相对较快地触发EWT,对健康结果和资源利用的影响尚不清楚。
我们的数据显示,尽管重症监护的服务水平降低,通气时间缩短,但ICU住院率的增加与成本的快速增长相关。我们的成本与最近一项欧洲研究中的成本相当,该研究报告需要ICU的儿童的成本比接受ICU治疗的儿童高出四倍沃德(8061欧元)与EUR1834) [17].
我们的研究表明,尽管缺乏对婴幼儿使用HFNC的大型试验,但HFNC治疗已成为澳大利亚和新西兰近年来婴幼儿毛细支气管炎危重症患者最常见的支持模式,2014年有超过70%的入院患者使用了HFNC。与此同时,虽然需要插管和有创通气的入院比例下降,但我们没有观察到需要有创通气的儿童绝对人数明显减少。我们的观察与几项单中心研究相一致,这些研究报告了在增加NIV和HFNC的使用后,严重毛细支气管炎患者的插管率下降[10,12,13,18–22]最近在成人中进行的大型随机试验证明HFNC治疗急性低氧性呼吸衰竭有效[23,24.].在新生儿人群中,HFNC治疗被证明不低于鼻CPAP [25.,26.].而HFNC治疗的生理效应,包括提供4-5 cmH2.O CPAP,通过提供与最大吸气流量相匹配或大于最大吸气流量的气流,减少呼吸的吸气功,以及冲洗鼻咽腔死区,已经得到独立证实[27.,28.,目前缺乏随机对照试验来支持儿科年龄组HFNC治疗的结果效益或成本效益。最近的一项成人单中心研究报告,需要延迟紧急插管的HFNC患者死亡率较高[29.].在我们的队列研究中,HFNC使用的增加与插管延迟无关,事实上,插管延迟的比例、死亡率、机械通气时间和ICU住院时间均降低。
与其他形式的呼吸支持相比,HFNC治疗的优点包括良好的安全性、较低的设备成本、易于应用和增加患者的舒适度。因此,在ICU设置以外的地方应用HFNC治疗已经越来越多地得到测试,单中心研究表明,HFNC治疗的安全性、可行性和有效性这种做法[18,尽管将这种方法转化为更好的结果仍有待证明。毛细支气管炎是一种相对统一的疾病,死亡率接近于零,患者大多表现为渐进而非陡然恶化,可使用预测指标对严重程度进行分层[30.]因此,这种疾病实际上可能最适合设计旨在减少重症监护住院人数的介入性试验[31.].
我们相信这项研究的结果对毛细支气管炎的进一步研究设计有一些启示。首先,它们强调迫切需要验证毛细支气管炎的早期预警工具,因为这些工具可能对重症监护住院率产生直接影响。其次,改进的严重程度标记,包括病毒基因组负荷[32.],可能有助于优化最有可能发生严重呼吸衰竭的目标人群的风险分层。第三,呼吸支持实践的差异表明缺乏标准化协议[5.,8.].第四,呼吸支持模式中看到的实践的戏剧性变化是HFNC治疗的儿科ICU试验与NIV与呼吸衰竭婴幼儿的低流量氧气[24.].最后,我们的数据表明,相当大比例的重症监护患者可能是ICU外治疗的良好候选者;HFNC疗法在这种环境下是否具有成本效益,还需进行大规模试验验证[31.].重要的是,ICU外最佳呼吸支持试验可为全球范围内制定和实施具有成本效益的相关干预措施提供信息,并有可能转化为资源贫乏国家的死亡率效益[33.].
需要考虑这项研究的几个局限性。虽然我们无法通过支气管炎评估整体医院入学,但我们捕获了在澳大利亚和新西兰提供的一般或儿科ICU的每位患者向登记处提供数据。虽然支气管炎被定义为临床实体[8.],与反应性气道疾病重叠可能导致诊断挑战,可能导致疾病过度诊断。HFNC的使用在2010年之前未被前瞻性记录,因此我们无法评论HFNC在2010年之前作为呼吸支持模式使用的频率。此外,我们无法获得详细的微生物学数据,在整个研究过程中,各中心并未持续进行扩展的鼻咽病毒聚合酶链反应检测。由于ICU收治的大多数毛细支气管炎患儿入院时未接受动脉内监测,我们无法根据低氧血症的程度进行分层。最后,激发氧分数(FIO2.)到脉搏血氧饱和度的比值不能作为真实值FIO2.在HFNC或低流量氧疗中尚不清楚。此外,我们无法获得入住ICU时测量的二氧化碳张力值;然而,升高的二氧化碳张力值在毛细支气管炎中很常见,可能并不一定表明需要插管[34.].
总之,严重的毛细支气管炎仍然是造成巨大疾病负担的原因。我们观察到在严重毛细支气管炎的管理实践中发生了重大变化,尽管在该年龄组缺乏治疗益处的高级证据,但HFNC治疗的使用显著增加。我们的数据表明,在过去十年中,细支气管炎患者接受重症监护的门槛已经降低,这对澳大利亚和新西兰icu的医疗保健相关成本和资源利用产生了重大影响。迫切需要在重症监护环境之外进行国际试验,以解决毛细支气管炎的风险分层和安全管理问题。
补充材料
致谢
我们感谢澳大利亚和新西兰重症监护协会的儿科研究小组对这项研究的支持(西蒙·埃里克森,澳大利亚珀斯玛格丽特公主儿童医院;Andreas Schibler, Anthony Slater, Debbie Long, Jan Alexander, Lady Cilento儿童医院,布里斯班,澳大利亚;John Beca, Claire Sherring, Starship儿童医院,奥克兰,新西兰;Gary Williams, Janelle Young, Mary Lou Morritt,悉尼儿童医院,Randwick,澳大利亚;Johnny Millar, Carmen Del Zoppo, Warwick Butt,皇家儿童医院,墨尔本,澳大利亚;Subodh Ganu, Georgia Letton,妇女儿童医院,阿德莱德,澳大利亚;Marino Festa, Westmead儿童医院,悉尼,澳大利亚)。我们感谢参与icu的重症监护人员、数据管理人员和其他工作人员对数据的贡献。我们感谢ANZICS CORE的Peter Hicks,感谢他在健康经济分析方面的帮助。澳大利亚和新西兰重症监护协会、卫生部(新西兰)以及州和地区卫生部门通过澳大利亚卫生部长咨询委员会支持澳大利亚和新西兰重症监护协会注册。
作者捐款如下:L.J.Schlapbach和L. Straney完全访问了研究中的所有数据,并负责数据的完整性以及数据分析的准确性。L.J.Schlapbach负责研究设计,准备了第一个稿件草案并批准了最终版本。L. Straney和A. Schibler参与了研究设计,分析,编制了第一稿草案和最终版本。A. Slater LED以自成立以来的anzpic注册表的设计和维护,参与了研究设计,并批准了最终版本。J.A.惠特和D.富兰克林进行了医疗保健与成本相关的分析和解释。J.Beca,B.Wilkins,S. Erickson,E. Croston,B.Gelbart,S.Ganu和J. Alexander参与了学习设计,数据收集和稿件准备,并批准了最终版本。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:资助Straney博士的国家医疗卫生和研究委员会(NHMRC)澳大利亚复苏结果联盟(Aus ROC)卓越研究中心未参与本手稿的设计、分析和撰写。本文的资金信息已存放在CrossRef Resder注册表.
利益冲突:无声明。
- 收到了2016年8月18日。
- 认可的2017年3月3日。
- 版权©2017人队