摘要
IREB2.是产生铁调节蛋白2(IRP2)的基因,这对细胞内铁稳态至关重要,涉及细胞增殖速率。IREB2.位于肺癌易感位轨迹中。目的是评估1)肺癌中铁载荷,细胞增殖和IRP2表达的关系;2)铁相关途径作为治疗靶标的潜力;3)IRP2在经营肺癌患者中的相关性。
两种非球细胞癌(NSCLC)系和原发性支气管上皮细胞(PBEC)的细胞培养,无熨斗;评估和增殖,细胞凋亡和迁移。逆转录酶PCR和Western印迹用于评估铁稳态基因/蛋白的表达。铁螯合和敲低IREB2.被使用了体外探索治疗剂。研究了一系列操作的NSCLC患者,用于全身性熨斗状态,肿瘤IRP2染色和生存率的标志物。
铁载荷导致癌细胞系中细胞增殖,不太能够调节IREB2.比PBECs表达式。铁螯合可使增殖率恢复到基线水平;击倒的IREB2.有类似的效果。IRP2阳性肿瘤较大(p = 0.045),与较差的存活相关的较高百分比(p = 0.079)。
铁调节功能的丧失是肺癌预后不良的标志。
摘要
铁负荷导致肺癌细胞增殖。铁螯合可使增殖率恢复到基线水平http:///ow.ly/zkes3093yyf.
介绍
肺癌是英国第二大常见癌症,也是癌症死亡的主要原因,占全球所有癌症相关死亡的18% [1].香烟烟雾含有60多种致癌物,有令人信服的证据表明,其中至少20种致癌物会导致肺组织中的肿瘤生长[2].然而,肺癌并不是吸烟者独有的疾病;据估计,15%的男性病例和53%的女性病例发生在从不吸烟的人身上[3.].尽管筛选改善[4和外科技术,存活率仍然很低,迫切需要新的治疗途径。
肺癌的最大遗传危险因素被认为与烟草吸烟和随后由于烟草受体内的轨迹而言,随后的尼古丁成瘾(CHRNA3-5)[5].然而,在这方面存在强烈的连锁不平衡(LD)和铁调节蛋白IRP2的基因编码(IREB2.),这意味着真正的基因座可以躺在里面IREB2。与此符合,IREB2.已被证明与基因组 - 宽协会研究中的慢性阻塞性肺病(COPD)相关[6]和其蛋白产物IRP2的表达在携带肺癌相关肿瘤的肺癌患者中发生改变CHRNA3-5多态性[7].IRP2的作用是通过调节各种铁的输入、输出和储存蛋白来控制细胞铁的水平[8].因此,错误的表达可以通过改变细胞铁水平来引起促致瘤的变化,并通过细胞内通过过量的铁载荷进行恶性肿瘤的发展[9].如果IRP2或铁通路能够被靶向治疗,它可能为肺癌的治疗提供一种新的方式。先前的证据表明,改变铁稳态可导致食管癌和结肠直肠癌的细胞增殖,这也说明了我们的假设在肺中的相关性[10.,11.].
我们假设肺癌细胞在铁存在的情况下会增殖得更快,而这可能会被铁的螯合和改变IREB2.表达式。此外,我们假设IRP2表达改变的肿瘤可能与临床表现和进展的变化有关。
材料和方法
细胞培养和铁刺激
使用从Sigma-Aldrich,Uset,英国多塞特群岛购买的试剂,在两个肺癌细胞系(A549和QG56)和原发性支气管上皮细胞(PBEC)上进行了一式三份进行了实验。使用RPMI-1640培养癌细胞,其中胎儿牛血清(FBS)和1%谷氨酰胺 - 青霉素 - 链霉素,并在达到彼此的融合时使用,如别处所述的1×胰蛋白酶EDTA [12.].使用Begm Bulletkit(Lonza Biologics Plc,Slough,UK)培养PBEC,这是无血清的。RPMI培养基没有铁;LONZA BEGM套件包含痕量的铁,即<2μm。
10mm FeSO溶液4和1mm的抗坏血酸钠在连续稀释至所需浓度前经过过滤消毒并冷藏≤7天。将细胞胰酶化、计数和稀释,然后留置过夜,然后用含铁培养基刺激24小时。然后再用无铁培养基替代此培养基24小时,在此时间点进行功能测定。
细胞功能检测,PCR和Western blotting
BrdU(罗氏应用科学,英国)根据生产商的说明书,使用7×10对扩散进行评估4 cells·mL−1.使用划痕伤口测定评估迁移[13.]细胞1×105 cells·mL−1;使用imagej软件拍摄并分析伤口。用流式细胞术用膜蛋白5 /碘化钛氟化物氟化物(Invitrogen,Loughborough,UK)进行双重染色,以区分凋亡和坏死,如前所述[14.].在1×10的细胞上评估铁载荷5 cells·mL−1使用Ferrozine,如前所述[15.].
TaqMan基因表达检测IREB2,TFRC,FTL, DMT1和HIF1A,哪种蛋白质代码(IRP2,转铁蛋白受体,铁蛋白,二价金属转运蛋白1和缺氧诱导因子1α亚基)。使用Trizol分离RNA,使用RNA聚合酶III转化为cDNA,并与适当的内脏基因一起使用(GAPDH.为了IREB2.,TFRC,DMT1和HIF1A,18S.为了FTL)在三重重复的实时PCR实验(所有试剂Fisher Scientific,拉夫堡,英国)。结果以折线变化表示。
从细胞中分离蛋白并用Bio-Rad (Bio-Rad Laboratories Ltd, Hertfordshire, UK)测定。Western blot检测IRP2抗体(ab181153, Abcam, Cambridge, UK)、转铁蛋白受体单克隆抗体(13-6800,Fisher Scientific, Loughborough, UK)、FTH1抗体(ab109373, Abcam, Cambridge, UK)和负载对照β-actin抗体(ab6276, Abcam, Cambridge, UK)。
用150µmol Fe对三种细胞系进行了类似的实验(增殖、凋亡、坏死、划痕创面实验和IREB2、FTH1和TFRC基因表达实验)3+.这些实验的方法和结果可以在补充材料中找到。
铁螯合
制备脱硫硅(10mm)的储备溶液,在黑暗中冷冻,在需要时在无菌培养基中连续稀释至工作浓度。如上所述进行螯合实验,在铁孵育后将细胞返回到含有脱司叶的培养基。剂量 - 反应实验如前所述进行[16.选择进一步的工作,选择了一种150μm的渗透血清。
IRP2击倒
用Silencer Select siRNA对肿瘤细胞株进行siRNA敲除IREB2.根据制造商的说明,使用Silencer Select阴性siRNA作为对照(英国拉夫堡的Fisher Scientific公司)。细胞在培养皿的当天与相关siRNA一起孵育,然后静置24、48或72 h。还探讨了铁暴露对与相关siRNA孵育48 h的敲除细胞的影响。
临床相关性
统计方法
所有统计分析都在SPSS 19.0(IBM,USA)中进行。配对的T检验用于比较体外状况。IRP2表达联想的单变量测试在活的有机体内根据数据类型使用Chi-Squared测试和Mann-Whitney U-Tests。COX回归用于评估IRP2表达对使用年龄和肿瘤阶段作为共变量的生存的影响。Spearman的秩系数用于评估IRP2表达与组织学和吸烟等变量之间的相关性。所有测试均为两个尾尾,假设具有P <0.05的重要性。
结果
用铁细胞培养物
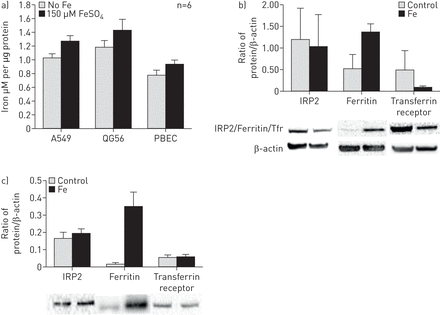
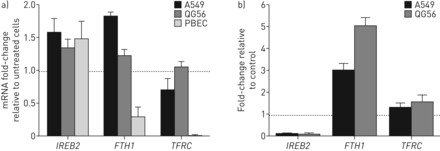
用150 uM FeSO4刺激所有细胞系,细胞铁负荷显著增加(A549和QG56, p<0.01;PBEC p < 0.05) (图1A).在正常细胞(PBECs)的蛋白水平上,IRP2无变化,铁蛋白显著升高,转铁蛋白受体受到抑制(图1B.);在癌细胞中,没有发生IRP2或转铁蛋白的变化,并且铁蛋白更加明显(图1C.).癌细胞的表达通常比PBEC在癌细胞上较低,如与β-肌动蛋白的比例所示。与PBEC不同,癌细胞系在铁的存在下更加激活,在150μmfeso下发生峰增殖4(图2A).氧化Fe没有看到对增殖的影响3+(补充材料)。在任何细胞系中,凋亡,坏死或迁移没有显着差异(图2罪犯).
孵化铁稳定性的效果及其在铁稳态中涉及的相关蛋白质。a)铁嗪测定:在与150μmfeso温育时,所有细胞系中发生大量的铁载量4(A549和QG56,P <0.01;初级支气管上皮细胞(PBEC)P <0.05)(n = 6)。b)PBEC中铁袜蛋白的Western印迹。显示的数据是平均值+SEM.对n=3个独立培养物的3个重复的印迹进行了评估,下面是具有代表性的图片x设在。铁蛋白表达增加(p=0.042)。转铁蛋白(Tfr)受体有抑制倾向(p<0.1)。c)癌细胞中铁稳态蛋白的Western blot(数据显示A549,平均值+)SEM.从n=3个文化,如前所述)。铁蛋白表达增加(p=0.02)。IRP2和转铁蛋白受体的变化较小且未检测到(p>0.05)。
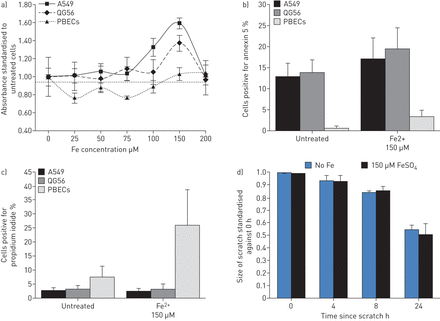
与铁孵育的影响体外关于蜂窝功能。a)Brdu测定。铁荷载导致癌细胞系中增殖的剂量依赖性增加,在原发性支气管上皮细胞(PBEC)中没有统计学意义(P = 0.01 A549,P = 0.03 QG56,P = 0.21 PBEC在150μm的铁).b)癌细胞系细胞凋亡高于PBEC(P <0.01)。铁培养后没有显着差异(所有p> 0.1)。c)PBEC的坏死比癌细胞系更高(P <0.01)。在癌症中,它在癌症存在下没有显着差异,尽管PBEC的增加趋势(P = 0.06)。d)铁的迁移在存在的情况下没有差异。数据显示为A549单元格。n = 6。
螯合和IREB2敲低
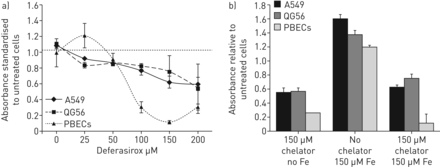
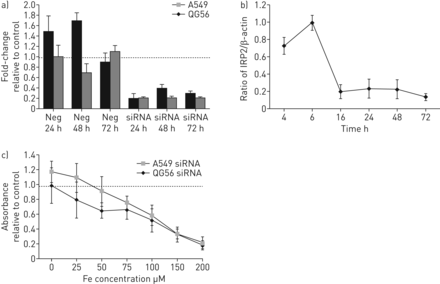
单独使用螯合剂或与150 μM FeSO同时使用时,可将铁诱导的癌细胞增殖降低至基线水平以下4(图3.).IREB2.敲低实现了基因表达减少了80%(图4A);详细的时间课程实验表明,IRP2的伴随变化在6到16小时之间,维持(图4B.).在铁的存在下看到了增殖的减少,类似于螯合(图4C.).细胞凋亡与敲低不同(平均值(SEM.)%凋亡细胞,A549 26.2(6.2)相对15.8 (3.5);p > 0.05)。对野生型和敲除型细胞进行基因表达分析,当与铁共孵育时,表现出更明显的差异Fth.响应和减毒TFR1抑制 (图5.).与铁孵育时野生型并敲下细胞,也显示出增加的表达DMT1和HIF1A(补充材料)。
铁螯合对铁诱导细胞增殖的影响。a)Brdu测定。剂量 - 响应曲线到脱绳索;所有细胞系都表现出降低的增殖,效果在原发性支气管上皮细胞(PBECs)中最多标记。在150μm和以上的P <0.05中,在150μm和上方,在100μm和以上的PBEC中,增殖的降低在统计学上显着,在150μm和上方(p <0.01)。b)即使在培养的额外铁存在下,螯合也能够消除增殖;同样,这种效果在PBEC中最多标记,并且在所有三条线中有统计学意义(A549和QG56中的P <0.05,PBEC中的P <0.01)。n = 5。
IREB2敲低对癌细胞IRP2和增殖的影响。a)在两种细胞系中,在24,48和72小时下敲至24,48和72小时的射击减少80%(P <0.01相对未经处理的细胞。阴性siRNA没有影响(p> 0.1)。n = 3。b)使用Western Blot的时间课程实验:敲低后16小时发生IRP2抑制。c)撞击细胞中的增殖降低,即使在先前导致野生型细胞中增殖增加的浓度(浓度为100μm及以上),也减少了隆起的细胞。在100μm和上方的两条线中,减少在两条线(p = 0.01)中显着。n = 3。
铁胁迫对ireb2敲低前后基因表达的影响a)野生型细胞表达:在原发性支气管上皮细胞(PBECs)中,IREB2 (p=0.24)和FTH (p=0.07)没有变化,而TFRC几乎完全受到抑制(p=0.02)。在癌细胞中,两种细胞系中IREB2和FTH1的表达均呈增加趋势(p<0.01)相对在A549中未经治疗)。在QG56中,基因表达的变化不显着。n = 6。b)敲击癌系的表达:与150μm的铁孵育后,敲击细胞继续具有低的ISB2表达。观察到的Fth1中的上升发生,比预敲击更标记(P <0.05)。在A549中,TFRC不再抑制。n = 3。
临床数据
评估了死亡率的患者的特征表1.在正常的肺中,IRP2染色在上皮组织和肺泡巨噬细胞上的所有样品中是明显的;肿瘤分离成IRP2阳性的那些,这构成了样品的少数群体,以及那些阴性的人(表1和图6.).每位患者IRP2表达的图形证明已包括在补充材料中。在单变量分析中,探讨阳性IRP2染色的决定因素,在较大的肿瘤中观察到更高的染色强度(中等或强烈强度,31.7%(T1A和B)相对42.4%(T2A和B)相对100% (T4);p = 0.045 x²= 12.9)。在死亡的患者中,IRP2阳性的肿瘤比例也有较大的趋势(27.5%)相对肿瘤的10.0%;p = 0.079)。Cox回归分析显示,年龄(p<0.0001)和肿瘤分期与生存率相关(p=0.021;1a/b期患者的死亡几率为0.23(0.07-0.81),但IRP2染色阳性则没有(p=0.31)。IRP2阳性染色与组织学无相关性(r年代=−0.035,p=0.785)或IRP2阳性与吸烟状态(r年代=−0.048,p=0.711)或pack-year history (r年代= -0.049,p = 0.784)。进一步分析,将血清血清水平与组织学,吸烟状态和包装年历史相关,可以在补充材料中找到血清血清素,铁蛋白,铁和转铁蛋白。
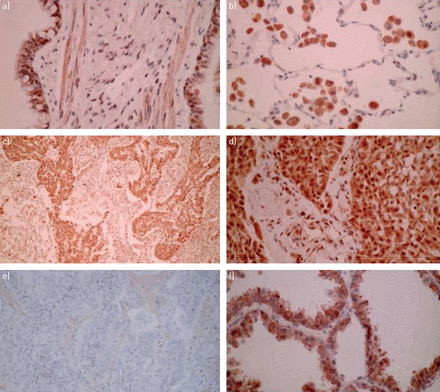
IRP2在正常肺癌和肺癌中染色。IRP2染色A)正常上皮和B)肺泡巨噬细胞。在c)腺癌中的阳性染色)低于和d)高功率。e)具有突出的支气管肺泡模式的腺癌中强烈染色。f)阴性肿瘤染色的例子。
没有一个全身铁稳态的标记显示与肿瘤大小或生存率有任何关系(所有p>0.51)。全身铁标记物与肿瘤IRP2之间未见明显关系(所有p>0.61)。
讨论
本研究表明,铁介导的异常细胞增殖可在肺癌中发生,且明显是由IREB2..这可能适用于治疗和临床重要性,如肿瘤和健康之间的IRP2染色的差异所示,并表明IRP2染色和肿瘤大小与存活之间的关系。
铁介导的癌细胞增殖
我们的数据显示,肺癌在铁的存在下迅速增长,其效果远低于正常细胞(PBEC)。几种肿瘤疾病与铁稳态异常有关。例如,在遗传性血管瘤中观察到高肝细胞癌率,其中铁积聚在肝脏中;这归因于增加的铁水平[20.].此外,在结直肠癌中,癌细胞系内细胞内铁的水平增加导致细胞增殖的相应增加[10.].在食管腺癌中也观察到类似的现象[11.].
有许多不同的原因为什么肿瘤细胞内的铁累积可能会驱动过度增殖。首先是通过WNT信号传导的增加,是主要的致癌信号传导途径,特别是在上皮衍生的肿瘤内[21.].WNT信号传导驱动细胞增殖由于β-连环素转录因子(TCF / LEF)复合物的积累,这导致靶基因的激活,例如c-myc.[22.].这些途径,而不是依赖于e -cadherin的途径,似乎与癌症中铁介导的Wnt信号最相关,并可能由癌细胞获得性突变驱动[23.].另外,铁可能通过氧化应激介导肿瘤的发生,因此氧自由基能够破坏细胞DNA,导致肿瘤抑制基因、致癌基因或先前突变的效果增强[24.].第三,铁可能影响核糖核酸还原酶的活性,这是DNA合成的限速步骤。如果细胞内铁含量增加,核糖核酸还原酶活性就会随之增加,因此DNA合成、细胞增殖和癌症的速度就会加快[25.].铁驱动过度增殖的最终机制是通过耐铁敏感性磷酸酶CDC14a的活性增加,其通过与p53的相互作用直接参与细胞周期检查点的调节。蜂窝烫发中的增加使磷酸酶通过检查点越来越快地进展细胞,并限制强迫逮捕和凋亡,从而导致或加剧癌症[26.,27.].在我们的研究中似乎没有影响凋亡;然而,由于铁而导致的自由基的生产可以解释PBEC中的坏死水平随着羟基的趋势,以多种方式对细胞造成伤害。
基因表达的研究旨在进一步了解铁稳态基因在肺癌中的可能失调。我们观察到IREB2.在铁暴露的细胞中,这将转化为未结合IRP2的增加;然而,这在我们的Western blot中几乎看不到。这很可能是因为在铁充足的、常氧的细胞中,IRP2通常会发生降解通过蛋白酶体(28.].在铁 - 新鲜条件下,IRP2不与IRE结合;结合稳定TFRCmRNA,因此在没有IRP2结合的情况下TFRC和在正常的PBECs中观察到的一样。在癌细胞系中,这种情况并没有发生到这种程度,事实上在我们的鳞状细胞系(QG56)中根本没有。有趣的是IREB2.击倒不起作用TFRC表达在我们的线条中;如果IRP2是主要的驱动力TFRC这些细胞中的稳定性(和因此水平)我们预计会看到这一点。TFRC可以受到癌症的影响[29.,这很可能会影响癌症系,并消除损失的影响IREB2..我们还观察到癌细胞系中的铁蛋白升高,其在正常的PBEC中较小。在含铁水平增加的细胞中,预计铁蛋白将增加以结合多余的铁和TFRC减少活动以防止进一步摄取铁[30.].因为癌细胞没有调节TFRC,铁进入持续畅通无阻,涨幅Fth.被要求赔偿。相反,在正常细胞中,通过减少抑制铁进入TFRC,因此,调节细胞内铁浓度需要较低的铁蛋白增加。值得注意的是,我们的细胞在铁中吸收铁2+表格,在看更广泛的文学时是不寻常的。结果,我们假设在这里有一种新的机制,可能是因为使用抗坏血酸钠如抗坏血酸钠氧化我们的FE2+Fe.3+.
结果与我们的增殖,铁载荷和铁稳态基因的研究结果一致,在结肠直肠癌中报告,其中表达增加总和生育率偶氮量的表达降低导致胃上皮内的铁载荷和腺癌的形成[10.].在食管腺癌中观察到类似的现象,尽管铁出口机械(铁乳蛋白)增加了蛋白质是细胞质,暗示缺乏功能[11.].
临床数据
免疫组化显示,只有一小部分肺癌表现为IRP2染色。由于IRP2通常在常氧、铁充足的细胞中被降解[28.]在肿瘤的背景下持续表达可以反映由于快速肿瘤生长而反映对局部缺氧或铁饥饿的反应。符合此,IRP2阳性肿瘤往往较大,生存率较差;该结果与乳腺癌一致,其中在较高级肿瘤中看到增加的IRP2表达[31.].然而,在多变量分析中,生存效应没有得到维持,这可能是因为肿瘤大小/分期和生存之间的已知关系,这可能打乱了IRP2生存分析。用现有的样本来评估IRP2阳性的肿瘤子集是否代表一群肿瘤中具有获得性突变的患者,这是不可能的,正如在未能调节铁稳态的结直肠癌中所建议的那样[32.]或者是否来自于对肺癌的先天遗传易感性患者。
治疗潜力
铁螯合实验表明,口服铁螯合剂可以减少癌细胞的增殖,尽管对正常细胞(PBECs)也有更大的影响。这与其他人看到的影响大致一致[16.],在肺部外的癌症[10.,33.].脱铁石的作用机制有两方面:通过形成细胞内现有铁复合物将铁从细胞中去除,并随后阻止新的转铁蛋白结合铁的摄取[20.].脱铁龙对肿瘤细胞也有直接影响,它显著上调了转移抑制因子NDRG1然后上调p21 [34.,并显著降低细胞周期蛋白D1 [35.].这导致细胞周期在g逮捕1/S检查点,导致增殖减少[36.].
除了对健康肺组织的潜在局部作用外,铁螯合螯合有可能导致心脏纤维化和贫血等显着副作用[37.].我们的队列没有表现出显着的贫血症,即使在癌症的晚期阶段,也明智地检查基线血红蛋白,如果临床使用铁螯合,请仔细监测这一点。我们假设局部铁调节(例如IRP2)的不同驾驶员代表同样良好的治疗靶标,用于减少不患有这些限制并与肺癌有关的细胞内铁。IRP2诱导在小鼠异种移植模型中增加了肿瘤生长,表明它是合理的目标[9].数据支持这一点,显示出与敲低的细胞增殖相似的降低IREB2.在癌细胞中,就像desferasirox。在乳腺癌中也发现了类似的结果[31.].最近被吸入的RNAi以新颖的形式开发并用于针对不同遗传靶标的小鼠治疗肺癌[38.],意味着这可能是发展的潜在方式IREB2.在NSCLC中作为治疗的调节。我们没有观察结果与全身熨斗状况之间的任何关系;这可能意味着只有当地(IE。气道)铁具有相关性,因为腔铁似乎与结直肠癌最相关[32.]但对全身铁参数的多重影响使得这种数据的解释更清楚。
限制和进一步的工作
我们的研究仅限于手术切除的NSCLC病例,这导致了生存分析的相对较少的数量;尽管如此,队列在现场仍然具有竞争力,以实现其尺寸和表征程度。雌性患者的比例相对较高,病理分期(第IIIA期或B阶段或B)的许多病例相当先进,这可能限制普遍性。我们没有正式占辅助治疗在我们的分析中使用,因为只有三名患者接受了它,但承认有可能影响结果的机会很小,例如Cisplatin可以在化疗期间操纵铁沉积物[39.].由于其在肺泡巨噬细胞在肺泡巨噬细胞的血液中的低灵敏度和困难,因此没有进行染色非丙铁的染色,因为在肺泡巨噬细胞中,吸烟者的颜料是刺激的[40].我们的补充材料表明,我们的研究结果在FE的条件下没有可重复3+.我们用Fe看到的缺乏效果3+有趣的是,因为铁被认为是在气道内腔内氧化的,但我们不知道这是多么重要的事情:更加重视可能需要放在组织和血液中的铁水平上。
进一步的工作可能包括评估气道内铁浓度,这在吸烟者中是不同的[41.]以及局部水平嗜中性粒细胞弹性蛋白酶,其先前已显示在支气管肺泡灌洗液中影响铁浓度[42.].这将有助于评估局部螯合治疗是否比全身螯合治疗有任何潜在的益处,如果有,吸烟者或COPD患者是否更有可能受益。在未来的工作中可以探索的其他机制包括线粒体功能障碍和铁下垂。最近的动物研究表明IRP2可促进COPD中的线粒体功能障碍和铁超载[43.].这表明,线粒体螯合剂可能在COPD的治疗中发挥作用,并可能在肺癌动物模型中进一步探索。动物模型对于研究铁螯合剂对癌症的副作用也是必不可少的。铁下垂是细胞死亡的一种新表现形式,与细胞凋亡和坏死不同,线粒体比正常细胞小,嵴减少,外膜破裂[44.].铁过载通过生产反应性氧物种来促成骨裂化。相反,抑制铁的摄取可防止Erastin诱导的硬化[45.].肾脏和睫毛细胞系似乎对Erastin最敏感[46.]但是进一步研究了欧式蛋白诱导的铁唑在肺螯合剂暴露于铁螯合剂中的肺癌细胞的作用可能有兴趣,为治疗干预创造一个机会。
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充方法ERJ-00711-2016_Supplementary_Methods.
补充PCR方法ERJ-00711-2016_SUPPLENCERY_PCR_METHODS.
补充表S1ERJ-00711-2016_SUPPLEMENTARY_TABLE_S1
补充图S1erj - 00711 - 2016 - _supplementary_figure_s1
披露的信息
补充材料
致谢
作者谨慎感谢英格兰胸部手术部的员工,在英国NHS信任的信任中,他们为提供了细胞系的组织收集和F. Berditchevski。
脚注
本文提供了补充材料www.qdcxjkg.com
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 已收到2016年4月7日。
- 接受2016年12月20日。
- 版权所有©2017